Анализ особенностей когнитивных нарушений в диагностике и дифференциальной диагностике хронических цереброваскулярных заболеваний
- Аннотация
- Статья
- Ссылки
- English

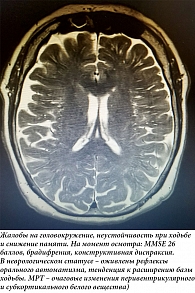


Для неврологов и врачей других специальностей актуален вопрос дифференциальной диагностики между сосудистыми когнитивными нарушениями (СКН) и болезнью Альцгеймера (БА). Как известно, указанные заболевания являются самыми частыми причинами КН в популяции. Подавляющее большинство эпидемиологических исследований подтверждает лидирующую позицию БА, в то время как распространенность СКН в два-три раза меньше [1, 2]. Однако в нашей стране диагноз БА устанавливается крайне редко, в большинстве случаев на поздних стадиях заболевания. Дифференциальная диагностика между двумя названными нозологическими формами базируется на анализе нейропсихологических особенностей когнитивных расстройств, наличии или отсутствии очаговой неврологической симптоматики, данных магнитно-резонансной томографии (МРТ).
Классификация и диагностика цереброваскулярных заболеваний
К цереброваскулярным заболеваниям относят инсульт и так называемую хроническую ишемию мозга (ХИМ). Вопросы диагностики церебрального инсульта тщательно проработаны и не вызывают каких-либо серьезных споров среди специалистов. В то же время до сих пор отсутствуют какие-либо диагностические критерии ХИМ, что делает этот диагноз весьма произвольным. При этом ХИМ представляет собой самый часто выставляемый в нашей стране неврологический диагноз у взрослых пациентов. Так, согласно статистическим данным, в 2017 г. на каждые 100 тыс. населения РФ было зарегистрировано 5566 пациентов с диагнозом «другие цереброваскулярные заболевания». В абсолютных числах в 2017 г. в России было официально зарегистрировано 6 527 568 пациентов с данным диагнозом, что составляет около 5% населения нашей страны [3]. Даже с учетом очевидной гипердиагностики ХИМ приведенные данные свидетельствуют о чрезвычайно широком распространении хронических форм нарушений мозгового кровообращения в клинической практике.
Как уже отмечалось, сегодня ХИМ считается достаточно неопределенным и произвольным диагнозом в повседневной практике. Многие лечащие врачи продолжают по инерции руководствоваться устаревшими представлениями о дисциркуляторной энцефалопатии как о заболевании с клиникой субъективных неврологических расстройств, таких как головная боль, головокружение, шум в ушах и общая слабость. Однако к настоящему моменту эксперты пришли к некоему консенсусу, который заключается в том, что главным ориентиром в диагностике и основополагающим клиническим признаком хронического цереброваскулярного заболевания должны быть КН [4].
Безусловно, не все случаи когнитивных расстройств на фоне артериальной гипертензии или других сердечно-сосудистых заболеваний имеют сосудистую этиологию. Причинно-следственная связь между КН и базисным сосудистым заболеванием должна быть четко аргументирована. В качестве аргументов международное научное сообщество рассматривает связь между временем возникновения когнитивных расстройств и острым нарушением мозгового кровообращения и/или характерные для хронического цереброваскулярного заболевания нейропсихологические особенности КН [5]. Именно поэтому неврологи и врачи других специальностей должны уделять особое внимание анализу качественных особенностей имеющихся у пациента когнитивных расстройств.
Нейропсихологические особенности СКН
Важнейшей клинической особенностью СКН при хроническом прогрессирующем безынсультном поражении головного мозга является их преимущественно подкорковый характер [6–8]. Это обусловлено тем, что наиболее частый этиопатогенетический вариант ХИМ – спорадическая церебральная микроангиопатия вследствие артериальной гипертензии или сахарного диабета. При этом в первую очередь страдают пенетрантные артерии, кровоснабжающие подкорковые структуры и глубинные отделы белого вещества. Не случайно типичной локализацией патоморфологических изменений при хроническом прогрессирующем течении цереброваскулярного заболевания становятся базальные ганглии и перивентрикулярное белое вещество [8, 9]. Поражение указанных структур приводит к нарушению связи между префронтальной корой, подкорковыми серыми узлами и другими отделами головного мозга с формированием дисфункции передних отделов головного мозга.
Аналогичный патофизиологический механизм лежит в основе когнитивных и эмоционально-поведенческих расстройств при подкорковых нейродегенерациях, других заболеваниях белого вещества (например, при рассеянном склерозе), нормотензивной гидроцефалии и некоторых других патологических состояниях. Многочисленные нейропсихологические исследования свидетельствуют о том, что при названных патологических состояниях наблюдается в целом сходный архетип когнитивных и эмоционально-поведенческих нарушений, получивший условное название подкорковой деменции [10–12]. На первый план выходят нарушение сложного внимания, снижение темпа познавательной деятельности (брадифрения), недостаточность управляющей функции (контроля поведения) и зрительно-пространственная диспраксия и дизгнозия. Характерны также трудности воспроизведения информации при сохранном запоминании (неспецифический тип мнестических расстройств). Почти всегда подкорковые когнитивные расстройства сопровождаются конгруэнтными изменениями в эмоционально-поведенческой сфере в виде депрессии, апатии или эмоциональной лабильности [13–16].
Снижение темпа познавательной деятельности (брадифрения) приводит к замедлению всех интеллектуальных процессов: восприятия, анализа, умозаключений, запоминания и обучения, построения сложных двигательных актов и др. В целом пациенту нужно значительно больше времени для любой умственной работы, чем в норме. При этом «инструментальные» способности познавательной деятельности не утрачены, то есть пациент не теряет ранее приобретенные знания и навыки: афазия, агнозия или апраксия отсутствуют. Потенциальная возможность справиться с заданиями различной степени сложности сохраняется, но для этого нужно больше времени, усилий и попыток. Для объективизации брадифрении требуются нейропсихологические методики, учитывающие время выполнения задания. К числу таких методик относятся проба Шульте, тест прокладывания пути (trail making test), тест «Символы и цифры» (digit symbol) и др. [27–29].
Трудности концентрации внимания при СКН проявляются значительными колебаниями темпа и эффективности познавательной деятельности, когда одинаковые по сложности когнитивные задачи выполняются с разным результатом. Типичные жалобы в таких случаях – повышенная утомляемость при умственной работе, утрата «нити» текущей деятельности, повышенная отвлекаемость. Для объективизации можно использовать те же методики, что и для диагностики брадифрении. При этом учитывается время или результативность выполнения равных по затратам труда частей задания. Например, фиксируется время прохождения первых пяти цифр в пробе Шульте (или в тесте прокладывания пути), потом вторых пяти цифр и т.д. Значительная разница свидетельствует о колебаниях уровня концентрации внимания.
Необходимо отметить, что темп познавательной деятельности и концентрация внимания очень подвижны даже в норме и зависят от функционального состояния головного мозга (например, снижаются при усталости и сонливости), эмоциональных переживаний, степени мотивированности и вовлеченности в умственную работу. Поэтому не следует преувеличивать значение негрубого и нестойкого снижения указанных показателей. Клиническую значимость данные когнитивные симптомы приобретают, когда они наблюдаются достаточно длительное время, воспроизводятся при повторных нейропсихологических исследованиях и вызывают субъективное беспокойство пациента.
Под управляющей функцией (executive function, буквально – исполнительная функция) в поведенческой неврологии принято понимать способность индивидуума произвольно управлять собственной познавательной деятельностью, то есть планировать ее и контролировать выполнение намеченного плана [17]. Нарушение управляющей функции в повседневной жизни проявляется нарушением планирования текущих дел, дезорганизацией и затруднениями при решении различных рабочих и бытовых вопросов. Характерны необдуманные или импульсивные решения и снижение интеллектуальной гибкости. Последнее выражается в чрезмерной и неоправданной приверженности одному поведенческому стереотипу (так называемое ритуальное, стереотипное и персевераторное поведение). На дементной стадии цереброваскулярного заболевания недостаточность управляющей функции может сопровождаться снижением чувства дистанции, некритичностью и дизингибицией. К проявлениям некритичности относятся многословность, патологическая обстоятельность, иногда излишняя откровенность, плоский «лобный» юмор и др. [13–16].
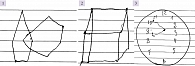
Нарушение зрительно-пространственных функций (зрительно-пространственная дисгнозия и конструктивная диспраксия) приводит к нарушениям конструирования и рисования, трудностям при совершении счетных операций в уме. Обычно данные когнитивные симптомы не вызывают существенных затруднений в повседневной жизни, но очень помогают в диагностике СКН, поскольку просты для объективизации. Для этого необходимо попросить пациента нарисовать объемную фигуру или объект: кубик, стол с четырьмя ножками либо домик (рис. 1 и 2).
Нарушения памяти у пациентов с СКН присутствуют почти всегда, но выражены в легкой или умеренной степени. Преимущественно страдает оперативная память: пациент забывает о текущих планах, быстро утрачивает информацию, необходимую для работы или решения бытовых вопросов. В то же время память на события жизни (так называемая эпизодическая память) остается сохранной. В основе нарушений при СКН лежит недостаточность воспроизведения информации при сохранном запоминании. При этом пациент сообщает об ощущении близости искомой информации («на кончике языка», «вертится в голове», «я же это знаю», «помню, но забыл» и т.д.). Нередко спустя время пациент вдруг припоминает то, что не мог вспомнить в нужный момент [18–20].
Проблема смешанной деменции
Качественные особенности мнестических расстройств крайне важны для дифференциальной диагностики между БА и СКН, поэтому на них следует обращать особое внимание. Изменение характера нарушений памяти, признаки их непрерывного прогрессирования по закону Рибо свидетельствуют о наличии сопутствующего нейродегенеративного процесса. Нейропсихологическим методом, который может помочь клиницисту в дифференциальной диагностике, является запоминание слов с процедурой контролируемого заучивания и подсказками при воспроизведении. При использовании подобной методики сортировка слов по семантическим категориям и дальнейшее использование семантической категории в качестве подсказки существенно помогают пациентам с «чистыми» СКН, но не влияют на показатель воспроизведения у пациентов с БА или смешанными сосудисто-дегенеративными КН [21–23].
Сосуществование цереброваскулярного заболевания и БА не является чем-то исключительным. Напротив, по данным патоморфологических исследований, у пациентов пожилого возраста с выраженными нейрокогнитивными расстройствами в большинстве случаев определяются характерные патологоанатомические маркеры обоих заболеваний [24–28]. В литературе имеются данные о своеобразной «синергии» сосудистого и нейродегенеративного заболевания в пожилом возрасте: когнитивные расстройства, которые наблюдаются при смешанном сосудисто-дегенеративном поражении центральной нервной системы, выражены в большей степени, чем этого можно было ожидать при простом наложении друг на друга симптомов двух заболеваний [29].
Подходы к диагностике смешанного сосудисто-дегенеративного поражения головного мозга различны. Некоторые авторы считают достаточным основанием для установления диагноза морфологические или радиологические признаки двух заболеваний, в то время как другие предлагают ориентироваться на клиническую картину. В последнем случае диагноз смешанных КН правомерен лишь при наличии в их структуре подкорковых симптомов (брадифрения, флуктуации, недостаточность планирования и контроля) и клинических признаков БА (нарушения памяти по гиппокампальному типу, аномия, апраксия и др.) [25, 27].
Некогнитивные симптомы ХИМ
Когнитивные нарушения составляют клиническое ядро хронического прогрессирующего цереброваскулярного заболевания. Однако симптоматика ХИМ не ограничивается когнитивными расстройствами. Как правило, им сопутствуют конгруэнтные изменения в эмоционально-поведенческой сфере, а на продвинутых стадиях заболевания – псевдобульбарный, пирамидный синдром и нарушения ходьбы.
Уже при первых описаниях так называемой подкорковой деменции исследователи обращали внимание на эмоциональные симптомы в виде снижения фона настроения, апатии или лабильности аффекта. У пациентов с хроническим цереброваскулярным заболеванием распространенность эмоциональных расстройств может достигать 50–80%, особенно на стадии начальной когнитивной недостаточности [30]. Предполагается, что эмоциональные расстройства при цереброваскулярной патологии являются прямым следствием поражения определенных церебральных структур, то есть представляют собой органический неврологический симптом [31, 32]. Об этом говорит связь с локализацией сосудистого поражения мозга. Как известно, риск развития депрессии особенно велик при локализации сосудистого очага в левой лобной доле или области базальных ганглиев слева [33]. При хроническом прогрессирующем сосудистом поражении головного мозга прослеживается связь между выраженностью депрессии и степенью изменений белого вещества (сосудистая лейкоэнцефалопатия) на МРТ [34, 35].
Сосудистая депрессия имеет ряд клинических особенностей, которые существенно отличают ее от классической психогенной депрессии. К числу таких особенностей относятся преобладание ангедонии над тоской и подавленностью, отсутствие или небольшая выраженность чувства вины и, напротив, значительная тяжесть соматических и когнитивных симптомов [31, 32]. Можно предположить, что сосудистая депрессия служит важным фактором, способствующим хронизации головной боли, несистемного головокружения и других субъективных неврологических расстройств, которые в свое время рассматривались как характерные для начальных стадий так называемой дисциркуляторной энцефалопатии.
В неврологическом статусе пациентов с ХИМ часто присутствуют псевдобульбарный синдром и нарушения ходьбы различной степени тяжести. Обычно неврологические расстройства присоединяются лишь на продвинутых стадиях сосудистого поражения головного мозга, в том числе у пациентов с повторными инсультами в анамнезе и выраженными нейрокогнитивными нарушениями. Наличие первичной неврологической симптоматики служит важным аргументом в пользу сосудистой природы патологического процесса. Однако в некоторых (достаточно редких) случаях не исключено развитие выраженных сосудистых КН без каких-либо значимых изменений в неврологическом статусе.
Нарушение ходьбы на поздних стадиях хронической ишемии головного мозга объясняется нарушением связи между лобной корой, подкорковыми базальными ганглиями и мозжечком. Играют роль также непосредственное сосудистое поражение подкорковых структур и мозжечка, пирамидные расстройства вследствие перенесенных инсультов, коморбидные заболевания периферической нервной системы (например, при сахарном диабете) и экстраневральная патология (заболевания суставов, ожирение и др.). Характерны ходьба на широкой базе, короткий шаг, шарканье и частые падения [36–38].
Диагностика СКН
Для скрининга сосудистых КН рекомендуется использовать Монреальскую когнитивную шкалу (MoCA), которая считается наиболее чувствительной в отношении легких когнитивных расстройств по подкорковому типу [39]. Однако тестирование по данной методике занимает 10–15 минут, что непозволительно долго для рутинного амбулаторного приема. В качестве альтернативы можно использовать методику Mini-Cog, но ее чувствительность значительно меньше [40].
Для верификации сосудистой природы КН, выявленных с помощью шкал, необходимо выполнить МРТ головного мозга. Без МРТ диагноз может быть только предположительным. Наиболее специфичными для сосудистого поражения головного мозга МР-изменениями являются церебральные инфаркты и микрокровоизлияния. В то же время гиперинтенсивность белого вещества наблюдается при очень большом спектре церебральных заболеваний, поэтому не может служить надежной верификацией сосудистой этиологии поражения мозга [41].
Лечение СКН
Диагноз хронического прогрессирующего цереброваскулярного заболевания требует полноценного обследования сердечно-сосудистой системы пациента для выявления основной причины сосудистого поражения головного мозга и всех иных имеющихся факторов сосудистого риска. Адекватный контроль заболеваний сердечно-сосудистой системы и оптимизация образа жизни (отказ от вредных привычек, физическая активность) имеют первостепенное значение для профилактики инсульта и прогрессирования сосудистых когнитивных расстройств.
Отметим, что наличие клинических и/или нейрорадиологических признаков сосудистого поражения мозга, в том числе немых инфарктов, само по себе не является основанием для назначения антиагрегантной или антикоагулянтной терапии [41]. Однако в подобной ситуации врачу следует повторно собрать подробный анамнез, уточнить, не было ли в прошлом недиагностированных инсультов, которые могли протекать со стертой или атипичной клиникой.
С патогенетической целью пациентам с СКН проводится терапия нейрометаболическими и вазотропными препаратами. В настоящее время хорошо известно, что наиболее ранним патогенетическим звеном микро- и макроангиопатии при различных сосудистых заболеваниях является эндотелиальная дисфункция. При этом в зонах дефектного эндотелия происходит синтез биологически активных веществ, инициирующих адгезию и дегрануляцию тромбоцитов. Одновременно с этим там же наблюдается активная экспрессия 5-HT-рецепторов к серотонину. В результате активация 5-НТ2-рецеторов гладкомышечных клеток тромбоцитарным серотонином приводит к длительной вазоконстрикции и локальной ишемии. Блокатор 5-НТ2-рецепторов нафтидрофурил (Дузофарм) способен предотвратить этот процесс или значительно уменьшить его последствия. Кроме того, блокада серотониновых рецепторов снижает проницаемость гематоэнцефалического барьера, что играет существенную роль в профилактике нарастания сосудистого лейкоареоза. Влияние Дузофарма ограничено зоной повышенной экспрессии серотониновых рецепторов, то есть препарат избирательно воздействует на поврежденные сосуды, не вызывая эффекта обкрадывания. Кроме того, Дузофарм блокирует 5-НТ-рецепторы собственно тромбоцитов, что предотвращает их агрегацию и может способствовать улучшению реологических свойств крови [42–46].
Положительный эффект Дузофарма в отношении когнитивных, эмоционально-поведенческих и неврологических симптомов ХИМ доказан в большой серии международных клинических исследований с использованием двойного слепого метода. Так, в четырех рандомизированных клинических исследованиях показан положительный эффект терапии Дузофармом в дозах 400–600 мг/сут длительностью 3–8 месяцев у пациентов с так называемой сенильной деменцией. Продемонстрированы достоверное улучшение результатов нейропсихологических тестов, оценки по эмоционально-поведенческим шкалам, положительная динамика биоэлектрической активности головного мозга по данным электроэнцефалограммы [47–50].
В двух других работах также с использованием двойного слепого метода отмечалась клиническая эффективность Дузофарма при сосудистой и смешанной деменции легкой и умеренной тяжести. Применение исследуемого препарата сопровождалось улучшением в когнитивной сфере и общей клинической оценки статуса пациентов [51, 52].
В 2011 г. был опубликован кокрейновский метаанализ, обобщивший результаты исследований препарата (девять публикаций, 847 пациентов). Его применение ассоциировалось с достоверным улучшением когнитивных функций и положительной динамикой в эмоционально-поведенческой сфере. Исследуемый препарат характеризовался оптимальной безопасностью и хорошей переносимостью [53].
В России также многократно изучали положительный эффект Дузофарма. В исследовании М.Н. Дадашевой и соавт. препарат назначали 200 пациентам с диагнозом ХИМ в дозе 300 мг/сут в течение двух месяцев. По окончании курса лечения у 34–43% (по разным шкалам) пациентов наблюдалась нормализация когнитивных функций, у 24% регрессировали тревожные расстройства, у 18,5% нормализовался сон. Одновременно зафиксирован достоверный регресс выраженности астенических расстройств [54].
В исследовании В.А. Парфенова и соавт. 30 пациентов с диагнозом умеренных сосудистых когнитивных расстройств получали терапию Дузофармом 300 мг/сут в течение месяца. В результате достоверно улучшились интегральный показатель интеллекта (МоСА), концентрация внимания (тест «Символы и цифры»), уменьшилась выраженность тревоги и депрессии [55].
О положительном эффекте Дузофарма при дисциркуляторной энцефалопатии в отношении когнитивного и психоэмоционального состояния пациента, а также равновесия и ходьбы (шкала Тиннетти) сообщают О.С. Левин и соавт. [56]. Следует отметить, что улучшение микрогемоперфузии и нейромедиаторной активности под влиянием Дузофарма лежит в основе антиастенического и антидепрессивного эффектов препарата, что особенно важно на наиболее ранних стадиях цереброваскулярной недостаточности. Дузофарм применяют в суточной дозе 300 мг, курсами от одного до трех месяцев.
На более поздних стадиях патологического процесса возрастает самостоятельная патогенетическая роль клеточных механизмов нейродегенерации, в частности глутаматергической гиперактивации. Считается, что конечным и необратимым этапом повреждения и в итоге гибели церебральных нейронов является перегрузка клеток ионами кальция. Поэтому с конца ХХ в. большой интерес ученых и практических врачей вызывают препараты, воздействующие на кальциевую нейротоксичность. В частности, широко изучались потенциальные нейропротективные свойства блокаторов кальциевых каналов. Наиболее изученным в этом отношении препаратом считается нимодипин (Нимопин), который характеризуется высокой степенью селективности в отношении церебральных сосудов. Давно и хорошо известна способность нимодипина уменьшать риск развития рефлекторного вазоспазма в остром периоде субарахноидального кровоизлияния [57]. Кроме того, Нимопин применяется у пациентов с умеренными и выраженными нейрокогнитивными нарушениями как сосудистой, так и нейродегенеративной этиологии. Помимо прямого нейропротективного эффекта в основе положительного действия Нимопина при цереброваскулярных заболеваниях лежит нормализация тонуса церебральных сосудов за счет расслабления гладкомышечных клеток сосудистой стенки [58].
В кокрейновском метаанализе 2002 г. проанализированы результаты 14 двойных слепых плацебо-контролируемых исследований, проведенных в европейских странах и США. В исследованиях участвовали около 2000 пациентов с сосудистой, первичной дегенеративной или смешанной деменцией. Нимодипин назначали в дозе 30 мг три раза в день в течение 8–24 недель. По окончании курса лечения наблюдалась достоверная положительная динамика по когнитивным тестам (Mini-Mental State Examination (MMSE), Wechsler Adult Intellegence Scale, Wechser Memory Scale, Trail Making Test и др.). Улучшение затрагивало в первую очередь сферы кратковременной памяти, внимания, ориентировки во времени и пространстве. Кроме того, увеличивалась скорость обработки информации [59].
Позже были опубликованы результаты крупного рандомизированного исследования эффективности нимодипина у пациентов с подкорковым вариантом сосудистой деменции. 242 пациента с указанным диагнозом получали нимодипин 90 мг/сут в течение 52 недель. Показано, что значительное когнитивное ухудшение (на 3 балла и более по шкале MMSE) в группе нимодипина в течение этого периода отмечалось достоверно реже, чем в группе плацебо. Таким образом, нимодипин доказательно снижает темп прогрессирования сосудистых КН [60].
W. Wang и соавт. (2006) отмечали клиническую эффективность нимодипина у пациентов с синдромом умеренных нейрокогнитивных нарушений в отношении интегрального показателя интеллекта (MMSE) и концентрации внимания (digit symbol) [61].
Таким образом, накопленные клинические данные позволяют говорить о том, что терапия нимодипином (Нимопин) обоснована для пациентов с умеренными или тяжелыми КН сосудистой, нейродегенеративной и смешанной этиологии. Нимопин применяют в дозе 90 мг в сутки, длительными курсами.
Заключение
Когнитивные нарушения рассматриваются в качестве основного проявления и наиболее важной мишени терапевтических стратегий при хроническом прогрессирующем цереброваскулярном заболевании. Специфической особенностью сосудистых когнитивных расстройств является преобладание в клинике нарушений внимания и управляющей функции при относительной сохранности памяти и первичных корковых симптомов. При сосудистых когнитивных нарушениях целесообразно использовать нейропротективные и вазотропные препараты, снижающие выраженность и темп прогрессирования симптоматики.
V.V. Zakharov, PhD, Prof., O.O. Martynova
I.M. Sechenov First Moscow State Medical University
Contact person: Vladimir V. Zakharov, zakharovenator@gmail.com
Cognitive impairment is the mail clinical presentation of chronic cerebral vascular diseases (CVD). The paper presents most important for diagnosis and differential diagnosis neuropsychological pattern of cognitive disorder in chronic CVD. It corresponds to the “subcortical” type of cognitive impairment with prevailing of attention and executive functions deficit and relative sparing of praxis, gnosis and language. Memory is characterized with mild-to-moderate retrieval insufficiency. Changing of memory disorder pattern with development of primary acquisition impairment, loss of recent memory according Ribot’s rule evidences the presence of concomitant neurodegenerative disease. Important argument for the vascular nature of cognitive impairment is coexistence of cognitive impairment with emotional disturbances (vascular depression), walking difficulties and other neurological signs. Specific MRI findings described in the article verify the diagnosis of vascular cognitive impairment. Treatment of vascular cognitive impairment should include the proper control of basic vascular disease plus neuroprotective and vasotropic drugs. The article presents existing clinical experience of naftidrofuril and nimodipine therapy in cognitive disorders.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.