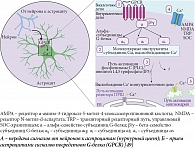
Астроцитарные сети и регуляция медленноволнового сна
- Аннотация
- Статья
- Ссылки
- English
От астроцитарного синцития к активной нейроглиальной среде
С. Рамон-и-Кахаль высказывал предположение, что глиальные клетки – «изоляторы», способные разобщать нейроны при развитии сна. Ростовский физиолог А.Б. Коган показал в экспериментах на кошках реципрокные изменения количества рибосом в нейронах коры и окружающих их глиальных клетках в медленноволновом сне (МВС), а также выявил инверсию этого процесса при развитии быстрого сна. По его мнению, это отражало направленность реорганизации нейроглиального метаболизма, обеспечивающего развитие таких фаз сна [1]. Позднее благодаря новым технологиям исследования глиальных клеток произошел настоящий переворот в нейрофизиологии нервной системы. Как оказалось, астроциты характеризуются разветвленной структурой клеточных отростков, создающих обширную глиальную сеть. В ней каждый астроцит способен контактировать с телами сотен нейронов и тысяч дендритов, охватывая сотни тысяч синапсов [2, 3]. Кроме того, астроциты в такой сети могут соединяться щелевыми контактами [4, 5]. Эту сеть стали называть астроцитарным синцитием. Похоже, она служит основой для реализации в головном мозге сложных функций астроцитов благодаря наличию на них множества различных рецепторов. Пока не представляется возможным оценить многообразие влияния астроцитов на физиологию синапсов. Известно, что охват подобного влияния достаточно широк – от структурной поддержки нейронов до регуляции внеклеточного пространства, от процессов контроля локального метаболизма до осуществления нейромодуляции [6–9].
Недавно представление об астроцитарном синцитии было дополнено понятием активной нейроглиальной среды. Согласно этому понятию, вокруг нейрона морфофункциональное единство представлено капиллярным руслом и микролимфатическими протоками, которые обеспечивают локальный метаболизм и реализацию глиатрансмиттерных функций [10]. Активная нейроглиальная среда – основа для таких астроцитарных функций, как высвобождение химических соединений D-серин и аденозинтрифосфата [11, 12]. Они обеспечивают обратную связь с синапсами нейронов на коротких временных интервалах. В реализации медленных, более длительных процессов влияние аденозина осуществляется через рецепторы A1 к аденозину, контролирующие рецепторный аппарат никотинамида динуклеотида (NMDA). Именно таким образом астроцитарная модуляция охватывает регуляцию быстрых и медленных процессов в синаптической передаче. Более глубокое изучение функционирования астроцитов в активной нейроглиальной среде, связанное с развитием сна и поведением, требует использования молекулярной методологии и методов опто- и хемогенетики [9, 13, 14].
Влияние G-белка (GPCR) на глубину и длительность МВС
Как известно, продолжительность МВС во многом контролируется циркадианными механизмами посредством нейромодуляторов [15–18]. Что касается глубины МВС, механизм ее регуляции иной. Здесь значительную роль играют цепи таламокортикальной реверберации [19, 20]. Нейроны коры также испытывают воздействие со стороны глии. Причем кортикальные нейроны подвержены не только быстрому (миллисекунды), но и медленному влиянию сигналов Ca+, вырабатываемых глиальными клетками [21, 22]. Многочисленные астроциты, расположенные в коре, контактируют с корковыми нейронами и влияют на их морфофункциональные свойства, транскрипционные процессы во время МВС [23] и пребывание под анестезией [24]. Кроме того, астроциты воздействуют на цикл «сон – бодрствование» посредством регуляции внеклеточного глутамата [25, 26], изменения динамики внеклеточных ионов [27], за счет высвобождения нейротрансмиттеров [27, 28], а также регуляции метаболизма [29–31]. В отличие от нейронов возбудимость астроцитов в основном опосредуется сигнализацией ионов Ca+, которая варьируется в зависимости от продолжительности амплитуды, частоты и клеточной локализации [32–35].
Установлено, что большая часть активности Ca+ обусловлена активацией рецепторов, связанных с G-белком (GPCR) [24, 36]. GPCR взаимодействуют с гетеротримерными G-белками альфа, бета и гамма. После активации GPCR альфа-субъединица, подразделяемая на семейства Gq, Gi и Gs, диссоциирует с бета- и гамма-белками. В результате запускаются нисходящие сигнальные каскады, включая путь фосфолипазы С (PLC)/инозитол 1,4,5-трифосфата (IP3), что в итоге приводит к высвобождению кальция из эндоплазматического ретикулума [36]. При этом большая часть рецепторов G-белка способна активироваться модуляторами цикла «сон – бодрствование», такими как норадреналин, ацетилхолин и гистамин. Механизмы G-белка являются одними из первых кандидатов на роль регуляторов сна, поскольку как Gi-, так и Gq-составляющие экскреции G-белка способствуют увеличению содержания внутриклеточного Ca+. Это влияет как на продолжительность МВС, так и на глубину его развития. Недавно было показано, что G-белок опосредованно влияет на рецептор инозитолтрифосфата второго типа (IP3 R2) и тем самым участвует в регуляции сна [37]. Наименее изучено дифференциальное влияние ионов Ca+ на процессы в отдельных нейронах. В настоящее время известно, что эндогенная активность Ca+ обратно коррелирует с МВС и демонстрирует двунаправленные изменения перед переходами «сон – бодрствование». Астроциты активно регулируют продолжительность или глубину МВС посредством разных сигнальных путей GPCR. Индуцированный астроцитами Gi Ca+ приводит к увеличению глубины МВС. Включение астроцитарных механизмов Gq-GPCR увеличивает продолжительность сна и инициирует переход «бодрствование – сон» [15], причем этот механизм способен вызвать как локальный, так и глобальный МВС.
Влияние предшествующей активности мозга на изменения сна
Похоже, сходные процессы наблюдаются и при запуске локальной активации или инициировании снижения МВС, вплоть до пробуждения. Этот эффект зависит от предшествовавших событию медленных волн. Так, локальный МВС развивается после паттернов дельта-волн, а глобальный МВС чаще запускается после медленных волн, частота которых ниже дельта-волнового диапазона [15]. То есть астроциты могут рассматриваться как центр управления не только глубиной, но и продолжительностью сна в коре головного мозга. Это реализуется за счет различного влияния астроцитов на популяции нейронов. Не следует забывать, что характер влияния астроцитов зависит не только от типа активированного GPCR, но и от их локализации в корковых нейронных цепях.
Как выяснилось, активация астроцитов Gi способна влиять на глубину МВС. В свою очередь активация Gq может изменять продолжительность сна, но не влияет на глубину МВС. Это говорит о наличии двух разных процессов регуляции. Один из них регулирует глубину, другой контролирует продолжительность МВС.
Ранее было показано, что после депривации сна глубина восстановительного сна всегда больше, чем до депривации. При этом продолжительность сна после депривации существенно не изменяется [38, 39]. Однако некоторые авторы продолжают связывать продолжительность и глубину сна воедино [21, 22], что не очень понятно, поскольку модель двух процессов позволяет связать продолжительность сна с давлением сна (по показателям МВС), а также с характеристиками циркадианного ритма [40, 41]. Концентрация Ca+ астроцитов изменяется в супрахиазматическом ядре в зависимости от циркадианного ритма [42]. Кроме того, она возрастает вместе с потребностью в сне после депривации сна. Помимо этого ранее были продемонстрированы изменения Ca+ астроцитов в быстром сне [37, 43]. Дальнейшее изучение астроцитарной регуляции быстрого сна может выявить интересные различия между регуляцией поведенческого сна и переходами в бодрствование. Похоже, передача сигналов Gi-GPCR будет значительно ослаблена во время быстрого сна, который приходит на смену МВС. Дальнейшие исследования в этом направлении представляются перспективными, ведь многие нейроглиальные взаимоотношения во время сна остаются невыясненными. Это касается внеклеточной регуляции глутамата [26], тонкой динамики внеклеточных ионов [27] и высвобождения аденозина [44, 45]. Неизвестно также, какие нижестоящие астроцитарные эффекты лежат в основе астроцитарного управления как глубиной, так и продолжительностью сна. Возможно, функциональный выход астроцитов является не простым следствием изменения уровня Ca+ в клетке, а сигналом по потоку от Gi- или Gq-GPCR рецепторов нижерасположенным каскадам регуляций (рисунок) [46–48].
Поскольку сигнальные пути после активации GPCR в астроцитах не выяснены полностью, они должны стать предметом дальнейших исследований. Понимание таких молекулярных механизмов поможет разработать подходы к нормализации глубины сна, а также найти эффективные способы лечения нарушений продолжительности ночного сна.
Заключение
На основании одновременной визуализации градиента ионов Ca+, отражающей деятельность астроцитов, и контроля электрофизиологии мозга удалось доказать, что кортикальные астроциты способны регулировать характеристики сна посредством дифференциальной передачи сигналов GPCR. Активность ионов Ca+, зависящая от IP3 R2, демонстрирует отрицательную корреляцию с развитием МВС. Концентрация ионов Ca+ меняется двунаправленно непосредственно перед переходом от сна к бодрствованию. В частности, астроциты способны активно регулировать отдельно продолжительность и глубину МВС посредством разных сигнальных путей GPCR. Индуцированный астроцитами Gi Ca+ увеличивает глубину МВС, а включение астроцитарных механизмов Gq-GPCR удлиняет сон и провоцирует переходы от бодрствования ко сну [15]. При этом, как выяснилось, такой механизм запускает как локальный, так и глобальный МВС в зависимости от характера предшествующих ритмических колебаний в электрокортикограмме. Выявленные закономерности дифференцированного управления астроцитарными процессами глубиной, с одной стороны, и продолжительностью МВС, с другой, представляют интерес для эффективной фармакотерапии расстройств сна. Обнаруженные различия позволяют выстраивать раздельные стратегии фармакологического влияния на коррекцию глубины или модификацию продолжительности МВС, что важно для решения вопросов клинической сомнологии.
E.V. Verbitsky, PhD, Prof.
Federal Research Center Southern Scientific Center of the Russian Academy of Sciences, Rostov-on-Don
Contact person: Yevgeny V. Verbitsky, e_verbitsky@mail.ru
A series of discoveries in brain physiology were followed by the 90s of the last century. Everyone's attention was focused on the electric silencers – glial cells. It turned out that astrocytes are not only a framework on which nerve cells sit like birds on tree branches. Astrocytes form a miniature cell of the active neuroglial medium around the neuron, combining blood capillaries and microlimphatic ducts for local metabolism. The activity of such a cell of the active medium is aimed at restoring the conductivity of the axon, destroying damage to the neuron and its elements, as well as regulating the flow of energy to the neurons. It turned out that such cells of the active medium are able to interact with each other. Thanks to this, the joint activity of many neurons can be coordinated. The way it happens during slow-wave sleep.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.