Блокаторы РААС в клинической практике: новые возможности применения
- Аннотация
- Статья
- Ссылки

Ингибиторы АПФ давно применяются в клинической практике. На протяжении последнего десятилетия проведены многочисленные исследования, в которых изучалась клиническая эффективность ингибиторов АПФ при различных сердечно-сосудистых заболеваниях. Результаты этих исследований нашли отражение в отечественных рекомендациях, согласно которым ингибиторы АПФ рекомендовано применять у больных артериальной гипертонией, сердечной недостаточностью, острым и перенесенным инфарктом миокарда и диабетической нефропатией (1, 2).
Что касается АРА, то за последние годы этот класс препаратов сделал огромный скачок вперед в плане приобретения новых ниш в различных клинических ситуациях. Если раньше этот класс препаратов пребывал в тени ингибиторов АПФ (их назначение при артериальной гипертензии (АГ) ограничивалось в основном ситуациями, связанными с побочными эффектами приема ингибиторов АПФ), то в настоящее время ниша их применения достаточно обширная (таблица 1).
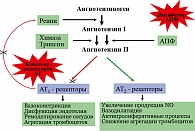
Обращают на себя внимание новые показания для применения АРА: профилактика мерцательной аритмии и хроническая сердечная недостаточность. Чтобы лучше понять возможности АРА, необходимо вспомнить их механизм действия. Он, как известно, заключается в блокировании АТ1-рецепторов ангиотензина II, через которые осуществляются основные негативные эффекты этого гормона. При этом, в отличие от ингибиторов АПФ, образование ангиотензина II не нарушается.
К числу негативных эффектов ангиотензина II относятся: вазоконстрикция, увеличение секреции эндотелина, стимуляция образования перекисных радикалов, гипертрофия гладкомышечных клеток, увеличение активности ингибитора тканевого активатора плазминогена 1 типа. Многие из этих эффектов являются атерогенными. В то же время стимуляция ангиотензином II незаблокированных рецепторов 2 типа (АТ2) вызывает эффекты, противоположные вышеперечисленным, а именно вазодилатацию, увеличение продукции оксида азота, стимуляцию антипролиферативных процессов. Таким образом, AРА обладают двойным положительным механизмом действия, в котором заложен мощный антиатеротромбогенный потенциал (рисунок 1).
Иллюстрацией возможностей АРА является исследование LIFE (изучение эффективности лозартана в отношении снижения достижения конечных точек у лиц с артериальной гипертонией) (3). В этом исследовании не только впервые была доказана антигипертензивная эффективность АРА в плане влияния на конечные точки, но и продемонстрированы другие их возможности.
В двойном слепом рандомизированном контролируемом международном исследовании участвовали 9193 больных с АГ и гипертрофией левого желудочка в возрасте 55-80 лет. Участники исследования были рандомизированы на две группы для получения в качестве первоначального лечения либо лозартана, либо атенолола. Начальная доза препаратов составила соответственно 50 мг лозартана 1 раз в сутки и атенолола 50 мг 1 раз в сутки. Препараты можно было комбинировать с гидрохлоротиазидом – 12,5 мг/сут. и далее повышать их дозу до 100 мг/сут., чтобы достичь целевого снижения АД – менее 140/90 мм рт. ст. Наконец, если максимальные дозы исследуемых препаратов в комбинации с диуретиком не обеспечивали адекватного контроля АД, то разрешалось назначать дополнительные препараты (за исключением АРА, ингибиторов АПФ и b-адреноблокаторов). Длительность исследования составила в среднем 4,7 года.
Основной целью исследования явилось изучение сравнительной эффективности лозартана и атенолола в плане снижения главной конечной точки, которая включала суммарно мозговой инсульт (МИ), инфаркт миокарда (ИМ) и смертность от сердечно-сосудистых причин. Другие конечные точки включали частоту возникновения новых случаев сахарного диабета (СД), смертность от всех причин, регресс гипертрофии миокарда левого желудочка, частоту госпитализаций по поводу стенокардии или сердечной недостаточности.
Частота главной конечной точки (смерть от сердечно-сосудистых причин, МИ и ИМ) на фоне лечения лозартаном оказалась 18%, а в группе пациентов, лечившихся атенололом, – 23% (р < 0,031). Частота фатального и нефатального МИ в группе лозартана была 9%, а в группе атенолола 11% (р < 0,204) несмотря на то, что АД в обеих группах снизилось практически одинаково – на 30/17 мм рт. ст. в группе лозартана и на 28/17 мм рт. ст в группе атенолола. Вместе с тем не было выявлено различий по частоте развития инфаркта миокарда в обеих группах. Другая важная находка – достоверно более низкая частота новых случаев СД в группе лозартана – на 25% (р < 0,001). Наконец, применение лозартана приводило к более выраженному регрессу гипертрофированного левого желудочка.
Новой областью применения блокаторов РААС стало снижение сердечно-сосудистого риска у пациентов с различными клиническими проявлениями атеросклероза. Новая область применения этого класса препаратов не имеет ничего общего с традиционным их применением при АГ, СД или хронической сердечной недостаточности (ХСН). Долгосрочный эффект блокаторов РААС основан на ряде механизмов. Одним из важнейших механизмов является улучшение эндотелиальной функции (4, 5). Коррекция эндотелиальной функции, в основе которой лежит увеличение синтеза оксида азота, является залогом антиатеросклеротического эффекта, который может иметь долгосрочное значение в плане улучшения прогноза пациентов, имеющих высокий риск смертельных исходов.
Впервые такая возможность была продемонстрирована для ингибиторов АПФ.
Это было показано в исследовании HOPE (6), в котором участвовали 9297 мужчин и женщин с подтвержденным атеросклерозом различной локализации (коронарная болезнь сердца, поражение периферических артерий, инсульт) или сахарным диабетом и по крайней мере еще одним фактором риска (артериальная гипертония, курение сигарет, микроальбуминурия или дислипидемия). 80% больных имели ишемическую болезнь сердца, 55% – стенокардию, 52% – инфаркт миокарда в анамнезе, 43% – атеросклероз периферических артерий, у 25% была нестабильная стенокардия в анамнезе, а у 26% – аортокоронарное шунтирование в анамнезе, у 18% – чрескожная реваскуляризация коронарных артерий, у 11% инсульт или транзиторная ишемическая атака.
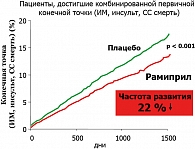
Почти половина пациентов страдала АГ и около 40% – СД типа 2. Больным назначали плацебо или ингибитор АПФ рамиприл (с титрованием доз от 1,25 до 10 мг) и продолжали наблюдение в среднем 5 лет. Первичная конечная точка (сердечно-сосудистая смерть, ИМ или МИ) была зарегистрирована у 17,8% больных группы плацебо и 14,0% больных группы рамиприла – снижение риска на 22%, р < 0001 (рисунок 2).
Терапия рамиприлом привела к снижению частоты важнейших компонентов конечной точки – ИМ, МИ. Кроме того, установлено снижение общей смертности (с 12,2 до 10,4% в течение 5 лет), необходимости реваскуляризации, диабетических осложнений, развития СД, остановки сердца, прогрессирования стенокардии или сердечной недостаточности. Представляет интерес тот факт, что снижение АД в группе рамиприла было сравнительно небольшим (АД –3/2 мм рт. ст.), поэтому результаты лечения нельзя объяснить только антигипертензивным действием препарата.
Таким образом, в этом исследовании была подтверждена протективная роль рамиприла в плане предупреждения развития осложнений у пациентов с клиническими проявлениями атеросклероза. Причем защитный эффект рамиприла никак не связан со снижением АД.
Вместе с тем с момента окончания исследования НОРЕ возникал вопрос: а почему АРА не способны на такое же снижение риска? Ведь как указывалось выше, АРА обладают механизмом действия, который способен приостановить развитие атеросклероза и улучшить прогноз пациентов. Именно такая гипотеза проверялась в исследовании ONTARGET (The Ongoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial).
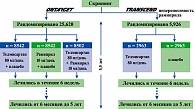
В данном исследовании изучали влияние телмисартана в сравнении с рамиприлом, а также комбинации этих двух препаратов на прогноз пациентов с различными проявлениями атеросклероза (поражения коронарных, периферических и церебральных артерий, СД типа 2, с органными поражениями) без признаков сердечной недостаточности (7). В двойном слепом рандомизированном исследовании в среднем в течение 56 месяцев 8576 больных получали рамиприл в дозе 10 мг; 8542 больных – телмисартан в дозе 80 мг; 8502 больных – оба препарата в указанных дозах дополнительно к ранее проводимой терапии (рисунок 3).
Препаратом сравнения для телмисартана был выбран рамиприл, ранее продемонстрировавший эффективность при лечении подобной категории пациентов. Проверялась гипотеза, что телмисартан будет не хуже, чем рамиприл, в профилактике осложнений у этой группы больных, а комбинация телмисартана с рамиприлом лучше, чем рамиприл.
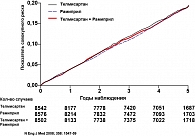
В качестве первичной конечной точки была выбрана комбинация смерти от сердечно-сосудистых причин, ИМ, инсультов и госпитализация в связи с сердечной недостаточностью. В течение исследования частота первичной конечной точки составила 1412 больных в группе рамиприла (16,5%) и 1423 больных в группе телмисартана (16,7%). Различия между группами оказались недостоверны (рисунок 4). Вместе с тем частота побочных эффектов в группе телмисартана была ниже. К примеру, частота кашля в группе телмисартана составила 1,1%, а в группе рамиприла 4,2%, р < 0,001.Соответствующие показатели для ангионевротического отека равны 0,1% и 0,3%, р = 0,01.
В группе комбинированной терапии при одинаковой частоте развития сердечно-сосудистых осложнений по сравнению с группой рамиприла (нет достоверных отличий) была хуже переносимость: повышенный риск развития гипотензивных проявлений (4,8% vs 1,7%, р < 0,001); синкопальных состояний (0,3% vs 0,2, р = 0,03) и почечной дисфункции (13,5% vs 10,2%, р < 0,001).
Таким образом, гипотеза, которая лежала в основе этого исследования, – «телмисартан будет не хуже в профилактике осложнений у больных с очень высоким риском их развития» – подтвердилась при лучшей переносимости лечения телмисартаном. А вот давно обсуждаемая потенциальная эффективность при сочетанном применении ингибиторов АПФ с АРА, особенно для усиления независимых от АД положительных механизмов, не только не подтвердилась, но и оказалась более опасной в плане развития нежелательных явлений.
Результаты исследования важны еще и потому, что, по данным завершившихся исследований, некоторыми учеными было сделано предположение о том, что АРА менее эффективны в профилактике ИМ, чем другие антигипертензивные препараты (8).
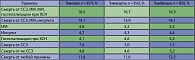
В исследовании ONTARGET частота развития ИМ на фоне лечения рамиприлом и телмисартаном достоверно не различались (таблица 2). В целом эта позиция не получила подтверждения в материалах опубликованного недавно всестороннего метаанализа, который показал одинаковую частоту ИМ в сравнении с другими препаратами.
В новом мета-регрессионном анализе Blood Pressure Lowering Treatment Trialist (BPLTT) оказалось, что АРА имеют ровно такие же связанные со снижением АД благоприятные эффекты на коронарные события, как и ингибиторы АПФ, однако последние могут иметь небольшое, не связанное с АД, благоприятное влияние. Прямое сравнение АРА (телмисартан) и ингибиторов АПФ (рамиприл) у больных с высоким риском развития осложнений в исследовании ONTARGET показало, что в обеих группах частота развития ИМ была одинаковой, т.е. кардиопротективное действие выражено одинаково.
Исследование TRANSCEND (Telmisartan Randomised Assessment Study in ACE intolerant subjects with cardiovascular Disease), которое является частью программы ONTARGET, было организованно для изучения эффективности телмисартана у больных с сердечно-сосудистыми заболеваниями или СД с органными поражениями, не переносивших лечения ингибиторами АПФ (9).
В исследование было включено 5926 больных, которые были рандомизированы на две группы – телмисартана 80 мг (n = 2954) и плацебо (n = 2972). Первичной конечной точкой в исследовании была сумма смертей от сердечно-сосудистых причин, ИМ, инсультов и госпитализаций по поводу сердечной недостаточности. Средняя продолжительность исследования составила 56 месяцев. Артериальное давление было ниже в группе телмисартана по сравнению с плацебо на протяжении всего исследования (в среднем на 4,0/2,2 мм рт. ст.). В группе телмисартана было отмечено 465 (15,7%) событий первичной конечной точки в сравнении с 504 (17,0%) событиями в группе плацебо (отношение рисков 0,91; 95% доверительный интервал 0,81-1,05, р = 0,216).
Следует отметить, что одна из вторичных конечных точек – сумма смертей от сердечно-сосудистых причин, ИМ и инсультов – была у 384 (13,0%) больных на телмисартане и у 440 (14,8%) больных на плацебо (отношение рисков 0,87; 95% доверительный интервал 0,76-1,00, р = 0,048), что оказалось достоверно меньше (см. рисунок 4). Именно по такому критерию была доказана эффективность рамиприла в сравнении с плацебо в исследовании HOPE (26). Больные, получавшие телмисартан, достоверно реже госпитализировались по сердечно-сосудистым причинам на 15% (р = 0,028). Телмисартан продемонстрировал хорошую толерантность у больных с непереносимостью ингибиторов АПФ.
Результаты исследования ONTARGET/TRANSCEND послужили основанием для регистрации нового показания для телмисартана – снижение риска осложнений у пациентов с клиническими проявлениями атеросклероза. В октябре 2009 г. FDA (США) одобрила применение телмисартана для снижения риска ИМ (сердечной атаки), инсульта и смерти от сердечно-сосудистых причин у больных старше 55 лет с высоким сердечно-сосудистым риском, которые не переносят ингибиторы АПФ.
В ноябре 2009 г. Европейская комиссия (EMEA) зарегистрировала новое показание для телмисартана. Телмисартан рекомендуется для снижения сердечно-сосудистой заболеваемости у больных с клиническими проявлениями атеросклероза (ИБС, инсульт, поражение периферических артерий) и СД типа 2 с документированными органными поражениями. Таким образом, телмисартан стал первым препаратом из класса АРА, рекомендованным для назначения больным с высоким сердечно-сосудистым риском.
Заключение
Блокаторы ангиотензиновых рецепторов обладают выраженными органопротективными свойствами, что значительно расширяет возможности их применения у больных с АГ. Благодаря выигрышному сочетанию хорошей переносимости, органопротекции, благоприятного метаболического профиля и доказанного в клинических исследованиях снижения риска развития осложнений этот класс антигипертензивных препаратов следует рассматривать как средство первого выбора для многих больных с повышенным АД. Недавно было доказано, что сартаны не уступают ингибиторам АПФ в эффективности при лечении больных с высоким риском осложнений (исследование ONTARGET/TRANSCEND), а телмисартан – первый и единственный представитель класса АРА – получил официальное показание для применения у этих больных.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.