Болезнь Ниманна – Пика типа C: диагностика, динамическое наблюдение и лечение больных в России
- Аннотация
- Статья
- Ссылки
- English
![Таблица 1. Распространенность редких (орфанных) лизосомных болезней накопления [3]](/upload/resize_cache/iblock/759/195_350_1/9_1.jpg)

![Таблица 3. Частота клинических проявлений болезни Ниманна – Пика, тип C [7]](/upload/resize_cache/iblock/16b/195_350_1/9_3.jpg)
![Таблица 5. Профиль безопасности препарата Завеска® [21]](/upload/resize_cache/iblock/a0b/195_350_1/9_5.jpg)
![Таблица 6. Симптоматическое лечение больных с болезнью Ниманна – Пика, тип C [11]](/upload/resize_cache/iblock/702/195_350_1/9_6.jpg)
За последние годы значительно повысилось внимание к редким (орфанным) болезням, и в частности к лизосомным заболеваниям. Прежде всего это связано с раскрытием сущности многих лизосомных болезней. Не менее важным стимулом к изучению лизосомных заболеваний стало открытие возможности их патогенетического лечения с помощью ферментозамещающих средств. К обширной группе лизосомных болезней накопления, включающей 45 нозологических форм, относится болезнь Ниманна – Пика типа C [1].
Определение, частота и этиология болезни Ниманна – Пика, тип C
Лизосомные болезни накопления характеризуются, как правило, ранней манифестацией заболевания, прогредиентностью течения, тяжелым поражением жизненно важных органов и систем организма, приводящим к ранней инвалидизации и преждевременным смертельным исходам, нередко начиная с неонатального периода. Болезнь Ниманна – Пика типа C четко отграничена от других форм лизосомных заболеваний, в том числе от болезни Ниманна – Пика типа А и типа В, является самостоятельным заболеванием и относится к категории редких (орфанных) болезней.
Частота (заболеваемость) болезни Ниманна – Пика типа C составляет 1:100 000–1:120 000 живых новорожденных [2]. Распространенность болезни Ниманна – Пика типа C, оцененная расчетным путем, составляет 0,85 на 100 000 населения [3]. В действительности распространенность, очевидно, выше, что может быть связано с наличием незарегистрированных случаев, неправильной постановкой диагноза, не доведенной до конца диагностикой и др. Заболевание носит панэтнический характер, распространено повсеместно. Высокая частота болезни Ниманна – Пика типа C1 отмечена среди некоторых генетических изолятов: французской колонии Акадия (Новая Шотландия), групп бедуинов в Израиле, испанских поселений в Колорадо и Нью-Мексико, что связано с эффектом основателя.
Среди других лизосомных болезней накопления по показателю распространенности болезнь Ниманна – Пика типа C занимает среднее положение. Сравнительные данные по распространенности отдельных форм лизосомных болезней представлены в табл. 1 [3].
В Российской Федерации диагностика болезни Ниманна – Пика типа C стала осуществляться с 2008 г. На начало 2013 г. диагностировано 11 больных, из них 2 иностранных гражданина. Среди диагностированных больных 10 детей от 3 до 18 лет и 1 взрослый (26 лет). Начато лечение 7 человек. Прогнозируемое количество больных – более 170 человек.
Болезнь Ниманна – Пика типа C – прогрессирующее аутосомно-рецессивное наследственное нейродегенеративное заболевание с гепатоспленомегалией, связанное с нарушением регуляции внутриклеточной транспортировки (англ. trafficking) липидов [4]. Характеризуется неблагоприятным прогнозом в отсутствие своевременно начатого адекватного специфического лечения (субстратредуцирующая терапия). Этиология заболевания связана с мутациями в гене NPC1 (в 95% случаев) или в гене NPC2 (около 5% случаев) – болезнь Ниманна – Пика, типы С1 и С2 соответственно [5], что ведет к нарушению внутриклеточного транспорта липидов и накоплению холестерина и гликосфинголипидов в головном мозге и других тканях (табл. 2).
Оба типа болезни наследуются аутосомно-рецессивно. Ген NPC1 картирован на длинном плече хромосомы 18, в локусе q11-q12 – 18q11-q12. Ген болезни Ниманна – Пика NPC2 локализован на хромосоме 14, в области ее длинного плеча – q24.3 – 14q24.3 [5].
Патогенез
Болезнь Ниманна – Пика типа C развивается в результате наследственной недостаточности внутриклеточной (лизосомальной) транспортировки липидов (холестерина) и их этерификации (нарушение жирового обмена), что приводит к накоплению свободного неэтерифицированного холестерина в клетках различных тканей, вторичному накоплению сфингомиелина и гликосфинголипидов (сфингомиелиновый липидоз) в основном в головном мозге с глубокими функциональными и структурными изменениями нейронов, а также Gm2- и Gm3-ганглиозидов [6]. При этом заболевании почти постоянно вовлечены другие органы (в частности печень и селезенка).
Для болезни Ниманна – Пика типа C свойственен нормальный уровень лизосомного фермента сфингомиелиназы.
Клиническая картина и диагностика
Наиболее часто (в 70% всех случаев) заболевание манифестирует в возрасте от трех до восьми лет. Реже дебют патологии может наблюдаться между 10 и 15 годами жизни. Наряду с этим описаны единичные случаи начала болезни в неонатальном периоде с желтухой и спленомегалией и у взрослых (55 и более лет) лиц. Как правило, до манифестации основных клинических симптомов заболевания психомоторное развитие больных остается нормальным.
Ранними типичными признаками болезни Ниманна – Пика типа C у детей дошкольного возраста являются нарушения координации движений, атаксия, тремор, дизартрия, хореоатетоз. Дебют заболевания в школьном возрасте и у взрослых обычно проявляется расстройствами познавательной деятельности с формированием в дальнейшем умственной отсталости. Снижение интеллекта характерно для всех случаев болезни, но степень ее выраженности может быть различной. Патогномоничным симптомом болезни является паралич взора при взгляде вверх и вниз. Довольно часто (примерно у одной трети больных) развиваются судорожные пароксизмы, носящие фокальный или генерализованный характер. Судороги обычно резистентны к противосудорожной терапии. Характерным признаком типов C1 и C2 считается гепатоспленомегалия, которая может проявляться как в начале заболевания, так и после развития неврологической симптоматики. Частота клинических проявлений заболевания отражена в табл. 3 [7].
Болезнь неуклонно прогрессирует, заканчиваясь летальным исходом, как правило, на 5–15-м годах жизни. Варианты с более поздним дебютом заболевания (в школьные годы и у взрослых) отличаются существенно более медленным прогредиентным течением [8, 9, 10].
Типы C1 и C2 сходны по своим клиническим проявлениям.
Выделяют следующие клинические формы заболевания [11, 12].
Неонатальная форма манифестирует до трехмесячного возраста; нередко дебютирует внутриутробной водянкой плода. В периоде новорожденности основными признаками могут быть затяжная желтуха, гепатоспленомегалия, асцит, мышечная гипотония.
Ранняя младенческая форма проявляется в возрасте от 3 месяцев жизни до 2 лет; характеризуется гепатоспленомегалией, задержкой психомоторного развития, мышечной гипотонией, прогрессирующими мозжечковыми расстройствами (атаксия).
Поздняя инфантильная форма манифестирует в 2–6 лет. Основные клинические проявления – прогрессирующая атаксия, дизартрия, нарушение поведения, гепатоспленомегалия, интеллектуальная недостаточность, вертикальный парез взора, эпилепсия, спастичность, катаплексия, дисфагия, дистония. Фатальный исход – в возрасте 7–12 лет.
Юношеская (ювенильная) форма манифестирует от 6 до 15 лет; характеризуется задержкой психоречевого развития, нарушением поведения, мозжечковыми (атаксия, интенционный тремор, дизартрия, изменение походки) и экстрапирамидными (мышечная гипотония, различные виды гиперкинезов) расстройствами, различными типами эпилептических приступов, иногда полинейропатией. Специфическим симптомом является вертикальный офтальмопарез.
Взрослая форма – начало заболевания в возрасте старше 15 лет, проявляется атаксией, дистонией, психиатрическими симптомами, гепатоспленомегалией, деменцией.
Для заболевания характерен широкий спектр клинических проявлений. Средний возраст постановки диагноза составляет 10,4 года, ожидаемая продолжительность жизни – 16,2 года, продолжительность жизни – 38 лет.
Терапевтические перспективы повышают важность своевременной диагностики болезни Ниманна – Пика типа C, в основе которой должна лежать клиническая настороженность неврологов, педиатров, психиатров, терапевтов, генетиков и других специалистов, в чье поле зрения могут попадать больные с рассматриваемым заболеванием [13].
Для диагностики используются биохимические методы (накопление неэтерифицированного холестерина в лизосомах, Филипин-окрашивание для выявления накопления липидов), гистологические методы (пенистые клетки в биоптатах костного мозга и селезенки, лазурные гистиоциты в биоптатах костного мозга, полиморфные тельца в цитоплазме клеток кожи, печени или мозга). Генетические методы (ДНК-диагностика) применяются для подтверждения диагноза, пренатальной диагностики, выявления гомозигот в семьях пробандов. Для выявления атрофических изменений мозговых структур используются магнитно-резонансная томография (МРТ), компьютерная томография, протонная магнитно-резонансная спектроскопия.
Используются также данные лабораторных, функциональных и патоморфологических исследований. МРТ головного мозга диагностирует симметричную атрофию коры, мозжечка и гипоплазию мозолистого тела. В биоптатах печени, селезенки, лимфатических узлов, костного мозга, миндалин, почек, легких и гладкой мускулатуры выявляют «пенистые» клетки с липидными ШИК-положительными включениями. Световая микроскопия констатирует наиболее глубокие повреждения нейронов бледного шара, хвостатого ядра и черепных нервов с накоплением в них ШИК-позитивных липидов. В клетках глии также фиксируют отложения жиров, холестерина и липидов. При электронной микроскопии в нейронах определяются концентрические пластинчатые тела, аналогичные по своей структуре включениям при Gm2-ганглиозидозах.
Дифференциальная диагностика, лечение и профилактика
Болезнь Ниманна – Пика типа C следует дифференцировать от других болезней накопления: Gm1- и Gm2-ганглиозидозов, мукополисахаридозов и болезни Гоше.
Очевидно, что при болезни Ниманна – Пика типа C наибольший эффект имело бы этиотропное лечение (генотерапия), однако оно пока не разработано.
Патогенетическая терапия
В связи с малой изученностью патогенеза заболевания патогенетические методы терапии болезни Ниманна – Пика типа C начали разрабатываться сравнительно недавно. Для успеха терапевтических вмешательств чрезвычайно важное значение имеет знание механизмов поражения нервной системы, в частности оценка количества жизнеспособных нейронов центральной нервной системы (ЦНС). Именно на этом основана таргетная терапия, применяющаяся при лечении наследственных нейродегенеративных заболеваний, одним из представителей которых является болезнь Ниманна – Пика типа C.
В клинических исследованиях изучалась эффективность использования гипохолестеринемических средств (снижающих внутриклеточный уровень холестерина) или ограничения приема холестерина. Несмотря на то что такая терапия вызывала снижение содержания холестерина в печени и плазме, улучшения неврологических проявлений отмечено не было [14, 15]. Предпринимались попытки трансплантации костного мозга или печени, что позволяло частично нормализовать накопление холестерина и сфингомиелина в тканях. Однако эти методы оказались неэффективны в лечении неврологических симптомов у пациентов с мутациями в гене NPС1 [16].
Поскольку болезнь Ниманна – Пика типа C, как правило, диагностируется поздно, у больных уже повреждена или погибла значительная часть нейронов ЦНС. В этом случае цель терапии – сохранить жизнеспособные нейроны, стабилизировать заболевание и снизить скорость прогрессирования патологического процесса. Тяжесть повреждения нервной системы у больных различна, поэтому выбор терапии должен быть индивидуальным [17].
Трудности в лечении болезни Ниманна – Пика типа C сохраняются до сих пор. В первую очередь это обусловлено малой изученностью патогенетических механизмов заболевания, поздней диагностикой и малочисленностью научных изысканий в этом направлении. Положение стало меняться после создания лекарственного средства нового поколения – миглустата (препарат Завеска®) и разработки нового направления в лечении лизосомных болезней – субстратредуцирующей терапии.
Установление молекулярно-генетической природы болезни Ниманна – Пика типа C, характера биохимических расстройств, идентификация мутантных генов и их хромосомной локализации дали возможность разработать новые подходы к лечению этого лизосомного заболевания, связанные с использованием средств, предупреждающих образование исходных продуктов (веществ), которые являются предшественниками накапливаемых субстратов. При болезни Ниманна – Пика типа C удалось уменьшить образование гликосфинголипидов как исходных продуктов накопления за счет подавления фермента гликозилцерамидсинтазы (первого фермента синтеза большинства гликолипидов) с помощью специфического лекарственного препарата – миглустата. Соответственно, снижение синтеза исходных биохимических продуктов обмена (гликосфинголипидов) приводит к уменьшению их накопления в органах и тканях организма. Субстратредуцирующую терапию можно назвать новым направлением патогенетического лечения, поскольку она направлена на прерывание начального патогенетического звена заболевания.
Миглустат (международное непатентованное название (МНН) – миглустат; торговое название – Завеска) разработан и внедрен для лечения больных с болезнью Ниманна – Пика типа C фирмой “Actelion” (Швейцария). По химической структуре миглустат – N-бутилдеоксиноджиримицин (NB-DNJ) и относится к иминосахарам. Важнейшим свойством миглустата, который является ингибитором синтеза гликозосфинголипидов, является его способность проникать через гематоэнцефалический барьер [18]. Миглустат, наряду с ингибированием гликозилцерамидсинтазы, начального фермента образования гликосфинголипидов, также ингибирует сукрозу-изомальтазу и другие дисахаридазы в тонком кишечнике, что лежит в основе побочных эффектов миглустата со стороны желудочно-кишечного тракта. Под влиянием миглустата предупреждается накопление токсических метаболитов (ганглиозидов GM2 и GM3, лактозилцерамида и гликозилцерамида) и их нейротоксическое действие. Однако миглустат не ингибирует синтез сфингомиелина и галактозилцерамида (основного компонента миелина), как и не вызывает аккумуляции церамида [11].
Препарат Завеска® (миглустат) был одобрен Управлением по контролю качества пищевых продуктов и лекарственных препаратов США (Food and Drug Administration – FDA) как первое медикаментозное лекарственное средство для лечения болезни Ниманна – Пика типа C, затем препарат был зарегистрирован в Европе (январь 2009 г.). Для применения на территории Российской Федерации препарат Завеска® зарегистрирован в ноябре 2009 г. (регистрационный номер: ЛСР-008892/09). Препарат выпускается в форме капсул (в 1 капсуле 100 мг) для приема внутрь.
В США в 2008 г. миглустату был присвоен статус редкого (орфанного) лекарственного средства.
На сегодняшний день Завеска® – первый и единственный препарат, зарегистрированный для лечения болезни Ниманна – Пика типа C. Учитывая механизмы действия миглустата, он применяется также при болезни Гоше в качестве субстратредуцирующей терапии.
В связи с появлением лекарственного средства для патогенетического лечения болезни Ниманна – Пика типа C возникли две острые проблемы: 1) необходимость ранней диагностики заболевания, 2) назначение лечения в наиболее ранние сроки. Пока, к сожалению, разработанный препарат рекомендован для применения у детей с болезнью Ниманна – Пика типа C начиная с четырехлетнего возраста. Ясно, что положительное решение о применении миглустата у детей раннего возраста не только вопрос времени, но и ранней диагностики заболевания, а также набора необходимой когорты больных и проведения соответствующих клинических испытаний.
Показаниями к применению препарата Завеска® являются:
- лечение прогрессирующих неврологических симптомов у взрослых и детей с болезнью Ниманна – Пика типа C, что может замедлять прогрессирование заболевания;
- пероральная терапия болезни Гоше I типа легкого и среднетяжелого течения, в том числе при непереносимости или невозможности применения заместительной ферментной терапии у взрослых [19].
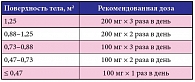
При болезни Ниманна – Пика типа C рекомендуемая доза препарата Завеска® для взрослых и детей старше 12 лет составляет 200 мг 3 раза в день, детям от 4 до 11 лет доза назначается исходя из площади поверхности тела (см. инструкцию к препарату, табл. 4).
Эффективность и безопасность миглустата (Завеска®) были продемонстрированы в ряде исследований. Оценка результатов многоцентровых исследований с участием 66 пациентов с болезнью Ниманна – Пика типа C показала, что у большинства больных после лечения миглустатом наблюдались стабилизация или улучшение состояния [19]. При этом скорость снижения суммарного индекса по модифицированной шкале инвалидизации значительно уменьшилась, и у 75% больных эффект от проводимой терапии был оценен как «хороший». Важно подчеркнуть, что у больных с болезнью Ниманна – Пика типа C терапия миглустатом оказывает положительное влияние на неврологические нарушения. Кроме того, при использовании препарата Завеска® отмечается замедление прогрессирования заболевания. В исследовании M.C. Patterson и соавт. на фоне терапии препаратом Завеска® у большинства пациентов всех возрастных групп состояние либо улучшалось, либо стабилизировалось как минимум по 3 из 4 параметров (атаксия, дистония, дизартрия, дисфагия) [20].
Препарат характеризуется благоприятным профилем безопасности и хорошей переносимостью как у детей, так и у взрослых (табл. 5) [21]. Как показано в исследовании M. Pineda и соавт., в котором среднее время использования препарата Завеска® у 67 больных составило 533 дня, у 45% больных отмечена минимум одна нежелательная реакция [21].
Существуют данные по эффективности лечения миглустатом у пациентов в возрасте от 7 месяцев до 44 лет (средний возраст 14,68 ± 10,84 года) при болезни Ниманна – Пика типа C1 и C2 [14]. На фоне терапии препаратом Завеска® у пациентов с мутациями в гене NPC1 отмечено улучшение функции глотания (воды, пюре, пасты, бисквита) (по данным видеомониторирования с использованием видеофлюороскопии (videofluoroscopic swallowing study, VFSS) – у 85% больных; стабилизация – у 81%; улучшение по параметру «дистония» – у 80%, «дисметрия» – у 74%, «дизартрия» – у 63%; возрастание DQ с 45 до 65 ед. (через 24 месяца лечения миглустатом). Через 36 месяцев лечения миглустатом улучшение состояния или стабилизация симптомов наблюдались у 22 пациентов с мутациями в гене NPC2. Так, улучшение по параметру «спонтанные движения глаз в вертикальной плоскости» отмечено у 7 пациентов на фоне терапии Завеской и у 1 пациента, не получавшего миглустат; отсутствие изменения зарегистрировано у 8 и у 1 больного; ухудшение – у 2 и 3 соответственно. Улучшение со стороны глазодвигательной сферы отмечено и в исследовании M. Pineda и соавт.: после 12 месяцев использования препарата Завеска® показано улучшение или стабилизация проявления симптома «спонтанные вертикальные движения глаз» у пациентов 12 лет и старше [21].
По данным D. Bruschini и соавт., применение миглустата в течение 2 лет у 4 больных в возрасте 11 месяцев, 9, 10 и 12 лет (3 с мутацией в гене NPC1 и 1 с мутацией в гене NPC2) способствовало нормализации функции глотания у всех больных [18].
Симптоматическая терапия
Наряду с патогенетическим лечением большое значение при болезни Ниманна – Пика типа C имеет и симптоматическая терапия. Основные ее направления отображены в табл. 6. [11].
Симптоматические средства, хотя и обладают широкой вариабельностью своего действия, могут оказаться весьма полезными для улучшения состояния больных и повышения качества их жизни.
Особое внимание следует обращать на питание больных и систематически оценивать способность глотать пищу (существуют специальные шкалы оценки глотания – глотание жидкой пищи, полужидкой, густой и т.д.). При лечении рекомендуется диета с низким содержанием холестерина и применение препаратов, снижающих его уровень в сыворотке крови. При значительном нарушении функции глотания больным рекомендуется зондовое питание или накладывание гастростомы, что дает возможность обеспечить больных необходимым количеством питательных веществ, достаточным количеством жидкости и калоражем.
Для коррекции функции слюноотделения у больных может использоваться атропин в каплях в небольших дозах.
Дисфагия нередко осложняется вторичным поражением легких. В этих ситуациях могут назначаться антибиотики для профилактики пневмонии.
При развитии желудочно-кишечных расстройств, наиболее часто диареи, рекомендуются антидиарейные средства и специальная диета. Однако диарея может быть следствием применения миглустата. В этих случаях для устранения побочных эффектов на фоне терапии миглустатом и при развитии диарейного синдрома рекомендуется пересмотр диеты и уменьшение приема лактозосодержащих продуктов или прием других углеводов. Положительный эффект может оказать разделение по времени приема миглустата и пищевых продуктов. В ряде случаев возможно назначение антидиарейных препаратов типа лоперамида или отмена препарата Завеска® на короткое время.
Для решения возникающих вопросов могут потребоваться консультации соответствующих специалистов (гастроэнтеролога, невролога, психиатра и др.).
В целом повышение эффективности лечения пациентов с болезнью Ниманна – Пика типа C возможно при соблюдении ряда основополагающих принципов:
- точная диагностика (учреждения, методы, региональные и федеральные регистры и др.);
- квалифицированные врачебные заключения (консультант, региональный консилиум, федеральный консилиум и т.д.);
- разработанные и утвержденные стандарты лечения (финансово-экономические расчеты, финансирование и др.);
- разработанные и утвержденные клинические рекомендации (международные, федеральные и др.);
- эффективное взаимодействие при оказании лечебной помощи (дети – взрослые, учреждения, врачи, утвержденная документация);
- консультативная помощь в процессе лечения (учреждения, эксперты);
- своевременное пополнение перечня жизненно необходимых и важнейших лекарственных препаратов (включение в него лекарственных препаратов, орфанных препаратов и др.).
Прогноз заболевания значительно улучшается при применении миглустата (препарата Завеска®).
Профилактика
Профилактика базируется на данных медико-генетического консультирования. Медико-генетический риск для сибсов пробанда составляет 25%. Если установлен генотип пробанда, типы мутаций у носителей, возможна пренатальная диагностика болезни Ниманна – Пика типов C1 и C2. Диагноз может быть установлен на 10–12-й неделе беременности при молекулярно-генетическом исследовании биоптатов ворсин хориона. В ряде случаев определенную помощь может оказать исследование активности сфингомиелиназы в амниоцитах и биоптатах хориона с помощью биохимических методов, однако для проведения подобного анализа нужна культура клеток.
Niemann-Pick type C disease: diagnosis, follow-up and therapy in Russia
P.V. Novikov
Federal State Budgetary Institution ‘Federal Research Institute for Pediatry and Pediatric Surgery’ of the Ministry of Health of Russia, Moscow
Contact person: Pyotr Vasilyevich Novikov, pnovikov@pedklin.ru
Niemann-Pick disease is a lysosomal storage disease with autosomal recessive pattern of inheritance. Niemann-Pick type C disease is of particular interest for pediatric neurologist due to marked clinical polymorphism (muscle hypotonia, psychomotor retardation, cataplexy, dysphagia, intellectual disability, ataxia etc.) depending on manifestation age. Substrate-reducing agent miglustat (Zavesca®) is the only pathogenetical therapy for Niemann-Pick type C disease. Studies have shown that treatment with miglustat effectively improved neurological symptoms (spontaneous vertical eyes movements, impaired swallowing and coordination disorder) and resulted in disease stabilization or delayed progression. Miglustat has good safety profile. To provide effective treatment of this orphane disease, early diagnosis is essential.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.