Эффективная фармакотерапия послеоперационного периода стандартной факоэмульсификации
- Аннотация
- Статья
- Ссылки
Неосложненного течения послеоперационного периода удается добиться у 96–98% пациентов после факоэмульсификации «обычной» катаракты. Во многом это достигается благодаря медикаментозной профилактике инфекционных осложнений. В обзоре рассматриваются современные схемы медикаментозного сопровождения послеоперационного периода, анализируются используемые в мировой практике лекарственные препараты. На основании собственного опыта и данных зарубежных и отечественных исследований автор предлагает схему эффективной фармакотерапии стандартного течения послеоперационного периода факоэмульсификации с применением нестероидных противовоспалительных препаратов (Индоколлир), антибиотиков (фторхинолоны 4-го поколения) и глюкокортикостероидов.
Неосложненного течения послеоперационного периода удается добиться у 96–98% пациентов после факоэмульсификации «обычной» катаракты. Во многом это достигается благодаря медикаментозной профилактике инфекционных осложнений. В обзоре рассматриваются современные схемы медикаментозного сопровождения послеоперационного периода, анализируются используемые в мировой практике лекарственные препараты. На основании собственного опыта и данных зарубежных и отечественных исследований автор предлагает схему эффективной фармакотерапии стандартного течения послеоперационного периода факоэмульсификации с применением нестероидных противовоспалительных препаратов (Индоколлир), антибиотиков (фторхинолоны 4-го поколения) и глюкокортикостероидов.
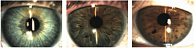

Стандартный период после факоэмульсификации «обычной» катаракты протекает спокойно, без заметных негативных субъективных ощущений пациента и в отсутствие жалоб. В первые часы пациент иногда отмечает ощущение инородного тела или легкого жжения, визуальные эффекты могут выражаться в виде различных оттенков (розоватого, голубоватого) или легкой размытости. Как правило, к первым суткам после операции пациент избавляется от непосредственных ощущений оперативного вмешательства. Роговица и влага передней камеры прозрачные, сохраняется реакция зрачка на свет. Согласно данным литературы и на основании собственного опыта, неосложненное течение послеоперационного периода отмечается у 96–98% пациентов с «обычной» катарактой (рис. 1). Осмотры пациентов после факоэмульсификации желательно проводить в день операции и обязательно на первые сутки, затем – через неделю и один месяц.
Гладкое течение послеоперационного периода обусловлено, по крайней мере, двумя факторами. Во-первых, современная технология факоэмульсификации предполагает щадящие параметры самого оперативного вмешательства при правильно выбранных показаниях, а также использование качественных расходных материалов (ирригационные растворы, вискоэластики, медикаменты, красители и др.) и интраокулярных линз. Во-вторых, принципиальное значение имеет медикаментозное сопровождение послеоперационного периода, в стандартную схему которого включено местное применение антибиотиков, стероидных и нестероидных противовоспалительных средств (НПВС).
Антибактериальная профилактика при факоэмульсификации
Особенности факоэмульсификации – использование большого количества жидкости, неоднократное проникновение в переднюю камеру, введение внутрикамерных анестетиков, вискоэластиков, интраокулярных линз. Соответственно, бактериальная контаминация влаги передней камеры может возникать на различных этапах операции [1–3]. В связи с этим правила асептики и антисептики с адекватной подготовкой операционного поля имеют принципиальное значение. Одноразовое белье, обработка рук хирурга, обработка операционного поля больного 5–10%-ным раствором повидон-йода (препарат Бетадин) и 0,05%-ным раствором хлоргексидина, конъюнктивальной полости – 0,05%-ным раствором антисептика Витабакт, ограничение операционного поля специальными стерильными салфетками с изоляцией ресниц – эти меры позволяют значительно снизить риск развития воспалительных осложнений. Это важно, так как наиболее частой причиной развития инфекционных осложнений являются экзогенные факторы – микрофлора век и конъюнктивы. По данным литературы, при отсутствии профилактической санации конъюнктивального мешка до операции потенциальные возбудители инфекции, преимущественно грамположительные кокки, обнаруживаются более чем в 50% случаев, а на коже век – в 100% случаев [4–7].
Поскольку наиболее частой причиной послеоперационных эндофтальмитов являются экзогенные факторы, одним из направлений профилактики инфекции является сокращение бактериальной микрофлоры на поверхности глазного яблока [8].
Появление в 80-х годах прошлого века антибактериальных препаратов фторхинолонового ряда (2-е поколение) по праву считается революцией в профилактике и терапии бактериальных воспалительных заболеваний не только глаза, но и организма в целом. Основными аргументами для активного использования современных фторхинолонов (Флоксал фирмы Bausch & Lomb, Офтаквикс фирмы Santen) с целью профилактики послеоперационных осложнений в офтальмологии являются их активность в отношении как грамположительных, так и грамотрицательных бактерий, более оптимизированная фармакокинетика, а также их высокая проникающая способность во влагу передней камеры глаза [9–14]. В 2011 г. в России зарегистрированы фторхинолоны 4-го поколения (Вигамокс фирмы Alcon), разработчики которых посчитали, что накопление в общей практике определенной резистентности к 3-му поколению фторхинолонов может стать причиной неэффективного лечения после офтальмологических операций [15].
Данные, полученные в рамках многоцентрового исследования, проведенного в 2003–2006 гг. с участием около 16 000 пациентов, послужили основанием для включения фторхинолонов в рекомендованную Европейским обществом катарактальных и рефракционных хирургов (European Society of Cataract and Refractive Surgeons, ESCRS) схему профилактики инфекционных осложнений у пациентов, перенесших факоэмульсификацию катаракты [16]. Так, одна из возможных схем предполагает назначение антибиотика группы фторхинолонов за 2 дня до операции 4 раза в день, непосредственно перед операцией за 60 и 30 минут, в конце ее и в течение 7 дней после операции; это позволяет достичь концентрации антибиотика в роговице и влаге передней камеры, превосходящей минимальную ингибирующую концентрацию – МIC 90 – для наиболее частых возбудителей послеоперационного эндофтальмита. Кроме того, возможна экспресс-подготовка, когда многократные инстилляции антибиотиков проводятся в течение 2 часов непосредственно перед операцией [17].
Противовоспалительная профилактика при факоэмульсификации
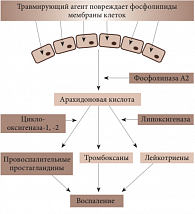
Послеоперационное воспаление считается одним из основных осложнений хирургии катаракты. Оно удлиняет срок реабилитации пациента и снижает функциональный результат лечения. Частота послеоперационного воспаления после факоэмульсификации составляет 2–5%. Основной действующей силой, приводящей к биологическим реакциям воспаления, являются так называемые медиаторы воспаления. Они образуются из фосфолипидов, входящих в состав мембран погибших в результате повреждающего действия клеток. Под действием фосфолипазы фосфолипиды расщепляются до арахидоновой кислоты, которая, в свою очередь, подвергается действию циклооксигеназы (в итоге образуются простагландины) и липоксигеназы (с образованием лейкотриенов). На рисунке 2 схематично представлен запуск синтеза воспалительных медиаторов, основными из которых по праву считают простагландины.
В соответствии с патофизиологией воспалительной реакции основным приложением медикаментозной профилактики и лечения должно быть блокирование синтеза медиаторов воспаления [18].
Стероидные препараты
В офтальмологической практике применяется 0,1%-ный раствор дексаметазона (самый эффективный препарат по силе глюкокортикоидной активности по сравнению с преднизолоном и кортизоном). Исторически стероидные препараты были первыми средствами противовоспалительной направленности в офтальмохирургии. Согласно теории Ганса Селье (Hans Selye), стресс – это неспецифический ответ организма на любое предъявляемое ему требование. При исследовании стрессовой реакции (в том числе и на хирургическую травму) отмечена некоторая эндокринная перестройка организма с увеличением коры надпочечников и увеличением уровня глюкокортикоидов.
Основные эффекты стероидов – иммуносупрессивный, противоэкссудативный, антипролиферативный – реализуются через мощную ингибицию синтеза всех медиаторов воспаления. В результате угнетения фермента фосфолипазы А2 и, следовательно, всей цепочки синтеза медиаторов воспаления происходит:
- стабилизация капилляров и уменьшение отека;
- стабилизация нейтрофилов и тучных клеток;
- уменьшение пролиферации фибробластами;
- уменьшение миграции лейкоцитов и макрофагов;
- уменьшение хемотаксиса лейкоцитов;
- дезактивация системы комплемента;
- вазоконстрикция.
Учитывая механизм действия, стероиды долгое время считались препаратом № 1 в подавлении воспалительной реакции на механическое повреждение с обширной травмой глазных тканей, что нашло свое выражение в схемах послеоперационного ведения в эру механической экстракции катаракты и больших разрезов (местное и общее применение) [19].
В настоящее время основная форма применения стероидных препаратов – инстилляции глазных капель (дексаметазон 0,1%), которые начинаются с первого дня после операции до 4–6 раз в день и продолжаются далее по различным схемам. Стероиды наиболее эффективны в профилактике и лечении послеоперационного ирита, иридоциклита, однако в профилактике макулярного отека их применение сдерживается риском повышения внутриглазного давления при длительном применении. Современная тенденция в использовании стероидов предполагает сокращение времени инстилляции с ранее традиционных 6 недель (по убывающей с 6 до 1 раза по неделе) до 2 недель (по 4 раза в день без необходимости убывающей схемы). Длительность приема препарата зависит от риска развития побочных эффектов и исходного состояния гидродинамики глаза, степени хирургической травмы и наличия сопутствующей патологии роговицы (перенесенные кератиты, рубцы).
На фоне применения глюкокортикоидов возникают следующие побочные эффекты:
- повышение внутриглазного давления (до 20% пациентов при инстилляции в течение недели). Данное обстоятельство диктует пересмотр длительных схем стероидной терапии после факоэмульсификации на фоне глаукомы или отказ от них в пользу нестероидных капель;
- снижение репаративных процессов. Этот побочный эффект необходимо учитывать при одновременной факоэмульсификации и кераторефракционных операциях, а также при arcus senilis и посттравматических рубцах [20];
- проинфекционный эффект за счет иммуносупрессии. Превышение в несколько раз длительности применения стероидов по сравнению с антибиотиками создает потенциально опасную ситуацию.
Современная факоэмульсификация представляет собой операцию практически без хирургического стресса, поэтому обоснованность активного и продолжительного применения стероидов становится все менее очевидной, тем более при наличии эффективной альтернативы – нестероидных противовоспалительных средств.
Нестероидные противовоспалительные средства
Из НПВС в отечественной офтальмологической практике применяются препараты в виде растворов для инстилляций – Индоколлир (действующее вещество индометацин), Наклоф (действующее вещество диклофенак). Главным и общим элементом механизма действия НПВС является угнетение синтеза простагландинов из арахидоновой кислоты путем ингибирования фермента циклооксигеназы (простагландин-синтетазы).
Эти препараты обратимо ингибируют циклооксигеназу и таким образом снижают биосинтез простагландинов и тромбоксана. В последние годы установлено, что существуют, по крайней мере, две разновидности циклооксигеназы – 1-го и 2-го типа (ЦОГ-1 и ЦОГ-2). ЦОГ-1 образуется в обычных условиях и регулирует в организме образование простагландинов, обеспечивающих гастропротективное действие, способность тромбоцитов к агрегации в системе свертывания крови и контролирующих просвет сосудов и кровоток в почках. ЦОГ-2 является главным фактором, индуцирующим процесс воспаления. Большинство НПВС ингибируют обе циклооксигеназы. Противовоспалительный эффект этих препаратов обусловлен угнетением ЦОГ-2. Одновременное угнетение ЦОГ-1 приводит к развитию побочных эффектов со стороны желудочно-кишечного тракта, вызывая образование язв, кровотечения и, кроме того, нарушение функции почек и агрегации тромбоцитов. Выраженной селективностью по отношению к ЦОГ-1 обладает индометацин, умеренной – диклофенак (классификация НПВС по селективности в отношении различных форм циклооксигеназы согласно Drugs Therapy Perspectives, 2000 [21]).
НПВС подавляют преимущественно фазу экссудации. Наиболее мощные препараты – индометацин, диклофенак – воздействуют также на фазу пролиферации (уменьшая синтез коллагена и связанное с этим склерозирование тканей), но слабее, чем на экссудативную фазу. На фазу альтерации НПВС практически не влияют. По противовоспалительной активности все НПВС уступают стероидам, которые, ингибируя фермент фосфолипазу А2, тормозят метаболизм фосфолипидов и нарушают образование как простагландинов, так и лейкотриенов, также являющихся важнейшими медиаторами воспаления.
НПВС эффективны в профилактике и лечении воспалительных осложнений в переднем (ириты, иридоциклиты) и заднем (макулярный отек) отрезке глаза [22–26].
Местные побочные эффекты от применения НПВС редки и могут проявляться в поверхностной мелкоточечной эпителиопатии роговицы, которая уменьшается при снижении дозы и назначении протекторов роговицы. Редки и аллергические реакции. Системные осложнения, характерные для пероральных НПВС (желудочно-кишечные кровотечения, нарушение свертываемости крови), при инстилляциях НПВС не отмечаются.
С точки зрения применения в реальной клинической практике наибольший интерес представляет Индоколлир (фирма Bausch & Lomb), который обладает некоторыми преимуществами:
- эффективен в поддержании мидриаза;
- синергичен со стероидами;
- обладает хорошей переносимостью;
- на фоне его применения малый риск роговичных осложнений;
- имеет выраженный анальгезирующий эффект.
Возможные схемы комбинации стероидных и нестероидных противовоспалительных препаратов в послеоперационном периоде при факоэмульсификации
Монотерапия НПВС
Современная факоэмульсификация может считаться операцией с минимальным хирургическим стрессом, поэтому в случаях «чистой» (англ. virgin) катаракты возможна монотерапия НПВС. Как правило, НПВС в виде монотерапии назначаются 4 раза в день за два дня до операции, в день операции и после операции в течение 4–6 недель. Обязательно проведение антибактериальной профилактики по описанной выше схеме (до, во время и после операции).
Монотерапия стероидами
Несмотря на большую противовоспалительную активность, изолированное использование стероидных препаратов не может обеспечить полную профилактику воспалительных осложнений (особенно макулярного отека). Это обусловлено тем, что побочные эффекты стероидной терапии (проинфекционный эффект, развитие вторичной гипертензии) ограничивают безопасную длительность их применения сроком не более 4 недель. А в случаях с сопутствующей глаукомой длительность применения стероидов не должна превышать 2 недель. Использование комбинированных лекарственных средств, которые включают антибактериальный и стероидный препараты, представляется вполне перспективным с учетом различных сроков обоснованного применения в послеоперационном периоде антибиотиков (до 1–2 недель), глюкокортикостероидов (до 3–4 недель) и риском формирования при постепенной отмене возможной резистентности к возбудителям инфекции [17, 27].
Комбинация стероидов и НПВС
Сочетание стероидов и НПВС – наилучший вариант терапии стандартного послеоперационного периода [27, 28]. Суммация противовоспалительного эффекта, возможность ограничить до минимального срок применения стероидов и продлить до необходимого применение НПВС позволяют обеспечить адекватную курацию больного после факоэмульсификации, а в сочетании с антибактериальной профилактикой инфекционного воспаления – максимально обеспечить неосложненное послеоперационное течение. Итоговая схема инстилляций при стандартном течении послеоперационного периода выглядит следующим образом: за 2 дня до операции – НПВС 4 раза в день; в день операции – НПВС 4 раза в день; после операции – НПВС 4 раза в день в течение 4–6 недель, стероиды 4 раза в день в течение 2 недель.
Таким образом, для местного применения в эффективной профилактике послеоперационных осложнений факоэмульсификации показаны антибиотики – фторхинолоны (офлоксацин, левофлоксацин, моксифлоксацин), стероиды (дексаметазон), нестероиды (индометацин (препарат Индоколлир), диклофенак). Мы рекомендуем следующую схему эффективной фармакотерапии стандартного течения послеоперационного периода факоэмульсификации (все инстилляции 4 раза в день):
- за 2 дня до операции – НПВС (Индоколлир), антибиотики (фторхинолоны);
- в день операции – НПВС (Индоколлир), антибиотики (фторхинолоны);
- после операции – стероиды (1–2 недели), антибиотики (фторхинолоны) (1 неделя), НПВС (Индоколлир) (4–6 недель).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.