Эффективность системной анальгетической терапии в комплексном лечении острого среднего отита
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. 50 пациентов с различными вариантами ОСО в возрасте 18–69 лет (средний возраст – 28,0 ± 9,76 года) были разделены поровну на две группы. Пациенты первой группы дополнительно к стандартной терапии получали нимесулид (Найз®) по одной таблетке два раза в день. Пациенты второй группы не получали этого препарата. Пациенты обеих групп были сопоставимы по половозрастным и анамнестическим характеристикам.
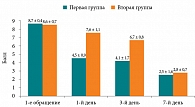
Результаты. На первые и третьи сутки лечения у пациентов первой группы болевой синдром значительно снизился – на 48,2 и 52,8% соответственно. Болевой синдром у пациентов первой группы был статистически достоверно ниже (p < 0,05) на первые и третьи сутки, чем у пациентов второй группы. На седьмой день от начала лечения болевой синдром был минимальный в обеих группах (p > 0,05).
По окончании курса терапии в группах отмечалось улучшение по всем восьми шкалам физического и психологического компонентов здоровья. Такие параметры, как роль физических проблем в ограничении жизнедеятельности, физическая боль, жизненная активность, на первые и третьи сутки от начала консервативного лечения были достоверно выше (p < 0,05) в группе пациентов, применявших системные анальгетики.
Выводы. При использовании нимесулида (Найз®) в комплексной терапии ОСО отмечалось более быстрое наступление анальгезирующего эффекта. Препарат способствовал более быстрому регрессу нарушений ночного сна, интенсивности болевого синдрома, а также восстановлению дневной активности.
Материал и методы. 50 пациентов с различными вариантами ОСО в возрасте 18–69 лет (средний возраст – 28,0 ± 9,76 года) были разделены поровну на две группы. Пациенты первой группы дополнительно к стандартной терапии получали нимесулид (Найз®) по одной таблетке два раза в день. Пациенты второй группы не получали этого препарата. Пациенты обеих групп были сопоставимы по половозрастным и анамнестическим характеристикам.
Результаты. На первые и третьи сутки лечения у пациентов первой группы болевой синдром значительно снизился – на 48,2 и 52,8% соответственно. Болевой синдром у пациентов первой группы был статистически достоверно ниже (p < 0,05) на первые и третьи сутки, чем у пациентов второй группы. На седьмой день от начала лечения болевой синдром был минимальный в обеих группах (p > 0,05).
По окончании курса терапии в группах отмечалось улучшение по всем восьми шкалам физического и психологического компонентов здоровья. Такие параметры, как роль физических проблем в ограничении жизнедеятельности, физическая боль, жизненная активность, на первые и третьи сутки от начала консервативного лечения были достоверно выше (p < 0,05) в группе пациентов, применявших системные анальгетики.
Выводы. При использовании нимесулида (Найз®) в комплексной терапии ОСО отмечалось более быстрое наступление анальгезирующего эффекта. Препарат способствовал более быстрому регрессу нарушений ночного сна, интенсивности болевого синдрома, а также восстановлению дневной активности.

Острый средний отит (ОСО) является одним из наиболее частых инфекционных заболеваний и поводов для обращения к врачу, особенно в раннем младенчестве и детском возрасте. ОСО – наиболее распространенный диагноз в мире. В возрасте до двух лет 70% детей хотя бы раз переносят эпизод ОСО [1, 2].
Оталгия, или боль, локализующаяся в ухе, считается наиболее распространенным симптомом, по поводу которого пациенты с ОСО обращаются к оториноларингологам, врачам общей практики и врачам скорой помощи. Примерно 4% обращений к врачу общей практики обусловлены исключительно ушной болью [3].
В зависимости от этиологического фактора оталгия подразделяется на первичную и вторичную. К первичной относят боль в ухе вследствие стимуляции ноцицепторных волокон. Примером может служить сильное механическое воздействие – травма, серная пробка или инородное тело. Однако чаще ноцицепторы активируются цепочкой клеточных и тканевых реакций, приводящих к высвобождению одного или более веществ (в частности, простагландинов, брадикинина, серотонина), которые затем служат непосредственными стимулами, возбуждающими и сенситизирующими ноцицепторы. О вторичной оталгии говорят, когда по ощущениям источником боли является ухо, а на самом деле источник «внеушной». Речь идет о воспалительных и инфекционных заболеваниях зубов, заболеваниях височно-нижнечелюстного сустава, невралгии тройничного нерва, отологических новообразованиях и опухолях головы и шеи, синдроме Игла, височном артериите. Первичная оталгия чаще встречается у детей, вторичная – у взрослых [3].
ОСО является наиболее частой причиной назначения антибиотиков у детей и взрослых. Однако антибиотики не оказывают быстрого эффекта при болевом синдроме, лишь незначительно влияют на него в первые несколько дней у пациентов с ОСО [4]. Анальгетики применяют с большой осторожностью, особенно в детском возрасте, из-за риска побочных эффектов или отсутствия четких инструкций по применению консультирующим врачом. Это нередко приводит к неоптимальному лечению ОСО, в частности болевого синдрома, а также к необходимости повторной консультации и назначения антибиотиков в будущем [5].
Нестероидные противовоспалительные препараты (НПВП) представлены разными классами химических соединений, которые различаются механизмом действия, фармакокинетическими и фармакодинамическими характеристиками. Одним из популярных и хорошо изученных НПВП считается нимесулид (Найз®). В России, согласно отчетам о продажах, он занимает одно из лидирующих мест [6].
Преимущества нимесулида (Найз®) обусловлены особенностями производства, рядом фармакокинетических и фармакодинамических характеристик. Важнейшая из них – быстрое достижение пиковой концентрации в крови вследствие хорошего всасывания из желудочно-кишечного тракта и проникновения в синовиальную жидкость [6]. Так, 55–80% максимальной концентрации достигается через 30 минут после перорального приема, анальгетический эффект регистрируется в первые 15–20 минут и сохраняется в течение 10–12 часов [7]. Быстрое всасывание препарата Найз® в желудочно-кишечном тракте прежде всего обеспечивается эффективной дезинтеграцией действующего вещества. При производстве препарата Найз® используется комбинация дезинтегрантов – крахмала и натрия крахмала гликолята (супердезинтегрант), которые обеспечивают хороший капиллярный эффект, быстрое проникновение жидкости внутрь таблетки, а также высокую степень набухания [8].
Другим важным показателем фармакокинетики нимесулида является период полувыведения – в среднем два с половиной часа. Чем меньше период полувыведения, тем безопаснее НПВП и быстрее ресинтез циклооксигеназы 1. С этим может быть связана не только низкая частота НПВП-гастропатий на фоне перорального приема препарата Найз®, но и высокая приверженность препарату врачей и пациентов [9].
По химической структуре нимесулид относится к производным N-(4-нитро-2-феноксифенил) метансульфонамида. Карбоксильная группа в молекуле препарата заменена сульфонанилидом, благодаря чему препарат оказывает протективный эффект на слизистую оболочку желудочно-кишечного тракта [6].
Нимесулид – единственный НПВП, который не является субстратом для окисления системой CYP2C9. Это подразумевает более низкий риск лекарственного взаимодействия по сравнению с другими препаратами группы (в частности, целекоксибом, лорноксикамом, диклофенаком, ибупрофеном, напроксеном, кетопрофеном, пироксикамом, мелоксикамом). Кроме того, нимесулид (Найз®) можно рассматривать в качестве альтернативного препарата при возникновении аллергической реакции на другие НПВП. Как минимум в двух исследованиях перевод пациентов на нимесулид не ассоциировался с повторным развитием реакции гиперчувствительности [10, 11].
Цель исследования – повысить эффективность лечения больных ОСО с оталгией с помощью системных анальгетиков.
Материал и методы
В исследовании участвовали 50 пациентов с различными вариантами ОСО в возрасте 18–69 лет (средний возраст – 28,0 ± 9,76 года), обратившихся за консультативной помощью в амбулаторный кабинет оториноларинголога Клинического медицинского центра им. Н.А. Семашко Российского университета медицины в 2022–2023 гг.
Всем пациентам проводились стандартное оториноларингологическое обследование, а также эндоскопическое исследование полости носа, околоносовых пазух, носоглотки, отоэндоскопия, аудиометрия, тимпанометрия.
Болевой синдром оценивали по визуальной аналоговой шкале (ВАШ), а качество жизни – по опроснику SF-36 (Shot-Form Health Survey) [6].
Всем пациентам назначали консервативную терапию в соответствии с клиническими рекомендациями «Острый средний отит» [12]: системные антибиотики, НПВП в таблетированной форме в течение десяти дней, деконгестанты среднего или длительного действия интраназально пять дней.
Критериями включения в исследование служили обращение в первые два дня от начала развития болевого синдрома, неиспользование системных антибактериальных, системных и местных анальгетических препаратов, доперфоративная стадия ОСО.
Критерии исключения: заболевания, приводящие к вторичной оталгии (воспалительные и инфекционные заболевания зубов, заболевания височно-нижнечелюстного сустава, невралгия тройничного нерва, отологические новообразования и опухоли головы и шеи, синдром Игла, височный артериит), возраст до 12 лет, острый гнойный средний отит.
В зависимости от использования системных НПВП в консервативной терапии пациенты были разделены на две группы. Первую группу составили 25 пациентов, получавших дополнительно к стандартной терапии НПВП нимесулид (Найз®) по одной таблетке два раза в день. Во вторую группу вошли 25 пациентов с ОСО, не получавших НПВП. Пациенты обеих групп были сопоставимы по половозрастным и анамнестическим характеристикам (p > 0,05).
Эффективность лечения пациентов с ОСО анализировали на первые, третьи и седьмые сутки от начала консервативного лечения по таким критериям, как удовлетворенность терапией и клинические результаты.
Удовлетворенность пациентов оценивали исходя из интенсивности болевого синдрома на основании ВАШ в день обращения, на первые, третьи и седьмые сутки от начала консервативного лечения, а также с помощью SF-36.
SF-36 – анкета, состоящая из вопросов, ответы на которые позволяют определить общее состояние, психическое и физическое здоровье, уровень социальной адаптации. Опросник помогает оценить качество жизни по следующим показателям: физическая активность (PF – physical functioning), роль физических проблем в ограничении жизнедеятельности (RP – role phisical), физическая боль (ВР – bodily pain), общее состояние здоровья (GH – general health), роль эмоциональных проблем в ограничении жизнедеятельности (RE – role emotional), жизненная активность (VT – vitality), социальная активность (SF – social functioning) и психическое здоровье (МН – mental health). Максимальной удовлетворенности соответствуют 100 баллов. Расчет баллов качества жизни по каждой из восьми трансформированных шкал осуществляется по формуле:
трансформированная шкала = [∑ - Min] × 100, [Max - Min],
где
∑ – суммарный счет шкалы;
Min – минимально возможное значение шкалы;
Max – максимально возможное значение шкалы.
Далее рассчитываются средние значения и стандартные отклонения по каждой шкале [13].
Клинические результаты оценивали по динамике регресса клинических симптомов на основании данных эндоскопии полости носа, околоносовых пазух и носоглотки, отоэндоскопии, аудиометрии, тимпанометрии в день обращения, на первые, третьи и седьмые сутки от начала консервативного лечения.
Уровень снижения слуха определяли по результатам тональной аудиометрии согласно международной классификации: 1-я степень – 26–40 дБ, 2-я степень – 41–55 дБ, 3-я степень – 56–70 дБ, 4-я степень – 71–90 дБ. Для интерпретации результатов тимпанометрии использовали систему классификации Jerger [14].
Результаты и обсуждение
До лечения основными жалобами у всех больных были боль в ухе, снижение слуха, чувство заложенности в ухе. При эндоскопическом исследовании полости носа, околоносовых пазух, носоглотки отмечались выраженный отек слизистой оболочки полости носа, отек в области глоточных устьев слуховых труб. При отоэндоскопии барабанная перепонка была:
- втянутой (стадия острого тубоотита) – 7 (14%) пациентов;
- гиперемированной, утолщенной (стадия катарального воспаления в среднем ухе) – 21 (42%);
- мутной, выбухающей (стадия серозного экссудата в среднем ухе) – 9 (18%);
- гиперемированной, утолщенной, выбухающей или желтоватого цвета, с уровнем жидкости (доперфоративная стадия острого гнойного воспаления в среднем ухе) – 9 (18%) больных.
Кроме того, геморрагические буллы на стенках наружного слухового прохода и барабанной перепонки (острый буллезный средний отит) имели место у 4 (8%) пациентов.
До лечения тугоухость 1-й степени зафиксирована у 19 (76%) пациентов первой группы и 2 (80%) – второй, 2-й степени – у 6 (24%) и 5 (20%) больных соответственно. В 64% случаев зарегистрирована тимпанограмма типа C, в остальных случаях – типа В.
Согласно результатам тестирования, у всех пациентов в первый день обращения отмечался выраженный болевой синдром. На первые и третьи сутки от начала лечения у пациентов первой группы болевой синдром значительно снизился – на 48,2 и 52,8% соответственно. Болевой синдром у пациентов первой группы был статистически достоверно ниже (p < 0,05) на первые и третьи сутки, чем у пациентов второй группы. На седьмой день лечения болевой синдром был минимальный в обеих группах (p > 0,05) (рис. 1).
Сравнительная оценка средних показателей восьми трансформированных шкал SF-36 у пациентов в день обращения, на первые, третьи и седьмые сутки от начала консервативного лечения представлена в таблице.
Параметры качества жизни у пациентов обследованных групп до начала лечения достоверно не различались (p > 0,05). По окончании курса терапии в группах отмечалось улучшение по всем восьми шкалам физического и психологического компонентов здоровья. Такие параметры, как роль физических проблем в ограничении жизнедеятельности (отражает степень ограничения выполнения обычных действий вследствие нарушений ночного сна), физическая боль (отражает интенсивность болевого синдрома), жизненная активность (оценивает дневную активность), на первые и третьи сутки от начала консервативного лечения были достоверно выше (p < 0,05) в группе пациентов, применявших системные анальгетики.
На первые сутки пациенты обеих групп указали на субъективное улучшение слуха, чувство заложенности ушей практически не изменилось.
К третьим суткам ощущение заложенности в ухе отмечали 13 пациентов первой группы и 17 пациентов второй группы. Проходимость слуховой трубы восстановилась полностью у 11 (22%) пациентов – тимпанометрия типа А, 23 (46%) – типа С, 16 (32%) – типа В. Аудиометрически: тугоухость 1-й степени определялась у 15 (60%) пациентов первой группы и 18 (72%) – второй, 2-й степени – у 3 (12%) и 3 (12%) больных соответственно. Слух восстановился до нормы у 7 (28%) пациентов первой группы, 4 (16%) пациентов – второй.
На седьмой день консервативного лечения костно-воздушный интервал был перекрыт у 22 (88%) пациентов первой группы и 21 (84%) пациента – второй. Тугоухость 1-й степени оставалась у 3 (12%) и 4 (16%) пациентов соответственно. На тимпанограммах регистрировался тип А у 41 больного, тип С – у 9 пациентов.
При эндоскопическом исследовании полости носа и глоточного устья слуховой трубы определялось значительное уменьшение отека к третьим суткам консервативного лечения.
Достоверно значимых различий в динамике регресса клинических симптомов у пациентов двух групп не выявлено.
Клинический случай
Пациент З., 34 года, обратился за консультативной помощью в амбулаторный кабинет оториноларинголога Клинического медицинского центра Российского университета медицины с жалобами на острую боль и снижение слуха, чувство заложенности левого уха.
Анамнез заболевания: продолжительность указанных симптомов – около суток, появились после переохлаждения. Лечился самостоятельно – согревающий спиртовой компресс в левое ухо, без эффекта. В связи с усиливающимися жалобами обратился к оториноларингологу.
Лор-статус:
- нос: форма наружного носа не изменена. Эндоскопия: преддверие носа свободное, перегородка носа искривлена влево. Слизистая полости носа розовая. В носовых ходах отделяемого нет. Нижние носовые раковины увеличены с двух сторон, после анемизации сокращаются хорошо;
- носоглотка: увеличены задние концы нижних носовых раковин;
- ротоглотка: небные дужки контурируются, розового цвета. Небные миндалины не увеличены. Задняя стенка глотки влажная, розового цвета, гранулы на задней стенке глотки. Глоточный рефлекс сохранен;
- гортаноглотка и гортань: форма гортани правильная, гортань пассивно подвижна. Эндоскопия: язычная миндалина не увеличена. В валлекулах отделяемого нет. Грушевидные синусы свободные. Надгортанник правильной формы, слизистая оболочка гортани розового цвета. Вестибулярные складки не изменены. Голосовые складки белого цвета, при фонации подвижные, полностью смыкаются, голосовая щель широкая, дыхание свободное. Подскладочное пространство свободное;
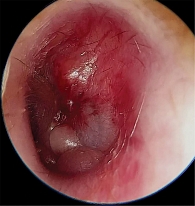
- уши: AD – ушная раковина правильной формы, пальпация сосцевидного отростка, ушной раковины, козелка безболезненна. Наружный слуховой проход широкий, свободный, отделяемого нет. Барабанная перепонка серая, опознавательные знаки четкие, перфорации нет, шепотная речь – 6 м. AS – ушная раковина правильной формы, пальпация сосцевидного отростка, ушной раковины, козелка безболезненна. Наружный слуховой проход сужен, содержит геморрагическую буллу в области нижней стенки наружного слухового прохода. Барабанная перепонка гиперемирована, отечна, на барабанной перепонке в задненижнем квадранте геморрагическая булла, шепотная речь – 3 м (рис. 2). Аудиометрия – снижение слуха на левое ухо по типу нарушения звукопроведения 1–2-й степени. Тимпанометрия – тип B слева.
Лечение: назначены системные антибиотики в таблетированной форме в течение десяти дней, деконгестанты среднего действия интраназально пять дней, НПВП Найз® (действующее вещество – нимесулид).
Болевой синдром – 9 баллов по ВАШ.
Показатели качества жизни в баллах: PF – 51, RP – 38, ВР – 31, GH – 65, VT – 60, SF – 60, RE – 68, МН – 72.
В течение первого дня терапии пациент отметил явное снижение болевого синдрома, субъективное улучшение слуха. При этом чувство заложенности практически не изменилось, равно как риноскопическая и отоскопическая картина, аудиометрия и тимпанометрия.
Болевой синдром – 6 баллов по ВАШ.
Показатели качества жизни в баллах: PF – 75, RP – 55, ВР – 79, GH – 77, VT – 79, SF – 71, RE – 78, МН – 80.
На третий день при эндоскопическом исследовании полости носа и глоточного устья слуховой трубы определялось значительное уменьшение отека. Результаты отоэндоскопии показали утолщенные участки кожи на месте вскрывшихся булл в области нижней стенки наружного слухового прохода и задненижнем квадранте. Барабанная перепонка гиперемирована, отечна. Аудиометрия – улучшение порогов слышимости на левое ухо до 10 дБ, нарушение звукопроведения 1-й степени. Тимпанометрия – тип С слева.
Болевой синдром практически не беспокоил – 2 балла по ВАШ, отмечены дальнейшее уменьшение заложенности и улучшение слуха.
Показатели качества жизни в баллах: PF – 84, RP – 75, ВР – 89, GH – 81, VT – 87, SF – 79, RE – 82, МН – 84.
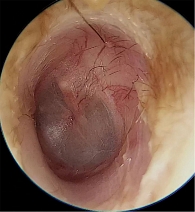
При осмотре на седьмой день от начала консервативного лечения жалоб пациент не предъявлял. При эндоскопическом исследовании полости носа и глоточного устья слуховой трубы отека слизистой оболочки не определялось. Данные отоэндоскопии: ширина просвета наружного слухового прохода не нарушена, барабанная перепонка серая, опознавательные знаки четкие, перфораций и булл нет (рис. 3). Аудиометрия – норма. Тимпанометрия – тип А слева.
Болевой синдром – 0 баллов по ВАШ.
Показатели качества жизни в баллах: PF – 97, RP – 95, ВР – 98, GH – 84, VT – 92, SF – 87, RE – 85, МН – 89.
Выводы
На основании результатов исследования были сделаны следующие выводы.
- При использовании нимесулида (Найз®) в комплексной терапии острого среднего отита отмечается более быстрое наступление анальгезирующего эффекта.
- У пациентов с доперфоративными формами острого среднего отита препарат Найз® благодаря противовоспалительному, анальгезирующему действию повышает эффективность терапии, способствуя более быстрому регрессу нарушений ночного сна, интенсивности болевого синдрома, а также восстановлению дневной активности.
Статья подготовлена при поддержке компании ООО «Др. Редди'с Лабораторис».
A.Yu. Ovchinnikov, PhD, Prof., M.A. Edge, PhD, Prof., A.Yu. Shcherbakov, PhD
Russian University of Medicine
Contact person: Andrey Yu. Ovchinnikov, lorent1@mail.ru
Purpose is to increase the effectiveness of treatment of patients with acute otitis media (AOM) with otalgia using systemic analgesics.
Material and methods. 50 patients with various AOM variants aged 18–69 years (average age – 28.0 ± 9.76 years) were divided equally into two groups. In addition to standard therapy, patients of the first group received nimesulide (Nise®) one tablet twice a day. Patients of the second group did not receive this drug. Patients of both groups were comparable in gender, age and anamnestic characteristics.
Results. On the first and third days of treatment, the pain syndrome in patients of the first group decreased significantly – by 48.2 and 52.8%, respectively. Pain syndrome in patients of the first group was statistically significantly lower (p < 0.05) on the first and third days than in patients of the second group. On the seventh day after the start of treatment, the pain syndrome was minimal in both groups (p > 0.05).
At the end of the course of therapy, the groups showed improvement on all eight scales of physical and psychological components of health. Parameters such as the role of physical problems in disability, physical pain, and vital activity were significantly higher on the first and third days after the start of conservative treatment (p < 0.05) in the group of patients using systemic analgesics.
Conclusions. When using nimesulide (Nise®) in the complex therapy of AOM, a faster onset of analgesic effect was noted. The drug contributed to a more rapid regression of nighttime sleep disorders, the intensity of pain syndrome, as well as the restoration of daytime activity.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.