Интрадуктальное зондирование. Выбор пациентов
- Аннотация
- Статья
- Ссылки
- English
Предложенное S.L. Maskin интрадуктальное зондирование мейбомиевых желез представляет собой патогенетически обоснованный метод лечения, направленный на механическое устранение внутрипротоковой обструкции и восстановление эвакуации секрета. Согласно данным клинических исследований, процедура способствует улучшению стабильности слезной пленки, нормализации качественных характеристик мейбума и регрессу субъективной симптоматики, особенно при сочетании с противовоспалительной терапией или аппаратными методами воздействия.
Предложенное S.L. Maskin интрадуктальное зондирование мейбомиевых желез представляет собой патогенетически обоснованный метод лечения, направленный на механическое устранение внутрипротоковой обструкции и восстановление эвакуации секрета. Согласно данным клинических исследований, процедура способствует улучшению стабильности слезной пленки, нормализации качественных характеристик мейбума и регрессу субъективной симптоматики, особенно при сочетании с противовоспалительной терапией или аппаратными методами воздействия.


Введение
Дисфункция мейбомиевых желез (ДМЖ) – распространенное заболевание, характеризующееся нарушением состава, выработки и оттока липидной фракции слезы, что приводит к разрушению липидного слоя слезной пленки и увеличению скорости испарения влаги. Чрезмерное испарение вызывает нестабильность слезной пленки, ее высыхание, гиперосмолярность, воспаление и апоптоз клеток поверхности глаза. В результате развивается синдром сухого глаза (ССГ).
ДМЖ является ведущей этиологической причиной возникновения ССГ у миллионов людей в мире [1, 2]. По оценкам специалистов, ССГ встречается у 5–50% населения развитых стран мира. В некоторых популяциях данный показатель достигает 75%. ССГ существенно снижает качество жизни пациентов [3, 4].
Порочный круг: ДМЖ – сухой глаз – воспаление – ДМЖ
Пациенты с ССГ жалуются на сухость, ощущение песка в глазах, жжение, покалывание, светочувствительность, боль, зрительную усталость и нечеткость зрения. При клиническом осмотре у них обнаруживаются уменьшение количества слезной жидкости, нестабильность слезной пленки и повреждение поверхности глаза [3, 5, 6]. В тяжелых случаях не исключены повреждения роговицы и инфекции [7].
ССГ условно подразделяют на три типа:
- ССГ с дефицитом слезной жидкости (снижается секреция слезной жидкости);
- ССГ с повышенным испарением (происходит чрезмерное испарение слезной пленки);
- их сочетание [8].
На ранних стадиях ССГ может наблюдаться повышенное слезоотделение из-за сенсорной стимуляции компенсаторной секреторной реакции слезных желез. Однако считается, что по мере прогрессирования ССГ эта сенсорная реакция ослабевает [8].
По оценкам, ССГ с дефицитом слезной жидкости встречается только у 10–15% пациентов с ССГ; в подавляющем большинстве случаев (свыше 85%) ССГ имеет испарительный компонент [9, 10]. Дефицит муцинов в глазу также может играть роль в этиологии ССГ, хотя распространенность такого дефицита пока неясна [11–13].
Основная цель лечения ССГ, связанного с ДМЖ, – восстановить липидный слой слезной пленки и уменьшить испарение влаги, ослабив глазные симптомы. Традиционные методы лечения включают консервативную терапию препаратами искусственной слезы, гигиену век и физиотерапию, но далеко не всегда обеспечивают стойкую ремиссию. Современный подход к решению данной проблемы предполагает интрадуктальное зондирование мейбомиевых желез (МЖ), направленное на восстановление проходимости выводных протоков за счет механической обработки специальным тонким инструментом. Это позволяет активизировать секрецию мейбума, обеспечить стабильное увлажнение роговицы и нормализовать стабильность слезной пленки.
Материал и методы
Проведен анализ публикаций, посвященных интрадуктальному зондированию МЖ при рефрактерной обструктивной форме ДМЖ. В обзор включены клинические исследования, оценивающие эффективность и безопасность метода
Маленькие железы – большие проблемы
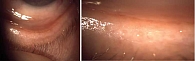
Мейбомиевы железы – видоизмененные голокринные сальные железы, расположенные в тарзальной пластинке века. Их отверстия находятся по краю век и выходят на поверхность глаза (рис. 1) [14]. МЖ выделяют липидно-белковую смесь (мейбум), которая выходит из их отверстий на краю века и попадает в слезную пленку при моргании. Средняя длина здоровых МЖ в верхнем веке составляет около 5,5 мм в центральной части века и около 3,5 мм в височной и носовой областях. В нижнем веке МЖ короче: их средняя длина достигает 2,0 мм в центральной части и около 1,8 мм в височной и носовой областях. Диаметр естественного отверстия МЖ около 100 мкм [15].
Изучение морфологии МЖ играет ключевую роль в понимании механизма их функционирования и выявления возможных отклонений. Основным методом, позволяющим детально визуализировать структуру желез, является мейбография.
Мейбография – специальная медицинская техника, основанная на получении высококачественных изображений МЖ с помощью цифровых камер высокого разрешения и специального освещения. Она позволяет детально изучить структуру желез, особенности расположения и размеры отдельных элементов, а также оценить функциональные характеристики.
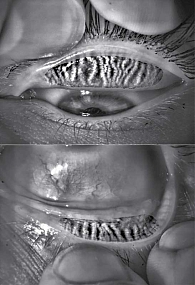
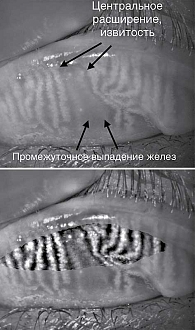
Функционирующие МЖ выделяют мейбум, который стабилизирует слезную пленку и предотвращает испарение влаги, защищая глаза от пересыхания (рис. 2) [14]. При ДМЖ этот защитный механизм нарушается из-за снижения количества и качества мейбума, вызванного уменьшением функциональной активности и атрофией желез (рис. 3) [14].
Наиболее распространенной формой ДМЖ является обструктивный тип, характеризующийся потерей функции МЖ вследствие закупорки их протоков (рис. 4). Следовательно, ключевым звеном патогенеза служит механическая обструкция, что определяет приоритетность мероприятий по восстановлению проходимости желез перед терапией сопутствующего воспаления [16].
К факторам, повышающим риск закупорки МЖ, относятся пожилой возраст, гормональные нарушения и внешние факторы, например ношение контактных линз, применение лекарственных средств и воздействие химических веществ [17]. В связи с широкой распространенностью ССГ особую актуальность приобретает разработка эффективных методов его лечения. Стандартная терапия ССГ предусматривает использование увлажняющих средств, гигиенический уход за веками, тепловые процедуры, массаж, а также местную или системную антибиотикотерапию [8]. Между тем у ряда пациентов после базового курса сохраняются клинические проявления, что требует более интенсивного терапевтического вмешательства [18].
Решение проблемы, о которой все говорят
С момента публикации в 2010 г. первой работы S.L. Maskin отмечается устойчивый рост научного интереса к интрадуктальному зондированию МЖ (meibomian gland probing, MGP). В ретроспективном исследовании автор сообщил о немедленном уменьшении выраженности симптомов после процедуры у 24 из 25 пациентов [19].
Исходя из гипотезы о том, что в основе симптомов синдрома сухого глаза лежат фиброзные изменения и сужение протоков МЖ, S.L. Maskin предположил, что механическое восстановление проходимости протоков может быть более эффективным по сравнению с традиционными методами терапии. Предложенная методика предусматривает введение стерильного зонда через устье железы в ее проток под местной анестезией. Цель вмешательства – расширение протока, снижение внутрижелезистого давления и восстановление физиологической секреции. Процедура выполняется амбулаторно под контролем щелевой лампы.
Первоначально использовался зонд длиной 2 мм: веко фиксировали в натянутом положении, а инструмент вводили перпендикулярно его краю. Критерием успешного зондирования считали появление мутного секрета из протока железы. В отсутствие эффекта применяли более длинный зонд (4 мм) [19].
Техника выполнения предполагает введение зонда в каждое устье перпендикулярно краю века движением, напоминающим направленный поступательный толчок. При прохождении через устье и дистальный отдел протока инструмент может встречать характерное сопротивление, описываемое как плотное, фиксированное и локализованное. Для его преодоления требуется дополнительное усилие. Момент устранения обструкции сопровождается своеобразным тактильным ощущением сброса давления, иногда сочетающимся с характерным звуковым феноменом (щелчок или скрежет), который может восприниматься как врачом, так и пациентом [20].
Возникающие при зондировании акустические и тактильные феномены (звук разрыва фиброзных спаек, изменение сопротивления тканей) рассматриваются как косвенные признаки выраженности, протяженности и локализации фиброзных изменений в просвете протока [21].
Так, наличие одиночной фиброзной бляшки, как правило, сопровождается одним эпизодом характерного сброса давления, тогда как при множественных фиброзных изменениях подобных эпизодов может быть несколько. В ряде случаев отмечается изменение интенсивности тактильного сопротивления по мере продвижения зонда по протоку, что может свидетельствовать о прогрессировании фиброзного процесса.
Акустические феномены, описываемые как щелчок или скрежет, возникают внезапно и имеют кратковременный характер, что указывает на локальное высвобождение участков фиброзной ткани. Иногда несколько подобных звуков регистрируются последовательно – в быстрой череде или с небольшой паузой – по мере продвижения инструмента в просвете протока.
Реже наблюдается умеренное противодавление, или так называемое мягкое сопротивление. В отличие от плотного фиксированного препятствия, оно не является жестким и преодолевается без значительных усилий. При этом зонд продвигается по каналу без выраженного дополнительного механического воздействия и без характерных акустических феноменов; возможно лишь ощущение трения при возвратно-поступательных движениях инструмента. Мягкое сопротивление, в отличие от плотного, не носит очагового или мультифокального характера.
В отдельных случаях отмечается полное отсутствие сопротивления («нулевое сопротивление»), при котором зонд свободно проходит через устье и проток без ощутимого трения [22].
Обсуждение
В ряде исследований показана эффективность интрадуктального зондирования МЖ при рефрактерной обструктивной форме ДМЖ. Так, N. Nakayama и соавт. при сравнительном анализе состояния МЖ до и после зондирования продемонстрировали улучшение липидных показателей и снижение вязкости мейбума во всех наблюдаемых случаях [23].
Дополнительные данные свидетельствуют о потенцировании терапевтического эффекта при комбинированном подходе. В частности, применение зондирования в сочетании с фторметолоном 0,1% сопровождалось более выраженным улучшением результатов бактериологического тестирования слезной жидкости и состояния МЖ по сравнению с монотерапией фторметолоном 0,1% [24]. Аналогичная тенденция отмечалась при комбинировании зондирования с традиционной терапией (теплые компрессы, массаж и гигиена век, прием омега-3-полиненасыщенных жирных кислот, пероральные антибиотики): клиническое улучшение наступало быстрее, чем при использовании только стандартного лечения [25].
В рандомизированном слепом исследовании X. Huang и соавт. предпринята попытка оптимизации лечения рефрактерной обструктивной ДМЖ путем включения интенсивного импульсного света (IPL) для усиления терапевтического эффекта. В исследование были включены 45 пациентов (90 глаз), разделенных на три группы:
- IPL – курс из трех процедур с интервалом три недели;
- MGP – однократное проведение зондирования МЖ;
- MGP + IPL – зондирование с последующим курсом IPL.
Оценка эффективности терапии включала субъективную степень выраженности симптомов сухости глаза, время разрыва слезной пленки, флуоресцеиновое окрашивание роговицы, характеристики мейбума и состояние краев век. Показатели регистрировали исходно, через три недели после завершения лечения в группах IPL и MGP + IPL, а также через три и 12 недель после проведения зондирования в группе MGP. Дополнительно через шесть месяцев во всех группах оценивали потребность пациентов в повторном лечении.
Согласно полученным результатам, во всех трех группах после проведенного лечения зафиксировано статистически значимое улучшение всех оцениваемых показателей (p < 0,01). При этом комбинированная терапия MGP + IPL продемонстрировала более высокую эффективность по сравнению с изолированным применением IPL или MGP. Преимущество комбинации выражалось в более быстром восстановлении после лечения, увеличении времени разрыва слезной пленки и уменьшении выраженности телеангиэктазий век (p < 0,05/3).
Кроме того, сочетание MGP + IPL оказалось более эффективным по сравнению с IPL в снижении болезненности век, а также превосходило MGP по влиянию на патологические изменения МЖ (p < 0,05/3).
Через шесть месяцев наблюдения в группе комбинированной терапии сохранялись лучшие показатели по сравнению с другими группами (p < 0,05/3). Более того, ни один пациент, получавший лечение MGP + IPL, не сообщил о необходимости повторной терапии, тогда как в группах IPL и MGP повторное лечение потребовалось 35,7 и 20% пациентов соответственно.
Таким образом, по сравнению с изолированным применением IPL или MGP комбинированный подход MGP + IPL продемонстрировал наилучшие результаты в отношении уменьшения клинических признаков и симптомов заболевания, обеспечивая более выраженный и длительный терапевтический эффект [26].
Ряд авторов указывает на необходимость повторного проведения интрадуктального зондирования МЖ (MGP). По данным пяти исследований, как минимум части пациентов выполнялось более одной процедуры в период между началом лечения и контрольным наблюдением [19, 27–30]. Так, в исследовании Z. Sik Sarman у 73,3% пациентов однократное зондирование не привело к достаточному облегчению симптомов, в связи с чем потребовалось повторное вмешательство; при этом четыре из 30 пациентов перенесли три и более процедур [29].
В целом частота нежелательных явлений в рассмотренных работах была низкой и преимущественно ограничивалась незначительными осложнениями. Чаще всего отмечались самопроизвольные интраоперационные кровотечения из тканей век и протоков МЖ [19, 24–26, 28, 29]. Несмотря на редкость, данные эпизоды свидетельствуют о наличии определенных рисков, связанных с процедурой. Вместе с тем в ряде исследований осложнений не зарегистрировано [23, 27, 30]. X. Ma и Y. Lu сообщали, что в отдельных случаях процедуру зондирования прекращали во избежание повреждения эпителия протоков [24]. На основании анализа интрадуктального положения зонда S.L. Maskin и S. Alluri пришли к выводу, что инструмент проходит по просвету железы, а техника его введения является безопасной [20].
Таким образом, вопрос о точной клинической эффективности MGP остается дискуссионным. Хотя большинство исследований демонстрирует улучшение состояния пациентов после зондирования, в ряде контролируемых работ не выявлено его убедительного преимущества по сравнению с группами контроля. При этом положительные результаты чаще регистрировались при комбинированном применении MGP с другими методами терапии, включая интенсивный импульсный свет (IPL), глюкокортикостероиды и традиционные схемы лечения.
Зондирование может рассматриваться как терапевтическая опция у пациентов с рефрактерным течением заболевания, не отвечающих на стандартную терапию [18]. В случае успешного вмешательства уменьшение выраженности симптомов возможно уже в течение первых суток после процедуры [24]. Вместе с тем MGP не всегда оказывается эффективным при однократном применении и нередко требует повторного проведения для достижения стойкого клинического эффекта [29].
Заключение
Интрадуктальное зондирование МЖ представляет собой патогенетически обоснованный метод лечения, направленный на механическое восстановление проходимости протоков, декомпрессию железистой ткани и устранение фиксированных фиброзных обструкций.
Клинические данные свидетельствуют о достоверном улучшении показателей стабильности слезной пленки (увеличение времени ее разрыва), нормализации характеристик мейбума и снижении выраженности субъективной симптоматики после проведения процедуры, особенно при ее сочетании с противовоспалительной терапией и аппаратными методами (IPL).
Эффективность метода зависит от стадии ДМЖ, степени мейбогланд-дропаута и выраженности фиброзных изменений. Значительная часть пациентов нуждается в повторном зондировании, что отражает хронический характер патологического процесса.
Профиль безопасности интрадуктального зондирования оценивается как благоприятный; осложнения носят преимущественно транзиторный характер и не сопровождаются стойким повреждением протокового эпителия при соблюдении техники выполнения.
MGP следует рассматривать как компонент персонализированной этапной терапии у пациентов с рефрактерной обструктивной формой ДМЖ. Для его полноценного внедрения в повседневную офтальмологическую практику необходимы дальнейшие исследования и накопление опыта.
Прозрачность финансовой деятельности. Никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
A.I. Fedorova, I.A. Loskutov, PhD
Moscow Regional Research and Clinical Institute
Contact person: Anastasiya I. Fedorova, FedorovaAnastasyaIg@yandex.ru
Dysfunction of the meibomian glands is the leading cause of the evaporative form of dry eye syndrome and is accompanied by obstruction of the excretory ducts, impaired secretion of meibum and secondary inflammation of the eye surface. Chronic ductal obstruction contributes to an increase in intra-ductal pressure, the formation of fibrous changes and progressive structural disorganization of the glands. The intraductal probing of the meibomian glands proposed by S.L. Maskin is a pathogenetically sound treatment method aimed at the mechanical elimination of intracurrent obstruction and the restoration of secretion evacuation. According to clinical studies, the procedure improves the stability of the tear film, normalizes the qualitative characteristics of meibum and regresses subjective symptoms, especially when combined with anti-inflammatory therapy or hardware methods of exposure.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.