Неинвазивная оценка состояния слезной пленки после кераторефракционной хирургии
- Аннотация
- Статья
- Ссылки
- English
Современная офтальмология располагает широким арсеналом диагностических методов, включая пробу Ширмера, тест Норна и неинвазивные методы, такие как оценка времени разрыва слезной пленки. Этот метод демонстрирует сопоставимую с инвазивными тестами точность и обеспечивает более комфортные условия для пациента. Наряду с этим исследователи обращают внимание на потенциальную взаимосвязь изменений слезной пленки и развития синдрома сухого глаза после кераторефракционной хирургии. Для получения объективной и полной клинической картины рекомендуется использовать комплексную диагностику, позволяющую оценить состояние слезной пленки с разных позиций и выявить скрытые патологические изменения, в частности снижение ее стабильности, нарушение липидного слоя, изменения осмолярности, микровоспаление, уменьшение плотности бокаловидных клеток и ухудшение регенерации эпителия роговицы. Применение комбинированных диагностических методик способствует более точной оценке состояния слезной пленки, повышает эффективность послеоперационного ведения пациентов, минимизирует риск развития дискомфортных ощущений и обеспечивает максимальное качество функциональных результатов.
Современная офтальмология располагает широким арсеналом диагностических методов, включая пробу Ширмера, тест Норна и неинвазивные методы, такие как оценка времени разрыва слезной пленки. Этот метод демонстрирует сопоставимую с инвазивными тестами точность и обеспечивает более комфортные условия для пациента. Наряду с этим исследователи обращают внимание на потенциальную взаимосвязь изменений слезной пленки и развития синдрома сухого глаза после кераторефракционной хирургии. Для получения объективной и полной клинической картины рекомендуется использовать комплексную диагностику, позволяющую оценить состояние слезной пленки с разных позиций и выявить скрытые патологические изменения, в частности снижение ее стабильности, нарушение липидного слоя, изменения осмолярности, микровоспаление, уменьшение плотности бокаловидных клеток и ухудшение регенерации эпителия роговицы. Применение комбинированных диагностических методик способствует более точной оценке состояния слезной пленки, повышает эффективность послеоперационного ведения пациентов, минимизирует риск развития дискомфортных ощущений и обеспечивает максимальное качество функциональных результатов.
Впоследнее время возникли противоречия между клиническими проявлениями и терминологией патогенеза синдрома сухого глаза (ССГ), что требует пересмотра существующей классификации. Современные научные открытия в сфере офтальмологии кардинально трансформировали понимание причин возникновения и механизмов развития данного заболевания [1].
При медицинском обследовании нередко обнаруживается, что диагностируемые симптомы не соответствуют традиционному представлению о ССГ. Кроме того, в ходе обследования (проба Ширмера, высота стояния слезного мениска и др.) иногда определяется нормальный объем слезопродукции, при этом жалобы больных и клинические признаки (снижение времени разрыва слезной пленки по Норну, повышение осмолярности и др.), характерные для ССГ, купируются при назначении терапевтической гигиены век и слезозаместительной терапии [1–3].
Изменения в прекорнеальной слезной пленке после кераторефракционных операций
Глаза защищены особым барьером – прекорнеальной слезной пленкой, которая выполняет несколько критически важных функций для здоровья органов зрения. Благодаря уникальной структуре она не только защищает от бактерий, но и механически очищает поверхность глаза от пыли и загрязнений. Оптическая система глаза во многом зависит от качества прекорнеальной слезной пленки (ПСП). Этот жидкий слой создает идеальную сферическую поверхность на роговице, что необходимо для правильного преломления света и четкого зрения. Роговица может эффективно выполнять роль оптической линзы только при наличии гладкой, увлажненной поверхности. Помимо защитных и оптических свойств слезная пленка выполняет трофическую функцию, являясь важнейшим компонентом системы защиты глаз от внешнего воздействия [4].
Прекорнеальная слезная пленка покрывает поверхность глаза и образует слой постоянной толщины, который непрерывно распределяется и изменяется в течение суток вследствие испарения. Исследования показали, что размер глазной щели влияет на толщину данного слоя, которая варьируется в пределах 6–10 мкм. Оптические свойства глаза и здоровье эпителия роговицы во многом зависят от этого состояния пленки [5].
Важное открытие было сделано в 1983 г. группой ученых под руководством J.D. Nelson. Они доказали, что ПСП распространяется не только на роговицу, но и на конъюнктивальную область [6].
Несмотря на значительные достижения в области коррекции зрения, пациенты после кераторефракционных операций (КРО) нередко сталкиваются с побочными эффектами. Появление транзиторного ССГ вызывает у многих ощущение дискомфорта. Пациенты часто жалуются на сухость, жжение и покраснение глаз, а также на ощущение инородного тела. В ряде случаев наблюдаются нестабильность и затуманивание зрения [7, 8]. Симптомы, связанные с транзиторным ССГ, могут существенно снижать удовлетворенность пациентов результатами операции, несмотря на достигнутое улучшение остроты зрения.
Таким образом, проблема послеоперационного дискомфорта остается актуальной, несмотря на высокую клинико-функциональную эффективность и предсказуемость современных методов коррекции зрения [9].
Множество исследователей в мире активно изучают постоперационный ССГ после КРО. Особенно важным представляется углубленное изучение причин возникновения и механизмов развития ССГ на разных этапах послеоперационного периода [10].
Исследователи отмечали у пациентов, перенесших операцию LASIK, временные нарушения, напоминавшие ССГ, хотя выработка слезной жидкости оставалась в норме. Проявления включали затуманенное зрение и эрозии эпителия на роговичном лоскуте. Интересно, что эти симптомы самопроизвольно регрессировали в течение полугода. Исследователи предположили, что причина связана с нарушением иннервации роговицы после операции. Для объяснения этого состояния был введен специальный термин «нейротрофическая эпителиопатия» (НЭ). Суть феномена заключается в том, что пересечение нервных окончаний роговицы во время вмешательства временно нарушает их трофическое влияние на эпителиальный слой, что и вызывает описанные изменения [11].
Пациенты после операции LASIK часто сталкиваются с НЭ на ранних стадиях восстановления, даже если до операции подобных проблем не возникало. Это патологическое состояние, характеризующееся колебаниями остроты зрения и симптоматикой, схожей с ССГ, в современной медицине достаточно хорошо изучено [12, 13].
Хирургические инструменты, такие как вакуумное кольцо фемтосекундного лазера или микрокератома, а также блефаростат, травмируют глазную поверхность, что приводит к нарушению ее нормальной работы. ССГ вторичного характера после КРО затрагивает не только эпителий роговицы с нейротрофическими изменениями, но и всю поверхность органа зрения, включая конъюнктивальную оболочку [14].
В послеоперационном периоде наблюдается значительное сокращение количества бокаловидных клеток в конъюнктиве. Как следствие – дестабилизация слезной пленки из-за недостаточной выработки муцина. Особенно остро данные нарушения проявляются у лиц с хроническим ССГ. Восстановление нормальной концентрации бокаловидных клеток до исходного уровня может занять полгода [15, 16].
При пересечении нервных волокон (фемтосекундным лазером, микрокератомом), а также непосредственно при эксимерлазерной абляции повреждаются, пересекаются нервные окончания роговицы. Сразу после процедуры снижается чувствительность глазной поверхности. Это временное явление оказывает комплексное воздействие на состояние глаза. Нарушение целостности нервных волокон считается главным фактором, провоцирующим ранние послеоперационные осложнения и воспалительную реакцию. Среди них прежде всего выделяют НЭ и дисфункцию слезной системы, вызванные процедурой LASIK [17–20].
Современная офтальмология стремительно развивается, совершенствуются методы исследования глаза. Основной задачей является комплексное изучение как самого глазного яблока, так и окружающих его тканей. В медицинской диагностике выделяют два основных направления обследования – основное и дополнительное. Подобная классификация обусловлена доступностью методов в амбулаторных учреждениях при первом обращении больного. Прогресс в области диагностических исследований характеризуется несколькими важными аспектами. Во-первых, постоянно увеличивается количество специализированных методик. Во-вторых, совершенствуются диагностические процедуры. В-третьих, современные технологии подразумевают наличие высококвалифицированного медицинского персонала, прошедшего специальную подготовку. И наконец, для правильной интерпретации полученных данных необходимо постоянное накопление практического опыта в проведении исследований [21].
Современные методы исследования прекорнеальной слезной пленки: классификация и сравнительный анализ
Методы оценки ПСП можно условно разделить на инструментальные и функциональные.Инструментальные методы включают аппаратные способы визуализации и количественной оценки ПСП и ее компонентов: интерферометрию, мейбографию, корнеальную топографию и видеокератоскопию, оптическую когерентную томографию (ОКТ), конфокальную микроскопию, тиаскопию, осмометрию, цифровые щелевые лампы, а также неинвазивные технологии оценки времени разрыва слезной пленки. Функциональные методы направлены на изучение стабильности, целостности и продукции слезной жидкости. К ним относятся проба Ширмера, тест Норна TBUT (время разрыва слезной пленки), субъективные шкалы оценки, например OSDI (Ocular Surface Disease Index), а также неинвазивные методы измерения времени разрыва ПСП.
Интерферометрия слезной пленки
Интерферометрия применяется для оценки толщины и распределения липидного слоя, определяющего испарение слезной жидкости. Метод основан на анализе интерференционных картин, возникающих при отражении света от границ между слоями ПСП. Он отличается неинвазивностью, высокой информативностью и краткой продолжительностью проведения (две-три минуты). Для обеспечения достоверности результатов пациентам рекомендуется прекратить ношение контактных линз за 48 часов до исследования, а также избегать использования жиросодержащей косметики в области глаз [22].
Мейбография
Мейбография позволяет визуализировать морфологическое состояние мейбомиевых желез, играющих ключевую роль в формировании липидного слоя. Методика особенно актуальна при подозрении на дисфункцию мейбомиевых желез, часто сопровождающую ССГ. Современные приборы, такие как Me-Check (Италия), обеспечивают быструю и качественную оценку плотности и проходимости желез, а также мониторинг состояния на фоне терапии [22].
Топография и видеокератоскопия роговицы
Корнеальная топография позволяет построить количественную и качественную карту передней поверхности роговицы на основании анализа отражения световых лучей или проекции щелевого света. Она широко используется при диагностике эктатических заболеваний, оценке ортокератологических изменений и при подборе контактных линз [23]. Видеокератоскопия, основанная на анализе отражения колец Плацидо, обеспечивает точное картирование кривизны роговицы и косвенно оценивает регулярность ПСП. Достоверность метода зависит от алгоритмов обработки и качества исходного изображения [24–26].
Проба Ширмера
Тест Ширмера остается одним из наиболее применяемых функциональных методов оценки общей слезопродукции. Он проводится путем размещения фильтровальной полоски за нижнее веко на пять минут. Модификация L. Jones с предварительным использованием анестетика позволяет исключить рефлекторную компоненту и оценить базальную секрецию. К недостаткам метода относят раздражение конъюнктивы, способное искажать результаты, а также низкую воспроизводимость данных [8].
Тест Норна
Время разрыва ПСП, измеряемое после инстилляции флуоресцеина, остается основным критерием оценки ее стабильности. TBUT менее десяти секунд свидетельствует о сниженной стабильности ПСП, а значения менее пяти секунд считаются диагностическими для ССГ. К недостаткам относят потенциальное влияние красителя на поверхностные свойства пленки. Современные автоматизированные платформы позволяют повысить точность и снизить субъективность измерений [27–30].
Тиаскопия
Тиаскопия, или интерференционная микроскопия, применяется для оценки структуры липидного слоя. Приборы типа Tearscope Plus помогают визуализировать паттерны распределения липидов и измерить временные параметры их распространения. У здоровых людей липиды равномерно распределяются в течение 0,3–0,4 секунды, тогда как при ССГ это занимает свыше трех секунд [8].
Осмометрия слезной жидкости
Измерение осмолярности – один из наиболее чувствительных маркеров ССГ. Значения выше 308–316 мОсм/л свидетельствуют о гиперосмолярности, типичной для данного состояния. Технологии, реализованные в системе TearLab, позволяют получить количественные данные за несколько секунд с минимальной инвазивностью. Методика характеризуется высокой специфичностью и воспроизводимостью [8].
ОКТ-менискометрия
ОКТ дает возможность получить изображение слезного мениска и определить его морфологические параметры: высоту, ширину и радиус кривизны. Эти показатели отражают объем слезной жидкости и используются при оценке степени ее недостаточности. В норме высота мениска составляет 0,2–0,3 мм. Метод особенно полезен для динамического наблюдения после КРО [31, 32].
Конфокальная микроскопия
Метод применяется для визуализации клеточной структуры роговицы in vivo. С помощью данной методики можно оценить морфологию эпителия, кератоцитов и нервных окончаний, что особенно важно при диагностике нейротрофических изменений после лазерной коррекции зрения и длительного ношения контактных линз. Кроме того, конфокальная микроскопия может выявить признаки воспаления и микрососудистые изменения [8].
Субъективные методы: опросник OSDI
Опросник OSDI – валидированный инструмент для оценки тяжести симптомов, связанных с нарушением ПСП. Он состоит из 12 вопросов и затрагивает частоту и интенсивность жалоб, а также влияние симптомов на повседневную активность. Метод позволяет количественно оценивать субъективную компоненту ССГ, а также проводить мониторинг в послеоперационном периоде [32].
Цифровые щелевые лампы
Современные цифровые щелевые лампы, например MediWorks S390L, оснащаются высокочувствительными камерами и модулями анализа, позволяющими оценивать стабильность пленки и ее разрыв без использования красителей. На основании данных о времени первого разрыва и площади испарения можно объективно оценить стабильность ПСП. Метод показывает высокую воспроизводимость и может стать альтернативой традиционным тестам [33].
Неинвазивное измерение времени разрыва ПСП
Методы неинвазивного измерения времени разрыва ПСП реализованы в устройствах Keratograph 5M, LacryDiag и др. Они обеспечивают автоматическую регистрацию момента нарушения целостности ПСП с высокой точностью. Однако вариативность результатов, установленная в ряде исследований, указывает на необходимость стандартизации методики и дальнейших сравнительных исследований [34, 35].
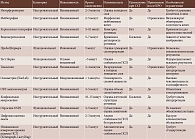
Сравнительная характеристика методов исследования ПСП представлена в таблице.
Заключение
Оценка состояния ПСП – сложная задача для специалистов. Необходима разработка методов визуализации, не нарушающих структуру слезной жидкости. Минимальное использование инвазивных техник, таких как применение флуоресцеина, способствует более точной диагностике. Специалисты стремятся разработать эффективные неинвазивные методики, позволяющие получить достоверную информацию о состоянии ПСП без нарушения ее целостности.
Комплексная диагностика состояния ПСП требует применения нескольких методов исследования, поскольку одного теста недостаточно. Современная офтальмология располагает как инвазивными, так и неинвазивными методами оценки. Особого внимания заслуживает метод неинвазивного измерения времени разрыва ПСП, который демонстрирует эффективность, аналогичную традиционным инвазивным подходам. Специалисты постоянно совершенствуют методики неинвазивного измерения времени разрыва ПСП, рекомендуя регулярные обследования с обязательным учетом всей симптоматики для получения максимально достоверных результатов. При мониторинге состояния пациентов с нарушениями ПСП, включая ССГ, необходимо придерживаться определенного протокола наблюдения. Это позволит эффективно отслеживать изменения и корректировать лечение в соответствии с динамикой заболевания.
Таким образом, неинвазивные методы исследования, используемые в диагностике ССГ, оптимальны, поскольку не нарушают целостности ПСП. Следует отметить, что для комплексной оценки состояния ПСП недостаточно применения одного метода – необходимо использовать комплекс диагностических инструментов. В этом случае клиническая картина будет более полной.
L.V. Reznikova, Jad Allah Amro Bilal Ahmad, Altameemi Faten M. Ali Abdulhussein, M. Chtioui
I.M. Sechenov First Moscow State Medical University
Contact person: Jad Allah Amro Bilal Ahmad, sadlover199411@gmail.com
The condition of the tear film plays a key role in ensuring the quality of vision and eye health. Despite significant progress in the field of surgical vision correction, such interventions are often accompanied by temporary side effects, including discomfort and dry eyes.
Modern ophthalmology has a wide range of diagnostic methods, including the Schirmer test, the Norn test, and noninvasive methods such as estimating tear film rupture time. This method demonstrates accuracy comparable to invasive tests and provides a more comfortable environment for the patient. Along with this, the researchers draw attention to the potential relationship between changes in the tear film and the development of dry eye syndrome after keratorefractive surgery. To obtain an objective and complete clinical picture, it is recommended to use a comprehensive diagnosis that allows to assess the condition of the tear film from different positions and identify hidden pathological changes, in particular, a decrease in its stability, a violation of the lipid layer, changes in osmolarity, microinflammation, a decrease in the density of goblet cells and a deterioration in the regeneration of the corneal epithelium. The use of combined diagnostic techniques contributes to a more accurate assessment of the condition of the tear film, increases the effectiveness of postoperative management of patients, minimizes the risk of discomfort and ensures maximum quality of functional results.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.