Как избежать ошибок в борьбе с болью. XI Ежегодная конференция «Вейновские чтения»
- Аннотация
- Статья
- Ссылки


Причины отрицательных исходов лечения боли в спине и способы их преодоления
Как отметил к.м.н. Алексей Николаевич БАРИНОВ (Первый МГМУ им. И.М. Сеченова), примерно 86% людей в течение жизни отмечают скелетно-мышечные боли в спине. Однако в подавляющем большинстве случаев эта боль имеет доброкачественное течение с высокой вероятностью самопроизвольной ремиссии без лечения. Так, у 50% населения боль проходит самостоятельно в течение недели, у 75% – в течение месяца и только у 10% пациентов боль в спине приобретает хронический характер, вызывая стойкую инвалидизацию1.
Безусловно, врачу необходимо знать признаки серьезной патологии («красные флажки»), дифференцированная диагностика которых считается залогом безопасности лечения боли в спине. Причиной специфической боли может быть патология межпозвонкового диска с рефлекторными и компрессионными синдромами (5%), метаболические нарушения (остеопороз) (2%), воспалительные инфекционные процессы (2%), опухоли (< 1%)1.
Выявление источников болевых импульсов при неспецифической боли требует пристального анализа всех данных. По мнению докладчика, необходимо тщательно оценивать анамнестические данные и статус пациента, поскольку причиной хронизации боли в спине, вплоть до инвалидизации, помимо вторичного характера боли, является назначенная терапия. В этой связи А.Н. Баринов предложил аудитории обсудить несколько клинических примеров ведения пациентов с одинаковыми болевыми симптомами из опыта работы клиники нервных болезней им. А.Я. Кожевникова Первого МГМУ им. И.М. Сеченова.
Во всех рассмотренных случаях пациенты обратились со следующими жалобами:
-
постоянные тянущие боли в поясничном отделе позвоночника с распространением в правую ягодичную область и далее по наружной поверхности правого бедра, голени;
-
чувство онемения и ползанья «мурашек» по наружной поверхности правого бедра и голени, больше выраженных на первом и втором пальцах стопы.
Клинический пример 1
Пациентка О., 21 год.
Анамнез. Три месяца назад во время ссоры муж толкнул пациентку так, что она упала. С тех пор ее беспокоят сильные боли, особенно после семейных ссор. Согласно магнитно-резонансной томографии, у пациентки имеется небольшая грыжа, локализованная в левой стороне. Так называемые хондропротекторы, миорелаксанты, нестероидные противовоспалительные препараты (НПВП) давали временный положительный эффект. Антиконвульсанты и антидепрессанты не переносит. Мать страдает радикулопатией справа.
Неврологический осмотр. Де-фицитарной неврологической симптоматики не выявлено, чувствительные расстройства отсутствуют. Имеется астено-ипохондрическая акцентуация в структуре личностных черт и наличествуют симптомы, описанные G. Waddell, – распространенная поверхностная болезненность, изменение угла подъема прямой ноги при отвлечении внимания.
Диагноз. Чем страдает пациентка? С этим вопросом докладчик обратился к участникам дискуссии, предложив выбрать из таких вариантов, как остеохондроз, грыжа; радикулопатия; неспецифическая боль в спине; соматоформное болевое расстройство. Большинство высказалось за последний диагноз, который и был поставлен больной в клинике нервных болезней.
«В данном случае это классическая психогенная боль. Полученная ранее негативная информация и преувеличивающаяся опасность заболевания способствовали развитию у пациентки ноцебо-эффекта. Между тем данные многочисленных исследований свидетельствуют, что корреляция между величиной грыж и наличием и интенсивностью болевого синдрома отсутствует. Еще в 1994 г. было установлено, что у пациентов после 20 лет бессимптомные грыжи и протрузии встречаются в 30% случаев», – пояснил А.Н. Баринов2. Докладчик также уточнил, что информирование пациента с неспецифической болью в спине о доброкачественном характере заболевания и благоприятном прогнозе выздоровления лечащим врачом является основным условием быстрого и полного выздоровления.
Лечение. Пациентке разъяснен доброкачественный характер ее расстройств, дан положительный прогноз на перспективы деторождения и рекомендована лечебная физкультура, что было воспринято пациенткой без энтузиазма. Виновником заболевания больная считала своего мужа, этот психологический фактор необходимо было учесть и преодолеть. Муж был обучен основам баночного массажа, в дальнейшем семейная жизнь наладилась. Таким образом, специалистам клиники удалось заменить ноцебо-эффект, спровоцированный посещениями предыдущих врачей, плацебо-эффектом, полученным от разъяснения пациентке механизмов боли и назначения массажа, который выполнял муж, – процедуры, которая несла в себе огромный психологический потенциал.
Клинический пример 2
Пациент Д., 57 лет.
Анамнез. Боли появились после возвращения из тропической страны с экзотического отдыха, сопровождавшегося тяжелыми физическими нагрузками (рафтинг, серфинг), пищевыми экспериментами (жареные насекомые, сырые моллюски и пр.), промискуитетом. Сопутствующие симптомы – потливость, субфебрилитет.
Диагноз. Мнения аудитории при определении диагноза (остеохондроз, вторичная боль в спине, миозит, неспецифическая боль в спине, соматоформное болевое расстройство) разделились. А.Н. Баринов отметил, что в данном случае пациент страдал от «вторичной боли в спине», которая особенно проявилась после того, как он обратился за помощью в коммерческую больницу. Там ему назначили физиотерапию, массаж, мануальную терапию, сделали блокаду глюкокортикостероидом, в результате произошла генерализация полученной им инфекции – стрептодермии. Когда пациент в тяжелом состоянии поступил в клинику нервных болезней им. А.Я. Кожевникова, проведенная магнитно-резонансная томография показала у него наличие спондилодисцита, поражений в грудном и поясничном отделах позвоночника.
Лечение. Пациенту прежде всего была проведена антибактериальная терапия. Однако исходом заболевания стала инвалидизация. Безусловно, если бы врачи коммерческой клиники сразу обратили внимание на «красные флажки», заподозрили наличие серьезной патологии и провели бы правильное обследование с назначением оптимальной схемы лечения, то пациент, по мнению А.Н. Баринова, имел бы шансы на выздоровление.
Клинический пример 3
Пациентка З., 46 лет.
Анамнез. Боли появились после переохлаждения шесть месяцев назад. Прием НПВП в начале заболевания дал лишь незначительный эффект. Затем лечилась стационарно, получила пять паравертебральных блокад с длительно действующим глюкокортикостероидом, а также 20 уколов хондропротекторов. На момент обращения в клинику нервных болезней им. А.Я. Кожевникова пациентка имела признаки синдрома Иценко – Кушинга и дисгормональную спондилопатию, которая была вызвана неумеренным приемом глюкокортикостероидов.
Прием НПВП является первым этапом лечения боли в спине. Однако, как показывают результаты исследований, 50% больных не отвечают на первый назначаемый НПВП, 25% – на второй, а 10% – на третий. Одна из причин кроется в генетическом полиморфизме, который обусловливает широкий спектр изменчивости фармакодинамического и фармакокинетического профиля лекарств, что непременно будет влиять на эффективность и безопасность их применения. В частности речь идет о полиморфизме генов системы CYP, которые кодируют ключевые ферменты биотрансформации НПВП3.
Неэффективность НПВП может быть объяснена парадигмой «экспорт воспаления в мозг» на продвинутой стадии заболевания. Иначе говоря, периферическое повреждение запускает целый каскад патофизиологических процессов, затрагивающих всю ноцицептивную систему, формируя вторичную гиперальгезию вне зоны повреждения4. «Только в том случае, когда мы назначаем НПВП, способные проникать через гематоэнцефалический барьер, мы воздействуем на центральную сенситизацию и препятствуем экспорту воспаления в мозг», – констатировал А.Н. Баринов.
В этом отношении особый интерес вызывает препарат Дексалгин® – водорастворимая соль правовращающегося энантиомера кетопрофена, который отвечает за обезболивающий эффект. По данным исследований (in vivo), Дексалгин® обладает способностью проникать через гематоэнцефалический барьер и отличается двойным механизмом действия – центральным и периферическим. Препарат блокирует циклооксигеназу и синтез простагландинов как в очаге воспаления, так и в сенситизированных структурах головного и спинного мозга5, 6.
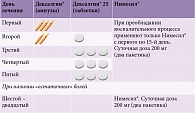
«Разработана оптимальная схема комбинированной терапии неспецифической боли в спине в период обострения с применением Дексалгина и Нимесила. Дексалгин® следует назначать в первые пять дней: два дня внутримышечно, затем перорально с последующим переключением на Нимесил®, который применяется в течение еще двух недель (таблица)7», – отметил А.Н. Баринов.
Именно с помощью последовательного назначения Дексалгина и Нимесила болевой синдром у пациентки был временно снят. Последующее расширенное неврологическое обследование позволило выявить невропатию седалищного нерва (симптом Бонне), или синдром грушевидной мышцы, который и был причиной боли.
Лечение. Каким должен быть следующий этап лечения? Докладчик предложил коллегам выбрать наиболее правильный подход к ведению больной с синдромом грушевидной мышцы из четырех предложенных вариантов: блокады с бетаметазоном, глюкокортикостероиды в/в; блокады с хондропротекторами или гомеопатическими препаратами; локальная блокада НПВП в грушевидную мышцу. Мнение аудитории об использовании локальной инъекции НПВП в очаг устойчивого мышечного спазма совпало с назначением специалистов клиники. «Мы ввели пациентке Дексалгин® для того, чтобы убрать спазм грушевидной мышцы. Этот препарат в отличие от глюкокортикоидов не задерживает жидкость, не повышает артериальное давление, не вызывает иммуносупрессию, не декомпенсирует сахарный диабет, не повышает массу тела, что очень важно для пожилых и соматически отягощенных пациентов», – пояснил А.Н. Баринов. Пациентке также были назначены курсы постизометрической релаксации, лечебная физкультура и рекомендовано ведение здорового образа жизни.
Клинический пример 4
Пациент П., 52 года.
Анамнез. Страдает хроническим алкоголизмом. Утром после алкогольного эксцесса остро развилось онемение и жжение по наружному краю правой стопы и голени, слабость тыльного сгибания стопы. Показания магнитно-резонансной томографии – грыжа L5–S1 6 мм.
Прежде всего докладчик поинтересовался у коллег – следует ли срочно оперировать больного или возможно консервативное лечение? Большинство высказалось за то, чтобы больному сделать блокаду нервных окончаний. По мнению А.Н. Баринова, прежде чем принять решение об оперативном вмешательстве, необходимо тщательно изучить характер чувствительности двигательных, рефлекторных нарушений при компрессии корешков L5, L4, S1. У пациента было онемение по наружному краю стопы, что позволяло предположить радикулопатию L5–S1, однако слабость – совсем в другой корешковой группе, что давало основание подозревать наличие радикулопатии L4–L5 либо туннельной невропатии.
Диагноз. Проведенная электронейромиография, а также ультразвуковое исследование показали: компрессию малоберцового нерва в фибулярном канале; выше сдавления нерв утолщен, контуры его нечеткие, отмечается утолщение отдельных нервных пучков в составе нерва. Налицо синдром двойного аксоплазматического сдавления.
Лечение. Была произведена блокада фибулярного канала комбинацией «новокаин 0,5% 1,0 + дексаметазон 4 мг/мл 2,0». Для восстановления корешка нерва назначена следующая схема лечения: альфа-липоевая кислота 600 мг натощак (за 30 минут до еды) по одной таблетке три раза в день в течение месяца; Мильгамма 2 мл в/м № 10, далее Бенфогамма 200 мг 2 р/сут в течение месяца; Нейромидин 15% 1 мл п/к № 10, далее перорально 20 мг 3 р/сут в течение месяца. Подобная терапия способствовала регрессу слабости, онемения и парестезий в ноге пациента.
Как отметил А.Н. Баринов, применение альфа-липоевой кислоты в составе комплексной патогенетической терапии при радикулопатии обоснованно. Согласно данным рандомизированного контролируемого исследования, применение альфа-липоевой кислоты в дозе 600 мг/сут в течение 60 дней способствовало восстановлению нерва в два раза быстрее, чем использование ацетил-L-карнитина в дозе 1180 мг/сут. Доказано, что прием альфа-липоевой кислоты 600 мг/сут за 30 минут до еды в течение одного – трех месяцев не только эффективно восстанавливает чувствительность, мышечную силу и сухожильные рефлексы, но и улучшает электрофизиологические показатели: амплитуду М-ответа и скорость проведения возбуждения по нерву8.
В заключение докладчик подчеркнул, что лечение боли в спине предполагает комплексный подход, который предусматривает не только медикаментозное лечение, но и поведенческую и когнитивно-поведенческую психотерапию, лечебную физкультуру. При острой боли назначаются НПВП, такие как Дексалгин®, при необходимости применяются миорелаксанты или производится блокада в триггерную точку. При хронической боли после препарата Дексалгин®, продолжительность применения инъекционной и пероральной форм которого ограничена пятью – семью днями, рекомендуется провести лечение препаратом Нимесил® в течение как минимум 14 дней. В качестве базисной терапии фасеточного синдрома, вызванного, например, остеоартрозом, при хронической боли в спине требуются таблетированные хондропротекторы, блокады с глюкокортикостероидами в фасеточные суставы. Если у пациента радикулопатия дает выраженный болевой синдром, назначаются антиконвульсанты и антидепрессанты. Оперативное лечение показано пациенту с радикулопатией при нарастающем парезе мышц, тазовых нарушениях. Для восстановления функций назначаются витамины группы В, антихолинэстеразные препараты и антиоксидант альфа-липоевая кислота.
Полиморфизм болей в дистальных отделах конечностей
Если распространенными причинами острой боли являются термические поражения, острая травма и избыточная физическая нагрузка, то спектр причин хронической боли, по словам д.м.н., профессора Игоря Владимировича ДАМУЛИНА (Первый МГМУ им. И.М. Сеченова), гораздо шире и разнообразнее.
К наиболее частым причинам хронической боли в руке относят вертеброгенное поражение корешков, невертеброгенное поражение цервикальных корешков, поражение периферических нервов в виде моно- и полиневропатии, дегенеративные изменения суставов и связок, поражение плечевого сплетения, сосудистые заболевания и избыточную физическую нагрузку. Вертеброгенное поражение корешков лидирует и среди частых причин хронической боли в ноге, которая также может быть вызвана поражением периферических нервов, узким позвоночным каналом, дегенеративными изменениями суставов и связок, заболеваниями сосудов нижних конечностей. По словам докладчика, спектр расстройств, которые могут приводить к возникновению болевых ощущений, этим не ограничивается. Иногда действия врача, который активно хочет помочь, но не знает, как правильно это сделать, могут сопровождаться тяжелыми последствиями для больного.
Постинсультные боли очень разные по характеру. Прежде всего это боли, обусловленные мышечным спазмом. Их возникновение связано и с наличием позитивной симптоматики (повышение мышечного тонуса по спастическому типу, оживление сухожильных рефлексов), и с изменением спастически сокращенных мышц (ригидность, контрактуры, фиброз), которое наступает через некоторое время и приобретает довольно выраженный характер. Все это происходит на фоне негативной симптоматики в виде снижения мышечной силы, замедленности движений и нарушений выполнения тонких движений пальцами рук. В основе возникновения боли после инсульта могут лежать центральные механизмы, которые принято обозначать как таламические боли. Туннельные невропатии также считаются частой причиной возникновения болей в конечностях.
Полиневропатия является одной из самых значимых проблем, которая возникает у пациентов, имеющих боли в дистальных отделах конечностей. В ее основе лежат дизиммунные, дисметаболические причины, например сахарный диабет, а также токсические, инфекционные и паранеопластические факторы. Симптоматика независимо от причин определяется пораженными периферическими нервными волокнами, например, в возникновении болевого синдрома повинны волокна A и C.
Зачастую встречается сочетанное поражение различных волокон, как при синдроме Гийена – Барре, основными вариантами которого могут быть острая демиелинизирующая полирадикулоневропатия, острая моторная аксональная невропатия, острая сенсомоторная аксональная невропатия, парапаретический вариант, фарингеально-цервико-бронхиальный вариант, лицевая диплегия с дистальными парестезиями, острая пандизавтономия и изолированный сенсорный вариант. Типичные проявления – мышечная слабость в конечностях, как правило, симметричная, сенсорные нарушения, иногда – симптомы поражения центральной нервной системы (головная боль, психические нарушения).
Характер боли при синдроме Гийена – Барре многообразен – это невропатическая, мышечная, радикулопатическая боль. Как диагностировать синдром Гийена – Барре? Как правило, у 85% больных повышен уровень белка в ликворе. Электромиографические данные у 80–90% больных подтверждают множественные блоки проведения, снижение скорости распространения возбуждения по периферическим нервам. В анализах крови и мочи специфические изменения отсутствуют.
Хроническая воспалительная демиелинизирующая полирадикулоневропатия (ХВДП) – еще одна причина, которая может приводить к возникновению болевых ощущений. Она диагностируется примерно в 20% случаев у пациентов с полиневропатией неясного генеза и отличается от синдрома Гийена – Барре подострым началом длительностью более четырех недель, в ряде случаев с обострением и ремиссией. Варианты течения ХВДП разнообразны – это могут быть периоды нарастания симптомов с последующим плато и медленным улучшением, либо постоянное нарастание симптомов, либо ступенеобразное прогрессирование, спонтанное обострение и ремиссии.
Клиническими особенностями ХВДП выступают мышечная слабость и в дистальных, и в проксимальных отделах конечностей, сочетающаяся с низкими рефлексами либо с их отсутствием, выпадение чувствительности преимущественно в ногах, парестезии и жгучие, ноющие невропатические боли, сопровождающиеся неприятным эмоциональным компонентом. Сложности при постановке диагноза могут вызвать варианты ХВДП с пирамидной рефлекторной симптоматикой в сочетании с невритом зрительного нерва, поскольку у 5–30% больных ХВДП имеют место церебральные нарушения.
Доминированием болевых ощущений, парестезиями дистальных отделов, нарастающих в ночные часы, нередко сочетающихся с вегетативными нарушениями в виде дистального гипогидроза, артериальной гипертензией, импотенцией и вазомоторными нарушениями сопровождается идиопатическая сенсорная полиневропатия.
Алкогольная полиневропатия, при которой поражаются аксоны и отмечается миелинопатия, по характеру является дистальной сенсомоторной полиневропатией. В ее основе лежат прямое токсическое действие ацетальдегида, дефицит витамина В1, нарушение питания, нарушение абсорбции, поражение печени.
Нервно-мышечные нарушения (полиневропатия и дисметаболическая миопатия) имеют место при гипотиреозе. Чаще всего это мышечные крампи, боли и парестезии, особенно в проксимальных отделах конечностей, снижение толерантности к физическим нагрузкам, синдром «повисшей головы», выраженная мышечная слабость, которая нарастает при низкой температуре. У 75% пациентов ситуация осложняется возникновением туннельных синдромов, компрессией периферических нервов или демиелинизирующей полиневропатией, которая может протекать до определенного момента субклинически. По этой причине клинически особенное внимание следует обращать на наличие гипорефлексии и на удлинение фазы релаксации мышц.
При сахарном диабете (СД) патологические изменения могут затрагивать периферические и краниальные нервы, сплетения и спинномозговые корешки. Полиневропатия возникает при СД 1 и 2 типа и в среднем встречается у 50% больных СД. Диагноз «диабетическая полиневропатия» (ДПН) ставится больному при наличии симптомов поражения периферической нервной системы после исключения всех других причин этого поражения. Современное представление о диабетической полиневропатии связано с ее гетерогенностью, а к наиболее распространенным формам относятся дистальная симметричная сенсомоторная полиневропатия, вегетативная полиневропатия. Гораздо реже встречаются асимметричная проксимальная моторная невропатия, диабетическая туловищная невропатия, острая болевая ДПН, невропатия мелких волокон и краниальная невропатия.
ДПН отличается не только разнообразием форм, но и клиническими проявлениями. Так, например, дистальная симметричная сенсомоторная полиневропатия характеризуется в первую очередь нарушениями чувствительности в дистальных отделах конечностей – гипестезией или невропатическими проявлениями в дистальных отделах ног с последующим вовлечением верхних конечностей. Выпадают глубокие рефлексы с ног, больные предъявляют жалобы на боли, дизестезии, сенситивную атаксию. Но даже при наличии мышечной атрофии в области больших пальцев ног пациенты редко предъявляют жалобы на мышечную слабость. Асимметричная проксимальная моторная невропатия клинически проявляется острым началом с выраженной болью, нередко носящей жгучий характер, с последующей слабостью, похуданием мышц бедра, выпадением коленного рефлекса.
По мнению профессора И.В. Дамулина, не стоит забывать и о таких причинах боли при сахарном диабете, как возникновение диабетических язв стопы, формирование сустава Шарко, а также таламические боли, причиной которых становится развившийся на фоне СД инсульт в области таламуса, или возможные фантомные боли после удаления конечности.
Патогенез ДПН сложен. Ключевая роль в нем принадлежит окислительному стрессу, который рассматривается в качестве ведущего механизма повреждения нервного волокна, и конечным продуктам гликирования.
Традиционно основным способом профилактики и лечения ДПН считается оптимальный контроль гипергликемии, сосудистых факторов риска и профилактика трофических нарушений. В связи с современными взглядами на патогенез ДПН большое значение имеют методы, направленные на восстановление антиоксидантной защиты и снижение продукции свободных радикалов кислорода. В настоящее время альфа-липоевую кислоту (например, препарат Берлитион®) рассматривают как один из эффективных и обязательных компонентов патогенетической комплексной терапии ДПН.
Эндогенный антиоксидант Берлитион® назначается при всех типах диабетической полиневропатии. Механизм действия препарата заключается в связывании свободных радикалов, стабилизации клеточных мембран, нормализации энергетического обмена нейронов, восстановлении аксонального транспорта. Профессор И.В. Дамулин акцентировал внимание аудитории на следующих доказанных клинических эффектах альфа-липоевой кислоты (препарат Берлитион®):
-
уменьшение выраженности болей, парестезий;
-
уменьшение выраженности сенсорных расстройств;
-
оживление глубоких рефлексов;
-
улучшение электрофизиологических показателей (амплитуды М-ответа, скорости распространения возбуждения по нервам).
Завершая выступление, докладчик также отметил, что в качестве симптоматического лечения ДПН с целью уменьшения болевого синдрома можно использовать анальгетики, НПВП, антидепрессанты, антиконвульсанты и местно – капсаицин, лидокаин.
Заключение
В ходе обсуждения был выработан наиболее оптимальный подход к ведению пациентов с болью в спине и дистальных отделах конечностей. Комплексный подход предусматривает при острой неспецифической боли в спине первоначально назначение НПВП. При хронической неспецифической боли в спине после препарата Дексалгин® можно рекомендовать Нимесил® в течение как минимум 14 дней. Обоснованной и доказанной является необходимость применения альфа-липоевой кислоты (препарата Берлитион®) в составе комплексной патогенетической терапии при радикулопатии, а также при всех типах диабетической полиневропатии. Альфа-липоевая кислота (Берлитион®) не только уменьшает выраженность боли и парестезий, но и способствует восстановлению чувствительности, мышечной силы, оживлению глубоких рефлексов, улучшению электрофизиологических показателей.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.