Холестаз: патофизиологические механизмы развития, диагностика и лечение
- Аннотация
- Статья
- Ссылки
![Рис. 2. Схема морфологических изменений у больных с холестазом (Адаптировано по [5].)](/upload/resize_cache/iblock/99e/195_350_1/99ee93c7589c68fa1597a8ae1afb5786.png)
![Рис. 6. Действие урсодезоксихолевой кислоты на холангиоцит (Адаптировано по [10].)](/upload/resize_cache/iblock/b7c/195_350_1/b7c86a64986770801ecf2a0b46f1b19d.png)
Холестаз – недостаточность выделения желчи, обусловленная нарушением ее выработки печеночными клетками (гепатоцитами) или прекращением тока желчи по желчным протокам вплоть до дуоденального сосочка. При холестазе наблюдаются уменьшение канальцевого тока желчи, печеночной экскреции воды и/или органических анионов (билирубина, желчных кислот), накопление желчи в гепатоцитах и желчевыводящих путях, задержка компонентов желчи в крови (желчных кислот, липидов, билирубина). Длительно сохраняющийся холестаз (в течение нескольких месяцев/лет) приводит к развитию билиарного цирроза печени [1, 2, 3, 4]. По анатомическому делению холестаз классифицируется как внутрипеченочный (интрапеченочный) и внепеченочный (экстрапеченочный).
К синдрому внутрипеченочного холестаза ведет нарушение жизненно важных функций образования и экскреции желчи под действием лекарств, инфекционных агентов, а также вследствие аутоиммунных, метаболических или генетических факторов. Причинами внепеченочного холестаза являются камни общего желчного протока, рак поджелудочной железы и фатерова соска, холангиокарцинома, доброкачественные стриктуры желчных протоков и инфекции желчных протоков. Доброкачественные стриктуры желчных протоков и холангиокарцинома могут являться причиной обструкции протоков при первичном склерозирующем холангите (ПСХ).
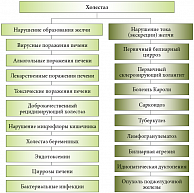
Диагностика внепеченочного холестаза, обусловленного обычно обструкцией внепеченочных желчных путей в результате аномалии развития, длительного спазма или наличия конкрементов, не вызывает значительных затруднений, тогда как для выявления внутрипеченочного холестаза требуется проведение комплекса исследований. Причины развития синдрома холестаза условно можно разделить на 2 группы: нарушение образования желчи и/или нарушение тока (экскреции) желчи (рис. 1).
У больных с холестазом в развернутой фазе происходит ряд гистологических изменений: расширение желчных капилляров; исчезновение микроворсинок на каналикулярной мембране; образование желчных тромбов в желчных капиллярах; повреждение клеточных мембран, ведущее к повышению их проницаемости; нарушение целостности плотных контактов и парацеллюлярная регургитация желчи в кровь; билирубиностаз, образование печеночных розеток; пролиферация дуктул в портальных трактах; перидуктальный отек и склероз; перипортальное и мезенхимальное воспаление; желчные инфаркты; развитие микроабсцессов; апоптоз; образование ксантомных клеток (рис. 2).
Этиология и механизмы развития холестаза
Этиология и механизмы развития холестаза многофакторны. Внепеченочный холестаз развивается при механической обструкции магистральных внепеченочных или главных внутрипеченочных протоков. Наиболее частой причиной внепеченочного холестаза являются камни общего желчного протока. Внутрипеченочный холестаз характеризуется уменьшением тока желчи и ее поступления в двенадцатиперстную кишку при отсутствии механического повреждения и обструкции внепеченочного билиарного тракта.
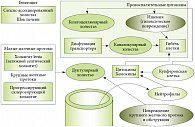
Внутрипеченочный холестаз может быть связан с нарушением механизмов образования и транспорта желчи на уровне гепатоцитов в результате гепатоцеллюлярной патологии, являться следствием повреждения внутрипеченочных протоков или их сочетанием. Соответственно, выделяют интралобулярный холестаз, обусловленный поражением гепатоцитов (гепатоцеллюлярный) и канальцев (каналикулярный), а также экстралобулярный (дуктулярный), связанный с поражением внутрипеченочных желчных междольковых протоков (рис. 3) [6, 7, 8].
Гепатоцеллюлярный и каналикулярный холестаз может быть обусловлен вирусными, алкогольными, лекарственными, токсическими поражениями печени, застойной сердечной недостаточностью, метаболическими нарушениями (доброкачественный возвратный внутрипеченочный холестаз, холестаз беременных, муковисцидоз, альфа-1-антитрипсиновая недостаточность). В патогенезе интралобулярного холестаза важную роль играет нарушение функций базолатеральной и каналикулярной мембран.
В основе этого явления могут лежать нарушения гепатобилиарного транспорта, такие как мутации генов белков-транспортеров и приобретенные дисфункции транспортных систем, обусловливающие нарушение каналикулярной или холангиоцеллюлярной секреции. Гепатоцеллюлярная аккумуляция токсических холефильных соединений вызывает множественные нарушения экспрессии гепатоцеллюлярных переносчиков. Кроме того, недостаток специфических компонентов желчи, вызываемый дисфункцией белков-переносчиков, раскрывает токсический потенциал других компонентов желчи.
Дуктулярный холестаз имеет место при первичном билиарном циррозе печени (ПБЦ), ПСХ и вторичном склерозирующем холангите (ВСХ), билиарной атрезии, болезни Кароли и других заболеваниях. При большинстве из перечисленных заболеваний наблюдается нарушение биохимических процессов в гепатоците, таких как трансметилирование и транссульфурирование (пересульфидирование). В результате угнетения реакций трансметилирования в гепатоцеллюлярных мембранах снижается содержание фосфолипидов, падает активность Na+-, К+-АТФазы и других белков-переносчиков, что нарушает текучесть мембран, а также захват и выведение компонентов желчи.
Нарушение реакций транссульфурирования уменьшает клеточные запасы тиолов и сульфатов (глютатиона, таурина и др.), которые являются главными детоксикационными субстанциями в отношении эндогенных и экзогенных ксенобиотиков, включая желчные кислоты, а также обладают выраженным антиоксидантным эффектом. Их дефицит обусловливает в конечном итоге цитолиз гепатоцитов при холестазах любого генеза. Дуктулярный холестаз развивается в результате повреждения эпителия желчных протоков и нарушения их проходимости, в ряде случаев с нарушением метаболизма желчных кислот, а также с изменением их состава.
Алгоритм дифференциальной диагностики холестатических заболеваний печени
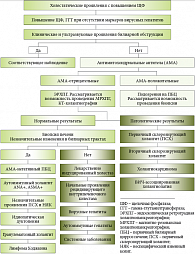
Различить виды холестаза по клиническим симптомам и биохимическим показателям не всегда возможно. Чрезвычайно важным является разграничение вне- и внутрипеченочного холестаза с использованием диагностического алгоритма. На рисунке 4 представлен алгоритм дифференциальной диагностики холестатических заболеваний с выявлением наличия маркеров аутоиммунных заболеваний печени: антимитохондриальные антитела (АМА), антинуклеарные антитела (ANA) и антитела к гладким мышечным клеткам (ASMA). Положительным результатом АМА считается титр выше 1:80 у женщин после 40 лет с ПБЦ, подтвержденным биопсией печени. При отрицательном результате АМА уточняется наличие положительного ответа на ANA с проведением эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ); при наличии клинических проявлений проводится магнитно-резонансная холангиопанкреатография (МРХПГ) и компьютерная томография (КТ). МРХПГ – это современная неинвазивная альтернатива ЭРХПГ.
Иногда для уточнения диагноза возможно их сочетание. КТ-холангиография также является неинвазивной технологией, она дает возможность визуализации билиарного дерева у 36% пациентов, которым невозможно провести другие инструментальные исследования. КТ-холангиография с введением внутривенного контраста имеет высокий риск побочных реакций, включающих анафилаксию и внезапную смерть, что ограничивает использование данной методики. При наличии выявленной патологии при холангиографии ПСХ и возможности ВИЧ-холангиопатии необходимо контролировать лабораторные и клинические тесты в динамике. При нормальных показателях ЭРХПГ проводится биопсия печени. Наличие незначительных изменений в билиарных трактах требует проведения дифференциальной диагностики между АМА-отрицательными пациентами с неизмененной холангиограммой и АМА-негативными пациентами с ПБЦ или аутоиммунным холангитом, проявляющимся наличием диагностического титра ANA и/или ASMA. Перспективы проведения биопсии печени зависят от поражений мелких желчных ходов при: ПСХ; идиопатической дуктопении; гранулематозном холангите; лимфоме Ходжкина [9]. Отсутствие изменений в мелких билиарных протоках требует дифференциальной диагностики таких заболеваний, как:
- лекарственный холестаз;
- рецидивирующий печеночный холестаз;
- вирусные гепатиты;
- аутоиммунные гепатиты;
- системные заболевания.
Лечение больных с холестазом
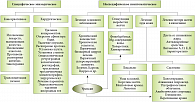
Лечение больных с холестазом можно разделить на специфическое эпизодическое и неспецифическое симптоматическое (рис. 5). Препаратом выбора при неспецифическом лечении больных с холестазом во многих случаях является урсодезоксихолевая кислота (УДХК) [9, 10, 11]. УДХК (Урсосан) – гидрофильная желчная кислота, которая с большой вероятностью имеет высокую эффективность, так как она снижает чувствительность мембран гепатоцита к токсичным воздействиям эндогенных гидрофильных желчных кислот. Она также уменьшает реабсорбцию желчных кислот в дистальном отделе подвздошной кишки и регулирует канальцевый транспорт, что объясняет снижение уровня билирубина в крови под ее влиянием (рис. 6). УДХК была изучена в начале 1980-х гг., и на сегодняшний день было проведено не менее 16 контролируемых рандомизированных клинических исследований по эффективности ее применения при заболеваниях печени. При холестатических заболеваниях печени различного генеза средняя суточная доза УДХК составляла 12–15 мг/кг веса. В зависимости от тяжести заболевания суточная доза увеличивалась до 20–30 мг/кг веса в 2–3 приема. Терапия проводилась от 6 месяцев до нескольких лет [10].
Механизмы действия препарата Урсосан
1. Антиапоптический. Урсосан посредством активации рецепторов эпидермального фактора роста вызывает в гепатоцитах реакции, направленные на выживание клетки, обусловливая, таким образом, антиапоптический эффект. Препарат тормозит выход цитохрома С из митохондрий и запуск каскада каспаз.
2. Антифибротический (предупреждает развитие фиброза печени):
- снижает высвобождение цитохрома С, щелочной фосфатазы и лактатдегидрогеназы;
- подавляет активность звездчатых клеток и перисинусоидальное коллагенообразование.
3. Антихолестатический (устраняет все виды внутрипеченочного холестаза):
- уменьшает концентрацию токсичных для печеночной клетки желчных кислот путем активации Ca-зависимой альфа-протеинкиназы и стимуляции экзоцитоза в гепатоцитах;
- индуцирует холерез, богатый бикарбонатами, что приводит к увеличению пассажа желчи и выведению токсичных желчных кислот через кишечник.
4. Гипохолестеринемический (снижает содержание холестерина в крови):
- снижает всасывание холестерина в кишечнике;
- уменьшает синтез холестерина в печени;
- снижает экскрецию холестерина в желчь.
5. Иммуномодулирующий (уменьшает аутоиммунные реакции против клеток печени и желчных путей и подавляет аутоиммунное воспаление):
- уменьшает экспрессию антигенов гистосовместимости: HLA-1 на гепатоцитах и HLA-2 на холангиоцитах;
- уменьшает образование сенсибилизированных к печеночной ткани цитотоксичных T-лимфоцитов, снижает «атаку» иммунокомпетентными Ig (в первую очередь IgM) клеток печени;
- снижает продукцию провоспалительных цитокинов (интерлейкинов ИЛ-1, ИЛ-2, ИЛ-6, ФНО-альфа, интерферона-гамма).
6. Литолитический (растворяет холестериновые камни в желчном пузыре, предупреждает образование новых конкрементов):
- снижает литогенность желчи;
- стимулирует выход холестерина из камней в желчь.
7. Холеретический (усиливает секрецию желчи):
- стимулирует экзоцитоз в гепатоцитах;
- индуцирует бикарбонатный холерез, усиливает выведение гидрофобных ЖК в кишечник.
8. Цитопротективный (защищает клетки желчных протоков и эпителиоциты слизистой оболочки желудка и кишечника от агрессивных факторов):
- встраивается в клеточные мембраны холангиоцитов и эпителиоцитов, стабилизируя их структуру;
- образует смешанные мицеллы с токсичными желчными кислотами (хенодезоксихолевой, литохолевой, дезоксихолевой) и предупреждает их повреждающее действие на клетки.
Таким образом, патофизиологические механизмы развития холестаза многофакторны и взаимосвязаны между собой, диагностика холестатических заболеваний печени может осуществляться по предложенному алгоритму, в основу которого заложен принцип пошагового исключения наиболее вероятных причин возникновения холестатических заболеваний. Успех лечения больных с холестазом зависит от своевременно поставленного диагноза и применения лекарственных препаратов первого выбора, позволяющих устранить или ослабить патогенетические механизмы развития холестаза. Наиболее изученными и часто применяемыми для лечения больных с холестазом являются препараты урсодезоксихолевой кислоты, к числу которых относится Урсосан.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.