Клинические и фармакоэкономические преимущества цефподоксима перед цефтриаксоном в терапии пациентов с острым бактериальным риносинуситом
- Аннотация
- Статья
- Ссылки
- English
Введение
В последние годы в мире происходят колоссальные изменения во многих сферах жизни, в частности в медицине. Пандемия SARS-CoV-2 постепенно уходит в историю, но ее последствия ощущаются до сих пор. Она продемонстрировала важность серьезного отношения к заболеваниям лор-органов и дыхательной системы в целом, способствовала повышению потребления антибиотиков на фоне присоединения бактериальных осложнений [1]. Пандемия сопровождалась нерациональным применением системных антибиотиков во всем мире при вирусной патологии. Как следствие – резкий рост антибиотикорезистентности. Подобная тенденция наблюдалась и в нашей стране. Антибиотики остаются одними из самых востребованных лекарственных препаратов, применяемых в современной медицине. Медицинская и социальная значимость инфекций, их склонность к эпидемическому распространению предъявляют высокие требования к эффективности и безопасности антибактериальной терапии.
Разработка новых антимикробных препаратов представляет сложную задачу из-за многообразия механизмов резистентности и риска возникновения в процессе этой разработки новых механизмов устойчивости. В связи с этим появление на российском фармацевтическом рынке цефподоксима проксетила (Доксеф), широко используемого в Европе, открывает клиницистам дополнительные возможности эффективной антибактериальной терапии.
Препарат Доксеф (цефподоксима проксетил) – таблетированный цефалоспорин третьего поколения, высокоактивен против всех основных возбудителей инфекций дыхательных путей и включен в международные клинические рекомендации по лечению респираторных инфекций, в том числе острого бактериального риносинусита [2]. Спектр антибактериальной активности Доксефа аналогичен спектру парентерального цефалоспорина третьего поколения – цефтриаксона. Доксеф характеризуется длительным периодом полувыведения, что позволяет принимать его два раза в день. Цефподоксима проксетил доказал свою эффективность при внебольничной пневмонии и инфекциях верхних дыхательных путей, кожи, мягких тканей и мочевыводящих путей. Препарат оценивали для использования в программах снижения затрат, в качестве понижающей терапии (переход с парентеральной на пероральную) при внебольничной пневмонии и в качестве сокращенной терапии при инфекциях верхних дыхательных путей [3, 4]. Замена парентеральной терапии пероральной может обеспечить значительную экономию затрат на приобретение, доставку и рабочую силу. Более того, пероральный прием удобен с точки зрения комфорта и мобильности, позволяет избежать опасностей, связанных с парентеральным введением, обеспечивает более раннюю выписку из стационара или даже домашнее лечение у пациентов с низким риском осложнений. Поскольку госпитализация обычно является основным компонентом затрат при лечении серьезных инфекций, используя Доксеф, можно добиться значительной экономии. Имеющиеся на сегодняшний день данные свидетельствуют о том, что цефподоксима проксетил потенциально может применяться в качестве понижающей терапии при внебольничной пневмонии и в сокращенных курсах терапии инфекций верхних дыхательных путей [3, 4]. Следует отметить, что цефподоксима проксетил в дозе 200 мг легко всасывается после приема внутрь и достигает уровней в плазме и тканевой жидкости, превышающих уровень минимальной подавляющей концентрации для 90% штаммов всех основных возбудителей респираторных инфекций [5–8].
Пероральный прием лекарственных средств технически проще парентерального введения. Бытовавшее долгое время во врачебной среде мнение о более высокой эффективности парентеральных форм антимикробных препаратов в последнее время опровергнуто результатами исследований и опытом применения современных лекарственных форм. Таблетированные формы цефалоспоринов третьего поколения имеют ряд преимуществ перед инъекционными [9]. Пероральные цефалоспорины значительно удобнее для пациентов. Их можно принимать в домашних условиях без необходимости посещения медицинского учреждения для выполнения инъекций. Это особенно важно для амбулаторных пациентов, поскольку позволяет снизить нагрузку на медицинские учреждения и минимизировать риск инфекций, связанных с инвазивными процедурами [10, 11]. При использовании инъекционных форм существует риск инфицирования в месте инъекции или возникновения других осложнений, связанных с введением иглы. Таблетированные формы препаратов полностью устраняют этот риск. Кроме того, значительная часть пациентов испытывают трудности с соблюдением режима лечения, особенно при назначении инъекций. Пероральные формы более удобны для соблюдения регулярного приема, что может способствовать достижению лучших клинических результатов [12]. По сравнению с парентеральными формами пероральные цефалоспорины могут оказаться более экономичными для системы здравоохранения и пациентов. Они не требуют специального оборудования для хранения и введения, что позволяет существенно сократить затраты на лечение [13]. Пероральные цефалоспорины, как правило, имеют лучшее соотношение пользы и риска по сравнению с парентеральными формами, менее агрессивны для организма человека и реже приводят к серьезным побочным эффектам, что делает их более предпочтительными, особенно у детей и пожилых пациентов [14].
С учетом вышеизложенного на кафедре оториноларингологии Российского университета медицины было решено провести исследование эффективности антибактериального препарата Доксеф у больных острым бактериальным синуситом.
Цель – оценить клиническую и микробиологическую эффективность, переносимость и безопасность препаратов цефтриаксон и цефподоксим (Доксеф) у пациентов с острым бактериальным риносинуситом средней степени тяжести.
Задачи исследования включали:
- анализ эффективности препаратов цефтриаксон и цефподоксим (Доксеф) в лечении больных острым бактериальным риносинуситом средней степени тяжести;
- определение степени бактериологической эрадикации при лечении больных острым бактериальным риносинуситом средней степени тяжести препаратами цефтриаксон и цефподоксим (Доксеф);
- оценку переносимости, удовлетворенности и комплаентности пациентов при лечении препаратами цефтриаксон и цефподоксим (Доксеф);
- определение частоты и выраженности нежелательных явлений у пациентов при лечении препаратами цефтриаксон и цефподоксим (Доксеф).
Материал и методы
В наблюдательное сравнительное исследование были включены пациенты в возрасте 18–65 лет с установленным диагнозом острого риносинусита средней степени тяжести, предположительно бактериальной этиологии.
Первую (основную) группу составили 30 больных, находившихся на лечении в консультативно-диагностическом центре (амбулаторные условия). Пациентам данной группы назначали перорально цефподоксим (Доксеф) 200 мг одна таблетка два раза в день в течение семи дней, местно сосудосуживающие, при необходимости – жаропонижающие и обезболивающие средства.
Вторую (контрольную) группу представляли 30 пациентов, находившихся на лечении в дневном стационаре. Пациенты данной группы получали внутримышечно цефтриаксон 1 г + 0,9%-ный раствор NaCl 3,6 мл один раз в день в течение семи дней, местно сосудосуживающие, при необходимости – жаропонижающие и обезболивающие средства.
График исследования включал в себя первичное обследование (сбор анамнеза и жалоб больного, оценку клинических проявлений заболевания), использование инструментальных методов исследования, рентгенографию околоносовых пазух с учетом критериев включения и исключения из исследования, забор биоматериала со слизистой оболочки полости носа для определения микрофлоры и ее чувствительности к антибиотикам, заполнение опросника SNOT-22, назначение терапии в соответствии с группой наблюдения. Все участники исследования подписали согласие на участие в нем. Затем проводилась терапия заболевания в соответствии с группой наблюдения в течение семи дней с промежуточным обследованием на 3 ± 1 день наблюдения. Промежуточное обследование включало анализ клинических показателей проявлений заболевания, объективную оценку состояния пациента, заполнение опросника SNOT-22. На контрольном обследовании на 7 ± 1 день проводились анализ клинических показателей проявлений заболевания, объективная оценка состояния, повторный забор биоматериала со слизистой оболочки полости носа для определения микрофлоры и ее чувствительности к антибиотикам, заполнение опросника SNOT-22. Кроме того, на 14 ± 2 день лечения был осуществлен заключительный телефонный контакт для уточнения информации об отсутствии рецидивов у пациентов. На всех этапах исследования оценивали переносимость препаратов цефтриаксон и цефподоксим (Доксеф), описывали характер побочных явлений при их наличии.
Результаты
Распределение больных в группах было сопоставимо по половозрастным характеристикам. Семь пациентов (трое из основной и четверо из контрольной группы) были выведены из исследования из-за отсутствия положительной динамики и необходимости смены антибактериальной терапии. Во всех случаях при бактериологическом исследовании отделяемого из верхнечелюстных пазух, полученного при лечебно-диагностической пункции на визите в 1-й день, была выявлена Pseudomonas aeruginosa. Данные клинической (опросники качества жизни, результаты риноскопии) и микробиологической эффективности терапии этих пациентов не учитывались. Таким образом, итоговый расчет всех показателей выполнялся в отношении 27 пациентов основной и 26 пациентов контрольной группы.
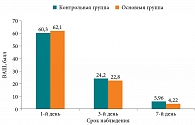
На фоне проводимого лечения положительная динамика самочувствия пациентов по визуальной аналоговой шкале (ВАШ) отмечалась в обеих группах уже ко второму визиту (3-й день лечения). Данные в зависимости от визита и группы наблюдения представлены на рис. 1.
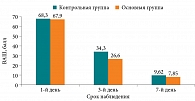
Кроме того, использовали опросник Sino-Nasal Outcome Test (SNOT-22) из 22 пунктов для количественной оценки качества жизни (психосоциальных последствий, симптомов назальной обструкции, продолжительности и выраженности клинических проявлений) при синуситах и ринитах, а также результатов терапии. Для этого больные заполняли опросники на визитах в дни 1, 3 и 7. Баллы, полученные при анализе опросников, распределились следующим образом: 0–29 баллов – не беспокоит/незначительно беспокоит; 30–69 баллов – слегка/умеренно беспокоит; 70–100 баллов – значительно беспокоит. Полученные результаты отображены на рис. 2.
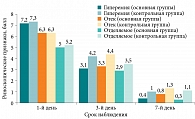
При объективном осмотре пациентов также фиксировались изменения слизистой оболочки полости носа по балльной системе. Гиперемия, отечность слизистой оболочки и наличие гнойного отделяемого оценивались от 0 (отсутствие признака) до 9 (сильно выражен) баллов (рис. 3).
Всем пациентам в 1-й и 7-й дни выполнялись лечебно-диагностическая и диагностическая пункции соответственно. Это требовалось как для окончательного подтверждения диагноза (1-й день), так и для забора биоматериала непосредственно из верхнечелюстных пазух (1-й и 7-й дни). Данные представлены на рис. 4 и 5.
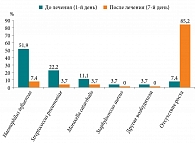
Результаты микробиологического исследования на первом визите, день 0 (1):
- основная группа: Haemophilus influenzae (51,9%), Streptococcus pneumoniae (22,2%), Moraxella catarrhalis (11,1%), Staphylococcus aureus (3,7%), другие возбудители (3,7%). Роста патогенной микрофлоры не выявлено в 7,4% случаев;
- контрольная группа: H. influenzae (46,2%), S. pneumoniae (19,2%), S. aureus (15,4%), M. сatarrhalis (7,7%). Роста патогенной микрофлоры не выявлено в 11,5% случаев.
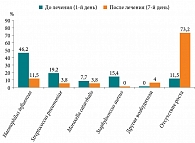
Повторный забор отделяемого из полости носа:
- основная группа: H. influenzae (7,4%), S. pneumoniae (3,7%), M. catarrhalis (3,7%). Роста патогенной микрофлоры не выявлено в 85,2% случаев;
- контрольная группа: H. influenzae (11,5%), S. pneumoniae (3,8%), M. catarrhalis (7,7%), другие возбудители (3,8%). Роста патогенной микрофлоры не выявлено в 73,2% случаев.
Необходимо отметить, что пациенты основной группы принимали таблетированные формы цефподоксима (Доксеф) (перорально), тогда как пациенты контрольной получали цефтриаксон в инъекциях (внутримышечно). В отношении микробиологической эффективности препарата Доксеф и цефтриаксона у пациентов с острым бактериальным риносинуситом установлена существенная разница – 85,2 и 73,2% соответственно. К тому же пациенты основной группы были более привержены терапии, поскольку таблетированная форма препарата наиболее комфортна. Внутримышечное введение препарата в амбулаторных условиях сопряжено с дополнительными временными и финансовыми затратами, а иногда невозможно и требует госпитализации в стационар без абсолютных к тому показаний.
У пациентов обеих групп не зафиксировано нежелательных явлений или побочных эффектов. Все пациенты соблюдали кратность и длительность приема назначенных препаратов: в основной группе – в условиях амбулаторного лечения, в контрольной – в условиях стационара.
Следует отметить и такой немаловажный аспект, как очевидное экономическое преимущество при использовании таблетированной формы при амбулаторном режиме лечения перед парентеральным применением препарата в условиях стационара. Это можно обосновать так: сутки нахождения в стационаре в среднем обходятся в 2900 руб. (в зависимости от клиники: 1500–5000 руб/сут), продолжительность пребывания – 5–6 дней. В то же время стоимость одной упаковки препарата Доксеф составляет 1044 руб., хотя может понадобиться две упаковки. Кроме того, к затратам следует отнести покупку нестероидных противовоспалительных препаратов (ибупрофена или парацетамола – 142,6 руб.) и местных деконгестантов (198 руб.) [15]. Подобное сравнение, безусловно, не претендует на точный экономический анализ, тем не менее дает четкое представление о реальных затратах при выборе той или иной схемы антибактериальной терапии при остром неосложненном синусите.
Выводы
Анализ результатов сравнительного наблюдательного исследования, проведенного на клинических базах кафедры оториноларингологии Российского университета медицины, продемонстрировал преимущество Доксефа перед цефтриаксоном у пациентов с острым бактериальным риносинуситом. На фоне применения Доксефа отмечалось быстрое улучшение самочувствия пациентов (уже на 3-й день лечения), что подтверждалось оценкой по ВАШ и SNOT-22. Данные, полученные при риноскопическом исследовании, подтвердили субъективное мнение пациентов и продемонстрировали быстрое купирование воспалительных изменений в полости носа, таких как отечность и гиперемия слизистой оболочки, а также уменьшение количества патологического отделяемого из полости носа.
На фоне применения препарата Доксеф зафиксирована высокая приверженность лечению, нежелательных явлений или побочных эффектов не наблюдалось.
Анализ результатов микробиологического исследования отделяемого из полости верхнечелюстных пазух, полученного путем пункции, показал высокую способность препарата Доксеф к эрадикации возбудителей, которые являются причиной развития бактериальных синуситов. Микробиологическая эффективность Доксефа составляет 85,2%, цефтриаксона – 73,2%.
Доксеф характеризуется высокой клинической и микробиологической эффективностью и безопасностью. Таблетированная форма препарата повышает приверженность пациентов лечению. Возможность приема препарата в амбулаторных условиях позволяет снизить нагрузку на стационар и экономические затраты на лечение пациентов с острым бактериальным риносинуситом.
Наглядно показано, что Доксеф – первый пероральный цефалоспорин с инъекционной эффективностью, который является удобной и экономически выгодной альтернативой цефтриаксону.
A.Yu. Ovchinnikov, PhD, Prof., N.A. Miroshnichenko, PhD, Prof., Yu.O. Nikolaeva, PhD, V.A. Ryabinin, PhD
Russian University of Medicine
Contact person: Andrey Yu. Ovchinnikov, lorent1@mail.ru
Antibiotics remain one of the most in-demand medicines used in modern medicine. The SARS-CoV-2 pandemic demonstrated the importance of taking diseases of the ENT organs and the respiratory system in general seriously, contributed to an increase in the consumption of antibiotics against the background of bacterial complications, as well as a sharp increase in antibiotic resistance due to the irrational and uncontrolled use of these drugs. The development of new antimicrobial drugs is a difficult task due to the variety of resistance mechanisms and the risk of new resistance mechanisms in the process of their development. In this regard, the appearance of cefpodoxime proxetil (Doxcef) on the Russian pharmaceutical market, which is widely used in Europe, opens up additional opportunities for clinicians for effective antibacterial therapy. The drug Doxef (cefpodoxime proxetil) is a tablet cephalosporin of the third generation, is highly active against all major pathogens of respiratory tract infections and is included in international clinical guidelines for the treatment of respiratory infections, including acute bacterial rhinosunusitis. Oral administration has advantages for the patient in terms of comfort and mobility, avoids the dangers associated with parenteral administration, provides earlier discharge from the hospital and even home treatment in patients with a low risk of complications, is more convenient to follow regular intake, which can guarantee better clinical results. At the same time, the use of Doxcef in patients with acute bacterial rhinosinusitis was accompanied by a higher result in terms of microbiological efficacy compared with ceftriaxone – 85.2 and 73.2%, respectively. This essentially demonstrates the effectiveness of an injectable drug in oral form.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.