количество статей
7385
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Новые возможности комплексной терапии аллергодерматозов
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Дерматология" №3
- Аннотация
- Статья
- Ссылки
Связь аллергических заболеваний кожи с патологией пищеварительной, нервной и эндокринной систем известна давно и подтверждена многочисленными научными исследованиями и клинической практикой. Установлено, что активная антигенная стимуляция, которой постоянно подвергается организм современного человека, активнее трансформируется из моновалентной в поливалентную при сопутствующих и многочисленных нарушениях в деятельности желудочно-кишечного тракта (ЖКТ).
Кожа является зеркалом нашего организма и отражает любое его неблагополучие. Известно, что кожа, а также нервная система, передний и задний отделы кишечника, органы чувств образуются из одного зародышевого листка – эктодермы, что и обуславливает их тесную функциональную взаимосвязь.
Наиболее распространенными заболеваниями в практике дерматолога являются аллергодерматозы. По данным государственного научного центра РФ «Институт иммунологии», в общей структуре аллергических заболеваний кожные аллергозы составляют 20%, а в структуре аллергопатологии детского возраста занимают от 50 до 66,4% и представлены в основном атопическим дерматитом. Проблема аллергических заболеваний кожи становится все более и более актуальной, поскольку отмечается рост предрасположенности населения к аллергическим заболеваниям, особенно среди жителей мегаполисов. Основными причинами роста аллергизации населения являются неблагоприятная экологическая обстановка, нерациональное питание и образ жизни, стрессовый фактор, бесконтрольное использование лекарственных и косметических средств, активное применение в быту средств бытовой химии и т.д. (1).
Не вызывает также сомнений, что ЖКТ и кожа играют важную роль в поддержании постоянства внутренней среды организма. Следовательно, нарушение барьерной функции кишечника, приводящее к повышенной эндотоксинемии, аллергизации и нарушению гомеостаза, может отразиться на состоянии кожи и течении дерматозов.
Таким образом, современные терапевтические схемы лечения дерматологических заболеваний должны быть комплексными с учетом всех изменений в организме в целом. Поэтому одним из компонентов успешного лечения аллергодерматозов является применение методов детоксикации. Известно, что энтеросорбция является неинвазивным методом детоксикации, используемым для выведения из организма аллергенов, продуктов аллергической реакции, различных эндогенных и экзогенных соединений, патогенных микроорганизмов и продуктов их жизнедеятельности. Современные энтеросорбенты должны соответствовать следующим основным медицинским требованиям: не обладать токсическими свойствами; быть нетравматичными для слизистых оболочек; хорошо эвакуироваться из кишечника; иметь хорошие функциональные (сорбционные) свойства; не вызывать дисбактериозов; иметь удобную лекарственную форму (2).
Установлено, что на фоне энтеросорбции происходит повышение функциональной активности клеточного и гуморального иммунитета, увеличивается число Т-лимфоцитов, уменьшается выраженность эозинофилии, снижается уровень ЦИК, уменьшается интенсивность зуда и отечность кожи. Существенным является и то, что сорбенты позволяют уменьшить дозу лекарственных препаратов и в частности глюкокортикоидных гормонов. Энтеросорбенты, находясь в просвете кишечника, связывают токсические вещества, не давая им всасываться и попадать в кровяное русло, что значительно уменьшает уровень интоксикации и аллергизации организма в целом.
Количество токсических веществ, проникающих из просвета кишечника в кровь, зависит от состояния слизистой оболочки кишечника (энтерогематического барьера). Эффективность энтеросорбционной терапии определяется характером взаимодействия энтеросорбента с энтерогематическим барьером. Обладая сорбционной активностью к субстратам, повреждающим энтерогематический барьер (деконъюгированные желчные кислоты, токсины бактерий и др.), сорбент в то же время должен иметь ограниченный спектр сорбируемых веществ, т.е. отличаться селективностью сорбционного действия. Так, продолжительное использование сорбента, способного связывать крупномолекулярные субстраты, например секреторный IgA, может привести к нарушению иммунного компонента энтерогематического барьера.
Большое значение имеет пористость сорбента (наличие пор между слоями, зернами, кристаллами). Сорбенты могут иметь микро-, макро- и мезопоры. Выбор сорбента с различной пористой структурой влияет на адсорбцию тех или иных токсинов и патогенов, а также определяет терапевтическую эффективность препарата (3, 4).
Энтеросорбенты различаются по ряду признаков. Прежде всего, по лекарственной форме (гранулы, порошки, таблетки, пасты, гели и др.); селективности и механизму сорбции (адсорбенты, абсорбенты, ионообменные материалы, сорбенты с сочетанным механизмом действия, сорбенты с каталитическими свойствами). Они отличаются и по химической структуре (углеродные энтеросорбенты, энтеросорбенты на основе природных и синтетических смол, синтетических полимеров и неперевариваемых липидов, кремнийсодержащие энтеросорбенты. В последнее время наиболее активно используются природные органические сорбенты на основе пищевых волокон, гидролизного лигнина, хитина, пектинов и альгинатов, а также комбинированные энтеросорбенты, имеющие в составе два и более типов вышеуказанных сорбентов (4).
Для современной общемедицинской практики, в частности для дерматологической, особый интерес представляют сорбенты, в состав которых включен пребиотик. К таким препаратам относится Лактофильтрум – растительный энтеросорбент с иммуномодулирующим действием. Лактофильтрум содержит пребиотик (лактулозу) и сорбент (лигнин). Свойства Лактофильтрума обусловлены высокой сорбционной способностью природного энтеросорбента на основе лигнина.
Лигнин гидролизный – сложное природное органическое соединение, продукт гидролизной переработки древесины. Он обладает неспецифическим дезинтоксикационным действием. Связывает, удерживает и выводит из организма различную патогенную микрофлору, экзо- и эндотоксины, лекарственные препараты, соли тяжелых металлов, алкоголь, аллергены, избыток некоторых продуктов обмена веществ (билирубина, холестерина, гистамина, серотонина, мочевины, иных метаболитов, ответственных за развитие эндогенного токсикоза). За счет большой площади поверхности и развитой системы пор лигнин обладает высокой сорбционной емкостью. Лигнин не токсичен, не всасывается, полностью выводится из кишечника в течение 24 часов.
Второй компонент Лактофильтрума – лактулоза – синтетический дисахарид, состоящий из остатка галактозы и остатка фруктозы. В толстом кишечнике лактулоза ферментируется нормальной микрофлорой кишечника в качестве пищевого субстрата. Лактулоза стимулирует рост бифидобактерий и лактобактерий в толстом кишечнике, способствует нормализации обмена белков, жиров и углеводов, способствует правильному всасыванию витаминов, макро- и микроэлементов, а также стимулирует неспецифический иммунитет. В результате гидролиза лактулозы образуются органические кислоты (молочная, уксусная и муравьиная), подавляющие рост патогенных микроорганизмов и уменьшающие вследствие этого продукцию азотсодержащих токсических веществ. Описанный процесс приводит к увеличению осмотического давления в просвете толстого кишечника и стимулированию перистальтики. Лактулоза не усваивается в кишечнике и полностью выводится из человеческого организма.
Преимущество препарата Лактофильтрум заключается в его двойном действии:
- сорбент нейтрализует патогенные микроорганизмы и выводит кишечные токсины и аллергены;
- пребиотик стимулирует рост бифидо- и лактобактерий.
Комплексное воздействие компонентов Лактофильтрума приводит к нормализации микробиоциноза кишечника, исчезновению симптомов аллергизации и интоксикации организма и, следовательно, к повышению ответа на терапию при аллергодерматозах. Препарат можно назначать с грудного возраста. Длительность одного курса лечения составляет 2 недели. Интервал между приемом Лактофильтрума и других лекарственных средств должен быть не менее 1 часа. При регулярном или постоянном приеме рекомендуется следующая последовательность: 2 недели приема Лактофильтрума, затем 1 неделя приема витаминов группы В, после чего цикл снова повторяется.
В работе В.А. Ревякиной показана клиническая эффективность Лактофильтрума в комплексном лечении тяжелой и среднетяжелой формы атопического дерматита (АД) у детей. Под наблюдением находилось 36 детей (20 девочек и 16 мальчиков) в возрасте от 2 до 5 лет, с длительностью заболевания от 1 до 4,5 лет. В основную группу были включены 26 детей, в контрольную – 10. Препарат назначали внутрь 3 раза в день между приемами пищи в следующей дозировке: от 2 до 3 лет – по 1/2 таблетки 3 раза в день, от 3 до 5 лет – 1 таблетка 3 раза в день, в течение 14 дней. Было выявлено, что включение в комплексную терапию энтеросорбента Лактофильтрум значительно повышает эффективность лечения. Так, индекс SCORAD при среднетяжелом течении АД снизился с 38,4 ± 1,8 до 14,6 ± 2,1 балла, а при тяжелой форме АД с 56,5 ± 1,5 до 28,4 ± 1,4 балла, а курсовое использование препарата также позволило сократить период обострения и продлить ремиссию в среднем на 4,6 ± 2,3 месяца, по сравнению 2,9 ± 1,8 месяца в группе контроля. Побочных эффектов на фоне приема выявлено не было.
В другом исследовании этого же автора была подтверждена клиническая эффективность Лактофильтрума лечении 30 детей с АД и сопутствующей патологией ЖКТ в возрасте от 3 до 15 лет. Применение препарата в составе комплексной терапии приводило к ускоренному улучшению кожного статуса (уменьшение гиперемии, сухости, зуда кожи), нормализации функции ЖКТ (5, 6).
На кафедре дерматовенерологии и дерматоонкологии МОНИКИ им. М.Ф. Владимирского было проведено исследование, посвященное оценке влияния Лактофильтрума на состав стафилококков как на один из основных условно-патогенных представителей микробиоценоза кожи. В исследовании приняли участие 60 здоровых женщин в возрасте от 25 до 27 лет (в среднем 25,6 года), которые были разделены на основную и контрольную группу. Материалом исследования являлись соскобы с кожи. Забор материала проводили одноразовыми скарификаторами, далее проводили количественную оценку репрезентативных представителей методом аграрных отпечатков стафилококка, посева и инкубацию в термостате. Выросшие колонии подсчитывали и окрашивали по Граму. По числу выросших колоний определяли уровень аутомикрофлоры кожи (АМФК). В результате исследования было обнаружено, что у 17 женщин (9 из основной и 8 из контрольной группы) отмечается повышенный уровень АФМК. После приема Лактофильтрума (2 таблетки 3 раза в день за 1,5 часа до еды) в основной группе у 7 женщин произошла нормализация микрофлоры кожи, и только у 2 женщин уровень АФМК остался повышенным. У всех женщин из контрольной группы снижения колониеобразующих единиц St. aureus отмечено не было. Препарат больными переносился хорошо, побочных эффектов отмечено не было. Полученные данные свидетельствуют о нормализации количества колониеобразующих единиц St. aureus, отражающие коррекцию аутомикрофлоры здоровой кожи (Лактофильтрум нормализует АМФК более чем у 80% женщин) после приема Лактофильтрума (7).
Калюжная Л.Д. и соавт. применяли Лактофильтрум в терапии АД у 26 детей в возрасте от 6 месяцев до 18 лет. У 21 больного АД был представлен среднетяжелой формой (индекс SCORAD от 24 до 62 баллов). Тяжелое течение на момент госпитализации было отмечено у 5 больных (индекс SCORAD более 62 баллов). Дети до 3 лет получали Лактофильтрум по 1/2 таблетки 3 раза в сутки, в возрасте от 3 до 12 лет – по 1 таблетке 3 раза в сутки, а в старшей группе – по 2 таблетки 3 раза в день. Препарат назначали за 1-1,5 часа до еды. Курс приема составлял 10-14 дней. На фоне приема препарата происходила нормализация диспепсических явлений, отмечалась положительная динамика кожного процесса в виде активного регресса воспалительных симптомов и зуда. После лечения у всех пациентов отмечалось существенное снижение индекса SCORAD (ниже 24 баллов), т.е. переход процесса в легкое течение, с полным регрессом субъективных ощущений. Побочных явлений выявлено не было (8).
Нами было проведено исследование эффективности и безопасности препарата Лактофильтрум в комплексной терапии аллергодерматозов. Под наблюдением находилось 26 пациентов в возрасте от 18 до 45 лет (12 мужчин и 14 женщин). По диагнозам больные распределялись следующим образом: АД – 10 человек, экзема – 10 пациентов с преимущественной локализацией в области кистей и стоп, крапивница – 6 человек. Средний возраст пациентов составил 28,6 лет. У больных с АД процесс локализовался в области лица, шеи, предплечий, локтевых сгибов, тыла кистей и подколенных ямках и характеризовался умеренной островоспалительной реакцией (эритема, шелушение, легкая инфильтрация) и зудом. У пациентов с экземой процесс носил подостровоспалительный характер. У 7 больных локализовался в области кистей и стоп, у 3 пациентов затрагивал туловище, проявляясь в основном эритемой застойного характера, экскориациями, шелушением и умеренным зудом, у 4 пациентов экзематозный процесс осложнился присоединением вторичной инфекции. Крапивница у всех исследуемых носила острый характер, появляясь уртикарными высыпаниями и сильным зудом. Помимо кожной симптоматики пациенты предъявляли жалобы со стороны ЖКТ (изжогу, запоры, метеоризм и др.). Пациенты в каждой нозологической группе были разделены на две одинаковые по количеству больных группы – основную и контрольную. В основной группе помимо традиционной противоаллергической и противовоспалительной терапии назначали Лактофильтрум по 2 таблетки 3 раза в день за 1-1,5 часа до еды. Длительность курса приема препарата составила 14 дней. В контрольной группе проводили лечение без энтеросорбента.
Включение препарата Лактофильтрум в состав комплексной терапии у пациентов основной группы позволило в более короткие сроки существенно уменьшить выраженность клинической симптоматики. Кожные проявления и зуд регрессировали быстрее на фоне приема препарата, также отмечалась нормализация большинства имеющихся нарушений со стороны ЖКТ. У пациентов из группы контроля процесс выздоровления происходил гораздо медленнее и сопровождался сохранением гастроэнтерологических жалоб. В основной группе в среднем у больных с АД улучшение кожного процесса можно было наблюдать на 9 день лечения, с экземой – на 7, с крапивницей – на 5. У больных группы контроля, улучшение кожного процесса наблюдалось соответственно на 14, 12 и 10 день лечения. Побочных эффектов при приеме препарата нами выявлено не было, все больные переносили лечение хорошо.
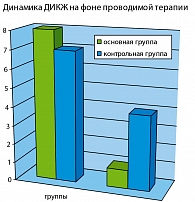
Пациенты также были протестированы по опроснику ДИКЖ (Finlay, русифицирован Н.Г Кочергиным, 2001) для оценки качества жизни до и после проведенной терапии. У всех пациентов до лечения было выявлено повышение баллов по ДИКЖ (в среднем 7,45 ± 1,8), что отражает снижение качества жизни. После лечения в основной группе все пациенты отмечали улучшение качества жизни, что отразилось в регрессе баллов по шкале ДИКЖ, в среднем показатели ДИКЖ снизились более чем в 4 раза и составили 1 ± 0,09 балла. В контрольной группе только треть больных на фоне проводимой терапии отметили повышение качества жизни в 1,5 раза (см. рисунок).
На основании проведенных исследований можно сделать следующие выводы:
- Лактофильтрум является высокоэффективным и безопасным препаратом, существенно расширяющим возможности терапии аллергодерматозов.
- Включение препарата в состав комплексной терапии приводит к более быстрому регрессу кожных высыпаний и субъективных ощущений, нормализации функции ЖКТ, что способствует существенному улучшению качества жизни.
- Препарат не токсичен, не вызывает побочных эффектов, удобен в применении и дозировании (таблетированная форма выпуска).
1. Данилычева И.В., Ильина Н.И. Аллергические поражения кожи: крапивница и атопический дерматит. Журн. постдипл. образов. для провизора. 2001; Т. 1, №2: 10-13.
2. Боткина А.С., Бельмер С.В. Дерматологические проявления заболеваний ЖКТ. Материалы XIV Конгресса детских гастроэнтерологов России. М., 2007.
3. Нагорная Н.В., Лимаренко М.П. Энтеросорбция в педиатрической практике: выбор оптимального сорбента. Медицина сегодня. 2010; 11-12 (331-332).
4. Применение метода энтеросорбции в практической медицине // Сборник клинических исследований препаратов Фильтрум-СТИ и Лактофильтрум. Часть III: Аллергология. Дерматология. Нефрология. Профессиональная патология. Наркология. М., 2006. 24 с.
5. Ревякина В.А. Энтеросорбенты в комплексной терапии атопического дерматита у детей // Эффективная фармакотерапия в дерматовенерологии и дерматокосметологии. 2010; №2: 14-16.
6. Ревякина В.А. Энтеросорбенты в терапии аллергических заболеваний у детей. М., 2010.
7. Молочков В.А., Караулов А.В., Николаева С.А. Лактофильтрум как фактор повышения бактерицидной функции кожи // Эффективная фармакотерапия в дерматовенерологии и дерматокосметологии. 2010; №1: 32-34.
8. Калюжная Л.Д., Милорава Т.Т., Турик Н.В. и др. Новый пребиотик в комплексной терапии атопического дерматита у детей. Применение метода энтеросорбции // Искусство лечения. 2006; 10(36).
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.