Оптимизация терапии пациентов с гипертрофическими рубцами
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – оценить эффективность комплексного применения внутриочагового введения ботулинического токсина типа А (БТА) и лазерной терапии с применением некогерентного широкополосного света (IPL) для лечения ГР сроками до одного года с помощью ультразвукового исследования, а также оценить клиническую эффективность комбинированного метода лечения с учетом динамики показателей японской шкалы исследования рубцов (JSS), визуальной аналоговой шкалы (ВАШ) и результатов общего осмотра.
Материал и методы. Под наблюдением в амбулаторных условиях находились 15 пациентов с ГР сроками существования до одного года. Среди них было 10 (67%) женщин и 5 (33%) мужчин в возрасте от 24 до 40 лет, длительность существования рубцов составляла от шести месяцев до одного года. Всем пациентам проводили внутриочаговое введение БТА в комбинации с применением некогерентного широкополосного света (IPL). Для оценки результатов использовали JSS, ВАШ, определяли толщину и эхогенность тканей патологического рубца с помощью ультразвукового исследования.
Результаты. Данные ультразвукового сканирования показали выраженную положительную динамику по сравнению с исходным уровнем. Достигнуто общее снижение значений показателей JSS и ВАШ. После проведенного комплексного лечения отмечалось уменьшение интенсивности окраски, размягчение, оседание рубцовых деформаций, значительное уменьшение выраженности субъективных ощущений. Ни у одного из испытуемых не было отмечено каких-либо побочных или нежелательных явлений от проведенного лечения.
Заключение. Комплексное лечение, включающее внутриочаговое введение БТА и лазерную терапию с применением IPL, оказалось эффективным. На фоне проводимой терапии отмечалось как улучшение эстетического вида гипертрофических рубцовых деформаций, так и уменьшение выраженности субъективных ощущений у пациентов.
Цель исследования – оценить эффективность комплексного применения внутриочагового введения ботулинического токсина типа А (БТА) и лазерной терапии с применением некогерентного широкополосного света (IPL) для лечения ГР сроками до одного года с помощью ультразвукового исследования, а также оценить клиническую эффективность комбинированного метода лечения с учетом динамики показателей японской шкалы исследования рубцов (JSS), визуальной аналоговой шкалы (ВАШ) и результатов общего осмотра.
Материал и методы. Под наблюдением в амбулаторных условиях находились 15 пациентов с ГР сроками существования до одного года. Среди них было 10 (67%) женщин и 5 (33%) мужчин в возрасте от 24 до 40 лет, длительность существования рубцов составляла от шести месяцев до одного года. Всем пациентам проводили внутриочаговое введение БТА в комбинации с применением некогерентного широкополосного света (IPL). Для оценки результатов использовали JSS, ВАШ, определяли толщину и эхогенность тканей патологического рубца с помощью ультразвукового исследования.
Результаты. Данные ультразвукового сканирования показали выраженную положительную динамику по сравнению с исходным уровнем. Достигнуто общее снижение значений показателей JSS и ВАШ. После проведенного комплексного лечения отмечалось уменьшение интенсивности окраски, размягчение, оседание рубцовых деформаций, значительное уменьшение выраженности субъективных ощущений. Ни у одного из испытуемых не было отмечено каких-либо побочных или нежелательных явлений от проведенного лечения.
Заключение. Комплексное лечение, включающее внутриочаговое введение БТА и лазерную терапию с применением IPL, оказалось эффективным. На фоне проводимой терапии отмечалось как улучшение эстетического вида гипертрофических рубцовых деформаций, так и уменьшение выраженности субъективных ощущений у пациентов.
Введение
Гипертрофические рубцы являются широко распространенной и тяжелой формой патологических кожных рубцов, возникающих в результате несостоятельности восстановления кожного покрова из-за чрезмерной реакции тканей на травму. Образование гипертрофических рубцов вызвано пролиферацией фибробластов и избыточной выработкой коллагена в месте повреждения. Эти поражения содержат активные миофибробласты, которые продуцируют структурные компоненты межклеточного матрикса, формирующие каркас патологического рубца. Гипертрофические рубцы не выходят за пределы исходного повреждения и могут разрешаться со временем.
Для гипертрофических деформаций характерны выраженные субъективные ощущения в виде чувства стягивания, натяжения, дискомфорта, а иногда зуда и боли в области поражения. Такие патологические рубцы могут оказывать негативное физическое и психологическое воздействие на пациентов, что значительно снижает показатели их качества жизни [1, 2].
Современные терапевтические подходы в ведении пациентов с гипертрофическими рубцами основываются на индивидуализированных протоколах и комплексных методах лечения. Они включают наложение силиконовых гелевых пластин, прессотерапию, физиотерапию, применение инъекционных, хирургических и аппаратных методов. В последние годы все чаще применяются комбинации методов инъекционной и лазерной терапии [1, 2].
Безопасность и эффективность применения ботулинического токсина типа А (БТА) в целях профилактики и лечения патологических рубцов стали актуальными темами исследований с тех пор, как этот препарат был одобрен FDA на территории США для применения в области медицинской косметологии еще в 2002 г. [3]. БТА – это экзотоксин анаэробной спорообразующей бактерии Clostridium botulinum. Его применение в эстетической медицине, хирургии, неврологии, урологии и других областях медицины стало универсальным инъекционным методом для лечения гиперактивности мышц ввиду ингибирующего действия по отношению к экзоцитозу ацетилхолина, что блокирует нервно-мышечную передачу. Препараты на основе БТА относятся к местным миорелаксантам длительного действия [4, 5].
Введение препаратов на основе БТА на глубину залегания подкожных мышц или субкутанно с дальнейшим распространением в мышечные волокна способствует достижению продолжительной миорелаксации, что приводит к разглаживанию кожи и прекращению ее растяжения во время мимических движений. Это создает эффект пролонгированной фармакологической иммобилизации кожи. Таким образом, инъекционное введение ботулотоксина на этапе формирования рубцовой деформации помогает снизить риск патологического рубцевания, связанного с избыточным натяжением тканей. Такая превентивная стратегия раннего послеоперационного введения БТА особенно важна для применения как в хирургической коррекции уже существующих рубцовых деформаций, так и для профилактики образования патологических рубцов после оперативных вмешательств у пациентов повышенного риска. При ведении пациентов с гипертрофическими рубцовыми поражениями инъекционное лечение препаратами на основе БТА способствует уменьшению выраженности субъективных ощущений в виде боли, зуда, дискомфорта, а также улучшению общей клинической картины [3, 6, 7].
На сегодняшний день существует множество исследований с подтверждением результативности применения БТА в тактике лечения пациентов с гипертрофическими рубцами. Эффективность использования БТА в таких клинических случаях обусловлена воздействием не только на нейрогенном, но также на клеточном и молекулярном уровнях. Так, действие этого вещества снижает напряжение мышечных волокон, стягивающих края раны, способствует ремоделированию и нормальному формированию рубца. Более того, было обнаружено, что БTA снижает экспрессию фактора роста соединительной ткани, который является нисходящим регулятором трансформирующего фактора роста β1, а также подавляет активность фибробластов и рост рубца. В других исследованиях было описано, что БTA подавляет выработку патологического межклеточного матрикса и ограничивает гипертрофическую пролиферацию фиброзной ткани [3–5].
Источники некогерентного оптического излучения излучают некогерентный широкополосный свет (IPL) с длиной волны в диапазоне от 500 до 1300 нм, который можно фильтровать для воздействия на кожу различными длинами волн. Подбор параметров индивидуален, он нацелен на определение прорабатываемого хромофора (например, гемоглобина, меланина или воды) в коже, что вызывает в процессе проводимой терапии селективный фототермолиз этой биологической цели. Соответственно, при использовании различных фильтров с помощью IPL-терапии можно проводить лечение пациентов с гипертрофическими рубцами смешанных признаков, свойственных как проявлению эритемы, так и гиперпигментации. Кроме того, последние исследования продемонстрировали улучшение качества и структуры патологических рубцов после проведения IPL-терапии в виде изменения рельефа, оседания, уменьшения плотности и натяжения в области поражения [8, 9]. Именно этот метод фототерапии чаще используют в современной косметологии. Эффективность IPL-терапии и терапии PDL (Pulsed Dye Laser – импульсный лазер на красителях) в лечении гипертрофических рубцов достаточно близка, однако при использовании метода IPL риск развития нежелательных и побочных явлений в виде постпроцедурной пурпуры и гематом значительно ниже. Преимущества IPL-терапии включают минимальную инвазивность этого метода, комфортную переносимость, короткие сроки реабилитации. Предположительно, механизм воздействия IPL связан с влиянием на ангиогенез путем поглощения гемоглобина, избирательного фототермолиза и коагуляции патологических микрососудов гипертрофического рубца. Это вызывает снижение оксигенации зоны поражения, тем самым запуская процесс ремоделирования межклеточного матрикса рубцовой деформации [2].
Существует множество факторов, влияющих на чувствительность кожи к применению IPL, в том числе тип кожи по Фицпатрику, при этом наилучшие результаты наблюдаются у пациентов с типом кожи I и II; толщина кожи, поскольку увеличение толщины приводит к снижению проникающей способности IPL-терапии; перфузия крови, так как низкая перфузия крови снижает эффективность проводимого лечения ввиду уменьшения количества основного рабочего хромофора (гемоглобина) [9]. В гипертрофических рубцах анаболические и катаболические процессы достигают равновесия примерно через шесть – восемь недель после исходного повреждения. В этот момент рубец обычно гиперемирован и слегка утолщен, но со временем гиперемия имеет тенденцию постепенно спадать по мере созревания рубца. Таким образом, можно сделать вывод о том, что применение IPL-терапии наиболее результативно при ведении пациентов со свежими гипертрофическими рубцами [8, 10, 11].
При ведении пациентов с рубцовыми поражениями чаще всего используется комбинирование различных методов для увеличения эффективности проводимой терапии. Клинический опыт многих специалистов и опубликованные научно обоснованные данные подтверждают, что использование нескольких методов различного профиля воздействия более результативно по сравнению с применением одного фактора в качестве монотерапии. Так, комплексное лечение с помощью сочетанных протоколов аппаратной и инъекционной терапии, а иногда и пластической хирургии является наиболее эффективным [12, 13].
Было показано, что лечение гипертрофических рубцов с помощью комбинированного протокола, включающего внутриочаговое введение препарата на основе БТА и IPL-терапию, может показывать выраженную клиническую эффективность в практике врача-дерматолога. Исходя из опубликованных M.D. Clague и соавт. данных, в ходе проводимого лечения и после его окончания у испытуемых отмечалась положительная динамика в виде уменьшения размеров, активности, плотности рубцовых деформаций, разрешения их гиперемии [11].
Цель исследования – оценить эффективность комплексного применения внутриочагового введения БТА и лазерной терапии с применением IPL для лечения гипертрофических рубцов с помощью ультразвукового исследования, а также оценить клиническую эффективность данного комбинированного метода лечения с учетом динамики показателей японской шкалы исследования рубцов (Japan Scar Workshop Scar Scale, JSS), визуальной аналоговой шкалы (ВАШ) и результатов общего осмотра.
Материал и методы
Под клиническим наблюдением в условиях амбулаторного приема находились 15 пациентов с гипертрофическими рубцами (10 (67%) женщин и 5 (33%) мужчин) в возрасте от 24 до 40 лет. Длительность существования рубцовых поражений была от шести месяцев до одного года. Эти поражения не выходили за пределы исходного повреждения, резко выступали над уровнем окружающей здоровой кожи, отличались плотной консистенцией, цветом от бледно-розового до багрового, четкими границами. У пациентов отмечались выраженные субъективные ощущения в виде чувства зуда, боли, стягивания, натяжения в области рубца. Инициация проводимой терапии зависела от сроков первичного обращения пациента, которые варьировали от шести месяцев до одного года от начала формирования патологического рубца.
Всем пациентам было назначено и проведено лечение гипертрофических рубцов. Проводилось внутриочаговое введение препарата на основе БТА в сочетании с воздействием IPL. Инъекционную терапию проводили каждые восемь – десять недель, аппаратное лечение – через две-три недели после первой процедуры инъекционного введения БТА. Длительность проводимой терапии составила шесть месяцев.
В работе использовали японскую шкалу исследования рубцов JSS, ВАШ, определяли толщину и эхогенность тканей патологического рубца с помощью ультразвукового исследования.
Все показатели оценивали до начала проведения комбинированного лечения и через шесть месяцев от начала терапии.
Результаты
Проведена оценка результативности лечения гипертрофических рубцов с помощью комбинированного протокола, включающего IPL-терапию и внутриочаговое введение препарата на основе БТА.
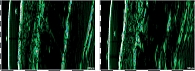
Данные ультразвукового сканирования (рис. 1) показали выраженную положительную динамику по сравнению с исходным уровнем в виде увеличения толщины эпидермиса на 25,3%, повышения эхогенности на 45,7%, снижения акустической плотности на 16,7% и толщины дермы на 48,1%.
Было достигнуто общее снижение значений показателей JSS по сравнению с исходным уровнем: уплотнения – на 74,7%, возвышения над уровнем кожи – на 62,5%, эритемы рубца – на 82,1%, эритемы вокруг рубца – на 82,5%, боли – на 93,7%, зуда – на 92,5%. При этом значения показателей ВАШ снизились: размера – на 31,2%, подвижности – на 74,4%, консистенции – на 77,5%, эритемы – на 80,5%, боли – на 80,4%, зуда – на 92,1%, влияния на повседневную деятельность – на 73,2%.
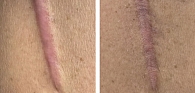
После проведенного комплексного лечения отмечалось уменьшение интенсивности окраски, размягчение, оседание рубцовых деформаций, значительное уменьшение выраженности субъективных ощущений у пациентов (рис. 2).
Ни у одного из испытуемых не было отмечено каких-либо нежелательных побочных явлений от проведенного лечения.
Выводы
- Гипертрофические рубцы вызывают выраженное снижение качества жизни пациентов вследствие влияния на функциональные и эстетические свойства кожного покрова и подлежащих тканей.
- Применение комбинированных индивидуализированных протоколов лечения гипертрофических рубцовых поражений позволяет добиться наиболее высоких результатов.
- Использование комбинации внутриочагового введения БТА и лазерной терапии с применением IPL представляет собой эффективный и перспективный метод ведения пациентов со свежими гипертрофическими рубцами.
E.D. Verbovaya, L.A. Rubtsova, M.S. Kruglova
Central State Medical Academy of Department of Presidential Affairs, Moscow
Institute of Plastic Surgery and Cosmetology, Moscow
I.M. Sechenov First Moscow State Medical University
Contact person: Lyubov A. Rubtsova, lubovrubtz@gmail.com
Hypertrophic scars (GR) are one of the urgent problems in modern aesthetic medicine due to a significant effect on the appearance and quality of life of patients. Modern trends in relation to these conditions are based on the use of combined protocols in order to achieve the most effective results of the treatment.
The purpose of the study is to evaluate the effectiveness of the integrated use of intracutal introduction of botulinum toxin type A (BTA) and laser therapy using a certain broadband light (IPL) for the treatment of GR with a term of up to one year using ultrasound, as well as evaluate the clinical efficiency of the combined treatment method, taking into account the dynamics of the Japanese scales of the scales of the scarves (JSS), visual analogue scale and general inspection results.
Material and methods. Under surveillance on an outpatient basis, there were 15 patients with GR dates of up to one year. Among them were 10 (67%) women and 5 (33%) men aged 24 to 40 years, the duration of the existence of scars was from six months to one year. All patients were carried out by the intracurrent administration of BTA in combination using a certain broadband light (IPL). To evaluate the results JSS and visual analogue scale were used, determined the thickness and echogenicity of the pathological scar tissues using ultrasound.
Results. Ultrasound scanning data showed some positive dynamics compared to the initial level. A general decrease in the values of JSS and visual analogue scale has been achieved. After comprehensive treatment, a decrease in the intensity of coloring, softening, settlement of cicatricial deformations, a significant decrease in the severity of subjective sensations was noted. None of the subjects had any side or undesirable phenomena from the treatment.
Conclusion. Complex treatment, which includes injections of BTA and laser therapy using IPL, turned out to be effective. The therapy leaded to an improvement of hypertrophic deformations structure and decrease of pathological sensations among patients.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.