Особенности функциональных нарушений при доброкачественной гиперплазии предстательной железы (фармакоэкономический анализ)
- Аннотация
- Статья
- Ссылки



Начальные изменения от первичных узелков и дальнейшей пролиферации железистых структур простаты с годами увеличиваются в размерах и становятся макроскопическими. Однако эти изменения не всегда сопровождаются клиническими симптомами.
При выраженной инфравезикальной обструкции, которая приводит к постепенному повышению внутрипузырного давления, возможно и нарушение оттока мочи из верхних мочевых путей, возникновение атонии мочевых путей и мочепузырно-мочеточниковых рефлюксов, уретерогидронефроза и хронической почечной недостаточности. Своевременное устранение обструкции и восстановление нормального пассажа мочи благоприятствуют нормализации функции почек у большинства больных ДГПЖ.
Ведение больных ДГПЖ в зависимости от выраженности симптомов нарушения мочеиспускания (СНМП) включает как «бдительное наблюдение», оперативное лечение, так и фармакотерапию. При «бдительном наблюдении» пациент с легкими симптомами ДГПЖ/СНМП периодически (1-2 раза в год) проходит обследование у уролога. Оперативное лечение по поводу ДГПЖ/СНМП включает как открытые и трансуретральные операции, так и малоинвазивные вмешательства.
Из лекарственных препаратов, отобранных с позиций доказательной медицины для фармакотерапии ДГПЖ/СНМП, имеют значение II группы препаратов: ингибиторы 5a-редуктазы и a-1 адреноблокаторы. Различные фитопрепараты, применяемые для лечения ДГПЖ, являются многокомпонентными, поэтому трудно выделить активное действующее вещество, тем более что различные травы экстрактируются разными способами. По применению фитопрепаратов имеется небольшое количество рандомизированных клинических исследований, малые сроки применения (2).
Наиболее изученным и широко применяемым ингибитором 5a-редуктазы является финастерид, блокирующий на уровне предстательной железы превращение тестостерона в ДГТ. Препарат хорошо переносится и не обладает побочными эффектами, характерными для гормональных средств. Действие ЛС в большей степени направлено на уменьшение механического компонента обструкции и связано с уменьшением объема простаты. Наилучшие результаты наблюдаются у пациентов с большими объемами простаты (> 40 г), в структуре которой преобладает эпителиальная ткань. У пациентов, получающих финастерид не менее 6 месяцев, отмечается снижение уровня ДГТ на 70-80%, уровня ПСА, на 50-60% и уменьшение объема предстательной железы, на 20-30%. СНМП улучшаются у 40-60% больных, увеличивается максимальная скорость потока мочи на 1,6-2,6 мл/с. Однако для купирования острой задержки мочеиспускания (ОЗМ) финастерид не пригоден, т. к. эффективность его применения достигается не ранее, чем через 6-12 месяцев. В то же время длительный прием финастерида позволяет уменьшить риск возникновения ОЗМ и необходимости операции (2). Дутастерид является ингибитором изоферментов
5-α-редуктазы I и II типов, в связи с чем отмечается более быстрый эффект лечения: уменьшение объема простаты (свыше 20%) отмечается через 1-3 месяца. Из нежелательных побочных действий ингибиторов 5α-редуктазы – снижение либидо (3,7-6,4%) и эректильная дисфункция (6-8%).
Инфравезикальная обструкция при ДГПЖ определяется не только статическим компонентом – в результате механического сдавления уретры гиперплазированной тканью предстательной железы, но и динамическим, обусловленным гиперактивностью a-адренорецепторов шейки мочевого пузыря, простатического отдела уретры и простаты. Около 40% уретрального сопротивления отводят на долю динамического компонента, таким образом, фармакологической блокадой a-адренорецепторов можно реально уменьшить симптомы обструкции. a-адренорецепторы являются конечным звеном симпатического отдела вегетативной нервной системы. Симпатические волокна распределяются в мочевом пузыре неравномерно. В области шейки мочевого пузыря их больше, далее – в области тела, в апикальной части, в правой и левой стенках мочевого пузыря. В мочевом пузыре обнаружены оба типа (a и b) адренорецепторов, в то время как повышение тонуса гладкой мускулатуры шейки, уретры, простаты связано с a-1адренорецепторами, имеющими здесь высокую плотность. Различают подтипы a-1адренорецепторов – А, В, D. В простате 69,3% a-1 адренорецепторов относится к подтипу А, при ДГПЖ их значительно больше – до 85% (5).
Известно, что инфравезикальная обструкция при ДГПЖ имеет четко выраженный симпатозависимый компонент. Уретральная обструкция вне зависимости от механизмов ее возникновения (механический, динамический) создает лишь условия для нарушения мочеиспускания на уровне нижних отделов мочевых путей. Клиническая симптоматика формируется при вовлечении в патологический процесс мышцы детрузора. Механизм преодоления инфравезикальной обструкции остается не до конца выясненным. При электронно-микроскопических исследованиях установлено, что миогипертрофия стенок мочевого пузыря, которую принято считать компенсаторного характера, на самом деле сопровождается коллагеновой инфильтрацией, что приводит к слабой сократительной способности. Задержка мочи может быть первым проявлением обструкции уретры при ДГПЖ – это следствие не только слабого, но и сильного сокращения детрузора при микции, которое угасает еще до того, как завершится опорожнение мочевого пузыря (5). Таким образом, симптоматика нарушений мочеиспускания у больных ДГПЖ не может быть обьяснима только обструкцией задней уретры увеличенной простатой. Нарушения внутриорганного пузырного кровообращения, гипоксия, ишемия стенки мочевого пузыря могут приводить как к гипер- так и к гипорефлексии мочевого пузыря. Декомпенсацию детрузора при ДГПЖ обычно рассматривают как итог длительно существующей уретральной обструкции, без учета нарушения его энергетического метаболизма. Причинами нарушения энергетического метаболизма и функции детрузора могут быть как повышение активности симпатической нервной системы (что наблюдается с возрастом), расстройства органного кровообращения, авитаминоза (группа В), так и, конечно, обструктивные нарушения уродинамики.
Своевременное выявление характера уродинамических нарушений и в первую очередь гиперактивности детрузора у больных ДГПЖ имеет важное практическое значение. У 25-30% оперированных больных уродинамические показатели до операции не подтверждают инфравезикальную обструкцию. Примерно столько же больных со сниженной сократительной способностью детрузора без признаков обструкции подвергаются операции – аденомэктомии (простатэктомии) или трансуретральной резекции предстательной железы. Гиперактивность детрузора исчезает у 60% больных ДГПЖ после хирургической ликвидации препятствия к оттоку мочи. В то же время у 15-20% больных ДГПЖ после операции сохраняются симптомы нарушенного мочеиспускания: дневная и ночная поллакиурия, повелительные позывы, императивное недержание мочи (1).
Эффект лечения селективными a-1адреноблокаторами связан с ограничением влияния симпатического отдела вегетативной нервной системы на мочевой пузырь, простату, уретру, шейку мочевого пузыря путем блокады a-1 адренорецепторов.
В мире имеется большой опыт по применению селективных a-1 адреноблокаторов (альфузозин, доксазозин, теразозин, тамсулозин) в лечении ДГПЖ/СНМП. Показана их клиническая эффективность через 1-2 недели применения, отмечается уменьшение степени выраженности расстройств мочеиспускания (по шкале IPSS) в среднем на 40-60%, улучшение качества жизни вдвое, снижается риск развития острой задержки мочеиспускания и оперативного лечения (2). По данным уродинамического обследования отмечено снижение уретрального сопротивления, и увеличение максимальной скорости потока мочи в пределах 1-3,5 мл/с; уменьшение количества остаточной мочи на 50%, снижение микционного давления на треть. Отсутствие эффекта лечения в течение 2-3 месяцев является основанием для пересмотра терапии. У пациентов с ДГПЖ и с артериальной гипертензией a-1адреноблокаторы приводят к существенному снижению артериального давления, вернее, к его нормализации, в то время как у пациентов с нормальными цифрами артериального давления гипотензивный эффект практически отсутствует. Однако у части пациентов симптоматическое улучшение отмечается без прямой связи с увеличением потока мочи, т. е. без заметного влияния на обструкцию. Очевидно, препараты действуют на кровообращение и функции детрузора, что приводит к увеличению его адаптационных свойств и резервуарной функции мочевого пузыря.
Грозным осложнением ДГПЖ/СНМП является острая задержка мочеиспускания (ОЗМ), требующая принятия неотложных мер: катетеризации мочевого пузыря; троакарной эпицистостомии или экстренного оперативного вмешательства.
При острой задержке мочеиспускания, обусловленной ДГПЖ (ОЗМ/ДГПЖ), структурно-функциональные изменения детрузора обструктивного характера могут заметно усугубляться стрессорными (прямое катехоламиновое воздействие) и ишемическими (вследствие спазма сосудов) повреждениями гладкомышечных элементов мочевого пузыря. При ОЗМ/ДГПЖ мочевой пузырь испытывает повышенное воздействие катехоламинов с последующим истощением их запасов в окончаниях симпатических нервов, которое сопровождается прогрессирующим угнетением его биоэнергетики и расстройствами функции.
ОЗМ в одних случаях это кульминация обструктивного процесса в сочетании с декомпенсацией сократительной способности детрузора, в других ОЗМ развивается внезапно, на фоне умеренно выраженных симптомов нарушенного мочеиспускания, а иногда становится первым клиническим проявлением ДГПЖ.
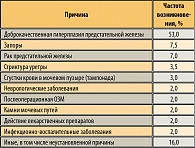
Данные эпидемиологических исследований связывают увеличение риска развития ОЗМ (почти в 3-4 раза) с увеличением объема предстательной железы (>40 мл) и с показателями простат-специфического антигена (ПСА>1,4 ннгр/мл) (7). Риск развития ОЗМ также увеличивается с возрастом и с выраженностью симптомов нарушения мочеиспускания, что оценивают по различным международным опросникам (IPSS, AUA, Boyarsky). Вероятность развития ОЗМ у мужчин старше 70 лет в 8 раз выше, чем у 40-летних. Основные причины возникновения ОЗМ у мужчин представлены в таблице 1.
Основным лечебным мероприятием для разрешения ОЗМ является катетеризация мочевого пузыря – быстрый и эффективный способ эвакуации мочи из мочевого пузыря. При невозможности катетеризации мочевого пузыря через уретру производят эпицистостомию, либо пункционную, либо при открытом оперативном вмешательстве. В то же время известно, что ОЗМ/ДГПЖ служит причиной выполнения экстренной операции каждой третьей трансуретральной резекции простаты (ТУР) или открытой аденом- простат-эктомии. Выполнение операции на фоне ОЗМ сопряжено с высоким риском возникновения осложнений (6):
- интраоперационных – 1,8 (1,3-2,5%);
- гемотрансфузии – 2,5 (1,8-3,3%);
- послеоперационные – 1,6 (1,2-2,0%);
- смертность в последующие 30 дней – 0,7-3,3% (1,2-9,3) по сравнению с 0,2% (больные без ОЗМ).
Проведенными ранее клиническими исследованиями показана эффективность восстановления самостоятельного мочеиспускания после катетеризации мочевого пузыря уретральным катетером у больных ОЗМ/ДГПЖ после однократной катетеризации – у 28% пациентов, после установки катетера на 2 дня – у 51%, после 7-дневной постоянной катетеризации – у 62% пациентов (7). Однако риск развития инфекционно-воспалительных осложнений после длительных катетеризаций мочевого пузыря велик, что не позволяет произвести отсроченное оперативное вмешательство и вынуждает направлять пациентов на амбулаторное лечение с эпицистостомическим дренажом на длительное время, до ликвидации воспалительных явлений.
Длительный международный опыт применения a-1адреноблокаторов у больных с СНМП/ДГПЖ помимо эффективности и безопасности лечения показал, что практически не было отмечено развития острой задержки мочеиспускания у пациентов, постоянно принимающих a-1 адреноблокаторы (2). Более того, профилактический прием a-1адреноблокаторов за 5 дней до и 3 дня после хирургических операций у больных с ДГПЖ, оперированных на других органах, позволил уменьшить риск развития ОЗМ в послеоперационном периоде: 2,7% против 19% в контрольной группе. По данным S.F. McNeill (11) у 55% больных, поступивших с ОЗМ/ДГПЖ и получавших альфузозин, после удаления уретрального катетера восстановилось самостоятельное мочеиспускание – против 29%, получавших плацебо.
В современных условиях при оценке новых медицинских технологий и лекарственных средств, помимо клинической эффективности и безопасности, необходимо оценивать и экономическую эффективность, т. е. ценность результатов, полученных при расходовании определенной суммы денег. Вмешательства или лекарственные средства, позволяющие не только уменьшить финансовые затраты, но также и избежать серьезных оперативных вмешательств, улучшить качество жизни пациентов, представляют не только медицинский, но и экономический интерес.
Экономическая эффективность означает наилучшее использование материальных, трудовых и финансовых ресурсов общества для ускорения достижения его целей. Повышение ее предусматривает достижение лучших результатов при наименьших затратах. Показатель эффективности должен характеризовать получаемый эффект в сопоставлении с затратами на его достижение.
Необходимость учета данных фармакоэкономических исследований обусловлена растущей долей лиц пожилого возраста, нуждающихся в продолжительном лечении и социальном обеспечении; стремлением улучшения качества жизни больных ДГПЖ и в то же время ограничением финансирования для организации медицинской помощи и эффективности работы системы здравоохранения в современных условиях; увеличением стоимости медицинских услуг и лекарственных препаратов.
В последнее десятилетие произошло фундаментальное изменение отношения к системе здравоохранения. Прежде всего произошло смещение приоритетов с технологий предоставления медицинских услуг, ориентированных в основном на экономию издержек (минимизация затрат), на вопросы об эффективном расходовании средств (затраты/эффективность).
Особенно это касается новых лекарственных препаратов при оценке ожидаемой от них отдачи. В этих условиях исследования по критерию «затраты/эффективность» становятся важным инструментом выбора тех или иных лечебных средств медицинскими учреждениями и сторонами, оплачивающими их услуги.
С развитием системы обязательного медицинского страхования в России также растет необходимость обоснования экономической эффективности затрат на приобретение лекарственных средств и медицинской техники. Экономическая оценка становится важным источником информации, помогающим в принятии решений потребителями, медицинскими учреждениями и предприятиями фармацевтической промышленности (3).
В теории экономики здравоохранения сложилось определенное деление затрат на различные категории. В первую очередь это прямые медицинские затраты, которые включают в свой состав все издержки, понесенные системой здравоохранения, в которые входят (4):
- расходы на содержание пациента в лечебном учреждении или же стоимость оказываемых ему на дому услуг, в том числе медицинскими сестрами;
- стоимость профессиональных медицинских услуг (плата за врачебные консультации, а также оплата рабочего времени врачей или медицинского персонала);
- стоимость лекарственных препаратов;
- стоимость лабораторного и инструментального оборудования;
- стоимость медицинских процедур (диагностические вмешательства, операции, реабилитационный период, санитарное просвещение);
- стоимость транспортировки больного санитарным транспортом
- амортизационные отчисления
В состав прямых расходов часто включают расходы, которые несут другие общественные службы и организации, а также пациенты и члены их семей.
В состав прямых не медицинских расходов входят:
- наличные (карманные) расходы пациентов;
- стоимость услуг, оказываемых пациентам на дому;
- затраты на перемещение пациентов.
Косвенные расходы представляют затраты, связанные с потерей трудоспособности пациентом из-за лечения, заболевания или смерти, или же производственные потери, которые несут навещающие пациента члены его семьи или друзья. К ним относятся:
- затраты за период отсутствия пациента на его рабочем месте из-за болезни или раннего выхода на пенсию;
- «стоимость» времени отсутствия на работе членов его семьи или друзей;
- экономические потери от снижения производительности на месте работы;
- экономические расходы от преждевременного наступления смерти.
Нематериальные расходы представляют такие человеческие факторы, которые трудно количественно измерить, например, боль, страдания, испытываемые пациентом, вследствие проходимого им курса лечения. Их трудно оценить в материальном плане, поэтому они зачастую остаются за рамками выполняемого стоимостного анализа. Учитывают и критерии оценки качества жизни.
В настоящее время одним из наиболее часто употребляемых экономических исследований в здравоохранении является анализ «затраты/эффективность». Он используется, если двумя или более медицинскими вмешательствами различной степени эффективности преследуется одна и та же цель, что позволяет учесть как расходы, так и эффективность (исходы) лечебных мероприятий.
При расчете стоимости курса лечения следует учитывать все затраты, понесенные за соответствующий период времени, т. к. применение какого-либо лекарственного средства может увеличить смету расходов на лекарственные препараты, однако по прошествии времени его использование может дать экономию по другим бюджетным статьям. К ним может относиться снижение расходов на содержание пациентов в стационаре и ведение за ними врачебного наблюдения, что частично или полностью компенсирует упомянутый выше рост расходов на лекарственные средства. Поэтому, для того чтобы эффективно распределять финансовые ресурсы, нужно оценивать все расходы, которые могут быть связаны с данным курсом лечения или препаратом на протяжении определенного периода времени.
В этой связи представляет интерес фармакоэкономическое исследование по оценке экономической эффективности препарата альфузозин при лечении острой задержки мочеиспускания в Бельгии в 2003 г. (Alfaur).
Авторы провели исследование исходов лечения после удаления уретрального катетера (исход катетеризации – ИК), установленного по поводу ОЗМ у больных ДГПЖ. Исследованиями, проведенными раньше, в начале 80-х годов прошлого века было показано, что после купирования ОЗМ оперативному лечению подвергались больные в течение первых 6 месяцев наблюдения, однако в 16-18-22% случаев оперативное лечение можно было избежать из-за отсутствия симптоматики (7, 8). Наблюдения за больными показало, что у 56% обследованных пациентов рецидив ОЗМ наступал в течение недели, у 62% – через месяц, а у 68% – через год (9). Необходимо отметить, что эти пациенты либо не принимали никакой лекарственной терапии, либо принимали нерегулярно a-1 адреноблокаторы.
Исследования по эффективности применения a-1 адреноблокаторов при лечении больных с
ОЗМ/ДГП показали, что восстановление самостоятельного мочеиспускания после извлечения уретрального катетера (через 24-72 часа) было в 64-84% случаев. Рецидив ОЗМ в течение первых 3 месяцев после ИК, потребовавший оперативного лечения был только у 7% пациентов. В контрольной группе больных не получавших лечение a-1адреноблокаторами положительный результат ИК был в 60% случаев (10).
Исследование ALFAUR (рандомизированное, многоцентровое, двойное слепое) было проведено на 357 пациентах с ОЗМ/ДГПЖ. Сравнивали эффективность лечения альфузозином (10 мг в день однократно) с плацебо по влиянию на ИК. Положительный результат был зарегистрирован в 61,9 и 47,9% соответственно (р=0,012). Из них 34 пациента с положительным результатом (22 – получали альфузозин и 12 – плацебо) находились под длительным наблюдением в течение 7,2 месяцев. В целом, у 23 пациентов (68%) рецидивов ОЗМ не было, а в 32% случаев возникала необходимость в оперативном лечении.
Была проведена экономическая оценка анализа «стоимости/последствий» для трех вариантов лечения ОЗМ/ДГПЖ: больные на фоне катетеризации мочевого пузыря в течение 24 часов получали либо альфузозин 10 мг, либо плацебо. Если у пациента не восстанавливалось самостоятельное мочеиспускание, ему либо производили операцию простатэктомию, либо выписывали с дренированным мочевым пузырем и впоследствии оперировали. При положительном ответе на ИК (больной размочился) его выписывали. При экономическом анализе больных, которых включали в модель, отбирали по двум критериям: 1) первый эпизод ОЗМ, вследствие ДГПЖ и 2) отрицательный результат в первом ИК. Целью исследования был сбор данных по издержкам, связанным с отрицательным результатом ИК, чтобы лучше понять и иметь возможность рассчитать экономию средств, которую можно получить, избежав отрицательного результата ИК.
Результаты исследования ALFAUR
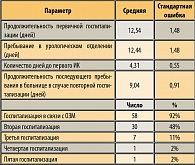
Исследовано 63 истории болезней пациентов из 5 клиник, период наблюдения – 6 месяцев. Средний возраст – 76 лет. В таблице 2 представленны данные по госпитализациям. В первый эпизод ОЗМ не все больные были госпитализированы.
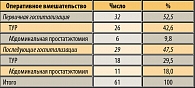
Важен тот факт, что из 63 случаев у 61 пациента с отрицательным результатом ИК простатэктомия выполнена в течение 6 месяцев после эпизода ОЗМ. В отношении двоих пациентов было принято решение о пожизненной катетеризации. Большинство пациентов (52,5%) подверглось простатэктомии во время первичной госпитализации (таблица 3). Больных, которые не подверглись оперативному вмешательству в ходе первичной госпитализации, выписывали домой с катетером, и им назначался срок следующей госпитализации.
Расходы на используемые ресурсы
Расходы вследствие использования медицинских ресурсов определяются как расходы на госпитализацию (факт пребывания в больнице и потребность в общем уходе и услугах младшего медицинского персонала), расходы на медикаментозное лечение, стоимость оперативного вмешательства и расходы на диагностические исследования.
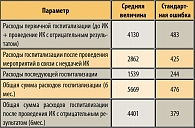
Важно отметить, что связанные с ОЗМ расходы, в случае отрицательного результата в первом ИК, начинают исчислять после этого первого ИК, но не в момент госпитализации по поводу ОЗМ (таблица 4).
Затраты на диагностические исследования включают использование разнообразных ресурсов, необходимых для лабораторных анализов, исследований, консультаций врачей начиная с момента получения отрицательного результата ИК. Затраты в ходе первичной госпитализации, последующих госпитализаций и амбулаторного лечения учитываются отдельно (таблица 5)
Как указывалось выше, в 61 случае из 63-х после первого эпизода ОЗМ пациентам с отрицательным ИК производилось оперативное вмешательство. В 52,5% случаев операция была произведена в первичную госпитализацию. В таблице 6 приведены затраты на лечение.
Общие расходы на ОЗМ
Средняя величина общих затрат первичной госпитализации (12,54 дней), в связи с первым эпизодом ОЗМ составляла 4 722 евро, расходы, связанные с отрицательным ИК во время первой госпитализации составляют 3 453 евро. Расходы периода, предшествующего ИК равны 1 269 евро (4722-5453).
Средняя полугодовая стоимость эпизода ОЗМ, если не исключать из рассмотрения дни, предшествующие ИК, составляла 6 766 евро (проживание в гостинице, диагностические исследования, лечение, операции, малые инвазивные вмешательства).
Общая сумма полугодовых затрат при отрицательном ИК составляет 5498 евро ( стандартная ошибка =393 евро), в то время как стоимость первичной госпитализации в связи с отрицательным результатом ИК равна 3453 евро ( станд.ошибка 470 евро).
Пациенты с положительным ИК выписываются после этой процедуры, поэтому в сумму издержек для них включаются только расходы пребывания в больнице до ИК (1 269евро).
Исходя из того, что у 32,35% пациентов, давших положительный результат ИК в дальнейшем, были проведены плановые операции, а 32 пациента были срочно оперированы в первичную госпитализацию, авторы рассчитали расходы на срочную и плановую простатэктомию. Стоимость пребывания в больнице до ИК при срочной операции не включается в расчеты, т. к. их оперируют экстренно, не дожидаясь 4-го дня (время до проведения первого ИК). Расходы простатэктомии, в зависимости от включения периода до ИК распределились следующим образом:
- экстренная ТУР простаты (период до ИК включен) = 7351 евро;
- экстренная простатэктомия (период до ИК включен) = 6036;
- экстренная ТУР простаты (период до ИК исключен) =6101;
- экстренная простатэктомия (период до ИК исключен) = 5539;
- плановая ТУР = 4237;
- плановая простатэктомия = 3722.
Стоимость одной упаковки 30 доз альфузозина (10 мг) равна 37,73 евро. Стоимость приема альфузозина в течение 3-х дней, как принимали больные в ALFAUR равна 2,75 евро.
По результатам ALFAUR рассчитывали величину непосредственного снижения затрат в первичную госпитализацию от использования альфузозина. Средняя стоимость экстренной госпитализации у пациентов, получавших альфузозин, составила 2588±235 евро. Эти расходы складываются из следующих величин: пребывание в больнице до ИК = 1269 евро, расходы на лечение альфузозином =2,75 евро, но лишь в 38,1 % случаев, т. е. у пациентов, имеющих отрицательный ИК будут иметь место связанные с этим расходы (3453 евро).
Для пациентов, лечение которых не включало лекарственную терапию, общая величина затрат составляет 3067±301 евро. Таким образом, лечение альфузозином позволяет сэкономить в среднем 479 евро на этапе экстренной госпитализации в связи с ОЗМ/ДГПЖ. Экстренная простатэктомия является наиболее дорогостоящим видом лечения (5996 евро), взвешенные величины стоимости ТУР (81%=6101 евро) и открытой простатэктомии (19%, 5539 евро).
Для расчета полугодовых затрат авторы исходили из того, что в группе пациентов с положительным ИК в 32,35% случаев простатэктомия выполнялась в течение последующих 6 месяцев. Для этого случая также были определены взвешенные величины стоимости плановой ТУР (62% – 4237 евро) и плановой открытой простатэктомии (38% – 3722 евро).
Таким образом, расходы на лечение пациентов альфузозином складываются из следующих величин: расходы до ИК составляют для всех пациентов 1269 евро; к этой величине следует прибавить полугодовые расходы после отрицательного ИК у 38,3% пациентов, величина которых равна 5498 евро, и расходы плановой простатэктомии у 32,35% пациентов с положительным ИК (61,7% – 4041 евро).
В таблице 7 и 8 приведены расходы.
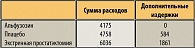
Исходя из того, что в Бельгии распространенность ОЗМ соответствует 3400-3500 случаев в год, вложив по 2,75 евро в лечение альфузозином этих пациентов, что равно расходу 9350-9625 евро из бюджета здравоохранения, можно сэкономить от 1985600 (584 евро*3400 пациентов) до 2044000 евро.
Экстраполируя ситуацию на Российское здравоохранение можно произвести анализ стоимости последствий для лечения больных ОЗМ/ДГПЖ альфузозином, плацебо и оперативного лечения в наших условиях.
Источником расходов используемых ресурсов являлись «Тарифы на медицинские услуги, предоставляемые взрослому населению в соответствии с Московской городской программой обязательного медицинского страхования за 2003 год».
Стоимость лекарственных препаратов использованных в исследовании на 6 месяцев лечения выполнена из расчета их средней розничной стоимости по данным крупнейшего дистрибьютора ПРОТЕК за декабрь 2003 года.
Расходы выражены в рублях. Все численные данные по расходам представляют собой средние величины.
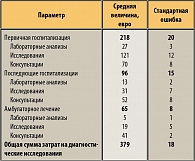
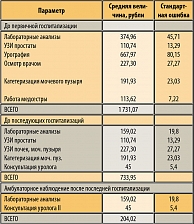
Затраты на диагностические исследования включают использование разнообразных ресурсов, необходимых для лабораторных анализов, УЗИ мочеполовой системы, рентгенографических исследований и стоимости врачебных осмотров, начиная с момента получения отрицательного результата ИК (в основу тактики диагностики и лечения больных ДГПЖ с ОЗМ положены Медико-экономические стандарты ведения больных). Использование ресурсов в ходе первичной госпитализации, последующих госпитализаций (они входят в стоимость койко-дня) и амбулаторного лечения учитываются отдельно. Расходы приведены в нижеследующей таблице 9.
Как сказано выше, больные оставались в больнице в течение 12 дней, а первое ИК проводилось через 4,3 дня после начала ОЗМ. В таблице 10 представлены средние величины общей стоимости госпитализации на одного больного. Расходы госпитализации включают расходы на койко-день по поводу пребывания пациента с диагнозом ОЗМ, медицинское наблюдение и услуги диагностики и лаборатории (ежедневная фиксированная плата).
Общие расходы на ОЗМ
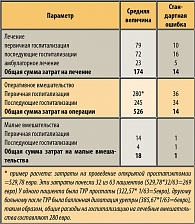
Средняя величина общих затрат первичной госпитализации (12,54 дней) в связи с первым эпизодом ОЗМ составляла 5 530,67 руб. (при стандартной ошибке 526,27 руб.). Эта величина получается путем сложения затрат на амбулаторные манипуляции до первичной госпитализации, проведенные 100% пациентов (1731,07 руб.), пребывание в стационаре по поводу данного заболевания, оперативное вмешательство, стоимость которого входит в стоимость койко-дня, что составляет для 92% пациентов (3 799,6 руб.).
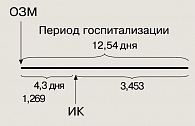
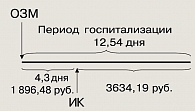
Таким образом, средние ежедневные расходы, связанные с первичной госпитализацией будут равны отношению 5530,67 руб. к 12,54 дням, т. е. 441,04 руб. Значит, схему стоимости первичной госпитализации можно разложить на две части: стоимость периода, предшествующего ИК, 4,3 дня, равная 1896,48 руб., и стоимость периода после ИК, равного 3634,19 руб.
Рисунок 2 обобщает сказанное выше.
Средняя полугодовая стоимость эпизода ОЗМ, если не исключать из рассмотрения дни, предшествующие ИК, составляла 7166,65 рублей (при стандартной ошибке 490,11 рублей). Эта величина получается путем сложения затрат на первичную госпитализацию
(5 530,67 руб.) и диагностические исследования перед последующими госпитализациями, а также стоимость всех последующих госпитализаций, взятых в процентном отношении, указанном в таблице 7 (733,95 + 1 539) * 0,63 = 1431,96 руб.). К полученному необходимо прибавить стоимость амбулаторного наблюдения, которому подвергались 100% пациентов, т. е. 204,02 рубля.
Полная схема стоимости лечения ОЗМ представлена на рисунке 3.
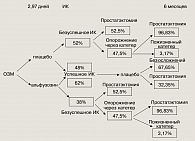
Вычислив стоимость ведения больных ОЗМ в российских условиях, строим модель стратегии лечения ОЗМ, основанную на результатах исследования ALFAUR, представляющую собой древо решений (рисунок 4).
Стоимость суточного применения альфузозина (ДальфазÒ) 10 мг равна 47,5 рублей. В испытании ALFAUR альфузозин (10 мг) принимался в среднем в течение 2,97 дней до ИК. В связи с этим в модели была использована стоимость альфузозина в течение 3 дней (142,5 рублей).
По результатам исследования ALFAUR рассчитывалась величина непосредственного снижения затрат (за период первичной госпитализации) на фоне использования альфузозина. Средняя стоимость госпитализации у пациентов, леченых альфузозином (10 мг) составила 2 040,36 ± 234,15 руб. Эти расходы объясняются следующим образом: пребывание в больнице до ИК дает для всех пациентов величину затрат, равную 1896,48 руб., а расходы лечения альфузозином – 142,5 руб.
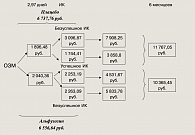
Распределение всех затрат обеих тактик ведения пациентов (с дополнением лекарственной терапии альфузозином и без) отображены в модели «древо решений» на рисунке 5.
Для пациентов, лечение которых не включало лекарственную терапию, общая величина затрат составляет 6 737,76 ± 301,57 руб. При лечении альфузозином эта сумма снижается до 6 556,64 руб. Таким образом, лечение альфузозином позволяет сэкономить в среднем 181,12 рублей на этапе первичной госпитализации в связи с ОЗМ.
Полугодовые расходы
После первичной госпитализации оперативное лечение у пациентов с положительным результатом ИК выполняется у 32,35% в течение последующих 6 месяцев. Это приводит к увеличению расходов на сумму, связанную с разницей в проведенных в течение госпитализации мероприятий. Пациентам с отрицательным результатом ИК простатэктомия может быть выполнена во время первичной госпитализации. В то же время значительное число пациентов остается с катетером и оперативное вмешательство планируется на будущее. Это распределение косвенным образом включается в величину полугодовых издержек отрицательного результата ИК.
Разница в стоимости полугодовых тактик ведения пациентов составляет 1401,6 рубля, соответственно для группы пациентов, получающих альфузозин, меньше на данную сумму, чем в группе плацебо.
В настоящем исследовании проведен анализ стоимости лечения пациентов ДГПЖ, перенесших первый эпизод ОЗМ/ДГПЖ.
Точных статистических данных распространенности ОЗМ/ДГПЖ в Российской Федерации нет. Однако, вложив в процесс лечения 1000 пожилых мужчин, обратившихся по поводу ОЗМ/ДГП, 142500 рублей для использования альфузозина, система здравоохранения экономит до полутора миллиона рублей в течение первого года ведения этих больных в связи с сокращением затрат на полугодовой процесс ведения этих пациентов.
Применение нетитруемого a-1 адреноблокатора альфузозина (Дальфаз СР – с постепенным высвобождением активного вещества) в виде одной таблетки в максимальной суточной дозе 10 мг патогенетически обосновано у больных с ОЗМ/ДГПЖ, находящихся в стрессовом состоянии (прямое катехоламиновое воздействие, спазм сосудов).
Лечение альфузозином больных ОЗМ, вследствие ДГПЖ сокращает расходы экстренной госпитализации и полугодового наблюдения за больными и, следовательно, позволяет рационально распределить бюджетные средства, выделяемые на ведение этой патологии. Несмотря на относительно высокую стоимость альфузозина, небольшой добавочный расход на лекарственный препарат (а точнее, его использование в течение трех дней) позволяет добиться значительной экономии средств больничного бюджета.
Более того, даже если у пациента с положительным результатом ИК в дальнейшем возникает необходимость хирургического лечения, оно производится в плановом порядке, что также приводит к сокращению издержек и уменьшению послеоперационной смертности.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.