Особенности раннего восстановления кожи у пациентов старшей возрастной группы после проведения комбинированного аппаратного воздействия игольчатого RF и лазерной технологии
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – оценить ранние регенеративные особенности кожи у возрастных пациентов с помощью гистологического исследования через месяц после проведения комбинированного аппаратного воздействия игольчатого RF и лазерной технологии 1927 нм (с индивидуальным подбором параметров и снижением уровня агрессии) на примере трех клинических случаев. Окрашивание срезов проводили стандартно – гематоксилин-эозином, также для полного представления изменений в коже после лечения использовали дополнительные методы окрашивания – по Ван-Гизону и по Массону. По результатам исследования установлена тенденция зависимости восстановительных процессов от сопутствующих патологий, которые влияют на процессы регенерации, однако при снижении аргессии параметров аппаратных технологий наблюдается восстановление кожи и улучшение ее качественных характеристик. Таким образом, комбинированное применение игольчатого RF и лазерной технологии с подбором параметров воздействия с целью снижения уровня агрессии у возрастных пациентов оказывает положительное влияние на качественные характеристики кожи, способствует обновлению коллагеновых структур кожи без формирования фиброза.
Цель исследования – оценить ранние регенеративные особенности кожи у возрастных пациентов с помощью гистологического исследования через месяц после проведения комбинированного аппаратного воздействия игольчатого RF и лазерной технологии 1927 нм (с индивидуальным подбором параметров и снижением уровня агрессии) на примере трех клинических случаев. Окрашивание срезов проводили стандартно – гематоксилин-эозином, также для полного представления изменений в коже после лечения использовали дополнительные методы окрашивания – по Ван-Гизону и по Массону. По результатам исследования установлена тенденция зависимости восстановительных процессов от сопутствующих патологий, которые влияют на процессы регенерации, однако при снижении аргессии параметров аппаратных технологий наблюдается восстановление кожи и улучшение ее качественных характеристик. Таким образом, комбинированное применение игольчатого RF и лазерной технологии с подбором параметров воздействия с целью снижения уровня агрессии у возрастных пациентов оказывает положительное влияние на качественные характеристики кожи, способствует обновлению коллагеновых структур кожи без формирования фиброза.




В настоящее время развитие косметологии неразрывно связано с применением инъекционных и аппаратных методов и постоянным их совершенствованием благодаря активному изучению процессов восстановления и синолитических эффектов, а также появлению нового направления – регенеративной медицины [1, 2].
Процесс восстановления кожи после различных травм является многоэтапным и должен строго контролироваться с целью обеспечения эффективного восстановления поврежденной ткани и ее структур [3–7]. Возможности клеточных структур кожи изменяются с возрастом. Так, инволютивные изменения кожи приводят к нарушению заживления ран ввиду снижения репаративного потенциала. При повреждении в фазе воспаления в коже происходят клеточные изменения идентичные старению вследствие секреции факторов SASP, в том числе PDGF-A. Стареющие фибробласты выделяют большое количество PDGF-A, что способствует активации миофибробластов из фибробластов и является важнейшим фактором SASP [8–11]. SASP – это сложная смесь воспалительных цитокинов и липидов, которые синтезируются и высвобождаются стареющими клетками [12]. Состав SASP может отличаться в зависимости от типа клеток и агента, вызывающего старение [13, 14]. Несмотря на то что точное определение еще не сформулировано, принято считать, что в состав SASP входят интерлейкин (ИЛ) 6, ИЛ-1β, ИЛ-8, фактор некроза опухоли бета (ФНО-β), матриксные металлопротеазы (ММП), биоактивные липиды (например, церамиды и простагландины), серпины и микро-РНК, которые способствуют развитию воспаления [15]. SASP является ключевым признаком стареющих клеток, но его регуляция изучена недостаточно и зависит от контекста, однако зачастую SASP усиливается вследствие передачи сигналов через NF-KB (универсальный фактор транскрипции) [16]. Различные факторы, вызывающие старение, могут приводить к формированию разных составов SASP, и, что наиболее важно, SASP может действовать на пока еще нестареющие клетки с помощью паракринных механизмов. Таким образом, стареющие клетки могут передавать сигналы другим нестареющим клеткам, чтобы те тоже «старели» [17]. Длительное присутствие таких измененных клеток в месте раны может препятствовать заживлению или приводить к фиброзу, в том числе у возрастных пациентов [18–20].
При биологическом старении в коже происходит накопление синтетически неактивных фибробластов, которые не восстанавливают внеклеточный матрикс кожи (ВКМ). Для белкового состава ВКМ используют термин «матрисома», объединяющий 43 субъединицы коллагена, 35 протеогликанов, 200 гликопротеинов (включая CCN – семейство белков, ассоциированных с внеклеточным матриксом и участвующих в межклеточной передаче сигналов). Стареющие фибробласты экспрессируют большее количество эндогенных оксидантов, протеаз, богатый цистеином белок 1 (CCN1) и ассоциированы с более низкими уровнями проколлагена и гиалуроновой кислоты. Основная функция белков CCN состоит в связывании с белками ВКМ и участии в процессах воспаления и регенерации кожи [21, 22]. CCN1-индуцированные изменения приводят к снижению коллагена типов I и III, повышению экспрессии провоспалительных цитокинов (ИЛ-1b, ИЛ-6, ИЛ-8). Исследование влияния снижения уровня старения кожи с помощью определения CCN1 у мышей показало, что старение, по-видимому, является механизмом, контролирующим заживление ран и фиброз [23]. Увеличение фазы воспаления замедляет регенерацию и снижает репаративный потенциал [24]. В других моделях заживления, таких как паракринная функция печени, старение, вызванное TGF-β, вырабатываемым SASP, также препятствовало заживлению ран [25]. Так, замедленное заживление часто встречается у пациентов с диабетом и у пожилых людей [26].
Различные проявления старения клеток, по-видимому, связаны с хроническими заболеваниями. В случае незаживающих ран при диабете было показано, что изменение специфических путей гибели клеток, таких как ферроптоз, замедляется, что способствует сохранению стареющих клеток [27, 28].
Именно по этим причинам использование современных интенсивных технологий ограничивается возрастом до 65 лет ввиду замедленной регенерации. Однако подбор оптимальных параметров воздействия на кожу, снижающих уровень агрессии, помогает добиться выраженных результатов [29].
Цель – оценить с помощью гистологического исследования регенеративные особенности кожи через месяц после проведения комбинированного аппаратного воздействия игольчатого RF и лазерной технологии, учитывая индивидуальный подбор параметров проведения процедуры для снижения уровня агрессии.
Материал и методы
Аппаратное воздействие включало комбинированное применение игольчатого RF и лазерной технологии; процедуры проводили после нанесения топической анестезии.
Высокочастотное излучение подается через одноразовые наконечники с изолированными микроиглами, через которые поступает энергия биполярной частоты для нагрева целевой ткани дермы. Иглы автоматически вводятся и извлекаются с помощью манипулы. Внутри кожи высокочастотная энергия 460 кГц проходит между положительными и отрицательно заряженными рядами игл, создавая электротермическую реакцию, благодаря которой достигается коагуляция целевой ткани.
Далее проводили фракционную лазерную терапию с длиной волны 1927 нм. Во всех трех клинических случаях параметры проведения каждой процедуры подбирали с учетом возраста и особенностей кожи и сопутствующих патологий пациентов. Гистологическое исследование кожи в заушной области через месяц после терапии с целью изучения репаративных процессов после сочетанных аппаратных воздействий проводили всем пациентам. Окрашивание срезов осуществляли стандартно – гематоксилин-эозином, также для фиксации точной картины изменений в коже после проведенного лечения использовали дополнительные методы окрашивания – по Ван-Гизону и по Массону. Так, окраска коллагеновых волокон по Ван-Гизону позволяет четко визуализировать структуру соединительной ткани и выявить степень фиброза, смесь кислого фуксина и пикриновой кислоты (пикрофуксин) – дифференцировать соединительную ткань. Коллагеновые волокна окрашиваются в ярко-красный цвет, а другие тканевые элементы, такие как мышечные и эластические волокна, а также ядра клеток, приобретают желтые, оранжевые или бурые оттенки. Окрашивание по Массону (трихром) придает коллагеновым волокнам синий или зеленый цвет, что позволяет им контрастировать с другими структурами ткани, такими как мышечные волокна (красный цвет) и ядра клеток (черный цвет). Таким образом, использование трихрома по Массону предоставляет более полную картину трехкомпонентного окрашивания и часто применяется для диагностики фиброзов, что имеет важное клиническое значение.
Клинические случаи
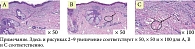
Пациентка 1., 74 года. В анамнезе рак щитовидной железы (тиреоидэктомия с двусторонней лимфодиссекцией в 2004 г.); состояние компенсации на момент процедуры, разрешение онколога на проведение процедуры получено. Объективно: смешанный тип старения, птоз мягких тканей лица, тонус и тургор значительно снижены, рельеф кожи неравномерный, цвет кожи тусклый, с сероватым оттенком. Параметры игольчатого RF: глубина от 1,3 до 2,0 мм с подачей энергии от 14 до 24 мДж. Лазерный фракционный термолиз 1927 нм, диаметр пучка – 200 мкм, мощность – 4 мДж на импульс в динамическом режиме, два прохода. Через месяц после проведенных воздействий отмечено клиническое улучшение качественных характеристик кожи: тонус и тургор значимо улучшились, рельеф стал более ровным, мелких морщин стало меньше, тон кожи выровнялся.
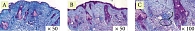
Гистологически в эпидермисе отмечается уменьшение гиперкератоза, сглаживание эпидермальных гребней. В дерме отмечены выраженные лимфоцитарные инфильтраты, что свидетельствует о незавершенном воспалительном процессе, а также единичные участки с увеличенным количеством упорядоченных коллагеновых волокон, что говорит о начале и продолжении синтеза коллагена и его реорганизации. Признаков фиброза не отмечено (рис. 1–3).
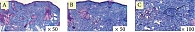
Пациентка 2., 71 год. В анамнезе сахарный диабет 2-го типа, компенсированный. Объективно: смешанный тип старения, тонус и тургор кожи лица снижены, рельеф кожи неравномерный, цвет кожи тусклый, птоз мягких тканей лица. Игольчатый RF: глубина от 1,2 до 2,0 мм с подачей энергии от 14 до 20 мДж. Лазерный фракционный термолиз 1927 нм, диаметр пучка – 200 мкм, мощность – 4 мДж на импульс в динамическом режиме, три прохода. Через месяц после процедур клиническая картина улучшилась: тонус и тургор стали лучше, рельеф изменился и стал более ровным, птоз мягких тканей лица уменьшился, тон кожи стал более ровным.
Гистологически в эпидермисе отмечается уменьшение гиперкератоза, сглаживание эпидермальных гребней. В сосочковом и сетчатом слоях дермы наблюдаются единичные слабовыраженные лимфоцитарные инфильтраты, что свидетельствует о завершении воспаления, также визуализируются локальное увеличение количества коллагеновых волокон и их упорядочение (рис. 4–6).
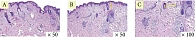
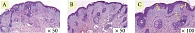
Пациентка 3., 69 лет. Соматический анамнез не отягощен. Объективно: смешанный тип старения, тонус и тургор снижены, рельеф кожи неравномерный, цвет кожи тусклый, птоз мягких тканей лица. Игольчатый RF: глубина от 1,3 до 2,0 мм с подачей энергии от 14 до 22 мДж. Лазерный фракционный термолиз 1927 нм, диаметр пучка – 200 мкм, мощность – 6 мДж на импульс в динамическом режиме, три прохода. Через месяц после проведенных процедур отмечены улучшение тонуса и тургора кожи, уменьшение птоза мягких тканей лица, улучшение рельефа и цвета кожи.
Гистологическая картина демонстрирует уменьшение гиперкератоза, сглаживание эпидермальных гребней. В сосочковом слое дермы отмечаются компактизация и реорганизация коллагеновых волокон, в сетчатом слое дермы коллагеновые волокна стали более структурированными и упорядоченными (рис. 7–9).
Гистологическое исследование кожи через месяц после проведенных процедур у возрастных пациентов показало наличие влияния сопутствующих патологий на процессы регенерации и восстановительные процессы. Однако полученная в результате исследования клиническая картина указывает на то, что проведение указанных процедур способствует восстановлению сетчатого слоя дермы, улучшению состояния поверхностных слоев кожи и, в результате, улучшению качества кожи. Для возрастных пациентов следует подбирать более низкие параметры аппаратного воздействия с учетом ослабленного регенераторного потенциала, исходного состояния кожи и их соматического статуса.
Заключение
Особенностью восстановительных процессов в коже через месяц после комбинированного аппаратного применения игольчатого RF и лазерной технологии у возрастных пациентов являются признаки воспаления, что свидетельствует о замедленной регенерации. При этом уменьшение уровня агрессии параметров в целом оказывает положительное влияние на качественные характеристики кожи без формирования фиброза. Необходимо проведение исследования в более поздний период (через 4–6 месяцев) после процедур для более полного представления о завершенности процессов регенерации.
T.R. Tiratsvian1, J.Yu. Yusova, PhD, Prof., A.Yu. Syryseva
Central State Medical Academy of Department of Presidential Affairs, Moscow
Lomonosov Moscow State University
Contact person: Zhanna Yu. Yusova, zyusova@mail.ru
The use of modern intensive technologies in patients of the older age group is limited due to delayed regeneration and the presence of chronic diseases. Therefore, an individual selection of hardware parameters is necessary, taking into account the skin characteristics of the older age patients to reduce the level of aggression of the procedure.
The aim of the study was to evaluate the early regenerative features of the skin in age–related the older age patients using histological examination one month after combined hardware exposure to radiofrequency microneedle and laser technology (with individual parameter selection and reduced aggression) using the example of three clinical cases. The sections were stained with standard hemotoxylin–eosin, and additional staining methods, Van Gieson and Masson, were used to fully represent the changes in the skin after treatment. According to the results of the study, it was established that the procedures performed help to improve skin quality, restore the reticular layer of the dermis, improve the condition of the surface layers of the skin, while a tendency has been established for the dependence of recovery processes on concomitant pathologies that affect regeneration processes, however, with a decrease in the argessia of the parameters of hardware technologies, skin restoration and improvement of its quality characteristics are observed. Thus, the combined use of radiofrequency microneedle and laser technology with the selection of exposure parameters to reduce the level of aggression in age-related patients has a positive effect on the quality characteristics of the skin, promotes the renewal of collagen structures of the skin without the formation of fibrosis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.