Изучение репаративных процессов у пациентов старше 65 лет после комбинированного воздействия игольчатого RF-лифтинга на аппарате Lutronic Genius и тулиевого лазера 1927 нм LaseMD Ultra
- Аннотация
- Статья
- Ссылки
- English
Цель – изучение кожи после проведения комбинированного аппаратного воздействия игольчатого RF-лифтинга на аппарате Lutronic Genius (РЗН 2022/16505 от 07.02.2022 г.) и тулиевого лазера 1927 нм LaseMD Ultra (РЗН 2024/23104 от 10.07.2024 г.) у возрастных пациентов старше 65 лет с помощью гистологического исследования на примере трех клинических случаев. Было проведено комбинированное аппаратное воздействие игольчатым RF-лифтингом и тулиевым лазером 1927 нм у возрастных пациентов. Оценивали клинические результаты с проведением гистологического исследования кожи и иммуногистохимического исследования с определением типов коллагена и эластина через 1 и 5 месяцев после процедуры. Окрашивание срезов проводили стандартно гематоксилин-эозином, также использовали дополнительные методы окрашивания по Ван-Гизону и по Массону, для полного представления изменений в коже после проводимого лечения использовали иммуногистохимическое исследование на коллагены I и III типов, а также на эластин. Клинические, гистологические и иммуногистохимические данные показали, что комбинированное аппаратное воздействие игольчатого RF-лифтинга на аппарате Lutronic Genius и тулиевого лазера 1927 нм LaseMD Ultra в режимах сниженной интенсивности приводит к улучшению качества кожи, способствует восстановлению сетчатого слоя дермы, при этом отсутствие избыточного накопления коллагена I типа свидетельствует о контролируемом, нефиброзном характере ремоделирования.
Цель – изучение кожи после проведения комбинированного аппаратного воздействия игольчатого RF-лифтинга на аппарате Lutronic Genius (РЗН 2022/16505 от 07.02.2022 г.) и тулиевого лазера 1927 нм LaseMD Ultra (РЗН 2024/23104 от 10.07.2024 г.) у возрастных пациентов старше 65 лет с помощью гистологического исследования на примере трех клинических случаев. Было проведено комбинированное аппаратное воздействие игольчатым RF-лифтингом и тулиевым лазером 1927 нм у возрастных пациентов. Оценивали клинические результаты с проведением гистологического исследования кожи и иммуногистохимического исследования с определением типов коллагена и эластина через 1 и 5 месяцев после процедуры. Окрашивание срезов проводили стандартно гематоксилин-эозином, также использовали дополнительные методы окрашивания по Ван-Гизону и по Массону, для полного представления изменений в коже после проводимого лечения использовали иммуногистохимическое исследование на коллагены I и III типов, а также на эластин. Клинические, гистологические и иммуногистохимические данные показали, что комбинированное аппаратное воздействие игольчатого RF-лифтинга на аппарате Lutronic Genius и тулиевого лазера 1927 нм LaseMD Ultra в режимах сниженной интенсивности приводит к улучшению качества кожи, способствует восстановлению сетчатого слоя дермы, при этом отсутствие избыточного накопления коллагена I типа свидетельствует о контролируемом, нефиброзном характере ремоделирования.













Современный прогресс в области аппаратных технологий для эстетической медицины стимулирует углубленное исследование механизмов регенерации тканей и синолитических процессов, что, в свою очередь, способствует формированию нового направления – регенеративной медицины. Особое внимание уделяется адаптации существующих терапевтических протоколов для пациентов старше 65 лет с более выраженными инволютивными возрастными изменениями. В связи с этим вопросы восстановления и реализации регенераторного потенциала кожи приобретают особую актуальность и являются предметом активных научных изысканий [1, 2].
Восстановление кожи – сложный, многоэтапный процесс с необходимостью строгого контроля с целью обеспечения эффективного восстановления поврежденной ткани и ее структур [3–7]. Способность кожи к регенерации клеточных компонентов снижается под воздействием экзогенных факторов и в процессе естественного старения организма [8, 9]. Из-за снижения репаративного потенциала кожи у возрастных пациентов заживление ран требует большего времени. При повреждении в фазе воспаления у человека в коже происходят клеточные изменения идентичные старению вследствие секреции факторов Senescence-associated secretory phenotype (SASP, сложная смесь воспалительных цитокинов и липидов), в том числе PDGF-A [10]. Большое количество PDGF-A, как важнейший фактор SASP, выделяется стареющими фибробластами, что, в свою очередь, способствует активации миофибробластов из фибробластов и нарушает один из этапов заживления [11]. SASP синтезируется и высвобождается стареющими клетками [12]. Точный состав SASP варьирует и может отличаться в зависимости от типа клеток и агента, вызывающего старение [13, 14]. Несмотря на то что точное определение еще не сформулировано, принято считать, что в состав SASP входят: интерлейкин (ИЛ) 6, ИЛ-1β, ИЛ-8, трансформирующий фактор роста бета (transforming growth factor, TGF-β), матриксные металлопротеазы, биоактивные липиды (например, церамиды и простагландины), серпины и микроРНК, которые способствуют развитию воспаления [15]. Считается, что SASP является ключевым признаком стареющих клеток, однако его регуляция изучена недостаточно. Во многих случаях секреция SASP усиливается вследствие передачи сигналов через NF-KB (универсальный фактор транскрипции) [16, 17]. Длительное присутствие таких измененных клеток в месте раны может препятствовать заживлению или приводить к фиброзу [18]. Этот механизм характерен и для возрастных пациентов [19, 20]. При биологическом старении в коже происходит накопление синтетически неактивных фибробластов, которые не восстанавливают внеклеточный матрикс кожи (ВКМ). Для белкового состава ВКМ выделен отдельный термин «матрисома», объединяющий 43 субъединицы коллагена, 35 протеогликанов, 200 гликопротеинов (включая CCN – семейство белков, ассоциированных с внеклеточным матриксом, участвующих в межклеточной передаче сигналов). Основная функция белков CCN состоит в связывании с белками ВКМ и участии в процессах воспаления и регенерации кожи [21, 22]. CCN-1-индуцированные изменения приводят к снижению коллагена I и III типов, повышению экспрессии провоспалительных цитокинов (ИЛ-1b, ИЛ-6, ИЛ-8). Исследование влияния снижения уровня старения с помощью определения CCN-1 у мышей на кожу показало, что старение, по-видимому, является механизмом, регулирующим заживление ран и фиброз [23]. Увеличение фазы воспаления замедляет регенерацию и снижает репаративный потенциал [24, 25]. Различные проявления старения клеток связаны с хроническими заболеваниями. Например, заживление протекает с затруднением у диабетиков и пожилых людей [26]. В случае незаживающих ран при диабете было показано, что изменение специфических путей гибели клеток, таких как ферроптоз, замедляется, что способствует сохранению стареющих клеток [27, 28].
Исходя из вышеуказанных причин, не рекомендуется проведение пациентам старше 65 лет многих интенсивных технологий. В свою очередь, благодаря снижению уровня агрессии аппаратных методик, у пациентов возрастной группы можно добиться выраженных клинических результатов улучшения показателей кожи [29].
В статье представлены клинические случаи по оценке регенеративных особенностей кожи у возрастных пациентов старше 65 лет с помощью гистологического и иммуногистохимического исследований через 1 и 5 месяцев после проведения комбинированного аппаратного воздействия игольчатым RF-лифтингом на аппарате Lutronic Genius и тулиевым лазером 1927 нм LaseMD Ultra с индивидуальным подбором параметров и снижением уровня агрессии.
Материал и методы
Аппаратное воздействие включало комбинированное применение игольчатого RF-лифтинга на аппарате Lutronic Genius (РЗН 2022/16505 от 07.02.2022 г.) и лазерной технологии 1927 нм LaseMD Ultra (РЗН 2024/23104 от 10.07.2024 г.). Процедуры проводили после нанесения топической анестезии. Высокочастотное излучение поступает через одноразовые наконечники с изолированными микроиглами, через которые подается энергия биполярной частоты для нагрева целевой ткани дермы. Иглы автоматически вводятся и извлекаются с помощью манипулы. Внутри кожи высокочастотная энергия 460 кГц проходит между положительными и отрицательно заряженными рядами игл, создавая электротермическую реакцию, вследствие чего достигается коагуляция целевой ткани. Затем проводили фракционную лазерную терапию 1927 нм. В каждом клиническом случае подбирали мощность используемого метода с учетом возраста, особенностей кожи и сопутствующих патологий. Далее проводили гистологическое и иммуногистохимическое исследования кожи в заушной области до, через месяц и через пять месяцев после терапии с целью изучения репаративных процессов после сочетанных аппаратных воздействий.
Операционный материал оценивали макроскопически и фотографировали, фиксировали в 10%-ном забуференном формалине (Ph 7,0–7,2) в течение 24–48 часов при комнатной температуре. После фиксации образцы подвергали стандартной процедуре гистологической проводки: дегидратация в спиртах восходящей концентрации (от 70% до 100%) и пропитывание парафином по стандартному протоколу. После процедуры гистологической проводки образцы заливали в парафиновые блоки. Гистологические срезы толщиной 3–5 мкм готовили на роторном микротоме НМ 355 S (Thermo Scientific, Германия), расправляли на предметных стеклах; для иммуногистохимических исследований – на положительно заряженных предметных стеклах (Gerhard Menzel GmbH, Германия).
Срезы толщиной 3 мкм окрашивали гематоксилин-эозином в качестве обзорного метода, а также двумя гистохимическими методиками – пикрофуксином по Ван-Гизону и трихромом по Массону для объективной идентификации очагов фиброза.
Иммуногистохимическое исследование выполняли на серийных парафиновых срезах отобранных образцов. Панель моноклональных антител включала: поликлональное кроличье антитело к эластину (Elastin antibody – Cat. No. GTX37428, GeneTex, Irvine, CA, USA) в разведении 1 к 100; коллагену I типа (Collagen I Ab – Cat. No. AF7001, Affinity Biosciences, Cincinnati, OH, USA) в разведении 1 к 150; коллагену III типа (Collagen III – Cat. No. RAH C33, Имтек, Россия) в разведении 1 к 1000.
Постановку реакций осуществляли в соответствии с методикой C.R. Taylor, R.J. Cote (1994) согласно протоколам, прилагаемым к используемым моно- и поликлональным антителам. Позитивные результаты иммуногистохимической реакции учитывали при наличии двух негативных контролей (на специфичность реакции и отсутствие активной эндогенной пероксидазы) и одного внутреннего позитивного на специфичность реакции.
Готовые гистологические, гистохимические и иммуногистохимические препараты анализировали и фотографировали с помощью светового микроскопа Axio Imager M2 (Carl Zeiss Microscopy, Германия), оснащенного цифровой камерой. Полученные цифровые изображения просматривали и анализировали в специализированной программе Pannoramic Slide Viewer (3DHISTECH, Венгрия), позволяющей проводить морфометрические измерения и детальное изучение топографических взаимоотношений тканевых структур.
Клинические случаи
Пациентка Л., 74 года. В анамнезе: рак щитовидной железы (тиреоидэктомия с двусторонней лимфодиссекцией в 2004 г.). Состояние компенсации на момент процедуры, разрешение онколога на проведение процедуры получено. Объективно: смешанный тип старения, птоз мягких тканей лица, тонус и тургор значительно снижены, рельеф кожи неравномерный, цвет кожи тусклый, с сероватым оттенком. Параметры игольчатого RF-лифтинга на аппарате Lutronic Genius: глубина – от 1,3 до 2 мм с подачей энергии – от 14 до 24 мДж. Тулиевый лазер 1927 нм LaseMD Ultra: диаметр пучка – 200 мкм, мощность – 4 мДж на импульс, процедуру проводили в динамическом режиме в два прохода. Через месяц после проводимых воздействий было отмечено клиническое улучшение качественных характеристик кожи, тонус и тургор значимо повысились, рельеф стал более ровным, мелких морщин меньше, цвет кожи стал ровнее. Клинический эффект к пятому месяцу наблюдения повысился.
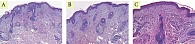
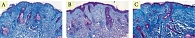
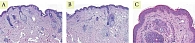
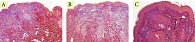
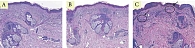
В гистологических исследованиях эпидермиса через месяц отмечается уменьшение гиперкератоза, сглаживание эпидермальных гребней. В дерме отмечены выраженные лимфоцитарные инфильтраты, что свидетельствует о незавершенном воспалительном процессе, а также единичные участки с увеличенным количеством упорядоченных коллагеновых волокон, что подтверждает начало и продолжение синтеза коллагена и его реорганизации. Через пять месяцев отмечается выраженное увеличение количества и упорядочение коллагеновых и эластиновых волокон. Значительное утолщение сосочкового и сетчатого слоев дермы. Признаков фиброза отмечено не было (рис. 1–3). До проведения процедуры экспрессия коллагена I типа в дерме была выражена слабо и неравномерно. Волокна преимущественно локализовались в сетчатом слое, имели разобщенный характер, с признаками дезорганизации и выраженными участками разрыхления межволоконного матрикса; в сосочковом слое экспрессия была минимальна (рис. 4А). Через месяц после процедуры отмечается умеренное усиление иммуногистохимической экспрессии коллагена I типа в верхних отделах сетчатого слоя дермы. Волокна становятся более четко очерченными и упорядоченными, формируется более компактная волокнистая структура, однако выраженного диффузного увеличения интенсивности окрашивания не наблюдается (рис. 4B). Через пять месяцев сохраняется тенденция к структурной организации дермального матрикса без существенного дополнительного нарастания экспрессии коллагена I типа. Коллагеновые волокна располагаются более равномерно и компактно, что свидетельствует о стабилизации ремоделирования дермы без признаков избыточного фибротического ответа (рис. 4C).
До проведения процедуры определялась выраженная, но неоднородная экспрессия коллагена III типа, преимущественно в сосочковом слое дермы и верхних отделах сетчатого слоя. Волокна располагались фрагментарно, с участками дезорганизации и выраженного разрыхления дермального матрикса, что отражало сниженную структурную упорядоченность соединительной ткани (рис. 5A). Через месяц после процедуры отмечается усиление иммуногистохимической экспрессии коллагена III типа с формированием более плотной и равномерно распределенной тонковолокнистой сети. В сосочковом слое дермы волокна становятся более компактными и упорядоченными, уменьшается выраженность межволоконных промежутков, что свидетельствует об активном неоколлагенезе (рис. 5B). Через пять месяцев сохраняется высокая экспрессия коллагена III типа с дальнейшей структурной организацией дермального матрикса. Коллагеновые волокна формируют компактную, хорошо интегрированную сеть с повышенной плотностью и целостностью, что отражает устойчивое ремоделирование дермы преимущественно за счет коллагена III типа (рис. 5C).
До проведения процедуры эластиновая сеть была представлена тонкими, разреженными и фрагментированными волокнами с низкой интенсивностью иммуногистохимического окрашивания. В сосочковом слое дермы волокна определялись единично, в сетчатом слое – разобщенно, с выраженными участками дезорганизации и разрыхления межволоконного матрикса, что отражало снижение структурной целостности эластического каркаса (рис. 6A). Через месяц после процедуры отмечается умеренное усиление экспрессии эластина, преимущественно в сосочковом и верхних отделах сетчатого слоя дермы. Волокна становятся более четко визуализируемыми и формируют более непрерывную, взаимосвязанную сеть, что свидетельствует об активации процессов эластогенеза на фоне ремоделирования дермы (рис. 6B). Через пять месяцев сохраняется сформированная архитектоника эластической сети с тенденцией к дальнейшей структурной упорядоченности волокон. Эластин распределяется более равномерно, интегрируясь в дермальный матрикс без признаков патологического утолщения или хаотичной гиперплазии, что отражает стабилизацию и функциональное восстановление.
Пациентка И., 71 год. В анамнезе: сахарный диабет 2-го типа, компенсированный. Объективно: смешанный тип старения, тонус и тургор снижены, рельеф кожи неравномерный, цвет кожи тусклый, птоз мягких тканей лица. Игольчатый RF-лифтинг на аппарате Lutronic Genius: глубина – от 1,2 до 2,0 мм с подачей энергии – от 14 до 20 мДж. Тулиевый лазер 1927 нм LaseMD Ultra: диаметр пучка – 200 мкм, мощность – 4 мДж на импульс, процедуру проводили в динамическом режиме в три прохода. В наблюдении через месяц после процедур клиническая картина улучшилась: тонус и тургор стали лучше, рельеф изменился и стал более ровным, птоз мягких тканей лица уменьшился, цвет кожи стал более ровным. К пятому месяцу наблюдалось улучшение клинического результата.
Гистологически в эпидермисе отмечается уменьшение гиперкератоза, сглаживание эпидермальных гребней. В сосочковом и сетчатом слоях дермы единичные, слабовыраженные лимфоцитарные инфильтраты, что свидетельствует о завершении воспаления, также визуализируются локальное увеличение количества и упорядочение коллагеновых волокон. Через пять месяцев отмечается выраженное увеличение количества и упорядочение коллагеновых и эластиновых волокон, значительное утолщение сосочкового и сетчатого слоев дермы (рис. 7–9).
Экспрессия коллагена I типа в дерме до проведения процедуры определялась умеренно, преимущественно в сетчатом слое, с неравномерной интенсивностью окрашивания. Коллагеновые волокна располагались разобщенно, местами с признаками дезорганизации и выраженными участками разрыхления межволоконного матрикса; в сосочковом слое экспрессия минимальна (рис. 10A). Через месяц после процедуры отмечается умеренное усиление интенсивности иммуногистохимической реакции в верхних отделах сетчатого слоя дермы с формированием более компактно расположенных волокон. Архитектоника дермального матрикса становится более упорядоченной, однако выраженного диффузного нарастания экспрессии не наблюдается (рис. 10B). Через пять месяцев сохраняется тенденция к структурной организации коллагеновых волокон без существенного дополнительного увеличения интенсивности окрашивания. Коллаген I типа представлен более равномерной и компактной волокнистой сетью, что свидетельствует о стабилизации процессов ремоделирования дермы без признаков избыточного фибротического ответа (рис. 10C).
До проведения процедуры определялась выраженная, но неравномерная экспрессия коллагена III типа, преимущественно в сосочковом и верхних отделах сетчатого слоя дермы. Волокна имели рыхлую, частично дезорганизованную архитектонику с участками фрагментации и разобщения, что отражало неоднородность дермального матрикса (рис. 11A). Через месяц после процедуры отмечается усиление иммуногистохимической экспрессии коллагена III типа с формированием более плотной и равномерной тонковолокнистой сети, преимущественно в сосочковом слое дермы. Волокна располагаются более упорядоченно, уменьшается выраженность участков разрыхления, что свидетельствует об активном неоколлагенезе (рис. 11B). Через пять месяцев сохраняется высокая экспрессия коллагена III типа с дальнейшей структурной организацией волокон и формированием компактной, хорошо интегрированной волокнистой сети. Отмечается стабилизация дермального матрикса и повышение его структурной целостности, что отражает устойчивое ремоделирование дермы преимущественно коллагеном III типа (рис. 11C).
Эластиновые волокна в дерме определялись в виде тонкой, разреженной и фрагментированной сети с низкой интенсивностью иммуногистохимического окрашивания. В сосочковом слое они были представлены единичными, слабо визуализируемыми структурами, в сетчатом слое – разобщенными и частично дезорганизованными волокнами, что отражало сниженный эластический каркас дермы (рис. 12A). Через месяц после процедуры отмечается умеренное усиление экспрессии эластина, преимущественно в сосочковом и верхних отделах сетчатого слоя дермы. Волокна становятся более четкими, формируют более непрерывную и взаимосвязанную сеть, что свидетельствует об активации процессов раннего эластогенеза и ремоделирования дермального матрикса (рис. 12B). Через пять месяцев сохраняется сформированная архитектоника эластической сети с тенденцией к дальнейшей структурной организации волокон. Эластиновые структуры интегрированы в дермальный матрикс более равномерно, без признаков патологического утолщения или хаотичной гиперплазии, что отражает стабильное восстановление эластического каркаса дермы (рис. 12C).
Пациентка В., 69 лет. Соматический анамнез не отягощен. Объективно: смешанный тип старения, тонус и тургор снижены, рельеф кожи неравномерный, цвет кожи тусклый, птоз мягких тканей лица. Игольчатый RF-лифтинг на аппарате Lutronic Genius: глубина – от 1,3 до 2,0 мм с подачей энергии – от 14 до 22 мДж. Тулиевый лазер 1927 нм LaseMD Ultra: диаметр пучка – 200 мкм, мощность – 6 мДж на импульс, процедуру проводили в динамическом режиме в три прохода. После проведенных процедур через месяц отмечается улучшение тонуса и тургора кожи, уменьшение птоза мягких тканей лица, улучшение рельефа и цвета кожи. Динамика клинического улучшения наблюдается и к пятому месяцу.
Гистологическая картина демонстрирует уменьшение гиперкератоза, сглаживание эпидермальных гребней. В сосочковом слое дермы отмечаются компактизация и реорганизация коллагеновых волокон, в сетчатом слое дермы коллагеновые волокна более структурированы и упорядочены. Через пять месяцев гистологический анализ демонстрирует уменьшение рогового слоя с уменьшением отслойки пластов роговых чешуек, в сосочковом слое дермы отмечается выраженный прирост коллагеновых и эластиновых волокон, а также выраженная компактизация волокон и утолщение сосочкового слоя (рис. 13–15).
До проведения лечения в дерме определялась умеренная экспрессия коллагена I типа с преимущественной локализацией в сетчатом слое. Коллагеновые волокна имели неравномерную толщину, располагались разобщенно, с участками разрыхления межволоконного матрикса; в сосочковом слое экспрессия была выражена слабо (рис. 16A). Через месяц после процедуры отмечается тенденция к умеренному усилению иммуногистохимической экспрессии коллагена I типа, преимущественно в верхних отделах сетчатого слоя дермы. Волокна становятся более упорядоченными, с формированием более плотной волокнистой сети, однако статистически значимого увеличения интенсивности окрашивания не наблюдается (рис. 16B). Через пять месяцев сохраняется ранее сформированная архитектоника дермального матрикса без признаков выраженного дополнительного нарастания экспрессии коллагена I типа. Волокна остаются структурированными и компактно организованными, что свидетельствует о стабилизации ремоделирования дермы без избыточного фибротического компонента (рис. 16C).
Экспрессия коллагена III типа определялась преимущественно в сосочковом слое дермы в виде тонких, фрагментарно расположенных волокон с неравномерной интенсивностью окрашивания. До процедуры сетчатый слой был представлен разобщенными и частично дезорганизованными волокнистыми структурами (рис. 17A). Через месяц после процедуры отмечается выраженное усиление иммуногистохимической экспрессии коллагена III типа, преимущественно в сосочковом и верхних отделах сетчатого слоя дермы. Формируется более плотная, тонковолокнистая и равномерно организованная сеть с уменьшением участков разрыхления дермального матрикса, что свидетельствует об активном неоколлагенезе (рис. 17B). Через пять месяцев сохраняется и усиливается экспрессия коллагена III типа с формированием компактной, хорошо структурированной волокнистой сети. Коллагеновые волокна располагаются более упорядоченно, отмечается выраженное утолщение сосочкового слоя и повышение структурной целостности дермального матрикса, что отражает устойчивое ремоделирование дермы преимущественно коллагеном III типа (рис. 17C).
Эластиновые волокна в дерме визуализировались в виде разреженной, фрагментированной сети с неравномерной интенсивностью окрашивания. В сосочковом слое дермы они были представлены тонкими, частично дезорганизованными структурами, в сетчатом слое – единичными, более плотными пучками с участками разрыхления межволоконного пространства (рис. 18A). Через месяц после процедуры отмечается усиление экспрессии эластина преимущественно в сосочковом и верхних отделах сетчатого слоя дермы. Волокна становятся более четко очерченными, формируют более равномерную и связанную сеть, что свидетельствует об активации процессов эластогенеза в ранние сроки ремоделирования (рис. 18B). Через пять месяцев сохраняется сформированная волокнистая архитектоника с более выраженной интеграцией эластиновых волокон в дермальный матрикс. Отмечается повышение плотности и структурной организованности эластической сети без признаков хаотичного гиперэластоза, что отражает стабильное восстановление эластического каркаса дермы (рис. 18C).
Гистологическое и иммуногистохимическое исследования кожи у возрастных пациентов через пять месяцев после комбинированного аппаратного воздействия игольчатого RF-лифтинга на аппарате Lutronic Genius и тулиевого лазера 1927 нм LaseMD Ultra показали, что проводимые процедуры приводят к улучшению качества кожи, способствуют физиологичному восстановлению сетчатого слоя дермы, улучшают состояние поверхностных слоев кожи. Для возрастных пациентов вследствие ослабленного регенераторного потенциала следует подбирать более низкие параметры аппаратного воздействия, учитывать исходное состояние кожи и соматический статус пациента.
Таким образом, проведение комбинированного аппаратного воздействия игольчатым RF-лифтингом на аппарате Lutronic Genius (РЗН 2022/16505 от 07.02.2022 г.) и тулиевым лазером 1927 нм LaseMD Ultra (РЗН 2024/23104 от 10.07.2024 г.) у возрастных пациентов со снижением уровня агрессии параметров оказывает положительное влияние на качественные характеристики кожи, способствует обновлению коллагеновых структур кожи без формирования фиброза.
Авторы заявляют об отсутствии конфликта интересов.
T.R. Tiratsvian, J.Yu. Yusova, PhD, Prof., L.S. Kruglova, PhD, Prof.
Medical Center “Clinic of Youth”, Moscow
Central State Medical Academy of Department of Presidential Affairs, Moscow
Contact person: Zhanna Yu. Yusova, zyusova@mail.ru
Intensive hardware technologies in aesthetic medicine are quite popular today, however, the use of aggressive methods is not recommended in patients with low regenerative potential, including the older age group after 65 years. Recently, the study of recovery processes and the selection of parameters of aggressive hardware correction methods used in patients of the older age group has been of increased interest, as demand is growing. When working with age-related skin, there are a number of features: reducing the intensity of exposure, increasing the interval between treatments, and increasing the number of treatments per course of treatment.
The aim of the work was to study the skin after combined hardware exposure to a radiofrequency microneedle Lutronic Genius (RH 2022/16505 dated 02/07/2022) and a 1927 nm LaseMD Ultra thulium laser (RH 2024/23104 dated 07/10/2024) in aged patients over 65 years of age using histological examination. We have presented 3 clinical cases. A combined hardware effect of an radiofrequency microneedle and a 1927 nm thulium laser was performed in elderly patients. The clinical results were evaluated with histological examination of the skin and immunohistochemical examination with the determination of collagen and elastin types 1 and 5 months after the procedure. The sections were stained with standard hemotoxylin-eosin, additional Van Gieson and Masson staining methods were also used, and an immunohistochemical examination for types I and III collagens, as well as elastin, was used to fully represent the changes in the skin after the treatment. Clinical, histological and immunohistochemical data have shown that the combined hardware effect of the Lutronic Genius radiofrequency microneedle and the 1927 nm LaseMD Ultra thulium laser in reduced intensity modes leads to an improvement in skin quality, promotes the restoration of the reticular layer of the dermis, while the absence of excessive accumulation of type I collagen indicates a controlled, non-fibrous nature of remodeling.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.