Пациенты с некоронарогенной желудочковой аритмией покоя: фокус на проведение нагрузочных проб
- Аннотация
- Статья
- Ссылки
- English
Цель – провести клинико-электрокардиографическую оценку аритмии во время нагрузочной пробы у пациентов с некоронарогенными ЖА, регистрируемыми в покое.
Материал и методы. В исследование вошли 140 пациентов (56 мужчин и 84 женщины; средний возраст – 43,8 ± 13,5 года) без известной диагностированной ранее ишемической болезни сердца (ИБС), с частыми ЖА, зарегистрированными преимущественно в покое при холтеровском мониторировании (ХМ). Всем пациентам выполнен тредмил-тест (ТТ) по стандартному протоколу Bruce с оценкой симптомности, гемодинамической значимости, количества, морфологии и комплексности ЖА. При наличии факторов риска и/или претестовой вероятности ИБС > 15% проводилась парная нагрузочная фармакологическая проба с нитроглицерином или применялись визуализирующие методики. После исключения ишемического характера ЖА у пациентов с прогрессирующими и сохраняющимися смешанными аритмиями выполнялся ТТ на фоне приема бета-АБ.
Результаты. В ходе ХМ зарегистрированы преимущественно мономорфные желудочковые эктопические комплексы, количество одиночных комплексов за сутки в среднем составило 12 147 ± 1476, парных – 246 ± 71, неустойчивых ускоренных идиовентрикулярных ритмов и желудочковых тахикардий – 95 ± 12. Суточное распределение ЖА носило смешанный характер: ЖА регистрировались как в дневное, так и в ночное время. Более чем у половины больных (n = 73; 52,1%), согласно классификации J.T. Bigger (1984.), ЖА относились к неопасным или доброкачественным, у остальных – к потенциально опасным. В зависимости от варианта поведения во время ТТ выявлены вагусзависимые ЖА у 78 (56%) пациентов, смешанные ригидные – у 27 (19%), смешанные прогрессирующие – у 29 (21%) пациентов. ИБС впервые установлена у 6 (4%) больных. Пациентам со смешанными ЖА проведена проба с бета-АБ. Положительная реакция на пробу в виде исчезновения или уменьшения ЖА во время ФН и одновременное появление желудочковых нарушений ритма в периоды покоя позволили подтвердить совместное влияние симпатического и парасимпатического отделов АНС и прогнозировать эффективность комбинированной терапии бета-АБ и препаратом класса 1С с холинолитической активностью.
Заключение. Проведение пробы с ФН пациентам с ЖА покоя целесообразно при условии, если: во время ХМ не достигнута субмаксимальная частота сердечных сокращении; ЖА сопровождаются клинической симптоматикой и/или их количество превышает 10% общего числа сердечных сокращений по данным ХМ; ЖА сохраняются или прогрессируют во время пробы с ФН целесообразна парная нагрузочная фармакологическая проба с бета-АБ.
Цель – провести клинико-электрокардиографическую оценку аритмии во время нагрузочной пробы у пациентов с некоронарогенными ЖА, регистрируемыми в покое.
Материал и методы. В исследование вошли 140 пациентов (56 мужчин и 84 женщины; средний возраст – 43,8 ± 13,5 года) без известной диагностированной ранее ишемической болезни сердца (ИБС), с частыми ЖА, зарегистрированными преимущественно в покое при холтеровском мониторировании (ХМ). Всем пациентам выполнен тредмил-тест (ТТ) по стандартному протоколу Bruce с оценкой симптомности, гемодинамической значимости, количества, морфологии и комплексности ЖА. При наличии факторов риска и/или претестовой вероятности ИБС > 15% проводилась парная нагрузочная фармакологическая проба с нитроглицерином или применялись визуализирующие методики. После исключения ишемического характера ЖА у пациентов с прогрессирующими и сохраняющимися смешанными аритмиями выполнялся ТТ на фоне приема бета-АБ.
Результаты. В ходе ХМ зарегистрированы преимущественно мономорфные желудочковые эктопические комплексы, количество одиночных комплексов за сутки в среднем составило 12 147 ± 1476, парных – 246 ± 71, неустойчивых ускоренных идиовентрикулярных ритмов и желудочковых тахикардий – 95 ± 12. Суточное распределение ЖА носило смешанный характер: ЖА регистрировались как в дневное, так и в ночное время. Более чем у половины больных (n = 73; 52,1%), согласно классификации J.T. Bigger (1984.), ЖА относились к неопасным или доброкачественным, у остальных – к потенциально опасным. В зависимости от варианта поведения во время ТТ выявлены вагусзависимые ЖА у 78 (56%) пациентов, смешанные ригидные – у 27 (19%), смешанные прогрессирующие – у 29 (21%) пациентов. ИБС впервые установлена у 6 (4%) больных. Пациентам со смешанными ЖА проведена проба с бета-АБ. Положительная реакция на пробу в виде исчезновения или уменьшения ЖА во время ФН и одновременное появление желудочковых нарушений ритма в периоды покоя позволили подтвердить совместное влияние симпатического и парасимпатического отделов АНС и прогнозировать эффективность комбинированной терапии бета-АБ и препаратом класса 1С с холинолитической активностью.
Заключение. Проведение пробы с ФН пациентам с ЖА покоя целесообразно при условии, если: во время ХМ не достигнута субмаксимальная частота сердечных сокращении; ЖА сопровождаются клинической симптоматикой и/или их количество превышает 10% общего числа сердечных сокращений по данным ХМ; ЖА сохраняются или прогрессируют во время пробы с ФН целесообразна парная нагрузочная фармакологическая проба с бета-АБ.


Несмотря на то что желудочковые аритмии (ЖА) считаются одними из самых опасных нарушений ритма (НР), их прогноз во многом зависит от патологии, на фоне которой они возникают. Именно поэтому верификация риска развития внезапной сердечной смерти и разработка диагностических алгоритмов ведения пациентов с ЖА остаются актуальными проблемами современной аритмологии.
Разрабатываются подходы к ведению пациентов с уже доказанным высоким риском внезапной сердечной смерти – на фоне ишемической болезни сердца (ИБС), кардиомиопатий и каналопатий [1, 2]. Среди них опасными признаны ЖА, которые провоцируются физической нагрузкой (ФН) [1–3].
Возможно, поэтому в клинических рекомендациях по диагностике и ведению пациентов с ЖА показаниями к проведению пробы с дозированной ФН являются средняя или высокая претестовая вероятность (ПТВ) ИБС (ЕОК IВ), подозрение на связь аритмии с ФН, а также оценка эффективности результатов медикаментозной терапии или аблации (ЕОК IА (УУР С, УДД 5) [1, 2].
«За кадром» остаются пациенты, у которых НР регистрируются преимущественно в покое, нет выраженных структурных изменений в сердце, низкая ПТВ ИБС. Но именно ЖА покоя часто сопровождаются выраженной симптоматикой и высоким бременем аритмии. При этом показания к проведению нагрузочной пробы в существующих рекомендациях четко не обозначены, в то время как получаемая во время ФН информация позволяет значительно расширить понимание механизмов ЖА. Проба с ФН считается идеальным и самым естественным видом провокации и активации симпатической нервной системы, вызывает ряд важнейших физиологических изменений, которые могут как спровоцировать развитие НР, так и привести к их исчезновению. С помощью пробы с ФН оценивают влияние автономной нервной системы (АНС) как дополнительного пускового механизма, приводящего к индукции ЖА. Этот факт необходимо учитывать не только при выборе антиаритмического препарата (ААП), но и для клинической оценки аритмии в целом.
По мнению С.П. Голицына, вполне убедительно участие АНС прослеживается в случаях некоронарогенной ЖА, когда нарушения нейровегетативной регуляции представляются единственным значимым фактором развития НР [4, 5].
М.С. Кушаковский учитывал аритмогенную роль АНС при оценке пароксизмальной фибрилляции предсердий, выделяя ее вагусную, адренергическую и смешанную формы [6].
Что касается ЖА, используемые протоколы проб с ФН, состоящие как из периодов покоя, так и периодов нагрузки, позволяют обнаруживать не только симпатозависимые нарушения ритма, считающиеся наиболее прогностически неблагоприятными, но и вагусзависимые ЖА [7–9]. Проба с ФН выявляет наименее изученные и сложные для клинического ведения формы ЖА, когда НР регистрируются у пациентов и в покое, и во время ФН, вследствие чего применение стандартных подходов к выбору ААП затруднено. Такие ЖА по сути являются смешанными с точки зрения участия АНС в аритмогенезе [1, 2, 7].
Представляем подробный анализ вариантов поведения НР во время пробы с ФН у пациентов с ЖА покоя.
Цель – провести клинико-электрокардиографическую оценку аритмии во время нагрузочной пробы у пациентов с некоронарогенными ЖА, регистрируемыми в покое.
Материал и методы
Из пациентов, находившихся на диспансерном наблюдении в НИЛ электрокардиологии НМИЦ им. В.А. Алмазова, для участия в проспективном несравнительном неконтролируемом исследовании отобрано 140 человек (56 мужчин и 84 женщины в возрасте от 20 до 68 лет, средний возраст – 43,8 ± 13,5 года) с частой ЖА, без установленного ранее диагноза ИБС, у которых, по данным холтеровского мониторирования (ХМ), ЖА регистрировались преимущественно в покое.
Критерии включения в исследование:
- возраст ≥ 18 лет;
- синусовый ритм;
- ЖА в покое;
- отсутствие достижения субмаксимальной частоты сердечных сокращений (ЧСС) во время ХМ;
- отсутствие противопоказаний к выполнению нагрузочной пробы.
В качестве нагрузочной пробы применяли тредмил-тест (ТТ). ТТ проводился по стандартному протоколу Bruce в утренние часы на оборудовании Schiller CS-200 с использованием регистрирующей 12 отведений ЭКГ-системы «Кардиотехника-07» (ЗАО «Инкарт», Россия) без какой-либо терапии, за исключением гипотензивной. Во время нагрузочной пробы оценивали симптомность, гемодинамическую значимость, количество, морфологию и комплексность ЖА. Субмаксимальная ЧСС рассчитывалась по формуле: (220 - возраст больного) × 0,85. Оценка сегмента ST проводилась в 12 отведениях. Выполняли поминутный анализ количества желудочковых эктопических комплексов (ЖЭК), фиксировали ЧСС исчезновения и возобновления ЖА в процессе ТТ. Артериальное давление измеряли сфигмоманометром методом Короткова. Для определения воспроизводимости результатов на следующий день при аналогичных условиях ТТ выполняли повторно. Прогрессированием ЖА во время ФН считалось увеличение количества одиночных ЖЭК в два раза и более, а также увеличение комплексности ЖА – появление/увеличение количества парных ЖЭК, эпизодов желудочковой тахикардии (ЖТ). Всем участникам исследования выполнялась эхокардиография (ЭхоКГ) на аппарате Philips iE33 Matrix. В лаборатории центра проводилось биохимическое исследование крови с целью исключения электролитных и гормональных нарушений, а также оценки липидного обмена. У каждого пациента рассчитывалась ПТВ ИБС с учетом пола, возраста, характера болевого синдрома в грудной клетке или одышки [10]. При наличии факторов риска и/или ПТВ > 15% (умеренный и высокий риск) с целью исключения ишемического характера нагрузочных ЖА при условии воспроизводимости результатов ТТ на следующий день проводились парная нагрузочная фармакологическая проба с 0,5 мг нитроглицерина или визуализирующие методики. После исключения ишемического характера ЖА у пациентов с прогрессирующими и сохраняющимися (смешанными) аритмиями выполнялась фармакологическая проба с бета-адреноблокатором (бета-АБ) короткого действия – пропранололом 60 мг. Через 60 минут после однократного приема внутрь бета-АБ короткого действия выполняли ТТ. Проба расценивалась как положительная, если фиксировалось уменьшение или исчезновение ЖА на высоте ФН или в раннем восстановительном периоде (ВП). Если же одновременно с этим в претесте одиночные ЖЭК увеличивались или сохранялись в том же количестве, то подтверждалось комбинированное влияние АНС на эктопический очаг и ЖА признавались смешанными. Такое поведение НР в ответ на принятый бета-АБ короткого действия также позволяло прогнозировать антиаритмическую эффективность комбинации бета-АБ и ААП класса IC с холинолитическим эффектом.
Исследование выполнено в соответствии со стандартами Надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации. Протокол исследования одобрен этическим комитетом. Все пациенты дали письменное информированное согласие на участие в исследовании.
Результаты
Жалобы на перебои в работе сердца, сердцебиение, головокружение, пресинкопальные состояния предъявляли 87% пациентов.
В результате ХМ регистрировались преимущественно мономорфные ЖЭК, количество одиночных за сутки в среднем составило 12 147 ± 1476, парных – 246 ± 71, неустойчивых ускоренных идиовентрикулярных ритмов и ЖТ – 95 ± 12. Суточное распределение ЖА носило смешанный характер: ЖА регистрировались и в дневное, и в ночное время. Более чем у половины больных (n = 73; 52,1%), согласно классификации J.T. Bigger (1984), ЖА относились к неопасным или доброкачественным, у остальных – к потенциально опасным.
В качестве основного заболевания были выявлены следующие нозологии: гипертоническая болезнь стадий I–II – 57 (40,7%) пациентов, постмиокардический кардиосклероз – 7 (5,0%), малые аномалии развития сердца – 9 (6,4%), в частности пролапс митрального клапана с митральной регургитацией 1–2-й степени (n = 5), ложные хорды левого желудочка (n = 4).
Из сопутствующих заболеваний чаще встречалась патология желудочно-кишечного тракта (хронический гастрит, гастроэзофагеальная рефлюксная болезнь, хронический холецистит) – 64 (45,7%) случая, хронический пиелонефрит – 7 (5,0%), дегенеративно-дистрофические заболевания позвоночника – 17 (12,1%), тревожные расстройства – 22 (15,7%) случая. У 31 (22,1%) пациента не обнаружено ни патологии сердечно-сосудистой системы, ни сопутствующих заболеваний.
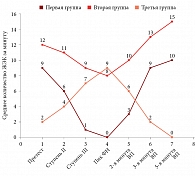
Среди 140 обследуемых с ЖА в покое у 105 пациентов ТТ был отрицательный. На основании поведения ЖА во время ТТ пациенты были разделены на три группы. В первую группу вошли 78 (56%) пациентов, у которых во время ТТ наблюдалось уменьшение количества или исчезновение ЖА на пике нагрузки, во вторую – 27 (19%) пациентов с аритмией, сохранявшейся на протяжении выполнения всей пробы без прогрессирования. У 35 (25%) больных третьей группы имевшиеся в претесте ЖА прогрессировали в ходе ТТ и/или в раннем ВП, при этом ишемического смещения сегмента ST не было. С учетом такого поведения НР у пациентов третьей группы проба расценена как сомнительная, что потребовало исключения ИБС. На основании жалоб, наличия умеренной и высокой ПТВ проведение пробы с нитроглицерином потребовалось 11 пациентам, у шестерых впервые была выявлена ИБС, ввиду чего они были исключены из исследования. Таким образом, в третьей группе осталось 29 человек.
Используемая нами программа обработки ЭКГ, зарегистрированной в ходе ТТ, позволила провести поминутный количественный анализ ЖЭК в течение всего периода выполнения пробы (рис. 1).
Первая группа (n = 78; 49 женщин, 29 мужчин; средний возраст – 45,1 ± 11,3 года) с наиболее частым вариантом поведения ЖА покоя – исчезающие во время ТТ, вагусзависимые или ингибируемые ФН – характеризовалась высокой толерантностью к ФН. Все пациенты этой группы достигли субмаксимальной ЧСС (таблица). В претесте регистрировались одиночные ЖЭК в среднем 9,4 ± 4,3 в минуту с прогрессирующим снижением их количества по мере увеличения ЧСС и мощности ФН. Средняя ЧСС, при которой исчезли ЖЭК, составила 117 ± 20 в минуту. На пике ФН ни у кого из пациентов первой группы ЖЭК не регистрировались, в ВП аритмия возобновилась у 50 (64%) пациентов при ЧСС 91,3 ± 5,2 в минуту. С третьей минуты ВП количество ЖЭК возвращалось к исходным значениям.
Характерное распределение ЖЭК во время ТТ в первой группе представлено на рис. 2.
Пациенты второй группы (n = 27; 16 женщин, 11 мужчин; средний возраст 58 ± 9,4 года) со смешанным ригидным распределением ЖА во время ТТ характеризовались также высокой, но несколько меньшей, чем в первой группе, толерантностью к ФН. Все пациенты второй группы достигли субмаксимальной ЧСС (см. таблицу).
Отличительной чертой в этой группе было наличие более частых одиночных ЖЭК в претесте (12,3 ± 4 в минуту). По мере увеличения ЧСС и мощности ФН отмечалось снижение количества ЖЭК, но полного исчезновения не было. Характерными для данной группы были появление сливных комплексов и отсутствие прогрессирования ЖА на пике ФН (7,9 ± 4,3 ЖЭК в минуту). При этом в позднем ВП желудочковая эктопическая активность возрастала. В отличие от остальных пациентов у больных этой группы регистрировались парные ЖЭК и неустойчивые ЖТ. Появление сливных комплексов указывало на парасистолический характер аритмии. Учитывая сохранение ЖЭК на протяжении всего периода выполнения пробы, то есть смешанный характер ЖА, свидетельствовавший об одновременном влиянии парасимпатического и симпатического отделов АНС на эктопический очаг, следующим этапом проводилась проба с бета-АБ [11]. Проба расценена как положительная: у всех пациентов ЖА на высоте ФН перестали регистрироваться, но сохранялись в претесте и позднем ВП (см. таблицу).
Представители третьей группы (n = 29; 16 женщин, 13 мужчин; средний возраст – 47,2 ± 13,1 года) со смешанными прогрессирующими ЖА во время ФН показали высокую толерантность к ФН, однако максимальная достигнутая ЧСС у них была ниже, чем у пациентов первой и второй групп, поскольку нагрузка прекращалась из-за прогрессирующего характера НР. Кривая динамики количества ЖА носила обратный характер: исходно минимальное количество ЖЭК, НР прогрессировали на пике ФН или в первые минуты ВП (см. таблицу и рис. 1), при этом увеличивалась комплексность ЖА (парные ЖЭК, неустойчивые ЖТ). Начиная с третьей минуты ВП количество ЖЭК уменьшалось до исходных значений. В группе также регистрировались сливные комплексы. Поскольку ЖЭК фиксировались у пациентов в претесте и прогрессировали во время ФН, с целью доказательства совместного влияния симпатического и парасимпатического отделов АНС проведена проба с бета-АБ. На фоне действия бета-АБ отмечался значительный прирост толерантности к ФН благодаря отсутствию прогрессирования ЖА. Проба расценена как положительная у 25 (86%) пациентов: ЖЭК не регистрировались на высоте ФН и в раннем ВП в 17 случаях, уменьшились в два раза и более в восьми случаях. У всех пациентов отмечалось увеличение ЖЭК в претесте и позднем ВП. Таким образом, во время фармакологической пробы у пациентов третьей группы при снятии симпатических влияний пропранололом мы спровоцировали еще большее повышение вагусной активности, которая и так присутствовала у них исходно. Четверо не ответили на пробу с бета-АБ, их дальнейшее ведение осуществлялось по общепринятым рекомендациям [1, 2].
Исчезновение ЖА в нагрузочной фазе пробы и сохранение ее в периоде вагусной активности (претест и поздний ВП) позволили прогнозировать эффект от комбинированной антиаритмической терапии (ААТ). Подходы к медикаментозному лечению пациентов второй и третьей групп подробно описаны в патенте «Способ лечения некоронарогенной желудочковой парасистолии, регистрирующейся в покое» [12]. Дальнейшее ведение пациентов первой группы осуществлялось по алгоритму, разработанному в НИЛ электрокардиологии [11].
Клинический пример смешанного прогрессирующего типа поведения ЖА
во время ФН
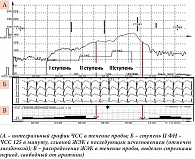
Пациент А., 40 лет, представитель третьей группы. Мужчина обратился к кардиологу с жалобами на снижение работоспособности, ухудшение переносимости ФН, возникшими в течение последних 10–12 месяцев. ЭКГ – вариант нормы. Данные ХМ: более 25 000 в сутки мономорфных ЖЭК, одиночных и парных; неустойчивые мономорфные ускоренные идиовентрикулярные ритмы (пять в сутки). НР с равномерным распределением в дневное и ночное время. При оценке ЭхоКГ в динамике за последний год отмечались начальные признаки дилатации правого желудочка, вероятно за счет высокого бремени ЖА. Диагноз на момент обследования: идиопатические ЖА из выходного тракта правого желудочка. Результаты исходного ТТ представлены на рис. 3 (проба 1). В претесте зарегистрировано десять ЖЭК в минуту, они исчезли на ступени I ФН. Проба прекращена на ступени III после достижения субмаксимальной ЧСС (164 в минуту). На первой минуте ВП зафиксированы сливные, одиночные и парные мономорфные ЖЭК – девять в минуту (см. рис. 3, проба 1 – указано стрелкой) с последующим возрастанием количества ЖЭК до 15–20 в минуту в позднем ВП. С учетом увеличения комплексности, появления парных ЖЭК в раннем ВП был сделан вывод о смешанном прогрессирующем парасистолическом характере ЖА.
На основании низкой ПТВ ИБС и смешанного прогрессирующего характера ЖА была выполнена проба с бета-АБ (см. рис. 3, проба 2), во время которой в претесте увеличилось количество ЖЭК – 15 в минуту, они исчезли на ступени I ФН при ЧСС 73 в минуту и далее не регистрировались. Результаты пробы подтвердили смешанный вариант желудочковой парасистолии и позволили прогнозировать положительный результат от комбинированной терапии бета-АБ с его приемом в первой половине дня и ААП класса IС с холинолитическим эффектом – во второй. После обсуждения с пациентом стратегии лечения, учитывая отсутствие значимой структурной патологии сердца, но наличие начальных проявлений кардиомиопатии, индуцированной высокой нагрузкой ЖА (> 10% от всех комплексов QRS в сутки), симптомный характер и типичную морфологию ЖЭК из выходного тракта правого желудочка, был выбран интервенционный метод лечения – радиочастотная аблация эктопического очага. Длительный период ожидания процедуры проходил благоприятно на фоне эффективной комбинированной ААТ, через год проведена успешная радиочастотная аблация.
Обсуждение
Пациентов исследуемой группы с умеренными структурными изменениями сердца отличало наличие множества сопутствующих заболеваний, чаще других отмечалась патология желудочно-кишечного тракта. Выраженная симптоматика и/или высокое бремя ЖА были поводом для обследования и выбора метода лечения. Наряду с преобладающей группой вагусных ЖА выявлены пациенты со смешанными НР, испытывавшими одновременно повышенную активность симпатических и парасимпатических влияний.
В более ранних работах указано на применение бета-АБ пациентами с симпатозависимыми и смешанными ЖА с целью доказательства вклада адренергических влияний и прогнозирования последующей терапии [11–14].
В литературе описана фармакологическая нагрузочная проба с бета-АБ у пациентов с нагрузочными ЖА, цель которой доказать вклад адренергических влияний и прогнозировать антиаритмический эффект лечения [11–15]. При этом поведение ЖА на фоне однократно принятого бета-АБ было различным:
- уменьшались вплоть до полного исчезновения;
- сохранялись;
- прогрессировали по количеству и комплексности;
- исчезали в фазе нагрузки, но увеличивались в периоде покоя.
По нашим данным, для пациентов со смешанными ЖА характерен последний вариант поведения. Он и был определен у представителей второй и третьей групп. Положительная реакция на пробу в виде исчезновения или уменьшения ЖА во время ФН и одновременное появление НР в периоде покоя позволили выявить таких пациентов и прогнозировать эффективность комбинированной терапии бета-АБ и препаратом класса 1С с холинолитической активностью.
Заключение
Пациенты с ЖА покоя без ИБС и значимых структурных изменений сердца являются наименее изученной и разнородной группой, ведение которой вызывает затруднения у специалистов. В ходе настоящего исследования вагусзависимый характер ЖА был подтвержден у 56% больных, смешанный ригидный – у 19%, смешанный прогрессирующий – у 21%. Впервые установлена ИБС у 4% пациентов. Знание особенностей поведения ЖА во время ФН помогает дифференцированно и осознанно подходить к ведению пациентов. Особенно важно при выявлении смешанных форм ЖА проводить дополнительные фармакологические пробы с бета-АБ, позволяющие прогнозировать эффективность комбинированной ААТ и избегать проаритмических влияний.
Таким образом, проведение пробы с ФН пациентам с ЖА покоя рекомендовано в следующих ситуациях:
- если во время ХМ не достигнута субмаксимальная ЧСС;
- если ЖА сопровождается клинической симптоматикой и/или ее количество превышает 10% от общего количества сердечных сокращений по данным ХМ;
- если ЖА сохраняется или прогрессирует во время пробы с ФН, фармакологическая проба с бета-АБ помогает уточнить характер аритмии и прогнозировать эффективность того или иного ААП.
Отношение и деятельность. Авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Благодарность. Авторы благодарят за помощь в подготовке материала для статьи заведующую НИЛ электрокардиологии Т.В. Трешкур.
Т.Е. Ivanova. PhD, Ye.S. Zhabina, PhD
V.A. Almazov National Medical Research Centre
Contact person: Tatyana E. Ivanova, PhD, tulinta@mail.ru
Non-coronary ventricular arrhythmias (VA) recorded at rest are often accompanied by severe symptoms and a high arrhythmia burden. A test with dosed physical exercise (PE), supplemented by a paired pharmacological exercise test with a short-acting beta-blocker (beta-AB), allows us to fully assess the effect of the autonomic nervous system (ANS) on the ectopic focus.
Purpose to conduct a clinical and electrocardiographic assessment of arrhythmia during a stress test in patients with non-coronary VA recorded at rest.
Material and methods. The study included 56 men and 84 women, average age 43.8 ± 13.5 years, without known previously diagnosed coronary artery disease (CAD), with frequent VA, recorded mainly at rest on a Holter monitor (HM). All patients underwent a treadmill test (TT) according to the standard Bruce protocol with assessment of symptoms, hemodynamic significance, quantity, morphology and complexity of ventricular arrhythmias. In the presence of risk factors and/or pre-test probability of coronary heart disease >15%, a paired pharmacological stress test with nitroglycerin or visualization techniques were performed. After excluding the ischemic nature of ventricular arrhythmias in patients with progressive and persistent mixed arrhythmias, TT was performed against the background of beta-AB intake.
Results. According to the results of HM, predominantly monomorphic ventricular ectopic complexes were recorded, the number of single complexes per day averaged 12 147 ± 1476, paired – 246 ± 71, unstable accelerated idioventricular rhythms and ventricular tachycardias – 95 ± 12. The daily distribution of VA was of a mixed nature: VA were recorded both during the day and at night. According to the classification of J.T. Bigger (1984), more than half of the patients (n = 73; 52.1%) had non-hazardous or benign VA, while the rest had potentially dangerous VA. Depending on the behavioral pattern during TT, vagus-dependent VA were detected in 78 (56%) patients, mixed rigid VA in 27 (19%), mixed progressive VA in 29 (21%), and ischemic heart disease was diagnosed for the first time in 6 (4%) patients. Patients with mixed VA underwent a beta-AB stress test. A positive reaction to the test in the form of disappearance or reduction of VA during physical activity and the simultaneous occurrence of VA during periods of rest allowed us to confirm the combined effect of both the sympathetic and parasympathetic divisions of the ANS and predict the effectiveness of combined therapy with beta-AB and a class 1C drug with anticholinergic activity.
Conclusion. Performing a physical activity test in patients with resting VA is useful under the following conditions: if submaximal heart rate is not achieved during HM; if ventricular arrhythmia is accompanied by clinical symptoms and/or its number exceeds 10% of the total number of heartbeats according to HM data; if ventricular arrhythmia persists or progresses during the physical activity test, a paired pharmacological stress test with beta-AB is advisable.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.