Применение препарата Генферон® лайт у детей разного возраста с ОРВИ
- Аннотация
- Статья
- Ссылки
- English
Несмотря на то что вопросы профилактики и лечения гриппа и острых респираторных вирусных инфекций (ОРВИ) не раз становились предметом клинических исследований, данная проблема не утрачивает актуальности и сегодня. Разработку профилактических средств и специфического лечения затрудняют этиологическая гетерогенность ОРВИ, высокая контагиозность возбудителей, изменчивость антигенных свойств вирусов, прежде всего гриппа [1, 2].
У детей первого года жизни имеют место высокий уровень заболеваемости ОРВИ, повышенный риск развития осложнений. Кроме того, весьма значителен удельный вес этих инфекций в структуре летальных исходов у детей раннего возраста [3]. Сказанное подтверждает актуальность вопросов рациональной терапии ОРВИ у детей данной возрастной группы [4].
В силу ряда факторов, прежде всего физиологической незрелости иммунной системы, организм новорожденного подвергается воздействию различных инфекционных агентов [5]. Слизистые оболочки респираторного тракта на первых месяцах жизни практически лишены локальной защиты, поскольку секреторный иммуноглобулин А к моменту рождения не вырабатывается. В сыворотке крови циркулирует значительное количество «ранних» интерферонов (ИФН). «Ранние» ИФН отличаются от интерферонов, синтезируемых клетками взрослого организма, физико-химическими и биологическими свойствами: они более гидрофобны, характеризуются сниженным противовирусным, антипролиферативным и иммуномодулирующим действием [6].
Трудности этиологического лечения респираторных вирусных инфекций у новорожденных обусловлены также ограничениями в применении специфических противовирусных средств.
Эффективное и безопасное лечение ОРВИ у детей раннего возраста ассоциировано с применением рекомбинантных ИФН. ИФН оказывают прямое противовирусное воздействие и эффективны против респираторных вирусов любой этиологии [7, 8]. Суппозитории – оптимальная лекарственная форма ИФН для детей, позволяющая использовать относительно низкие дозы ИФН и избежать типичных для инъекционных препаратов ИФН побочных явлений благодаря постепенному проникновению в системный кровоток [9–11].
Одним из современных препаратов рекомбинантного человеческого интерферона (рчИФН) альфа-2b является Генферон® лайт (российская биотехнологическая компания «БИОКАД», номер регистрационного удостоверения ЛСР–005614/09, дата регистрации – 13 июля 2009 г.). В состав препарата входит аминокислота таурин, оказывающая положительный эффект при воспалительных процессах. Таурин в виде глазных капель широко применяется при ряде заболеваний, входит в состав растворов для парентерального питания у новорожденных. Таурин оказывает антиоксидантный эффект, непосредственно взаимодействуя с активными формами кислорода, избыточное накопление которых способствует развитию патологических процессов (воспаление, интоксикация и т.д.) [12, 13].
Целью исследования была оценка клинико-лабораторной эффективности препарата Генферон® лайт в комплексном лечении ОРВИ у детей разного возраста.
Материал и методы исследования
Рандомизированное сравнительное клиническое исследование эффективности и безопасности препарата Генферон® лайт проводилось в нескольких лечебных учреждениях: Московском областном научно-исследовательском клиническом институте им. М.Ф. Владимирского, Центральном научно-исследовательском институте эпидемиологии Роспотребнадзора (Москва), НИИ гриппа, Детской городской поликлинике № 35 (Санкт-Петербург), Смоленской государственной медицинской академии, Саратовском государственном медицинском университете
им. В.И. Разумовского.
Всего в исследование было включено 302 ребенка: 102 пациента в возрасте от ноля до шести месяцев и 200 – от шести месяцев до семи лет. Дети находились на стационарном лечении с диагнозом ОРВИ, установленным на основании клинических данных. Продолжительность катаральных явлений на момент включения в исследование не превышала 48 часов.
Критериями исключения служили:
- установленная ВИЧ-инфекция или любой иной подтвержденный иммунодефицит;
- наличие любых сопутствующих заболеваний, которые, по мнению исследователей, могли повлиять на течение ОРВИ и оценку результатов лечения;
- гиперчувствительность к ИФН и другим компонентам исследуемых препаратов;
- необходимость применения глюкокортикостероидов;
- использование иммуномодулирующей терапии в течение месяца, предшествовавшего включению в исследование;
- одновременное участие в других клинических исследованиях.
Для проведения суммарного анализа эффективности и безопасности лечения пациенты были разделены на две возрастные группы. Первую составили 102 ребенка в возрасте от ноля до шести месяцев, вторую – 200 детей в возрасте от шести месяцев до семи лет. Каждая группа подразделялась на две подгруппы – основную и сравнения.
Пациенты основной подгруппы получали препарат Генферон® лайт в суппозиториях 125 000 МЕ ректально два раза в сутки в течение пяти дней одновременно с симптоматической и антибактериальной терапией при наличии соответствующих показаний. В подгруппе сравнения схема лечения включала суппозитории рчИФН альфа-2b 150 000 МЕ, аскорбиновую кислоту, токоферола ацетат ректально два раза в сутки в течение пяти дней в сочетании с симптоматическим лечением и антибактериальной терапией при наличии соответствующих показаний.
До начала лечения и на шестой-седьмой день у всех больных методом полимеразной цепной реакции (ПЦР) выявлены респираторные вирусы в мазке с носоглотки (определены антигены/генетический материал вируса гриппа А и В, аденовирусов, респираторно-синцитиального вируса, вирусов парагриппа 1, 2 и 3 типов, риновируса, метапневмовируса и бокавируса). Кроме того, были проведены клинический анализ крови и мочи, тщательный общий осмотр, оценка состояния верхних дыхательных путей. Зарегистрированы случаи развития осложнений и нежелательных явлений. На протяжении всего периода лечения (пять дней) в мультипараметрической таблице фиксировалась выраженность основных симптомов ОРВИ (лихорадка, интоксикация, катаральные изменения со стороны респираторного тракта). На 30-й день был запланирован телефонный контакт с родителями детей с целью выявления повторных эпизодов ОРВИ, случаев возникновения иных заболеваний и нежелательных явлений.
Эффективность терапии оценивали по срокам купирования симптомов ОРВИ, элиминации возбудителя по данным ПЦР, отсутствию осложнений.
Статистическая обработка данных выполнена с использованием программ Microsoft Offiсe, Excel 2003 с определением критериев Стьюдента, Шапиро – Уилка, Фишера, непараметрических критериев Манна – Уитни и Вилкоксона.
Клинические симптомы, наблюдавшиеся у больных при поступлении, отражены в таблице.
Результаты и их обсуждение
Симптомы интоксикации
В первый день наблюдения симптомы интоксикации отмечались у всех детей первой группы и 74% пациентов – второй. Среднее время до купирования симптомов интоксикации в основных подгруппах обеих групп составило 3,23 ± 0,92 дня (медиана – 3,00 дня [3,00–4,00]), в подгруппах сравнения – 3,19 ± 0,80 дня (медиана – 3,00 дня [3,00–4,00]) (р > 0,05). На шестой-седьмой день исследования, по окончании приема препаратов, симптомы интоксикации отсутствовали у пациентов основных подгрупп обеих групп. В подгруппе сравнения первой группы указанные симптомы имели место у 1 (1,96%) ребенка (р > 0,05).
Результаты статистического анализа, частота и сроки купирования интоксикации в исследуемых группах не имели достоверных отличий, характеризовались одновекторной направленностью и сопоставимой динамикой.
Лихорадка
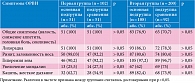
На момент включения пациентов в исследование лихорадка наблюдалась в 100% случаев в первой группе и 82,5% случаев – во второй.
Длительность лихорадочного синдрома в основных подгруппах первой и второй групп составила в среднем 2,88 ± 0,73 дня и 2,79 ± 1,4 дня, в подгруппах сравнения – 3,17 ± 0,88 дня и 2,7 ± 1,5 дня соответственно (р > 0,05).
К четвертому дню исследования лихорадка отсутствовала у детей основной подгруппы первой группы (рис. 1), а в подгруппе сравнения наблюдалась у 3 (5,88%) пациентов (р > 0,05). На шестой-седьмой день, по окончании приема исследуемых препаратов, лихорадка отсутствовала у всех пациентов раннего возраста (р > 0,05).
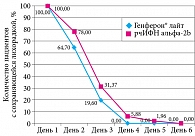
Во второй группе по окончании лечения субфебрильная температура (37,0–37,2 0С) сохранялась у 7% больных (у 7 из 100 детей с лихорадкой) основной подгруппы и 8,1% (у 5 из 74 детей с лихорадкой) подгруппы сравнения (р > 0,05) (рис. 2).
Общая динамика симптомов ОРВИ
Для оценки общей динамики симптомов ОРВИ (затруднение носового дыхания, гиперемия слизистой оболочки ротоглотки, кашель) проанализированы результаты итогового балла – суммы баллов по каждому симптому, согласно данным мультипараметрической таблицы (рис. 3 и 4).
В среднем срок купирования катаральных явлений ОРВИ в основной подгруппе первой группы составил 3,67 ± 1,14 дня, медиана – 4,00 дня [3,00; 5,00], в подгруппе сравнения – 3,71 ± 1,09 дня, медиана – 4,00 дня [3,00; 4,00] (р > 0,05).
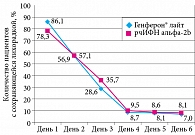
До лечения в основной подгруппе итоговый балл составил 3 [2–3], в подгруппе сравнения – 3 [3–4] (критерий Манна – Уитни, р > 0,05). На пятый день от начала терапии медиана итогового балла достигла 3 [0–4] в обеих подгруппах (критерий Манна – Уитни, р > 0,05) (рис. 3).
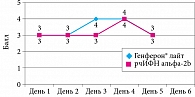
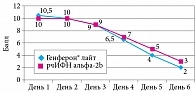
До лечения в основной подгруппе второй группы (рис. 4) итоговый балл составил 10,5 [8–12], в подгруппе сравнения – 10 [8–12], что не имело статистически значимых различий (критерий Манна – Уитни, р > 0,05). К шестому дню от начала терапии медиана итогового балла в основной подгруппе достигла 2 [0–6], в подгруппе сравнения – 3 [0–7] (критерий Манна – Уитни, р > 0,05).
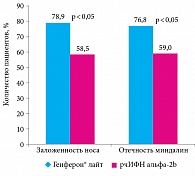
Важный момент: регресс некоторых симптомов ОРВИ во второй группе наблюдался у достоверно большего числа детей, получавших препарат Генферон® лайт (рис. 5). На фоне лечения купирование заложенности носа зарегистрировано у 78,9% пациентов основной подгруппы и 58,5% – подгруппы сравнения (р < 0,05), регресс отечности миндалин – у 76,8 и 59% больных соответственно (точный критерий Фишера, р < 0,05).
Элиминация возбудителя
По данным проведенного на скрининге ПЦР-исследования в отношении возбудителей ОРВИ (вирусы гриппа А и В, парагриппа, аденовирус, риновирус, респираторно-синцитиальный вирус, бокавирус и метапневмовирус), вирусы выявлены у равного числа детей первой группы обеих подгрупп (по 20–39,2%) (р > 0,05).
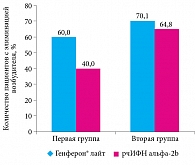
Доля пациентов, у которых на шестой-седьмой день от начала терапии установлена элиминация возбудителя, в основной подгруппе составила 60% (12 из 20 случаев), в подгруппе сравнения – 40% (8 из 20 случаев, выявленных методом ПЦР до лечения) (р > 0,05).
Во второй группе до начала лечения вирусы обнаружены у 62% пациентов основной подгруппы и 58,7% подгруппы сравнения (р > 0,05). Элиминация вирусов зафиксирована у 70,1% пациентов (47 из 67 случаев) основной подгруппы и 64,8% (35 из 54 случаев) – подгруппы сравнения (р > 0,05).
У детей обеих групп, получавших препарат Генферон® лайт, элиминация возбудителей ОРВИ регистрировалась несколько чаще, без достоверной разницы с группой сравнения (рис. 6).
Достижение критериев реконвалесценции к шестому-седьмому дню исследования
Пациент считался реконвалесцентом в случае отсутствия лихорадки (температура тела, измеренная в подмышечной впадине, не выше 37,2 0С), признаков интоксикации, осложнений ОРВИ и полного отсутствия катаральных явлений или остаточных проявлений ОРВИ, выраженность которых, согласно итоговому баллу, не превышала 2.
К шестому-седьмому дню исследования в отношении количества детей обеих подгрупп первой и второй групп, достигших реконвалесценции, статистически значимые различия не установлены (р > 0,05).
Осложнения ОРВИ и потребность в антибактериальной терапии
Доля пациентов, у которых к шестому-седьмому дню от начала терапии зарегистрировано развитие осложнений ОРВИ, и доля пациентов в исследуемых группах, которые нуждались в назначении системной антибактериальной терапии в течение пяти дней применения исследуемого препарата, не имели достоверных различий (р > 0,05).
Анализ изменений гемограммы
В клиническом анализе крови не выявлено достоверной отрицательной динамики по всем исследуемым параметрам (уровни гемоглобина, эритроцитов, лейкоцитов, нейтрофилов, лимфоцитов, тромбоцитов, скорость оседания эритроцитов), кроме незначительного увеличения процентного соотношения лимфоцитов, не выходившего по значению медиан за пределы нормы. По окончании лечения (шестой-седьмой день исследования) прослеживалась тенденция к увеличению числа пациентов с нормализацией показателей клинического анализа крови. Различий между группами детей, получавших и не получавших препарат Генферон® лайт, не зафиксировано (р > 0,05).
Безопасность препаратов
Ректальное введение суппозиториев не вызывало у детей побочных и аллергических реакций, как местных, так и общих. Не зарегистрировано ни одного случая развития нежелательных явлений, связанных с исследуемыми препаратами.
Заключение
Результаты многоцентровых открытых сравнительных рандомизированных проспективных исследований показали, что лечение ОРВИ у детей разного возраста с использованием препаратов Генферон® лайт и рекомбинантного человеческого интерферона альфа-2b в дозе 150 000 МЕ одинаково эффективно по клинико-лабораторным параметрам в отсутствие побочных и аллергических реакций.
У детей в возрасте от шести месяцев до семи лет на фоне применения препарата Генферон® лайт регресс симптомов ОРВИ (заложенность носа, отечность миндалин) наблюдался достоверно чаще, чем в группе сравнения.
После лечения у детей (особенно в возрасте до шести месяцев), получавших Генферон® лайт, отмечалась тенденция к более высокой элиминационной активности в отсутствие статистически значимых различий.
Полученные данные подтвердили хорошую переносимость и безопасность препарата Генферон® лайт на фоне ОРВИ как у детей от ноля до шести месяцев, так и у детей от шести месяцев до семи лет. Это свидетельствует в пользу применения данного препарата в педиатрической практике у детей разного возраста.
Использование меньшей дозы ИФН альфа-2b в составе препарата Генферон® лайт 125 000 МЕ по сравнению с препаратом рчИФН альфа-2b 150 000 МЕ позволяет достичь сопоставимого терапевтического действия при снижении количества вводимого экзогенного ИФН.
A.V. Gorelov, Ye.Ye. Tselipanova, I.L. Alimova
Central Research Institute of Epidemiology
Moscow Regional Research and Clinical Institute MONIKI
Smolensk State Medical Academy
Contact person: Yelena Yevgenyevna Tselipanova, elena-tselip@yandex.ru
Here we present summarized results from multi-center, open, comparative, randomized, prospective studies on clinical efficacy and safety of Genferon® Lite in a combination therapy of 302 children of various age (102 children aged 0-six months, 200 – six months-seven years) with acute respiratory viral infections (ARVIs). By using polymerase chain reaction, several respiratory viruses were examined dynamically in nasopharyngeal swabs. Intensity of major ARVI symptoms were recorded in multi-parameter table. Study results confirmed that Genferon® Lite 125 000 ME exhibited clinical and laboratory efficacy comparable to recombinant human interferon alpha-2b 150 000 ME, and lacked side and allergic reactions.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.