Сложности диагностики первичной гиперферритинемии
- Аннотация
- Статья
- Ссылки
- English


Введение
Ферритин является одним из важных показателей как обмена железа, так и таких патологических процессов в организме, как воспаление или развитие злокачественного новообразования. Ферритин представляет собой крупномолекулярное соединение, состоящее из белка апоферритина и атома трехвалентного железа. Каждая молекула сывороточного ферритина способна аккумулировать до 4500 атомов железа [1, 2]. Основная роль этого белка в организме – депонирование железа. Кроме этой функции ферритин является также маркером острофазового процесса. Снижение уровня ферритина в сыворотке крови, как правило, коррелирует с низким содержанием железа и является показателем истинного железодефицита. Повышение уровня ферритина может быть обусловлено различными патологическими процессами. Значительное повышение этого показателя отмечается при воспалительных, опухолевых и деструктивных заболеваниях [1]. Повышение уровня ферритина в крови может быть обусловлено высвобождением его из гепатоцитов при заболеваниях печени. Также возможно значимое повышение его секреции под воздействием цитокинов, онкогенов и других гуморальных факторов, продуцируемых при патологических процессах [2].
При воспалительных или онкологических заболеваниях нередко наблюдается сниженный уровень сывороточного железа при повышенной концентрации ферритина, а также повышение других маркеров воспалительного процесса.
Значительно более редкой причиной повышения уровня ферритина и сывороточного железа может явиться истинное увеличение этих показателей, приводящих к так называемой «перегрузке железом». В результате длительного повышения концентрации железа в организме происходит его отложение в тканях разных органов, что приводит к развитию гемохроматоза. Причинами гемахроматоза могут быть передозировка препаратов железа, повышенная абсорбция, ускоренный гемолиз или частое переливание эритроцитарной массы [3, 4].
По данным разных авторов, повышение уровня ферритина, как правило, связано с системным воспалением или опухолевым заболеванием и только 10% случаев говорят об истинной перегрузке железом [5].
При изучении патогенетических особенностей гиперферритинемии при воспалительных заболеваниях, особенно в период пандемии COVID-19, было высказано предположение, что чрезмерное повышение содержания ферритина в сыворотке крови усиливает процесс воспаления, стимулируя выработку провоспалительных гуморальных агентов, приводя к так называемому «цитокиновому шторму» [5, 6].
Железо проникает преимущественно в гепатоциты, но также в паренхиматозные клетки сердца, поджелудочной железы, щитовидной железы и центральной нервной системы, приводя к функциональной недостаточности данных органов [3–5].
Заболевания, вызывающие перегрузку железа, можно разделить на первичные (генетически обусловленные) и вторичные, развивающиеся в результате различных патологических процессов. При заболеваниях, связанных с генными изменениями, происходит нарушение синтеза гепсидина или снижение его функции. В результате повышается как абсорбция железа в кишечнике, так и высвобождение его из макрофагов. Наследственная перегрузка железом также может быть связана с нарушением синтеза трансферрина.
Причинами вторичной перегрузки железом являются такие патологии, как заболевания печени (вирусные гепатиты, алкогольное поражение). Связан этот механизм с высвобождением депонированного железа при разрушении гепатоцитов. Особое внимание в настоящее время уделяется синдрому перегрузки железом у пациентов с неалкогольной жировой болезнью печени и метаболическим синдромом. Прогностическая важность влияния повышенного содержания железа в ткани печени у пациентов с метаболическим синдромом послужила основанием для введения термина «дисметаболический синдром перегрузки железом» (ДСПЖ, Dysmetabolic Iron Overload Syndrome, DIOS). Для этого заболевания характерно наличие не менее двух признаков метаболического синдрома: ожирение, нарушение жирового обмена, высокое артериальное давление и проблемы с углеводами. Кроме того, наблюдается повышение уровня ферритина в крови, при этом насыщение трансферрина железом остается в пределах нормы, а также развивается стеатоз печени. Перегрузка железом при данном синдроме приводит также к повреждению клеток поджелудочной железы, что повышает и без того высокий риск развития сахарного диабета [7–9].
Еще одной патологией, приводящей к перегрузке железом, являются как врожденные, так и приобретенные гемолитические анемии. Необходимо учитывать и возможный ятрогенный механизм перегрузки железом в результате передозировки препаратами железа, бесконтрольного применения железосодержащих пищевых добавок, частого переливания эритроцитарной массы [3].
При подозрении на гемохроматоз необходимо не только оценить уровень сывороточного железа и ферритина, но и определить сатурацию трансферрина. При повышении уровня ферритина > 200 мкг/л у женщин и 300 мкг/л у мужчин, сатурации трансферрина > 45% у женщин и 50% у мужчин и отсутствии явной причины перегрузки железом необходимо проведение генетического обследования [4].
Помимо отложения избыточного железа в тканях печени, поджелудочной железы, миокарда, возможно также поражение клеток мозга. Эта генетически обусловленная патология носит название «нейроферритинопатия» или нейродегенерация с накоплением железа в мозге (в международной литературе NBIA – Neurodegeneration with Brain Iron Accumulation). Существует много клинических разновидностей нейроферритинопатии, проявляющихся различными вариантами неврологической патологии, в зависимости от локализации отложения железа – экстрапирамидные расстройства, нарушение зрения, когнитивная дисфункция. Связаны эти проявления с мутациями различных генов. Одним из генов, мутация которого приводит к развитию нейроферритинопатии, является FTL. Данный ген кодирует белок легкой цепи ферритина. Мутации этого гена приводят к развитию неврологической патологии, как правило экстрапирамидных расстройств во взрослом возрасте [10]. Но также встречаются мутации гена FTL, проявляющиеся редкой аутосомно-доминантной гиперферритинемией с развитием катаракты. Наследственный синдром гиперферритинемии-катаракты (Hereditary Нyperferritinemia – Сataract Syndrome – HHCS) характеризуется высоким уровнем сывороточного ферритина без перегрузки железом. Катаракта развивается из-за отложений L-ферритина в хрусталике и имеет характерный «порошкообразный вид». Впервые информация об этом синдроме появилась в конце 90-х гг. XX в. Разные авторы занимались описанием семейных случаев данной патологии, но нам не удалось найти убедительных статистических данных о встречаемости этого синдрома в доступных источниках литературы. При анализе описанных в научных источниках случаев были сформулированы основные клинико-лабораторные критерии постановки данного диагноза [11]:
- постоянно высокий уровень сывороточного ферритина;
- нормальная концентрация растворимого сывороточного железа и трансферрина;
- нормальные показатели клинического анализа крови и биохимических маркеров поражения печени;
- характерный «порошкообразный» вид катаракты;
- наличие подобной патологии у близких родственников;
- отсутствие клинических симптомов, кроме нарушения зрения из-за катаракты.
При подтверждении данного диагноза лечение не требуется, кроме замены хрусталика, так как эта патология характеризуется благоприятным прогнозом и отсутствием каких-либо клинических проявлений.
Клинический случай синдрома гиперферритинемии с катарактой
В реальной амбулаторной практике наблюдался такой клинический случай: обратилась женщина, 60 лет, без хронических заболеваний в анамнезе, не обследовалась, лекарственные препараты не принимала.
Наследственность не отягощена.
Впервые в 2022 г. появились жалобы на слабость, сыпь на тыльной поверхности правой стопы геморрагического характера, периодическую боль в суставах. Обратилась к врачу-ревматологу, была обследована.
Показатели клинического и биохимического анализов крови были в пределах референсных значений. Ревматоидный фактор составил 7 МЕ/мл, АЦЦП (антитела к циклическому цитруллинсодержащему пептиду) – 4 Ед/мл.
Выявлено повышение уровня ферритина до 4000 нг/мл (норма до 200 нг/мл).
Учитывая появление геморрагической сыпи и высокий уровень ферритина, был выставлен диагноз «васкулит» и назначен метилпреднизолон в дозе 8 мг в день. На фоне терапии состояние не менялось.
Спустя пять месяцев терапии при повторном осмотре сохранялись жалобы на слабость, периодическую боль в суставах. При уточнении характера боли оказалось, что боль появлялась при физической нагрузке или после нее, преимущественно в вечерние часы, иногда возникала при изменении положения тела. Исходя из этого, можно сделать вывод о развитии у пациентки боли механического характера. Сыпь с момента первого эпизода не появлялась. Уровень ферритина сохранялся в пределах 2000–4000 нг/мл.
При рентгенографии тазобедренных и плечевых суставов выявлено сужение суставной щели менее чем на 1/3 от нормы, единичные остеофиты.
С учетом боли в суставах механического, а не воспалительного характера, результатов рентгенографии, отсутствия динамики заболевания на фоне медикаментозной терапии, поставлен диагноз «остеоартрит».
Так как геморрагическая сыпь полностью прошла и рецидивов ее не было, диагноз «васкулит» был снят. Диагноз васкулита как одного из проявлений аутоиммунного заболевания мог быть правомочен при сочетании боли в суставах воспалительного характера, геморрагической сыпи и повышенного уровня нескольких маркеров воспаления. Пациентка же испытывала боль механического характера в сочетании с единичным эпизодом сыпи, к тому же были выявлены нормальные уровни СОЭ, СРБ, РФ, АЦЦП, что не может являться критерием для постановки диагноза «васкулит». Однако диагноз «остеоартрит» объяснял боль в суставах, но не высокий уровень ферритина.
Пациентке постепенно был отменен метилпреднизолон, проведен онкоскрининг, в рамках которого патология не выявлена.
Документальных подтверждений нет, но со слов пациентки проводились рентгенография органов грудной клетки, маммография, гастро- и колоноскопия, УЗИ органов брюшной полости, УЗИ органов малого таза. Все результаты обследования находились в пределах нормы. Рекомендовано обратиться к гематологу для исключения синдрома перегрузки железом.
После консультации гематолога были проведены дополнительные исследования: ферритин – 3100 нг/мл, КНТЖ (коэффициент насыщения трансферрина железом) – 32,4%, ОЖСС (общая железосвязывающая способность сыворотки) – 45 мкмоль/л, железо –14 нмоль/л, НЖСС (ненасыщенная железосвязывающая способность) – 30 мкмоль/л. Все показатели обмена железа, за исключением ферритина, были в пределах нормы. По результатам анализов синдром перегрузки железом исключен.
Проведено генетическое тестирование гена HFE, ответственного за регуляцию обмена железа в организме. Данный ген расположен на коротком плече шестой хромосомы и может подавлять перенос комплекса «трансферрин – железо» через мембрану клеток, в результате чего железо в виде ферритина накапливается в энтероците. Поэтому данное генетическое тестирование предназначено для выявления наиболее частых мутаций в гене HFE, который отвечает за развитие наследственного гемохроматоза. Результат тестирования отрицательный. Гематолог исключил развитие перегрузки железом и наследственный гемохроматоз.
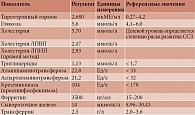
В дальнейшем, на приеме у врача-терапевта, пациентка жаловалась на слабость, повышенную тревожность на фоне переживаний о своем диагнозе. Результаты лабораторных исследований представлены в табл. 1 и 2.
Так как основные причины гиперферритинемии (онкологический процесс, воспалительные заболевания, заболевания печени, перегрузка железом, наследственный гемохроматоз) были исключены, после изучения научных источников было сделано предположение о наличии у пациентки синдрома наследственной гиперферритинемии. В пользу этого диагноза свидетельствовали постоянно высокий уровень сывороточного ферритина, нормальная концентрация сывороточного железа и трансферрина, нормальные показатели клинического анализа крови и биохимических маркеров поражения печени. Однако эта гипотеза требовала уточнения анамнеза.
В ходе повторного опроса и подробного сбора анамнеза врач выяснила, что в раннем детстве диагностирована врожденная двухсторонняя катаракта, проведено оперативное вмешательство. Кроме того, у ближайших родственников (у матери, двух сестер, сына, племянников) также диагностирована врожденная катаракта. Все родственники, имеющие в анамнезе врожденную катаракту, сдали анализ на уровень ферритина. Выявлена концентрация ферритина ≈ 2000–4000 нг/мл. Также прицельно были уточнены обстоятельства возникновения сыпи: пациентка вспомнила, что сыпь на ноге появилась после того, как она уронила тяжелый предмет на ногу.
В результате обследования и повторного сбора анамнеза был выставлен диагноз: «наследственная гиперферритинемия», так как отмечалось соответствие всем критериям, а именно:
- постоянно высокий уровень сывороточного ферритина;
- нормальная концентрация растворимого сывороточного железа и трансферрина;
- нормальные показатели клинического анализа крови и биохимических маркеров поражения печени;
- наличие катаракты в анамнезе;
- наличие подобной патологии у близких родственников;
- отсутствие клинических симптомов, кроме нарушения зрения из-за катаракты.
Пациентке разъяснили, что дальнейшая терапия не требуется, поскольку в данном случае избыток ферритина накапливается в хрусталике глаза, вызывая катаракту, но после оперативного вмешательства этого происходить не будет. Другие органы и системы не повреждены.
После консультации самочувствие пациентки улучшилось, тревожность больше не беспокоила. Даны рекомендации по медикаментозной и немедикаментозной терапии остеоартрита. Этапы обследования и установки диагноза пациентки представлены на рисунке.
Обсуждение
Если у пациента выявлена гиперферритинемия, необходимо провести тщательное обследование, чтобы определить причину этого лабораторного отклонения. В клинической практике повышение уровня ферритина в сыворотке крови может быть связано как с воспалительными или онкологическими процессами, так и с патологиями, вызывающими перегрузку организма железом. В связи с этим в первую очередь необходимо исключить синдром перегрузки железом, проявлениями которого являются немотивированная слабость, гиперпигментация кожи, признаки поражения печени, аритмия, сердечная недостаточность, упорные артралгии. Лабораторные критерии данного синдрома следующие [12]:
- стойкое повышение содержания сывороточного ферритина (свыше 1000 мкг/л) в отсутствие очевидного воспалительного, деструктивного или опухолевого процесса;
- снижение содержания трансферрина в сыворотке крови и ОЖСС;
- повышение коэффициента насыщения трансферрина железом (> 60%);
- повышенная экскреция железа с мочой (спонтанная и индуцированная введением дефероксамина – «десфераловый тест»).
При выявлении лабораторных и клинических признаков перегрузки железом дальнейшее обследование в зависимости от клинической ситуации может включать:
- гистологическое исследование костного мозга с выявлением повышенного количества сидеробластов;
- биопсию печени с определением содержания железа в ткани;
- магнитно-резонансную томографию печени и сердца в режиме Т2.
Тщательный сбор анамнеза – ключевой процесс для выявления причин перегрузки железом. Поэтому необходимо выяснить следующие моменты:
- наличие в анамнезе гематологических заболеваний, проявляющихся гемолизом;
- прием железосодержащих препаратов и пищевых добавок;
- наличие хронических заболеваний, в терапии которых применялись повторные гемотрансфузии;
- наличие хронических заболеваний печени.
Следует иметь в виду, что у необследованных ранее пациентов гемолиз может быть выявлен впервые. Поэтому при обследовании необходимо оценивать содержание свободного (непрямого) билирубина, повышение которого характерно именно для гемолиза. При оценке показателей клинического анализа крови необходимо обращать внимание на количество ретикулоцитов, так как ретикулоцитоз характерен для гемолиза.
У большинства пациентов при наличии длительно существующего гемолиза обычно развивается нормоцитарная анемия. Но у части пациентов при хорошей регенераторной способности костного мозга уровень гемоглобина может быть в норме или незначительно понижен.
При диагностике заболеваний печени, основываясь на клинических, лабораторных и инструментальных данных, следует учитывать, что существует два возможных пути взаимосвязи между патологией печени и перегрузкой железом.
Во-первых, любая болезнь печени, сопровождающаяся разрушением гепатоцитов, может привести к избытку железа в организме из-за его выхода из клеток. Во-вторых, избыток железа, образовавшийся в результате перечисленных выше факторов, может откладываться в печени.
Чтобы установить точную причину и следствие поражения печени и перегрузки железом, необходимо тщательно изучить анамнез, включая наследственный фактор. Также рекомендуется провести МРТ и биопсию печени. При наличии признаков перегрузки железом и отсутствии выявленных причин этой патологии предполагают ее первичный характер, что требует проведения генетического обследования [3, 4].
Другой, наиболее частый вариант гиперферритинемии – отсутствие перегрузки железом. В таких случаях выявляется повышение уровня сывороточного ферритина при нормальных или пониженных концентрациях железа и сатурации трансферрина. Нередко выявляется и гипохромная или нормохромная анемия, так называемая анемия хронических заболеваний. В таких случаях повышение уровня ферритина является маркером воспалительного или онкологического процесса. У таких пациентов при сборе анамнеза, физикальном и лабораторном обследовании необходимо выявлять признаки воспаления или злокачественного новообразования – немотивированную слабость, гипертермию, снижение массы тела, а также повышение уровня других маркеров воспаления: СОЭ, СРБ, фибриногена и т.д.
У большинства пациентов с повышенным уровнем ферритина в сыворотке крови при тщательном обследовании удается выявить воспалительный или онкологический процесс либо ситуацию, приведшую к перегрузке железом. Но в тех случаях, когда не удается выявить никакой патологии, кроме повышения уровня сывороточного ферритина, следует помнить о гиперферритинемическом катарактальном синдроме, подтверждая свои предположения тщательным сбором анамнеза, в том числе семейного, и проведением генетического исследования.
Заключение
В рутинной амбулаторной практике врач в основном сталкивается с типичными клиническими ситуациями, при которых алгоритм диагностического поиска диктуется как клиническими рекомендациями, так и опытом, собственным или своих коллег. Однако иногда возникают ситуации, которые выходят за рамки привычного.
Каковы же должны быть действия врача в подобных ситуациях? Во-первых, тщательно собранный анамнез заболевания и семейный анамнез. Пациенту необходимо задавать конкретные наводящие вопросы, нередко касающиеся давно прошедших событий, о которых он не считает возможным сообщать.
Во-вторых, тщательное обследование, которое позволит выявить дополнительные признаки имеющегося заболевания.
В-третьих, врач должен изучить научную литературу, как отечественную, так и зарубежную, чтобы найти похожие клинические случаи и лучше понять, как действовать в подобных ситуациях.
На примере истории болезни этой пациентки, у которой наблюдалось стойкое повышение уровня ферритина, можно увидеть, как важно провести полное обследование, чтобы исключить другие заболевания. Также необходимо собрать анамнез, чтобы установить наличие семейного синдрома гиперферритинемии-катаракты. Только после этого можно поставить точный диагноз и завершить затянувшийся процесс диагностики.
Конфликт интересов. Авторы заявляют об отсутствии возможного конфликта интересов.
A.A. Gavrilova, E.V. Kudina, V.N. Larina
Pirogov Institute of Clinical Medicine of the Ministry of Health of the Russian Federation, Department of Polyclinic Therapy
Contact person: Alina A. Gavrilova, 89531815375@mail.ru
Ferritin is one of the important proteins in the human body and is responsible for the deposition of iron. In addition, it is a marker for the acute phase response. An increase in ferritin levels, or hyperferritinemia, can be caused by several factors. This often occurs in the development of inflammatory, tumorous, and destructive conditions. More rarely, elevated ferritin levels and serum iron concentrations can be due to a true increase in these markers leading to what is known as 'iron overload’. As a result of prolonged increases in iron concentrations in the body, iron can accumulate in the tissues of different organs, leading to hemochromatosis. Some common causes of secondary iron overload include liver disease (such as viral hepatitis and alcohol-related damage), hemolytic anemias, and inappropriate administration of iron supplements. Therefore, if hyperferritinaemia is detected, doctors should conduct a thorough evaluation to identify the underlying cause of the laboratory abnormality. However, there are also rare diseases manifested by hyperferritinaemia and presenting significant diagnostic challenges. The purpose of describing this clinical case is to report on a rare pathology – the hyperferrinemiacataract syndrome. The article presents characteristic signs of the hereditary hyperferri-nemic-cataract syndrome: constantly high levels of serum ferritin, normal results from complete blood count tests and biochemical markers for liver damage, concentrations of soluble serum iron and transferrin, a characteristic 'powder'-type of cataract, the presence of this pathology in close relatives, lack of clinical symptoms except for vision impairment caused by cataract. The results of laboratory and instrumental examination made it possible to rule out other causes of hyper-ferritinemia and end the complex diagnostic process.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.


