Возможности применения Канефрона Н при лечении хронического цистита
- Аннотация
- Статья
- Ссылки



Современная медицина научилась работать с растениями и использовать их потенциал. Так, появилась возможность получения экстрактов, в состав которых входят определенные действующие вещества в точно подобранных пропорциях. Это обеспечивается благодаря тщательному возделыванию культур и применению специальных методов изготовления лекарственных средств. Изучение мира растений позволяет создавать фитопрепараты, наиболее полно отвечающие потребностям современной медицины. Сегодня фитотерапия особенно привлекательна, так как на многих примерах показано, что экстракты лекарственных растений ни в чем не уступают по эффективности химическим веществам, а часто даже превосходят их. К фитопрепаратам больше не относятся, как к препаратам второго сорта. Каждый из них имеет собственный профиль. Об их клинической значимости говорит тот факт, что крупнейшие фармакологические предприятия, десятилетиями производившие только синтетические препараты, буквально прочесывают леса в поисках целебных растений.
Современные растительные препараты производятся с применением высоких технологий и проходят многоступенчатый контроль качества. Одним из фитопрепаратов нового поколения, широко применяемым в урологии, является КанефронâН (Bionorica, Германия).
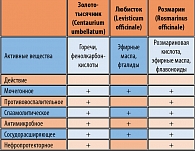
КанефронâН – комбинированный препарат, в состав которого входят золототысячник (Centaurium umbellatum), любисток (Levisticum officinale) и розмарин (Rosmarinus officinale). Входящие в состав препарата вещества оказывают антисептическое, спазмолитическое, противовоспалительное действие на органы мочевой системы, уменьшают проницаемость капилляров почек, обладают диуретическим эффектом, улучшают функцию почек, потенциируют эффект антибактериальной терапии (см. таблицу 1).
Различные виды действия КанефронаâН обусловлены входящими в его состав эфирными маслами, фенолкарболовыми кислотами, фталидами, горечами. Например, диуретическое действие препарата обусловлено сочетанием различных точек приложения его компонентов. Эфирные масла расширяют сосуды почек, что способствует улучшению кровоснабжения почечного эпителия, а также оказывают влияние на процессы обратного всасывания клетками почечных канальцев. Это проявляется главным образом в уменьшении реабсорбции ионов натрия и соответствующего количества воды. Диуретическое действие фенилкарбоновых кислот объясняется осмотическим эффектом: при попадании в просвет почечных канальцев они создают высокое осмотическое давление (обратному всасыванию эти вещества не подвергаются); при этом значительно снижается реабсорбция воды и ионов натрия. Таким образом, увеличение выведения воды происходит без нарушения ионного баланса (калий-сберегающий эффект).
Спазмолитический эффект обусловлен флавоноидной составляющей препарата. Аналогичное действие проявляют фталиды (любисток) и розмариновое масло. Слабыми спазмолитическими свойствами обладают фенолкарбоновые кислоты (1-4).
Противовоспалительный эффект в основном обусловлен наличием розмариновой кислоты, которая блокирует неспецифическую активацию комплемента и липооксигеназы с последующим угнетением синтеза лейкотриенов. Как и другие фенольные соединения, розмариновая кислота проявляет антиоксидантное действие и прерывает свободнорадикальные цепные реакции.
Все лекарственные растения, входящие в состав КанефронаâН, содержат вещества, обладающие широким антимикробным спектром действия: фенолкарболовые кислоты влияют на бактериальный белок; эфирные масла разрушают цитоплазматическую мембрану бактерий и уменьшают активность аэробного дыхания, что приводит к уменьшению выделения энергии, необходимой для синтеза различных органических соединений; флавоны, флавоноиды и флавонолы способны связываться с белками клеточной стенки и разрушать клеточные мембраны бактерий. Это обеспечивает активность препарата даже при устойчивой к синтетическим средствам микрофлоре.
Достоинством КанефронаâН является также сочетание противомикробного и противовоспалительного эффектов, что особенно ценно при хронических процессах в мочевыводящих путях. Кроме того, выделение органических фенолкарбоновых кислот и их глюкуронидированных и сульфатированных метаболитов с мочой приводит к изменению ее кислотности, что противодействует росту бактерий. Помимо перечисленных свойств элиминации бактерий из мочевых путей способствуют следующие факторы:
- биофлавоноиды тормозят бактериальную гиалуронидазу и таким образом ограничивают распространение бактерий в тканях;
- диуретический эффект препятствует адгезии микроорганизмов.
Установлено, что КанефронâН усиливает выведение солей мочевой кислоты. Эта сторона действия лишь отчасти связана с мочегонным эффектом и довольно специфична. Усиление выделения мочевой кислоты препятствует выпадению в мочевыводящих путях кристаллов, росту имеющихся камней и формированию новых. Также было отмечено, что данный препарат подщелачивает мочу, если она резко кислая, и поддерживает значение рН в пределах 6,2-6,8, что также препятствует образованию уратных камней.
Фармакологически доказанное действие КанефронаâН на тубулярный аппарат почки четко показывает, что выделение белка с мочой из-за ранее перенесенных патологических процессов, повреждающих тубулярный аппарат, значительно снижается.
Материал и методы
В урологической клинике ММА им. И.М. Сеченова было обследовано 55 женщин, страдающих хроническим циститом, в возрасте от 18 до 45 лет. Длительность заболевания на момент обращения составляла от 3 месяцев до 15 лет (у большинства больных – от 1 года до 3 лет).
При обследовании больных применялись следующие методы:
- сбор анамнеза, физикальное обследование;
- микроскопическое исследование мочи и мочевого осадка;
- бактериологическое исследование мочи;
- анализ мазков из влагалища и цервикального канала на наличие специфических возбудителей (методами ПЦР и ПИФ) и общую чистоту;
- ультразвуковое исследование органов мочевой системы;
- экскреторная урография с нисходящей цистографией;
- цистоскопия.
Сопутствующих заболеваний (камней, кист, опухолей, пороков развития) органов мочевой системы не было выявлено ни в одном из случаев.
С помощью ПЦР и ПИФ у 7 больных были обнаружены специфические возбудители: у 2 больных была выявлена Clamydia trachomatis, у 2 больных – Mycoplasma hominis, у 3 больных – Ureaplasma urealiticum. Эти больные были исключены из последующего анализа.
Дальнейшее обследование проводилось у 48 больных.
При бактериологическом исследовании мочи в большинстве (52%) случаев (у 25 больных) выявлялась Escherichia coli. У 18 (37,5%) больных результаты посева мочи были отрицательными; у 5 (10,5%) больных были обнаружены другие возбудители – Proteus spp., Enterococcus spp., Staphylococcus spp.
Результаты цистоскопии представлены в таблице 2. Учитывая, что у многих больных выявлено сочетание различных изменений слизистой оболочки мочевого пузыря, итоговый показатель превышает 100%.
Таким образом, у большинства (79,1%) обследованных нами больных имелся шеечный цистит; другие отделы мочевого пузыря были вовлечены в патологический процесс значительно реже (в 20,9% случаев).
Во время цистоскопии патологических новообразований мочевого пузыря не было выявлено ни у одной из больных.
Оставшиеся 48 больных были подразделены на 2 группы с учетом наличия пиурии.
В группу А вошли 20 больных, количество лейкоцитов в анализе мочи у которых превышало 10 (от 10 до 20) в поле зрения. В группу Б вошли 28 больных, пиурия у которых отсутствовала.
Каждая из групп была дополнительно разделена на 2 равные подгруппы в зависимости от применения препарата КанефронâН. В подгруппы были включены больные, сравнимые по своим характеристикам (возрасту, анамнезу, клиническим проявлениям и т. д.).
Больные из подгруппы А1 (n=10) получали фосфомицин (монурал) по 3 г с интервалом 24 часа – всего 2 приема.
Больные из подгруппы А2 (n=10) получали фосфомицин (монурал) по описанной выше схеме в сочетании с приемом КанефронаâН по 2 драже 3 раза в сутки в течение 30 дней.
Больным из подгруппы Б1 (n=14) был проведен инициальный курс лечения, включавший противовоспалительные средства, препараты, улучшающие кровоток, местную терапию и физиотерапевтические процедуры, в течение 10 дней. Затем проводилось динамическое наблюдение в течение 1 месяца, в течение которого никакие дополнительные препараты не назначались.
Больным из подгруппы Б2 (n=14) был проведен аналогичный инициальный курс лечения. Однако в течение последующих 30 дней они получали КанефронâН по 2 драже 3 раза в сутки.
Контрольное обследование больных из группы А проводилось двукратно – через 10 и 30 дней после начала лечения. Критерии оценки: клинические проявления, наличие пиурии, наличие бактериурии.
Контрольное обследование больных из группы Б проводилось через 30 дней после окончания курса комплексной инициальной терапии. Критерии оценки – клинические проявления. Учитывая, что все 18 больных с отрицательными результатами бактериологического исследования мочи вошли в группу Б, а у оставшихся 10 больных возбудитель высевался в низких титрах (103-104 КОЕ/мл), наличие бактериурии не рассматривалось в качестве критерия оценки эффективности лечения.
Результаты и обсуждение
Результаты лечения больных из группы А После проведенного лечения у большинства больных из группы А наступило клиническое (см. таблицу 3) и лабораторное улучшение различной степени выраженности.
В подгруппе А1 пиурия через 10 дней лечения отсутствовала у 9 (90%) больных, в то время как в подгруппе А2 – у 100% больных.
При бактериологическом исследовании мочи, проведенном через 10 дней, исходно выделенный возбудитель был обнаружен только у 1 больного из подгруппы А1; в подгруппе А2 результаты посева мочи были отрицательными в 100% случаев.
Сходные результаты были получены через 30 дней. У всех больных, принимавших КанефронâН, клинические проявления заболевания отсутствовали, в то время как у 3 (30%) больных, получавших монотерапию фосфомицином (монуралом), они были выражены в той или иной степени. Пиурия по-прежнему не выявлялась у 100% больных из подгруппы А2. В подгруппе А1 повторное повышение количества лейкоцитов в моче было отмечено у 3 (30%) больных.
Таким образом, становится очевидным, что, несмотря на достаточно высокую лабораторную эффективность фосфомицина (монурала), достигающую 90%, добавление к терапии КанефронаâН, повышает клиническую эффективность лечения с 70 до 100% (при длительном приеме препарата). Вероятно, это связано с комплексным антимикробным, противовоспалительным, спазмолитическим и диуретическим эффектом последнего. Потенцируя действие фосфомицина (монурала), КанефронâН обеспечивает дополнительный противовоспалительный и симптоматический эффект, который сохраняется и после прекращения активной антибактериальной терапии. Кроме того, оказалось, что длительный прием КанефронаâН обеспечивает устойчивый противорецидивный эффект, о чем свидетельствует отсутствие клинических и лабораторных проявлений цистита через 30 дней лечения.
Результаты лечения больных из группы Б
После проведенного курса инициальной терапии клиническое улучшение наступило у 25 (89%) больных – 13 (92,8%) больных из подгруппы Б1 и 12 (85,8%) больных из подгруппы Б2.
Через 30 дней наблюдения жалобы по-прежнему отсутствовали или были выражены незначительно у 10 из 14 (71%) больных, не получавших поддерживающей терапии КанефрономâН. У 3 (21%) больных, несмотря на достигнутый ранее положительный эффект, было отмечено повторное развитие клинической картины цистита (см. таблицу 4).
Что касается больных из подгруппы Б2, получавших поддерживающую терапию КанефрономâН, то через 30 дней жалобы отсутствовали у 13 из 14 (92,8%) больных (см. таблицу 4).
Таким образом, прием КанефронаâН не только способствовал поддержанию достигнутого ранее эффекта, но и дополнительно повышал эффективность инициальной терапии на 7%. В общем, через 30 дней наблюдения эффективность лечения с применением КанефронаâН была выше эффективности терапии без приема данного препарата на 21,8%.
По-видимому, в отсутствие выявляемого возбудителя (или при выявлении его в низких титрах) и пиурии эффективность применения КанефронаâН обусловлена его противовоспалительным, спазмолитическим и диуретическим эффектом, что делает целесообразным применение данного препарата с целью профилактики рецидивов хронического цистита после достигнутого клинического улучшения, а также для повышения эффективности курса инициальной комплексной терапии.
Следует отметить, что в процессе применения КанефронаâН в группах А и Б не было зарегистрировано ни одного случая развития побочных эффектов или непереносимости препарата.
Результаты нашего исследования свидетельствуют о том, что:
- применение фитопрепарата КанефронâН в комплексной терапии хронического цистита не только повышает эффективность инициальной терапии (антибактериальной или комплексной, проводимой в отсутствие пиурии), но и способствует достижению более длительной ремиссии заболевания;
- длительный прием КанефронаâН не сопровождается развитием побочных эффектов.
Таким образом, КанефронâН следует рекомендовать к широкому применению у женщин, страдающих хроническим циститом.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.