Патология билиарного тракта: от МКБ-10 к МКБ-11
- Аннотация
- Статья
- Ссылки
- English
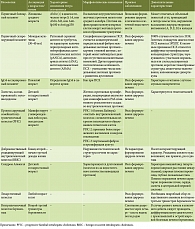
![Таблица 1. Сравнение Международной классификации болезней 10-го и 11-го пересмотров [14]](/upload/resize_cache/iblock/8b5/195_350_1/Livzan1.jpg)



Распространенность патологии билиарного тракта (БТ), по эпидемиологическим данным, достигает 10–15% среди взрослого населения и имеет неуклонную тенденцию к росту. Максимальный рост отмечается в странах с наиболее высокой распространенностью факторов риска [1].
Патология БТ подразделяется на органическую и функциональную. При этом характерной особенностью всей группы заболеваний БТ независимо от их природы является наличие общих факторов риска, а также схожих клинических проявлений.
К формированию, прогрессированию и рецидивированию патологии БТ предрасполагают следующие факторы: нарушение режима и особенностей питания (однообразное питание, прием пищи всухомятку, переедание, обильный прием пищи на ночь, избыточное употребление продуктов, богатых жирами), ожирение, гипер- и дислипидемия, женский пол, прием некоторых лекарственных препаратов (гормональные контрацептивы, цефтриаксон и др.), генетическая предрасположенность. Вышеперечисленные факторы способны повышать литогенность желчи и в итоге приводить к двигательным нарушениям БТ. Кроме того, двигательные расстройства и стаз желчи ассоциируются с перенесенной холецистэктомией (ХЭ), врожденными и приобретенными аномалиями БТ, глистно-паразитарными инвазиями и бактериальными кишечными инфекциями. Сахарный диабет является еще одним независимым фактором риска ввиду снижения сократительной способности стенки желчного пузыря (ЖП) из-за формирования диабетической нейропатии [2–6].
Основным проявлением патологии БТ является билиарная боль, которая локализуется в эпигастрии и/или правом верхнем квадранте при обязательном наличии следующих критериев [7]:
- достигает устойчивого уровня и длится 30 минут или дольше;
- возникает в различные промежутки времени (не каждый день);
- достаточно выражена, чтобы прервать повседневную деятельность, или требует обращения за неотложной помощью;
- незначительно (< 20%) связана с перистальтикой кишечника;
- незначительно (< 20%) уменьшается при изменении положения тела или приеме кислотосупрессивных препаратов.
К дополнительным/вспомогательным диагностическим критериям относят связь боли с одним или более симптомов:
- тошнота и рвота;
- иррадиация в спину и/или правую подлопаточную область или подключичную область, шею;
- пробуждение среди ночи.
Следует подчеркнуть, что билиарная боль может возникать в ночные часы даже при функциональной патологии БТ, что является отличительной характеристикой по сравнению с другими функциональными заболеваниями пищеварительного тракта, для которых традиционно появление боли в ночное время суток считается симптомом тревоги и стигмой органической патологии [7, 8].
К другим проявлениям заболеваний БТ относятся чувство горечи во рту, тошнота и общие симптомы, такие как повышение температуры тела, снижение аппетита, похудение, а при хроническом течении некоторых заболеваний могут появляться кожный зуд (холестаз), признаки билиарной недостаточности (диспепсия, нарушения стула, метеоризм), а также относительной панкреатической недостаточности с развитием синдрома мальабсорбции и нутритивной недостаточности. Еще одной особенностью билиарной патологии является нередкое сочетание функциональных расстройств с органическими заболеваниями [2]. Одним из таких примеров является формирование дисфункционального расстройства сфинктера Одди (СО) у лиц, перенесших ХЭ, вследствие нарушения реципрокного взаимодействия и скоординированной двигательной активности между ЖП и СО [9, 10].
Принимая во внимание общие факторы риска, схожие клинические проявления и высокую вероятность прогрессирования билиарной патологии, пациенты с впервые выявленными стигмами поражения БТ нуждаются в своевременном установлении этиологии процесса и назначении рациональной терапии, последующем динамическом наблюдении, частота которого и объем необходимых исследований определяются исходя из варианта выявленной патологии, сопутствующих заболеваний и ассоциированных состояний [2, 11].
Поскольку основным клиническим проявлением заболеваний БТ, значительно снижающим качество жизни пациентов, является билиарная боль, представляем пошаговый алгоритм диагностического поиска ее причины. Так, на первом этапе обследования пациента с билиарной болью необходим тщательный сбор анамнеза, что в ряде случаев уже при первом контакте позволяет правильно выбрать объем лабораторно-инструментальных методов исследования. Следует уточнить локализацию боли, наличие иррадиации и ночной симптоматики, провоцирующие факторы, продолжительность и характер (сжимающая, колющая, жгучая, постоянная, приступообразная), выяснить, что провоцирует приступ боли и чем он купируется. Уточняется эпидемиологический и лекарственный анамнез, сведения о перенесенных в прошлом оперативных вмешательствах на органах брюшной полости. При общем осмотре пациента с билиарной болью необходимо исключить острый воспалительный процесс органов брюшной полости (холецистит, панкреатит, перитонит). При заболеваниях, сопровождающихся холестазом, возможно обнаружение иктеричности склер, пожелтения кожного покрова и следов от расчесов (экскориаций). У части пациентов возможно обнаружение так называемых печеночных знаков – пальмарной эритемы, телеангиоэктазий или сосудистых звездочек. При осмотре живота необходимо обратить внимание на его размер, участие в акте дыхания, наличие видимой перистальтики, при пальпации исключить пузырные симптомы (симптомы Кера, Мерфи, Мюсси – Георгиевского, Ортнера, Лепене), симптомы раздражения брюшины, оценить состояние поджелудочной железы с помощью ее пальпации по Гротту, в зонах Шоффара и Губергрица, точках Кача и Мейо – Робсона; сфинктера Одди – при пальпации в точке Дежардена; оценить симптом флюктуации (положительный при асците) [2, 11–13].
Следующим шагом в соответствии с алгоритмом является назначение необходимого минимума лабораторно-инструментальных методов исследования, в том числе для исключения «симптомов тревоги». Всем пациентам с билиарной болью необходимо проведение общего (признаки воспаления, наличие анемии), биохимического анализов крови (функциональные пробы печени/ферменты поджелудочной железы), копрограммы и исследования кала на паразитов и яйца гельминтов сверхчувствительным методом. К обязательным инструментальным методам диагностики для исключения органической патологии относятся абдоминальное ультразвуковое исследование (УЗИ), эзофагогастродуоденоскопия (ЭГДС) с осмотром области большого дуоденального сосочка, а при необходимости – магнитно-резонансная холангиопанкреатография. При выявлении на данном этапе причины билиарной боли пациент подлежит лечению согласно действующим алгоритмам оказания медицинской помощи для установленной патологии. В отсутствие явных органических причин билиарной боли рекомендуется дополнить диагностический поиск такими методами исследования, как аутоиммунный печеночный профиль, допплерография для оценки портального кровотока, УЗ-холецистография с применением стимулятора сокращения – холецистокинина, эластометрия большого дуоденального сосочка, билиосцинтиграфия с имидодиацетиловой кислотой, эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), манометрия СО, колоноскопия [2, 11–13].
Рассмотрим особенности проявлений наиболее часто встречающихся в клинической практике терапевтов и гастроэнтерологов вариантов патологии БТ в свете перехода от Международной классификации болезней 10-го пересмотра (МКБ-10) к Международной классификации болезней 11-го пересмотра (МКБ-11).
Следует отметить, что в МКБ-11 произошли изменения в кодировании и трактовании патологий БТ (табл. 1). Так, дисфункция (дискинезия) СО в МКБ-10 кодировалась как «K83.4 – спазм сфинктера Одди», что с патогенетической точки зрения является не совсем корректной формулировкой, поскольку дискинезия СО подразумевает нарушение тонуса гладкой мускулатуры СО (спазм, дилатация). В обновленной версии заболеванию присвоен код «DC14.2 – дискинезия сфинктера Одди». Изменению в кодировании подверглись и холестатические заболевания. Ранее для первичного билиарного холангита (ПБХ) в литературе применялся термин «первичный билиарный цирроз (ПБЦ)», а в МКБ-10 заболевание обозначалось как «К74.3 – первичный билиарный цирроз». Кроме того, первичный склерозирующий холангит (ПСХ) рассматривался как один из вариантов возможных холангитов в рубрике «Другие болезни желчевыводящих путей (K83.0 – холангит)». В рамках МКБ-11 ПБЦ официально предложено заменить на ПБХ, что обусловлено успехами современной медицины, позволяющими диагностировать заболевание до развития цирротических изменений в печени. Обращает на себя внимание и то, что в обновленной версии МКБ оба заболевания перемещены в рубрику «Аутоиммунные заболевания печени» (DB96.1 – первичный билиарный холангит; DB96.2Y – другой уточненный первичный склерозирующий холангит).
К наиболее часто встречаемым органическим причинам билиарной боли относят холецистит, желчнокаменную болезнь (ЖКБ), полипы ЖП и поражение внутри- и внепеченочных желчных протоков.
Под хроническим холециститом понимают пролонгированный воспалительный процесс, вызванный нарушением опорожнения ЖП вследствие механических или функциональных причин. Хронический холецистит подразделяется на калькулезный (наиболее частый вариант) и акалькулезный (бескаменный) [15]. Ведущим проявлением является тянущая боль в правом подреберье, иррадиирующая назад в спину или правую лопатку. Боль, как правило, усиливается после приема жирной пищи. Характерны тошнота и периодическая рвота, усиленное вздутие, возникающие ночью. Длительность симптомов может варьировать от недели до нескольких месяцев, резкое их утяжеление может быть связано с возникновением острого холецистита. У части пациентов при обострении возможно повышение температуры тела. Следует также помнить, что у пожилых пациентов клинические проявления могут быть нечетко выраженные [2]. Основным методом диагностики является трансабдоминальное УЗИ, в пользу хронического холецистита свидетельствует увеличение толщины стенки ЖП (2–4 мм). Утолщение стенки ЖП ≥ 4 мм, наличие жидкости в околопузырном пространстве или резкой болезненности при надавливании датчиком в точке ЖП на высоте вдоха (ультразвуковой симптом Мерфи) свидетельствуют в пользу острого холецистита и требуют немедленной госпитализации больного [15–18].
ЖКБ является довольно распространенной патологией, на долю которой приходится примерно 10–20% среди взрослого населения планеты. Следует отметить, что примерно у 80% пациентов ЖКБ протекает бессимптомно. К основным факторам риска относят возраст 40–69 лет, женский пол, избыточную массу тела, быстрое похудение, сахарный диабет, цирроз печени, беременность, заместительную гормональную терапию в период постменопаузы и отягощенную наследственность [12, 19–23]. Ожирение увеличивает вероятность образования камней в ЖП, особенно у женщин, из-за увеличения секреции холестерина с желчью. С другой стороны, пациенты после резкого снижения массы тела или длительного голодания также имеют высокий риск образования камней вследствие застоя желчи. Кроме того, было продемонстрировано, что у женщин репродуктивного возраста или принимающих эстрогенсодержащие контрацептивы образование камней в ЖП увеличивается в два раза по сравнению с мужчинами вследствие увеличения уровня холестерина в желчи и снижения сократимости ЖП [24–27].
Клинические симптомы при ЖКБ могут отсутствовать или проявляться скудно (тяжесть в правом подреберье). Желчная колика (билиарная боль) развивается при вклинении камня в шейку ЖП, пузырный или общий желчный протоки. Приступ билиарной боли может быть спровоцирован употреблением жирной, жареной пищи и большого объема пищи накануне, а также тряской, ездой и наклонами туловища [7, 12].
При воспалении стенки ЖП на фоне обструкции его шейки или протока камнем формируется острый холецистит. Боль при этом более продолжительная, чем при желчной колике, сопровождается фебрильной лихорадкой и симптомами раздражения брюшины. При несвоевременно назначенном лечении исходами могут быть эмпиема, гангрена, перфорация ЖП или перитонит [16, 19].
Распространенность полипов ЖП в общей популяции варьирует от 0,3 до 13,8% [28]. Частота малигнизации полипов ЖП достигает 0–27% при размере полипов до 10 мм в диаметре и 34–88% при образованиях более 10 мм [29]. Холестериновые полипы считаются самыми распространенными, на их долю приходится до 60–70% всех случаев. В исследовании N. Akyürek и соавт. среди пациентов с полипами ЖП пациенты предъявляли жалобы на боль в правом подреберье (59%), дискомфорт в эпигастрии (32%), тошноту (41%), метеоризм (22%) и пищевую непереносимость (15%) [30]. Тактика ведения пациентов с полипами ЖП напрямую зависит от их размеров, наличия клинических проявлений и факторов риска. Обнаружение полипов 10 мм и более диктует необходимость проведения плановой ХЭ. При размерах менее 10 мм в отсутствие клинических проявлений рекомендовано динамическое наблюдение с помощью УЗИ с периодичностью один раз в шесть месяцев. Пациенты с полипами ЖП размерами от 6 до 9 мм при наличии факторов риска (возраст старше 50 лет, конкременты ЖП, ПСХ) должны быть обсуждены на консилиуме с целью решения вопроса о необходимости проведения плановой ХЭ [31, 32].
ПБХ является аутоиммунным заболеванием печени. Чаще встречается у женщин среднего возраста, чем у мужчин (в соотношении 9:1). Типичный пациент с ПБХ – это женщина среднего возраста с жалобами на кожный зуд и/или выраженную общую слабость. Другие симптомы включают боль в правом подреберье, похудение и желтушное окрашивание кожи. Длительно существующий холестаз сопряжен с недостатком желчных кислот, необходимых для полноценного переваривания и всасывания нейтральных жиров, в связи с этим у пациентов с ПБХ может отмечаться диарея с объемным пенистым стулом, приводящая к потере массы тела. Нередко у пациентов с ПБХ происходит нарушение всасывания жирорастворимых витаминов (А, D, Е, К) и кальция. Гистологически воспалительный процесс локализуется исключительно во внутрипеченочных желчных протоках малого или среднего калибра. Характерными признаками являются плотная инфильтрация мононуклеарных клеток вокруг желчных протоков (хронический негнойный деструктивный холангит) и образование гранулемы, что приводит к разрушению мелких внутрипеченочных желчных протоков, нарушению желчеотделения. В исходе прогрессирования заболевание ведет к формированию фиброза, цирроза и печеночной недостаточности [33–35].
ПСХ также является аутоиммунным заболеванием, характеризующимся воспалением и фиброзом внутри- и внепеченочных желчных протоков, при этом отмечается их облитерация и формирование мультифокальных стриктур, что в конечном итоге приводит к циррозу печени и печеночно-клеточной недостаточности. Заболевание чаще встречается у молодых мужчин, чем у женщин (в соотношении 2:1). Как правило, заболевание дебютирует в возрасте 30–40 лет. В 80% случаев сочетается с воспалительными заболеваниями кишечника (ВЗК), что обусловливает необходимость проведения колоноскопии с биопсией. К типичным клиническим признакам ПСХ относятся кожный зуд, боль в правом подреберье, слабость, потеря массы тела [35, 36].
Следует помнить и о редких формах поражения холангиоцитов (табл. 2). Одним из таких вариантов является IgG4-ассоциированный холангит. Как правило, заболевание встречается у пожилых пациентов и характеризуется биохимическими и холангиографическими признаками ПСХ, для него не характерно сочетание с ВЗК, но нередко у данной группы пациентов диагностируется аутоиммунный панкреатит [35].
Функциональные билиарные расстройства относятся к моторно-двигательным нарушениям и вызываются либо метаболическими расстройствами, либо первичными расстройствами моторики (развитие преходящей функциональной обструкции) и повышением висцеральной гиперчувствительности.
В соответствии с рекомендациями согласительного совещания Международной рабочей группы по совершенствованию диагностических критериев функциональных заболеваний желудочно-кишечного тракта (Римские критерии IV пересмотра, 2016 г.) [13, 37], к функциональным билиарным расстройствам относят: E1 – билиарная боль; E1а – функциональные расстройства желчного пузыря; E1b – функциональное билиарное расстройство сфинктера Одди; E2 – функциональное панкреатическое расстройство сфинктера Одди.
Функциональные нарушения ЖП подразумевают отсутствие ЖКБ или других структурных изменений БТ и верхних отделов пищеварительного тракта. Дисфункция сфинктера Одди определяется как доброкачественное, некалькулезное обструктивное расстройство. Согласно Милуокской классификации, выделяют три типа дисфункции билиарной и панкреатической порции СО (табл. 3, 4) [8, 38].
Согласно современным представлениям, развитие билиарной дисфункции связано с нарушением координированной перистальтики желчных путей на различных уровнях и появлением преходящей функциональной обструкции (по сути – спазма), а также с повышением висцеральной чувствительности. Получены косвенные данные о развитии преходящей функциональной обструкции в области шейки ЖП при его дискинезии, вследствие чего объем сокращения ЖП оказывается недостаточным. Кроме того, изменяется динамика самого сокращения. Уже при небольшом повышении давления в шейке могут возникать болевые ощущения. Немаловажную роль в развитии дискинезии ЖП и СО отводят литогенной желчи. В условиях перенасыщения холестерином нарушаются сократимость мышечных волокон и восприятие двигательных импульсов [8, 13].
Основным проявлением функциональных билиарных расстройств являются приступы билиарной боли в отсутствие явного органического поражения желчных путей. Функциональная билиарная боль схожа с органической билиарной болью (желчной коликой), но для нее не характерны озноб, лихорадка и желтуха. Также отсутствует связь между погрешностями в питании, однако боль может провоцироваться стрессовыми факторами и некоторыми лекарственными препаратами (опиоиды, эстрогены, соматостатин). Нередко функциональной патологии БТ могут сопутствовать функциональная диспепсия или гастропарез [39].
Диагностические критерии функционального расстройства СО по билиарному типу [8, 13]:
- критерии, характерные для билиарной боли;
- повышенные ферменты печени или дилатация желчных протоков, но не оба признака;
- отсутствие камней или других структурных аномалий в желчных протоках.
Поддерживающие критерии:
- нормальный уровень амилазы/липазы;
- аномальные результаты манометрии СО;
- гепатобилиарная сцинтиграфия.
Диагностические критерии функционального расстройства СО по панкреатическому типу (все следующее):
- документированные рецидивы эпизодов панкреатита (типичная боль при уровне амилазы или липазы в крови выше трех норм, признаки острого панкреатита по данным визуализации);
- другие причины панкреатита исключены;
- отрицательные данные эндоскопического УЗИ;
- аномальные данные манометрии СО.
Таким образом, для установления причины билиарной боли пациент должен пройти обследование в соответствии с вышеуказанным алгоритмом. Вместе с тем крайне важным уже на этапе диагностического поиска представляется эффективное купирование боли. При этом важно, чтобы лекарственный препарат не влиял на результаты обследования, не маскировал острую хирургическую патологию и не обладал выраженными побочными эффектами. В этой связи не рекомендовано назначение анальгетиков и нестероидных противовоспалительных препаратов, а в качестве препаратов выбора рассматриваются спазмолитики (табл. 5) [40].
Ведущее значение в купировании билиарной боли отводится миотропным спазмолитическим препаратам. Одним из таких препаратов является оригинальный мебеверина гидрохлорид. Являясь селективным миотропным спазмолитиком, он оказывает прямое регулирующее действие на гладкую мускулатуру кишечника [40, 41]. Механизм его действия основан на снижении проницаемости мембран гладкомышечных клеток для внеклеточного Na+ и, как следствие, подавлении вхождения ионов Ca++ в клетку через медленные кальциевые каналы. Ввиду особенностей механизма действия мебеверина гидрохлорид устраняет спазм, не вызывая при этом атонии кишечника [42], что позволяет применять данный препарат без ограничений по длительности курса лечения.
Помимо устранения спазма и боли, важным условием лечения заболеваний билиарной системы является уменьшение литогенности желчи. В ряде исследований отечественных ученых доказано, что применение мебеверина гидрохлорида в составе комбинированной терапии способствует нормализации биохимических показателей желчи [43], что, в свою очередь, снижает риски камнеобразования.
В отличие от других спазмолитических препаратов оригинальный мебеверина гидрохлорид не метаболизируется семейством цитохромов, вследствие чего обладает минимальными рисками лекарственных взаимодействий, что упрощает его назначение совместно с другими препаратами [42–45]. Кроме того, препарат не имеет системных побочных эффектов, в том числе антихолинергических [42]. Благодаря своей эффективности и безопасности препарат вошел во многие клинические рекомендации и стандарты оказания медицинской помощи [2, 11–13].
Согласно обновленной инструкции по применению препарата, продолжительность его приема не ограничена. Уже в первые две – четыре недели терапии отмечается стойкое улучшение симптомов, а наиболее выраженная эффективность может наблюдаться после шести – восьми недель терапии, что подтверждено клиническими исследованиями. Рекомендованный режим дозирования оригинального мебеверина гидрохлорида составляет 200 мг (одна капсула) на прием два раза в день до еды в течение как минимум шести – восьми недель. Важно, что длительность курса терапии и дозировка препарата зависят от непосредственной причины билиарной боли, индивидуальных особенностей течения заболевания и выраженности клинических симптомов [42].
После установления причины билиарной боли лечение пациентов проводится в соответствии с клиническими рекомендациями и стандартами оказания медицинской помощи при конкретной патологии. В целом курация пациента с патологией БТ в обязательном порядке должна включать комплекс мероприятий по коррекции диеты, изменению образа жизни (модификация факторов риска), которые негативным образом отражаются на моторике желчевыводящих путей, а также назначение средств этиологической (дегельминтизация, антибактериальные препараты), патогенетической (спазмолитики, урсодезоксихолевая кислота, холестирамин) и симптоматической (ферменты) терапии. Применение прокинетических препаратов может быть оправдано при возникновении сопутствующих симптомов диспепсии на фоне ЖКБ [13, 46].
Предлагаем рассмотреть реализацию представленного диагностического алгоритма на примере клинического случая.
Пациентка А. 59 лет обратилась к гастроэнтерологу на кафедру факультетской терапии и гастроэнтерологии Омского государственного медицинского университета.
Основные жалобы на момент осмотра: тяжесть в правом подреберье, периодически боли в правом подреберье давящего характера после употребления жирной и жареной пищи, с иррадиацией под правую лопатку, длительностью от 30 минут и более, тошнота, чувство тяжести в эпигастрии после приема пищи, горечь во рту, преимущественно в утренние часы. Аппетит сохранен, вес стабильный, патологических примесей в кале (слизи, крови, гноя) нет.
Анамнез заболевания: считает себя больной с 2015 г., когда впервые при плановом абдоминальном УЗИ обнаружен конкремент в полости ЖП диаметром 15 мм. В 2019 г. на фоне погрешности в диете возник приступ резкой боли в правом подреберье схваткообразного характера, с иррадиацией в спину, под правую лопатку, сопровождающийся тошнотой, рвотой, повышением температуры тела, без эффекта от приема спазмолитиков. По неотложной помощи доставлена в хирургический стационар, где в экстренном порядке проведена лапароскопическая ХЭ по поводу острого кулькулезного холецистита. После операции чувствовала себя удовлетворительно, в дальнейшем у врача не наблюдалась. В течение года до настоящего обращения беспокоят тяжесть в правом подреберье, периодически боли в правом подреберье давящего характера после употребления жирной и жареной пищи, с иррадиацией под правую лопатку, длительностью от 30 минут и более, тошнота, чувство тяжести в эпигастрии после приема пищи, горечь во рту, преимущественно в утренние часы. Самостоятельно принимала ферментные препараты, без должного эффекта.
Анамнез жизни: вирусные гепатиты, ВИЧ-инфекцию отрицает; операции, травмы, переливание чужой крови отрицает; курение, употребление спиртных напитков отрицает. Аллергоанамнез не отягощен. Эпидемиологический анамнез – без особенностей. В анамнезе артериальная гипертензия второй стадии, риск – 3, контролируемая.
Объективно: рост – 165 см, вес – 92 кг, индекс массы тела (ИМТ) – 33,8 кг/м2. Состояние удовлетворительное, в сознании. Питание обычное. Кожный покров и видимые слизистые оболочки – без особенностей. Подкожно-жировая клетчатка развита избыточно, распределена равномерно. Пальпируемые лимфатические узлы не увеличены, безболезненные. Щитовидная железа нулевой степени (по ВОЗ). Дыхание везикулярное, хрипов нет, частота дыхательных движений – 16 в минуту. Тоны сердца ритмичные, без патологических шумов. Отеков нет. Артериальное давление – 125/75 мм рт. ст. Пульс – 72 удара в минуту. Температура тела – 36,6 °С. Сатурация – 99%. Живот мягкий, болезненный в эпигастрии, околопупочной области, преимущественно справа. При глубокой пальпации живот чувствительный в эпигастрии, в зоне Шоффара. Печень не увеличена. Симптомы Кера, Мерфи, Ортнера – отрицательные. Симптом поколачивания по поясничной области – отрицательный с обеих сторон.
В связи с наличием синдром билиарной боли пациентке рекомендовано дообследование в следующем объеме: общий анализ крови, биохимический анализ крови (аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), щелочная фосфатаза (ЩФ), гамма-глутамилтрансфераза (ГГТП), глюкоза, билирубин прямой, общий белок, общий холестерин, глюкоза, панкреатическая амилаза, мочевая кислота, креатинин), общий анализ мочи, копрограмма, кал на паразитов и яйца гельминтов сверхчувствительным методом, кал на цисты лямблий, ЭГДС, УЗИ абдоминальное.
С целью купирования билиарной боли на этапе дообследования пациентке назначен оригинальный препарат мебеверина гидрохлорида в дозе 200 мг по одной капсуле два раза в день за 20 минут до приема пищи. Пациентка отметила хороший эффект от приема препарата уже на третий день от начала терапии.
При повторном визите с результатами назначенного обследования выявлено:
- общий анализ крови: лейкоциты – 6,54 × 109/л, нейтрофилы – 59,1%, лимфоциты – 33,0%, моноциты – 4,6%, эозинофилы – 2,7%, базофилы – 0,6%, эритроциты – 4,94 × 1012/л, гемоглобин – 142 г/л, тромбоциты – 377 × 109/л, скорость оседания эритроцитов – 10 мм/ч;
- биохимический анализ крови: АЛТ – 27 Ед/л, АСТ – 30 Ед/л, ЩФ – 110 МЕ/л, ГГТП – 40 ЕД/л, глюкоза – 5,2 ммоль/л, мочевая кислота – 352 ммоль/л, креатинин – 86 ммоль/л, общий белок – 70,2 г/л, общий билирубин – 18,4 мкмоль/л, холестерин –
- 7,1 ммоль/л (↑), амилаза – 56 Ед/л;
- общий анализ мочи: прозрачная, цвет – желтый, pH – 5,0, плотность – 1020, белок – нет, глюкоза – нет, лейкоциты – 0–1 в п/з, эритроциты – 0 в п/з, эпителий – нет в п/з;
- копрограмма: без патологических изменений;
- кал на паразитов и яйца гельминтов методом PARASEP трехкратно: не обнаружено;
- кал на цисты лямблий (Giardia lamblia) иммуногистохимическим методом: не обнаружено;
- ЭГДС: признаки поверхностного гастрита антрального отдела желудка, поверхностного дуоденита. Экспресс-анализ на Helicobacter pylori – отрицательно;
- гистологическое исследование биоптатов желудка: хронический антральный гастрит, H. pylori-негативный, без кишечной атрофии, без метаплазии;
- УЗИ абдоминальное: состояние после ХЭ, внутрипеченочные желчные протоки и холедох не расширены, диффузные изменения в поджелудочной железе.
Пациентке выставлен заключительный клинический диагноз: «дисфункциональное расстройство сфинктера Одди по билиарному типу. Состояние после лапароскопической холецистэктомии по поводу ЖКБ (2019 г.). Хронический поверхностный гастрит (морфологически верифицированный), Н. pylori-негативный. Синдром диспепсии по типу эпигастрального болевого синдрома. Дуоденит. Дислипидемия. Ожирение I степени (ИМТ – 33,8 кг/м2)».
Рекомендовано: диета (частое, дробное питание с ограничением жареной и жирной пищи, консервированных продуктов и газированных напитков), не допускать длительныех промежутков между приемами пищи. Рекомендации по физической активности: дозированные аэробные физические нагрузки по 30–60 минут средней интенсивности – не менее пяти дней в неделю.
Медикаментозная терапия:
- продолжить прием оригинального мебеверина гидрохлорида в дозе 200 мг два раза в день за 20 минут до еды до восьми недель в качестве спазмолитического препарата;
- урсодезоксихолевая кислота в дозе 250 мг два раза в день в течение восьми недель для профилактики формирования камней во внутрипеченочных желчных протоках и холедохе с учетом сохраняющихся факторов риска;
- ферментные препараты по требованию при более обильных приемах пищи.
Таким образом, патология БТ представляет собой группу гетерогенных по своей природе заболеваний и актуальную проблему в клинической практике. Ввиду высокой распространенности, схожести клинических проявлений особую сложность у врачей терапевтов и гастроэнтерологов вызывает проведение дифференциального поиска для своевременного установления диагноза и назначения рациональной терапии. Немаловажным при курации пациентов является быстрое и безопасное купирование билиарной боли как основного симптома заболеваний БТ, в том числе на этапе обследования. С этой целью целесообразно применение селективных спазмолитических препаратов с миотропным действием, в частности оригинального мебеверина гидрохлорида, который продемонстрировал свою эффективность, безопасность и преимущество перед другими спазмолитиками в целом ряде клинических исследований.
M.A. Livzan, PhD, Prof., Corresponding member of the RAS, O.V. Gaus, PhD, M.A. Lisovskiy
Omsk State Medical University
Contact person: Olga V. Gaus, gaus_olga@bk.ru
Pathology of the biliary tract is widespread among the adult population of many countries around the world. This is due to the high incidence of risk factors in these populations. In addition to the commonality of risk factors and progression, another characteristic feature of the entire group of biliary diseases of both organic and functional nature is the presence of similar clinical manifestations. The main manifestation of biliary tract pathology is biliary pain. This article reflects modern data on the most common variants of biliary tract pathology in the practice of general practitioners and gastroenterologists in the light of the transition from ICD X to ICD XI, and presents a step-by-step diagnostic algorithm and approaches to the management of patients with biliary pain, including an example own clinical case.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.