Синдром внутрипеченочного холестаза: патогенетические подходы к терапии
Синдром внутрипеченочного холестаза является клиническим проявлением лекарственной токсичности, и выбор терапии данного заболевания – проблема, регулярно встающая перед гастроэнтерологами и врачами других специальностей. Свой доклад профессор кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ А.Н. КАЗЮЛИН, д.м.н., начал с описания клеточных и молекулярных механизмов, лежащих в основе холестаза. Их можно разделить на три группы:
- нарушения синтеза натриевой и калиевой АТФазы и транспортных белков под влиянием различных повреждающих факторов, таких как желчные кислоты, медиаторы воспаления, лекарственные препараты и их дериваты;
- изменения липидного состава и проницаемости мембран;
- нарушения целостности структур цитоскелета и микрофиламентов, которыми обусловлена моторика канальцев.
Внутрипеченочный холестаз связан с нарушением оттока желчи, вызванным механическими факторами. Последние располагаются в области крупных желчных ходов и могут быть обнаружены с помощью эндоскопической ультрасонографии, чреспеченочной и ретроградной холангиографии и компьютерной томографии. Однако существует и другая форма холестаза – внутрипеченочная, которая развивается под действием лекарств и инфекционных агентов, а также вследствие аутоиммунной агрессии и под воздействием метаболических и генетических факторов. Формирование желчи в печени идет в три этапа. Это захват из крови и перенос в гепатоциты компонентов желчи, собственно синтез желчи и секреция ее в желчные канальцы. Из канальцев желчь поступает в экстралобулярные желчные протоки, эпителий которых секретирует гидрокарбонаты и воду – именно они обусловливают окончательный состав желчи. Внутрипеченочный холестаз (ВХ) может развиться или на уровне гепатоцитов (интралобулярный, гепатоцеллюлярный или каналикулярный холестаз), или в районе внутрипеченочных желчных протоков (экстралобулярный холестаз).
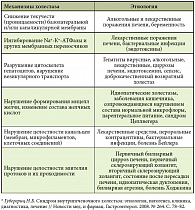
В основе различных видов холестаза лежат разные патогенетические механизмы. Так, внутридольковый холестаз вызывается недостаточной секрецией желчи клетками печени и желчными канальцами, а она, в свою очередь, обусловлена повреждением клеточных органелл. Междольковый холестаз связан с деструкцией и сокращением числа малых междольковых протоков, дуктул. Дуктулярная деструкция, исчезновение междольковых и септальных желчных протоков характерны для таких хронических холестатических заболеваний печени, как первичный билиарный цирроз и аутоиммунная холангиопатия, болезней, при которых желчные протоки становятся мишенью для аутоиммунного воспаления. Различные метаболические нарушения, отметил профессор А.Н. Казюлин, – дефицит ферментов синтеза желчных кислот, формы внутрипеченочного семейного холестаза, прогрессирующего и доброкачественного рецидивирующего холестаза и хронический холестаз беременных – сочетают признаки как гепатоцеллюлярного, так и обструктивного канальцевого холестаза, то есть в ряде случаев холестаз может иметь смешанные гистологические признаки.
Установлена связь между патогенетическими механизмами холестаза и этиологией заболевания (табл.). При этом, анализируя причины возникновения тех или иных гистологических нарушений, легко заметить, что одну из ведущих ролей в их развитии играет гепатотоксичность лекарственных препаратов. При лекарственных поражениях печени или в случае возникновения заболеваний какой-либо другой этиологии важнейшую роль в развитии холестаза играет нарушение строения цитоскелета гепатоцитов, приводящее к исчезновению микроворсинок на апикальной поверхности клеток и обратному току желчи в синусы. Другим патологическим механизмом ВХ, работающим на клеточном уровне, является нарушение внутриклеточного транспорта везикул, оно также способствует развитию холестаза. Накапливаясь в гепатоцитах, желчные кислоты вызывают повреждение клеточных мембран, блокируют синтез аденозинтрифосфата (АТФ), а также способствуют накоплению свободных радикалов, что в конечном итоге приводит к апоптозу клеток билиарного эпителия.
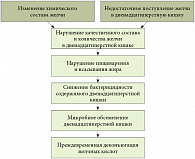
В поврежденных гепатоцитах снижается активность фермента S-аденозилметилсинтетазы, а значит, нарушается продукция S-адеметионина, что приводит к нарушению течения биохимических процессов в клетках. Запускающийся при этом каскад приводит к цитолизу гепатоцитов, наблюдающемуся при холестазе любого генеза. Клинические проявления холестаза также не зависят от этиопатогенеза заболевания, они сводятся к избыточному поступлению элементов желчи в кровь, уменьшению ее количества в кишечнике и разрушительному воздействию желчи на печеночные клетки и канальцы. Кроме того, холестаз приводит к развитию характерных нарушений в функционировании желудочно-кишечного тракта (рис. 1). ВХ со временем приводит к развитию таких состояний, как синдром раздраженного кишечника, дуоденальная панкреатическая недостаточность, цирроз печени и др. Последний, в свою очередь, снижает выработку адеметионина, а снижение количества эндогенного метионина провоцирует развитие функциональных и биохимических нарушений в работе печени. Возникает порочный круг, разорвать который можно, назначив больному препараты адеметионина. Данное назначение является более обоснованным с патогенетической точки зрения, чем применение фосфолипидов, поскольку эндогенные фосфолипиды синтезируются в организме при участии адеметионина.
Фосфолипиды – далеко не единственные вещества, в синтезе которых адеметионин играет важную роль. Он также участвует в выработке нейротрансмиттеров, нуклеиновых кислот, белков, порфиринов и гормонов, то есть в значительном числе анаболических процессов, идущих в организме. Не обходится без адеметионина и метаболизм лекарственных препаратов. И наконец, что особенно важно в лечении пациентов с ВХ, увеличение количества адеметионина в организме улучшает функционирование транспортных систем желчных кислот, связанных с мембранами гепатоцитов. Адеметионин обладает и антиоксидантным эффектом, при этом его метаболиты не токсичны, не провоцируют развитие окислительного стресса, что выгодно отличает его от многих (к сожалению, регулярно назначаемых) антиоксидантов. Помимо антиоксидантного, холеретического и холекинетического механизмов действия адеметионин обладает детоксикационным, регенерирующим, антидепрессивным и нейропротекторным эффектами, что позволяет не только защитить печень, но и улучшить общее состояние пациента. Профессор А.Н. Казюлин рассказал о ступенчатой схеме применения препарата Гептрал, действующим веществом которого является S-адеметионин: в течение 10–14 дней внутривенно вводится 800–1600 мг/сут, затем пациента переводят на поддерживающую терапию, в ходе которой препарат принимается перорально в суточной дозе от 400 до 3200 мг.
Адеметионин в практике терапевта и нарколога
Выступление профессора кафедры факультетской терапии Российского университета дружбы народов П.П. ОГУРЦОВА, д.м.н., было посвящено различным аспектам использования препаратов адеметионина в реальной клинической практике. В последнее время такая группа лекарственных средств (ЛС), как гепатопротекторы, стала популярной и пользуется спросом в нашей стране, несмотря на то что в зарубежных справочниках ЛС данной группы препаратов нет. Химических веществ, способных полностью защитить печень от всех неблагоприятных воздействий, не существует, однако соединения, в той или иной степени уменьшающие вред от алкоголя, погрешностей в диете, вирусных агентов и других неблагоприятных факторов, уже открыты и используются в клинической практике. «В ряду гепатопротекторов адеметионин я бы отметил в первую очередь, – сказал профессор П.П. Огурцов, – поскольку он обладает максимально широким спектром действия и защищает печень от наибольшего числа неблагоприятных факторов».
Проблема лекарственной гепатотоксичности по-прежнему актуальна, несмотря на многочисленные исследования, посвященные изучению безопасности тех или иных препаратов. Многие жизненно важные лекарственные средства, например противотуберкулезные или противоопухолевые, необходимо принимать на протяжении нескольких месяцев, несмотря на то что многие из этих препаратов обладают более или менее выраженной гепатотоксичностью. Именно поэтому при назначении гепатотоксичных препаратов необходимо своевременно назначать пациенту препараты, имеющие гепатопротективное действие, например Гептрал. Эффективность данного средства в плане уменьшения негативных последствий лекарственной терапии доказана многочисленными исследованиями. В частности, D. Santini и соавт. (2003) описали влияние адеметионина на состояние онкологических больных, получающих химиотерапию. Они получали по 400 мг адеметионина 2 раза в сутки1. Уже через 1 неделю приема препарата активность аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ) и лактатдегидрогеназы (ЛДГ) снизилась на 30%. Эффект препарата не ослабевал во время повторных курсов, что позволило завершить противоопухолевую терапию при минимальной частоте отсрочек лечения и снижении дозы противоопухолевых препаратов.
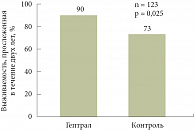
Широко используется адеметионин и в наркологической практике, причем не только в ходе лечения алкогольного цирроза печени, известного исхода хронической алкогольной интоксикации (рис. 2), но и для снижения гепатотоксичности таких препаратов, как налтрексон или дисульфирам, применяющихся для того, чтобы мотивировать пациента отказаться от спиртных напитков. Существует ряд особенностей применения Гептрала наркологами в качестве антидепрессанта. Адеметионин является уникальным антидепрессантом, который можно назначать больным с ВИЧ-инфекцией или пациентам, принимающим гепатотоксичную терапию. На фоне применения Гептрала снижается потребность в антидепрессивных препаратах. Гептрал положительно зарекомендовал себя в наркологической практике, где препарат используется для лечения пациентов с алкогольной и наркотической зависимостью, особенно если их состояние отягощается вирусными гепатитами, ВИЧ-инфекцией и абстинентным синдромом. Гептрал перспективен для использования в тройной терапии гепатита С, пока не внедренной в российскую клиническую практику, но уже продемонстрировавшей эффективность в регистрационных испытаниях. Тем не менее, назначая пациенту третий (а возможно, в скором времени, и четвертый) препарат для лечения гепатита С, врач должен помнить о проблеме лекарственной гепатотоксичности и своевременно назначать препараты для защиты от нее.
Ятрогенные поражения печени в практике интерниста
Проблему гепатотоксичности многих лекарственных препаратов, используемых в клинической практике, трудно переоценить. Так, 3–5% случаев желтухи и 10% случаев острой печеночной недостаточности вызваны именно приемом различных лекарственных средств. О том, какие препараты обладают выраженной гепатотоксичностью, как предотвратить развитие лекарственных поражений печени, рассказала д.м.н., профессор кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ Т.Е. ПОЛУНИНА. Потенциальной гепатотоксичностью обладают около 1000 лекарственных средств, в том числе «безобидный» парацетамол и препараты на основе лекарственных растений, например чистотела.
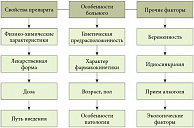
Лекарственные поражения печени могут проявляться по-разному: в форме сладж-синдрома, гранулематоза, острого и хронического гепатитов, стеатогепатита и некоторых других нозологий. Различаются и механизмы, через которые реализуется лекарственное поражение печени: прямое повреждение гепатоцита; прямое повреждение холангиоцитов; митохондриальная токсичность; иммунообусловленная гепатотоксичность; синусоидальная токсичность и др. Вероятность развития нежелательных реакций на прием того или иного лекарственного препарата и степень их выраженности зависят от ряда факторов: возраста и пола пациента, наличия у него сопутствующих заболеваний, общего количества принимаемых препаратов и наличия среди них гепатотоксичных, а также от режима питания и наследственности пациента. Не менее важны и характеристики самого препарата, как физические (очевидно, что кремы и мази гепатотоксичности не вызовут), так и биохимические (например, метаболизируется ли данный препарат с участием системы цитохрома P450) (рис. 3).
Среди механизмов, лежащих в основе гепатопротективного действия адеметионина, наряду с антиоксидантным, цитопротективным эффектами, описанными в предыдущих докладах симпозиума, профессор Т.Е. Полунина упомянула о благотворном воздействии адеметионина на иммунитет, а также об антифибротическом и детоксикационном эффектах применения препаратов адеметионина (последний реализуется преимущественно за счет нормализации оттока желчи в ЖКТ). Назначение Гептрала является обоснованным не только на начальных стадиях поражений печени. Способность адеметионина стимулировать регенерацию и пролиферацию гепатоцитов позволяет компенсировать функции печени и повысить выживаемость пациентов даже при выраженных изменениях в печени, в том числе цирротического характера. Эффективность адеметионина подтверждена многочисленными клиническими исследованиями, 6 из которых были включены в метаанализ, проведенный М. Frezza (1993)2. Установлено, что на фоне приема адеметионина значительно чаще, чем при употреблении плацебо, снижался уровень билирубина, АЛТ, АСТ и щелочной фосфатазы (ЩФ). Профессор Т.Е. Полунина отметила, что сегодня в руках лечащих врачей есть мощный инструмент для защиты печени, способный либо предотвратить развитие нежелательных явлений на фоне фармакотерапии, либо существенно уменьшить их выраженность.
Заключение
Поражения печени различного генеза занимают важное место в практике гепатологов и гастроэнтерологов, сталкиваются с ними и врачи других специальностей, например онкологи, наркологи и терапевты. Особенно актуальной стала эта проблема по мере увеличения доступности и распространенности различных лекарственных средств и, как следствие, полипрагмазии. Чем больше сложных многокомпонентных схем лечения входит в клиническую практику, тем выше риск развития нежелательных явлений, в том числе гепатотоксичности. Для предотвращения развития поражений печени используются препараты с гепатопротективным действием, в том числе один из несомненных лидеров данной группы как по числу механизмов действия, так и по количеству проведенных исследований – Гептрал производства компании «Эбботт». Использование данного препарата в клинической практике позволяет не только уменьшить выраженность поражений печени, но и улучшить общее состояние больного, что особенно важно при лечении коморбидных пациентов.