Проведен ретроспективный анализ медицинской документации 145 пациентов, получавших лечение в Научном центре неврологии в период с 2000 по 2011 г. по поводу установленного диагноза «синдром Гийена – Барре» (СГБ), cреди них 79% c острой воспалительной демиелинизирующей полиневропатией (ОВДП), 21% с острой моторной и моторно-сенсорной аксональной невропатией. У большинства (50%) пациентов наблюдалось тяжелое течение СГБ, 21% больных нуждались в респираторной поддержке. В остром периоде заболевания (медиана 10 [6; 15] суток от начала СГБ) всем пациентам проводилась патогенетическая терапия: плазмаферез (92%) или введение внутривенного иммуноглобулина (8%). На фоне лечения у 76% больных наблюдался регресс неврологической симптоматики (терапия считалась эффективной), у 15% состояние стабилизировалось (недостаточная эффективность терапии), у 9% продолжал нарастать неврологический дефицит (неэффективная терапия).
Сравнение неврологического статуса больных в остром периоде до и после лечения, получивших полноценный (суммарно за курс плазмафереза было изъято плазмы в объеме 120 мл/кг массы тела или введено 2 г/кг массы тела иммуноглобулина G) и редуцированный (количество изъятой плазмы менее 120 мл/кг массы тела) объем лечения, показало достоверное улучшение по шкалам NIS, MRS, INCAT, САШ, R-ODS и индексу Бартел в обеих группах (p < 0,05).
Дополнительный анализ, включивший пациентов с тяжелым и крайне тяжелым течением ОВДП, а также больных с аксональными формами СГБ, показал, что только полный объем патогенетической терапии обеспечивает достоверно более полный регресс неврологического дефицита в остром периоде и уменьшает степень инвалидизации (по шкалам INCAT, САШ, NIS и MRC и индексу Бартел). Вместе с тем объем патогенетической терапии не влияет на выраженность неврологического дефицита и степень инвалидизации в отдаленном периоде (через шесть и 12 месяцев после начала СГБ). Следовательно, главная цель проводимого лечения – уменьшение тяжести течения заболевания и минимизация рисков развития осложнений в остром периоде заболевания (острых венозных тромбозов, тромбоэмболий, гипостатических и вентилятор-ассоциированных пневмоний, сепсиса).
Таким образом, обязательным является проведение полного курса патогенетического лечения всем больным СГБ, особенно при тяжелом его течении, а также пациентам с аксональными формами заболевания.
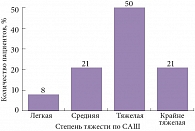
Рис. 1. Степень тяжести двигательного дефицита по САШ в остром периоде у исследованных пациентов с СГБ
![Таблица 1. Оценка неврологического статуса пациентов в зависимости от объема полученной патогенетической терапии (Ме [Ме25%; Ме75%])](/upload/resize_cache/iblock/5e1/195_350_1/5e1bc4f98485f79c7951978141a265ef.JPG)
Таблица 1. Оценка неврологического статуса пациентов в зависимости от объема полученной патогенетической терапии (Ме [Ме25%; Ме75%])
![Рис. 2. Сравнение неврологического статуса до и после лечения в группах с полным и редуцированным объемом патогенетической терапии (Ме [Ме25%; Ме75%])](/upload/resize_cache/iblock/dec/195_350_1/dec539ca40dba61ebff6fbf8fa651ae8.JPG)
Рис. 2. Сравнение неврологического статуса до и после лечения в группах с полным и редуцированным объемом патогенетической терапии (Ме [Ме25%; Ме75%])
![Таблица 2. Неврологический статус в остром периоде и после лечения в зависимости от объема проведенной терапии у тяжелых (стадия IV и V по САШ) пациентов с ОВДП (Ме [Ме25%; Ме75%])](/upload/resize_cache/iblock/ad8/195_350_1/ad8b2936f1f425cc0bf014a78afcd249.JPG)
Таблица 2. Неврологический статус в остром периоде и после лечения в зависимости от объема проведенной терапии у тяжелых (стадия IV и V по САШ) пациентов с ОВДП (Ме [Ме25%; Ме75%])
![Таблица 3. Неврологический статус в остром периоде до и после лечения в зависимости от объема проведенной терапии у пациентов с аксональными формами СГБ (Ме [Ме25%; Ме75%])](/upload/resize_cache/iblock/e49/195_350_1/e49062ed702445878ec2806e98cc5761.JPG)
Таблица 3. Неврологический статус в остром периоде до и после лечения в зависимости от объема проведенной терапии у пациентов с аксональными формами СГБ (Ме [Ме25%; Ме75%])
Введение
Синдром Гийена – Барре (СГБ) – это спорадически возникающая острая аутоиммунная полиневропатия, которая считается наиболее частой причиной постинфекционных неврологических нарушений периферической нервной системы [1]. Мировые показатели заболеваемости СГБ колеблются от 0,4 до 4 человек на 100 тыс. населения [2–5]. Заболеваемость в стандартном регионе России (например, в Ярославской области), по современным данным, составляет 1,8 на 100 тыс. человек [6].
Клинический симптомокомплекс при СГБ включает в себя прогрессирующие двигательные и чувствительные нарушения в виде периферических парезов рук и ног, чувствительных нарушений в конечностях и болевой синдром. В каждом третьем случае развивается тяжелая форма заболевания с нарушением ходьбы. Каждый четвертый больной нуждается в искусственной вентиляции легких из-за вовлечения в патологический процесс дыхательной мускулатуры [4, 7, 8].
В зависимости от точки приложения аутоиммунной атаки выделяют три основные формы СГБ:
- острую воспалительную демиелинизирующую полиневропатию (ОВДП) – 70–80% от всех случаев СГБ в мире, а в Европе и Северной Америке до 95% [3, 5, 9];
- острую моторную аксональную невропатию (ОМАН) – 10–15% от всех случаев СГБ в мире;
- острую моторно-сенсорную аксональную невропатию (ОМСАН) – до 5% от всех случаев СГБ в мире.
Две последние формы СГБ часто объединяют в одну группу аксональных форм, так как считается, что они являются разной степенью проявления одного и того же патологического состояния [10]. Согласно эпидемиологическим исследованиям, в Японии, Китае и Южной Америке аксональные формы развиваются гораздо чаще, чем в Европе (до 30–47% от всех случаев СГБ) [3, 11, 12].
СГБ характеризуется монофазным самоограничивающим течением. Несмотря на тяжесть острого периода, у большинства больных (60–80%) наблюдается полное восстановление двигательных функций и хороший ответ на патогенетическую терапию (курс программного высокообъемного плазмафереза или внутривенного иммуноглобулина класса G) [5, 8, 13, 14]. Проведение такой терапии формально считается допустимым, поскольку действующие на сегодняшний день медико-экономические стандарты по полиневропатиям не содержат детализированных схем. Схожие проблемы существуют и в других развивающихся странах, например Бангладеш и Индии. Вместе с тем из-за скудной оснащенности российских клиник аппаратами для высокообъемного плазмафереза и достаточно низкой доступности внутривенного иммуноглобулина пациенты зачастую не получают должного объема лечения [6]. Особенности ответа на патогенетическую терапию, в том числе в редуцированном объеме, а также исходы СГБ в российской популяции детально не изучены.
Следует напомнить о необходимости проведения специфического лечения заболевания, которое позволяет предотвратить прогрессирование СГБ до степени глубокого тетрапареза и пареза дыхательной мускулатуры и предупредить развитие жизнеугрожающих осложнений [5, 7, 8]. Однако лечение не всегда оказывается достаточно эффективным: около 20% пациентов, перенесших данное заболевание, не могут самостоятельно ходить спустя шесть месяцев после СГБ, а 12% больных – и через год [15–17].
По приблизительным подсчетам, в России ежегодно заболевают СГБ не менее 2700 человек, в Москве – около 200 пациентов. К настоящему времени накоплен большой опыт наблюдения и ведения таких больных в ведущем неврологическом центре России – Научном центре неврологии (Москва), более 40 лет специализирующемся в этой области.
Цель исследования
Изучение эффективности патогенетической терапии (плазмафереза) СГБ в полном и редуцированном объеме на примере жителей г. Москвы и Московской области.
Материал и методы исследования
Исследование проводилось на базе Научного центра неврологии.
Субъект исследования – жители Москвы и Московской области, которые отвечали критериям исследования.
Объект исследования – истории болезни, выписные эпикризы, амбулаторные карты, протоколы обследований пациентов с СГБ, получавших консультацию или проходивших лечение в Научном центре неврологии в период с 2000 по 2011 г.
Всего проанализировано 145 клинических случаев, включенных в общую выборку для последующего статистического и системного анализа. В исследование включались пациенты с первично выявленным и подтвержденным диагнозом СГБ (по диагностическим критериям СГБ, ВОЗ, 1993 г. [8]) любого возраста и степени тяжести, заболевшие в период с 2000 по 2011 г., обращавшиеся за консультативной помощью, проходившие лечение в Научном центре неврологии или лечебно-профилактических учреждениях г. Москвы. Из исследования исключались пациенты с тяжелой соматической патологией в стадии декомпенсации, а также больные с ошибочным или неподтвержденным диагнозом СГБ.
Метод исследования: ретроспективный анализ медицинской документации (формы № 027/у, 003/у, 25/у).
Форма СГБ уточнялась по результатам электронейромиографии (ЭНМГ) согласно нейрофизиологическим критериям классификации СГБ по R. Hadden [18]. В сомнительных случаях (по данной классификации «неопределенная группа») окончательное решение о принадлежности к той или иной форме принималось по совокупности изменений ЭНМГ-параметров, полученных в процессе динамического наблюдения с повторным проведением ЭНМГ. Степень нарушений двигательных функций при СГБ в остром периоде заболевания оценивалась по Североамериканской шкале тяжести двигательного дефицита (САШ) [8]. Так, легкой степени тяжести соответствовали стадии I и II, средней степени – стадия III, тяжелой степени – стадия IV, крайне тяжелой степени – стадия V.
Описание неврологического статуса пациентов проводилось по шкале оценки невропатических нарушений (Neuropathy Impairment Score – NIS) [8], шкале оценки мышечной силы Британского совета по медицинским исследованиям (Medical Research Council Weakness Scale sum score – MRC-SS) [19], шкале инвалидизации (Inflammatory Neuropathy Cause and Treatment – INCAT) [8], индексу активности повседневной жизни Бартел [20], шкале инвалидизации на основе модели Rasch (Rasch-built Overall Disability Scale – R-ODS) [21].
Пациентам проводилась патогенетическая терапия курсами плазмафереза или внутривенного иммуноглобулина G. Согласно общепринятым мировым стандартам [7, 8, 14, 22], терапия считалась выполненной в полном объеме, если суммарно за курс плазмафереза было изъято плазмы в объеме 120 мл/кг массы тела пациента, а при внутривенной иммунотерапии было введено 2 г/кг массы тела иммуноглобулина G. Если количество изъятой плазмы составляло менее 120 мл/кг массы, объем терапии считался редуцированным. Во всех случаях внутривенной иммунотерапии был проведен полноценный объем лечения, а поскольку патогенетическая терапия обоими способами признана равнозначной [8, 13, 23], эти пациенты были включены в общую выборку.
Эффективность лечения оценивалась по сумме нескольких критериев. Во-первых, изменение клинической картины. Эффективным лечение считалось при регрессе неврологической симптоматики, недостаточным результат признавался при стабилизации состояния больного, при нарастании симптоматики несмотря на проводимые мероприятия регистрировалось отсутствие эффекта. Во-вторых, сравнение результатов оценки неврологического статуса пациентов по шкалам, перечисленным выше, а также сроков наступления стадии III по САШ в периоде восстановления (у тяжелых и крайне тяжелых больных). В-третьих, отдаленные результаты. Оценивалось влияние проведенного лечения на состояние больных через шесть и 12 месяцев по шкалам САШ, MRC, INCAT, R-ODS и индексу Бартел.
Статистическая обработка результатов проводилась с использованием общепринятых параметрических и непараметрических методов сравнения. После теста на нормальность распределения (Шапиро – Уилка) количественные данные были представлены в виде медианы и интерквартильного размаха (Ме [Ме25%; Ме75%]). В силу того что распределение отличалось от нормального, применялись методы непараметрической статистики. Межгрупповое сравнение значимости клинических и параклинических параметров при равном количестве наблюдений проводили с помощью парного W-критерия Уилкоксона, а при неравном количестве наблюдений – U-критерия Манна – Уитни (гипотеза о различиях между группами принималась при р < 0,05). Качественные данные были представлены в виде абсолютных значений и процентов. Взаимосвязь качественных показателей исследовали с помощью критерия χ2 Пирсона, χ2 Пирсона с поправкой Йетса, точного критерия Фишера. Для исследования взаимосвязи количественных признаков независимо от вида их распределения, количественного и качественного порядкового признака применяли непараметрические методы корреляционного анализа (коэффициент корреляции Спирмена (R)). Статистическая обработка результатов выполнена с помощью пакета прикладных программ Statistica 6.0 (StatSoft, США). При проведении статистической обработки данных и интерпретации полученных результатов учитывались современные международные требования к представлению результатов статистического анализа в статьях и диссертациях на соискание ученой степени [24].
Результаты исследования
Характеристика пациентов с СГБ
В общую выборку было включено 145 пациентов с СГБ: 71 мужчина и 74 женщины (49 и 51% соответственно). Возраст на момент начала заболевания варьировал от 12 до 79 лет, медиана дебюта симптомов приходилась на 46 [33; 58] лет. Распределение пациентов с СГБ по степени тяжести в остром периоде представлено на рисунке 1. По результатам ЭНМГ ОВДП диагностирована в 116 (80%) случаях, ОМАН и ОМСАН – в 17 (12%) и 12 (8%) случаях соответственно.
Искусственная вентиляция легких проводилась 30 (21%) пациентам, медиана длительности респираторной поддержки составила 22 [14; 48] дня. Сроки начала искусственной вентиляции легких приходились на седьмые [5-е; 12-е] сутки. Бульбарные расстройства наблюдались у 52 (36%) пациентов, 30 (21%) больных были обеспечены зондовым питанием, сроки начала которого приходились на восьмой [5-й; 12-й] день с продолжительностью 26 [13; 53] суток.
В остром периоде заболевания всем пациентам проводилась патогенетическая терапия: плазмаферез (n = 138, 78%) или введение внутривенного иммуноглобулина (n = 13, 7%). Сроки начала лечения приходились на десятые [6-е; 15-е] сутки.
На фоне лечения у 76% больных наблюдался регресс неврологической симптоматики (терапия считалась эффективной), у 15% – состояние стабилизировалось (недостаточная эффективность терапии), у 9% – продолжал нарастать неврологический дефицит несмотря на проводимую терапию (неэффективная терапия).
Эффективность патогенетической терапии
Для выявления факторов, которые могут повлиять на успех патогенетического лечения, были оценены группы пациентов, у которых терапия была признана эффективной (n = 110) и недостаточно эффективной (n = 35). В обеих группах различия по объему проведенной терапии, времени ее начала, возрасту и полу больных не были достоверными (p > 0,05). Разница обнаружилась между формами СГБ (p < 0,05). Среди больных с хорошим эффектом терапии 97 (88%) человек перенесли ОВДП и только 13 (12%) пациентов – аксональные формы СГБ. Недостаточный эффект наблюдался у 19 (51%) больных с ОВДП и у 16 (49%) больных с аксональными формами СГБ. Кроме того, обнаружены достоверные различия в ближайшем восстановительном периоде (p < 0,05): медиана срока наступления стадии III по САШ после лечения у тяжелых пациентов составляла в случае эффективности терапии 36 [23; 56] суток, а в случае недостаточной эффективности терапии – 131 [71; 215] день.
В то же время стоит отметить исходно более тяжелое состояние пациентов в группе с недостаточной эффективностью терапии (p < 0,05). В искусственной вентиляции легких (стадия V по САШ) нуждались 14 (40%) пациентов, 16 (46%) больных были обездвижены, остальные пять (14%) человек перенесли СГБ средней и легкой степени тяжести. При этом среди больных, показавших хороший ответ на лечение, стадия V по САШ отмечалась только у 16 (15%) человек, стадия VI –
у 57 (52%) больных, а средняя и легкая степень СГБ наблюдалась в 37 (33%) случаях.
Оценки по шкале NIS тоже были различными (p < 0,05): при недостаточном эффекте терапии медиана составляла 131 [114; 156] балл, в случае эффективности – 104 [78; 129] балла. По шкале MRC-SS медиана суммарного балла у больных с недостаточной эффективностью лечения была равна 24 [16; 34], у пациентов с хорошим действием терапии – 46 [30; 56]. Поскольку состояние больных в остром периоде оказалось достоверно разным, сравнение групп по шкалам в позднем восстановительном периоде не проводилось.
Оценка результатов лечения у пациентов, получивших патогенетическую терапию в редуцированном и полном объеме
Все пациенты были разделены на две группы по объему проведенного патогенетического лечения: полный объем получили 108 (74%) человек, редуцированный –
37 (26%). Достоверной разницы при сравнении двух групп по возрасту, полу, времени начала лечения и формам СГБ обнаружено не было.
При сравнении неврологического статуса оказалось, что независимо от объема патогенетической терапии состояние пациентов обеих групп после лечения достоверно улучшилось по всем приведенным выше шкалам, то есть предварительно оба варианта лечения были эффективны (табл. 1). Однако в ходе более детального анализа этих двух групп оказалось, что неврологический статус в остром периоде достоверно различался (p < 0,05): пациенты, получившие редуцированный объем терапии, до лечения имели меньшую степень неврологического дефицита, то есть их состояние было исходно легче. Неврологический статус сразу после лечения в сравниваемых группах оказался примерно одинаковым. Следовательно, больший объем патогенетической терапии оказал большее влияние и способствовал восстановлению более тяжелых пациентов до уровня менее тяжелых. Иными словами, проведение патогенетической терапии в полном объеме уменьшает тяжесть состояния больных в остром периоде (рис. 2).
Сравнение двух групп в отдаленном периоде не обнаружило достоверных различий по всем оцениваемым шкалам. В частности, оценка по шкале САШ показала, что через полгода среди пациентов, получивших редуцированный объем терапии, 16% передвигались с поддержкой (стадия III), остальные 84% могли ходить самостоятельно (стадия 0–II), четверть из них к этому сроку восстановились полностью. Среди пациентов, прошедших полный объем лечения, 11% были обездвижены (стадия IV), 21% передвигались с поддержкой, а остальные 68% могли ходить самостоятельно, причем полностью восстановилось 20% пациентов (р = 0,408). Медиана оценки по шкале MRC-SS у больных, получивших лечение в редуцированном объеме, составила 74 [64; 80] балла, у пациентов, пролеченных полностью, – 72 [63; 79] балла (p > 0,05).
Через год в группе пациентов, получивших редуцированный объем терапии, все больные могли ходить, полностью восстановились 68% из них. Среди пациентов, пролеченных в полном объеме, к этому сроку 4% оставались еще обездвиженными, 8% пациентов передвигались с поддержкой, большинство (88%) могли ходить самостоятельно, полное восстановление наблюдалось в половине случаев (53%) (р = 0,136). По шкале MRC-SS состояние больных, получивших редуцированный объем лечения, оценивалось на 80 [76; 80] баллов – так же, как и в группе пациентов, получивших полный объем терапии (80 [80; 80]).
Таким образом, патогенетическая терапия, проведенная как в редуцированном, так и в полном объеме, в остром периоде СГБ (первые две недели от начала заболевания) улучшает состояние больных. В позднем восстановительном периоде (через шесть и 12 месяцев от начала заболевания) состояние пациентов, получивших разный объем терапии, как по выраженности неврологического дефицита, так и по степени инвалидизации достоверно не отличается.
При этом больший объем терапии, вероятно, обладает более высокой эффективностью, что отражается в равноценной выраженности неврологической симптоматики после курса лечения как у исходно более тяжелых и получивших полный объем лечения больных, так и у исходно более легких пациентов, получивших редуцированный объем. Этот факт заслуживает особого внимания, поскольку именно у пациентов, находящихся в тяжелом состоянии, достоверно более значимое улучшение в остром периоде имеет жизненно важное значение.
Известно, что демиелинизирующие и аксональные формы СГБ существенно отличаются по тяжести протекания, в частности при ОМАН/ОМСАН в два раза чаще развивается дыхательная недостаточность, а продолжительность искусственной вентиляции легких в шесть раз дольше, чем при ОВДП [25]. Это послужило поводом для оценки эффективности полного и редуцированного объема лечения в зависимости от формы СГБ.
Сравнение результатов лечения у пациентов с ОВДП в зависимости от полученного объема терапии
В группе ОВДП полный объем терапии получили 85 (73%) человек, редуцированный объем – 31 (27%). Как редуцированный, так и полный объемы терапии в данном случае эффективны и достоверно улучшают неврологический статус пациентов по всем оцениваемым шкалам. Однако оказалось, что у пациентов с ОВДП, получивших полный объем лечения, наблюдалось достоверно более глубокое поражение по сравнению с пациентами, которым был проведен редуцированный курс терапии. В этой связи было принято решение о сравнении эффективности лечения в зависимости от объема только у тяжелых больных с ОВДП.
Среди пациентов с тяжелым и крайне тяжелым течением ОВДП редуцированный объем терапии получили 17 (22%) пациентов, полный – 61 (78%). Результаты сравнения в этих двух группах оказались более информативными: больные, получившие полноценное лечение, имели достоверно больший регресс неврологической симптоматики, что подтверждалось улучшением по всем шкалам (табл. 2). Среди пациентов, получивших редуцированный объем терапии, тоже определялось улучшение по шкалам NIS, MRC, R-ODS и индексу Бартел, но по шкалам INCAT и САШ, отражающим инвалидизацию, прогресса не отмечалось, что имеет важное социальное значение. Можно считать, что тяжелые пациенты с ОВДП, получившие недостаточный объем патогенетической терапии, показывают некоторое улучшение состояния, но не настолько выраженное, чтобы это повлияло на их способность к ходьбе и самообслуживанию, в то время как улучшение после полноценного лечения наблюдается и в этой сфере.
Сравнивалась также динамика восстановления тяжелых пациентов с ОВДП после разного объема патогенетического лечения. У больных, получивших редуцированный объем терапии, регресс неврологического дефицита до стадии III по САШ произошел в среднем на 33-и [25-е; 53-и] сутки болезни, у получивших полный объем терапии – на 43-й [24-й; 68-й] день, но показанная разница не оказалась статистически значимой.
Отдаленные результаты лечения также не показали достоверной разницы по шкалам САШ, INCAT, MRC, R-ODS и индексу Бартел. Так, через полгода в группе пациентов, получивших редуцированный объем терапии, 15% больных (n = 2) передвигались с поддержкой, остальные 85% (n = 11) ходили самостоятельно, из них полное восстановление наблюдалось в 15% случаев (n = 2). Среди больных с ОВДП, получивших полный объем терапии, в поддержке при движении нуждалась четверть пациентов (26%), остальные ходили самостоятельно (74%), из них 15% больных к этому моменту восстановились полностью.
Через год в группе больных, получивших редуцированный объем лечения, все пациенты могли передвигаться самостоятельно и более половины (58%) восстановились полностью. Среди тех, кто был пролечен в полном объеме, к этому сроку только один (2%) человек передвигался с поддержкой, остальные ходили самостоятельно, и также половина из них (51%) восстановилась полностью.
Таким образом, среди пациентов с тяжелыми формами ОВДП наблюдалось достоверно лучшее восстановление в остром периоде при проведении полного объема терапии, хотя на отдаленные результаты лечения это не повлияло.
Сравнение результатов лечения у пациентов с аксональными формами СГБ в зависимости от полученного объема терапии
Среди пациентов с ОМАН/ОМСАН полный объем терапии получили 23 (80%) человека, редуцированный объем – шесть (20%) больных. Тем не менее несмотря на малую выборку было выполнено сравнение неврологического статуса до и после лечения (табл. 3).
Оказалось, что у пациентов с ОМАН/ОМСАН, получивших полный объем терапии, наблюдалось достоверное уменьшение неврологического дефицита по шкалам NIS и MRC, хотя по шкалам INCAT, САШ и индексу Бартел прогресс не отмечался. Между тем у больных, получивших редуцированный объем лечения, вообще не было зарегистрировано достоверного улучшения ни по одной из шкал.
Оценка эффективности проведенной терапии не показала статистически значимых отличий между двумя группами. Среди пациентов, получавших терапию в редуцированном объеме, в половине случаев наблюдался недостаточный эффект лечения – стабилизация состояния без регресса (n = 3, 50%), остальные продемонстрировали хороший эффект с регрессом неврологической симптоматики на фоне терапии. Среди больных, пролеченных полноценным курсом, у трех (13%) эффект лечения отсутствовал (ухудшился неврологический статус на фоне терапии), у 13 (44%) больных наблюдалась стабилизация состояния и у 10 (43%) был отмечен хороший эффект с регрессом неврологической симптоматики.
Интересно, что период восстановления до стадии III по САШ (прохождение 5 м с поддержкой) у пациентов, получивших редуцированный объем лечения, длился до 45 [18; 82] дней, а у больных, пролеченных полным курсом терапии, – до 183 [80; 246] суток, разница достоверна. Другими словами, несмотря на то что, вероятно, ввиду малого количества человек сравнение неврологического статуса данных больных в остром периоде не обнаружило достоверных различий между двумя группами, состояние пациентов, получивших достаточный объем терапии, было гораздо тяжелее, чем состояние пациентов, пролеченных редуцированным курсом. Тем не менее отдаленные результаты лечения через полгода и год не обнаружили достоверных различий между двумя группами.
Так, через полгода 40% больных с ОМАН/ОМСАН, получивших редуцированный объем терапии, передвигались с поддержкой, остальные 60% могли ходить самостоятельно, но еще не восстановились полностью. Среди пациентов, получивших полный объем лечения, 46% были обездвижены, 27% нуждались в поддержке при движении, остальные 27% ходили самостоятельно, один из них полностью восстановился к этому сроку.
Через год все пациенты, получившие редуцированный объем лечения, ходили самостоятельно, один из них полностью выздоровел. Среди больных, получивших полный курс терапии, 18% оставались обездвиженными, 27% передвигались с поддержкой, остальные 56% могли ходить самостоятельно, причем шесть (27%) человек полностью восстановились.
Такие различия в группах, где не было обнаружено достоверной разницы, могут быть объяснены слишком маленьким размером выборки (шесть человек в группе с редуцированным объемом терапии), которая тем не менее вписывается в большую группу по своим статистическим параметрам.
Таким образом, в остром периоде полноценно проведенная патогенетическая терапия при аксональных формах СГБ достоверно ускоряет темп восстановления, но значимо не влияет на степень инвалидизации больных. Как и при ОВДП, отдаленные результаты при ОМАН/ОМСАН существенно не зависят от объема лечения.
Обсуждение результатов
В настоящем исследовании был получен большой объем статистических данных, касающихся клинической картины, течения и исходов СГБ в российской популяции. Стоит отметить: статистические показатели, полученные при описании выборки пациентов в данном исследовании, в подавляющем большинстве случаев соответствуют подобным данным зарубежных авторов [5, 7, 9, 13, 17].
В процессе анализа эффективности патогенетической терапии было выявлено, что больные с ОМАН/ОМСАН более чем в половине случаев (66%) демонстрируют недостаточный ответ на лечение. Кроме того, среди пациентов с недостаточной эффективностью патогенетического лечения оказалось в 2,5 раза больше нуждающихся в искусственной вентиляции легких: 40% в сравнении с 15% больных, на которых терапия произвела ожидаемый эффект. Эти результаты соответствуют многим иностранным источникам, которые относят аксональные формы СГБ и проведение искусственной вентиляции легких к неблагоприятным прогностическим признакам для исхода болезни [8–10, 26, 27]. Возраст старше 60 лет также расценивается в качестве неблагоприятного фактора выздоровления. Однако в настоящем исследовании в данной возрастной категории не было обнаружено подобных различий по результатам терапии (эффективная и недостаточно эффективная).
Сравнение показало хорошие результаты лечения в обеих группах, о чем свидетельствует достоверное улучшение неврологического статуса независимо от объема проведенной терапии. Тем не менее состояние больных, получивших полноценное лечение, изначально было более тяжелым, но после лечения сравнялось с состоянием пациентов, получивших редуцированный объем, исходный неврологический статус которых оценивался как менее тяжелый. На этом основании можно предположить, что полноценное лечение все-таки более эффективно в остром и раннем восстановительном периодах. В то же время сравнение больных этих групп в отдаленном восстановительном периоде не показало достоверных различий в неврологическом статусе, что указывает на отсутствие влияния объема патогенетической терапии на темпы восстановления двигательных функций, инвалидизацию и остаточные явления в позднем периоде СГБ.
Считается, что аксональные формы СГБ отличаются более тяжелым течением по сравнению с демиелинизирующими и имеют менее благоприятный прогноз [8, 10, 25, 27–31]. Нами была оценена эффективность патогенетической терапии в редуцированном и полном объемах в этих двух группах отдельно.
Анализ результатов лечения пациентов с ОВДП показал, что у больных с тяжелым и крайне тяжелым течением заболевания терапия редуцированным объемом не приводит к достоверному улучшению в неврологическом статусе по шкалам INCAT и САШ, тогда как полноценное лечение дает достоверное улучшение по всем оцениваемым шкалам. Это свидетельствует о меньшей эффективности лечения в редуцированном объеме у тяжелых пациентов, поскольку в этом случае достоверные изменения отмечаются только при оценке по более точным шкалам NIS и MRC, которые рассматривают поражение отдельных групп мышц, тогда как результаты по шкалам, оценивающим инвалидизацию и тяжесть течения, остаются на прежнем уровне. Однако поздний восстановительный период у пациентов с благоприятной формой СГБ протекал одинаково, демонстрируя достаточно быстрый регресс неврологического дефицита у основной массы больных.
Сравнение эффективности полного и редуцированного объема лечения у пациентов с аксональными формами показало, что улучшение неврологического статуса больных на фоне полноценной терапии регистрировалось только по шкалам NIS и MRC, тогда как достоверных изменений по шкалам INCAT, САШ и индексу Бартел отмечено не было. Это имеет важное социальное значение, поскольку большинство этих больных нуждаются в ежедневном уходе и помощи. Однако улучшения состояния пациентов, получивших лечение в редуцированном объеме, ни по одной из шкал не отмечалось. Сравнение отдаленных результатов терапии у этих больных не только через полгода, но и через год не показало статистически достоверных различий, как и в случае с тяжелыми формами ОВДП.
Таким образом, при тяжелых и крайне тяжелых формах ОВДП, а также при ОМАН/ОМСАН проведение полного объема патогенетической терапии имеет достоверно большую эффективность и определяет степень инвалидизации в остром периоде, хотя и не влияет на темп восстановления и остаточный дефицит. Следует подчеркнуть значимость как можно более скорого прерывания острого периода СГБ с выходом на плато и дальнейшим регрессом. Особенно это важно для больных с тяжелым и крайне тяжелым течением, поскольку эта фаза заболевания грозит широким спектром осложнений, связанных с пребыванием на искусственной вентиляции легких и глубоким тетрапарезом (сердечно-сосудистые и дыхательные осложнения, главным образом тромбозы, тромбоэмболии, гипостатические и вентилятор-ассоциированные пневмонии, сепсис).
По данным литературы, риск неблагоприятного прогноза и смерти при СГБ зависит от продолжительности периода обездвиженности, проведения искусственной вентиляции легких, а также возраста пациента [32–37]. Именно поэтому мы рекомендуем неукоснительно придерживаться рекомендаций по лечению СГБ, проводя пациентам с тяжелым течением СГБ или аксональными формами заболевания полноценную терапию. Это позволит минимизировать риск неблагоприятного исхода или смерти. Поскольку оснащенность российских лечебно-профилактических учреждений в большинстве случаев не позволяет проводить высокообъемный плазмаферез [6], целесообразно выделить особую группу пациентов, обязательно нуждающихся в полноценном патогенетическом лечении в остром периоде СГБ. В нее следует включить всех пациентов с тяжелым и крайне тяжелым течением СГБ, а также больных с ОМАН/ОМСАН.
При этом нельзя забывать, что на ранних сроках СГБ определение формы с помощью ЭНМГ по нейрофизиологическим критериям R. Hadden бывает затруднительным или ошибочным. По данным А. Uncini и соавт. [26], оценка результатов ЭНМГ-исследования в динамике в 13% случаев позволяет изменить первоначально установленную форму ОВДП на ОМСАН, а также уточнить формы в «неопределенной» группе. В этой связи необходимо выполнить повторное ЭНМГ-исследование у больных с СГБ для оценки эффективности проводимой терапии, контроля состояния пациента, а также возможного уточнения первоначально установленной формы заболевания с последующей коррекцией лечения.
Таким образом, патогенетическая терапия в полном объеме необходима во всех случаях СГБ, когда нет возможности точно установить форму заболевания (недоступность ЭНМГ, попадание пациента в «неопределенную» группу по нейрофизиологическим критериям по результатам первичного исследования). Строго обязательно проведение полноценного лечения, если у больного наблюдается СГБ тяжелого течения с развитием глубокого тетрапареза или дыхательной недостаточности или при установлении аксональной формы. Следовательно, пациентам с ОВДП легкой и средней степени тяжести возможно, хотя и крайне нежелательно, проводить редуцированный курс патогенетической терапии.
Заключение
В ходе настоящего исследования при сравнении терапии СГБ была показана сходная эффективность патогенетического лечения в полном (изъято плазмы в объеме 120 мл/кг массы тела пациента за курс лечения) и редуцированном (менее 120 мл/кг) объемах. При более детальном рассмотрении этого аспекта оказалось, что у пациентов с тяжелым и крайне тяжелым течением формы ОВДП, а также у больных с аксональными формами СГБ регресс неврологического дефицита в остром периоде при лечении редуцированным курсом достоверно меньше по сравнению с пациентами, получившими полноценную терапию. В этой связи следует рекомендовать обязательное проведение полноценного курса патогенетического лечения всем больным с тяжелым течением СГБ, а также пациентам с аксональными формами. Кроме того, в полном курсе терапии нуждаются больные, которым по каким-либо причинам не была установлена форма СГБ. Такой дифференцированный подход позволит проводить патогенетическую терапию пациентам с СГБ в оптимальном режиме, с учетом тяжести их состояния и оснащенности лечебно-профилактических учреждений конкретного региона.
