Профилактическая эффективность аллергенспецифической иммунотерапии
- Аннотация
- Статья
- Ссылки
- English
Введение
Аллергические заболевания признаны одними из самых распространенных в мире. Согласно официальной статистике, в настоящее время около 30% взрослого и 50% детского населения земного шара имеют различные формы проявления аллергии [1]. Рост заболеваемости аллергией отмечается повсеместно по всем нозологическим формам. Наиболее распространенными считаются аллергический ринит (АР) и бронхиальная астма (БА) [2].
Современные фармакологические противоаллергические препараты для лечения АР и БА лишены тяжелых побочных эффектов и в большинстве случаев позволяют контролировать состояние пациентов. Тем не менее ни один препарат симптоматической терапии не способен изменить характер реагирования организма на причинно-значимый аллерген и повлиять на течение заболевания. Аллергенспецифическая иммунотерапия (АСИТ) имеет принципиальные преимущества перед другими методами лечения аллергии, поскольку ее действие заключается не в устранении симптомов заболевания, а в изменении характера реагирования организма на аллерген. АСИТ вмешивается в собственно патогенез заболевания и воздействует на все патогенетические звенья аллергической реакции [3].
АСИТ является одним из основных методов патогенетического лечения аллергических заболеваний, связанных с IgE-опосредованным механизмом аллергии, и предполагает введение в организм пациента возрастающих доз аллергена, ответственного за клинические симптомы заболевания.
Эффективность АСИТ выражается в уменьшении или полном отсутствии клинических симптомов при естественной экспозиции аллергена. После проведения АСИТ снижается продолжительность обострений и потребность в препаратах базисной и симптоматической терапии. АСИТ позволяет предупредить трансформацию АР в БА, расширение спектра аллергенов, к которым формируется повышенная чувствительность пациента. АСИТ действует как на раннюю, так и на позднюю фазу аллергического ответа, способствует не только торможению аллергенспецифической реакции, но и угнетению тканевой гиперреактивности, проявляющейся повышением чувствительности к медиатору аллергии – гистамину [4]. Наконец, еще одно преимущество АСИТ заключается в модифицирующем и профилактическом эффектах, а также пролонгированном действии по окончании лечения.
Сказанное обусловливает уникальность и перспективность применения АСИТ.
Метод АСИТ имеет более чем 100-летнюю историю, широко применяется во всем мире. В России он используется с 1960-х гг. На данном этапе развития практической аллергологии АСИТ стала стандартным способом лечения АР и атопической БА. Трудно переоценить роль АСИТ в профилактике респираторной аллергии. Сегодня клиническая ценность АСИТ общепризнана. Активно изучаются режимы проведения АСИТ, анализируется роль скорости увеличения дозы и длительность лечения. Подкожный способ введения аллергенов рассматривается как классический метод специфического лечения. Сублингвальная АСИТ (СЛИТ – сублингвальная иммунотерапия) получила широкое распространение во многих странах, в том числе в нашей, вследствие чего возрос интерес к АСИТ в целом. Эффективность и безопасность АСИТ подтверждены результатами многочисленных крупномасштабных двойных слепых плацебоконтролируемых рандомизированных исследований [5–7].
Лечебные аллергены, применяемые при АСИТ
Всемирная организация здравоохранения рекомендует использовать в клинической практике только стандартизированные аллергены [8]:
- водно-солевые экстракты (ВСЭ) аллергенов пыльцы деревьев, злаковых и сорных трав, домашней пыли, клещей рода Dermatophagoides (для подкожной АСИТ (ПКИТ – подкожная иммунотерапия));
- аллергоиды, полученные путем полимеризации аллергена формальдегидом или карбамелированием;
- аллергены, адсорбированные на суспензии фосфата кальция или гидроокиси алюминия (для ПКИТ);
- аллергены для сублингвального применения [4].
На сегодняшний день в России зарегистрированы и разрешены к широкому медицинскому использованию:
- ВСЭ аллергенов пыльцы деревьев, злаковых и сорных трав, домашней пыли, клещей рода Dermatophagoides;
- аллергоиды (полученные путем полимеризации аллергена формальдегидом) из домашней пыли, пыльцы деревьев, злаковых и сорных трав;
- Фосталь – аллерген из пыльцы деревьев, адсорбированный на суспензии фосфата кальция (компания Stallergenes, Франция);
- Алюсталь – аллерген клещей домашней пыли, адсорбированный на суспензии гидроксида алюминия (компания Stallergenes, Франция);
- Алюсталь – аллерген пыльцы луговых трав, адсорбированный на суспензии гидроксида алюминия (компания Stallergenes, Франция);
- аллергены с 50%-ным содержанием глицерина для сублингвального применения: весенняя смесь ранняя (аллергены пыльцы деревьев), смесь трав I (аллергены пыльцы луговых трав), осенняя смесь пыльцевая (аллергены пыльцы сорных трав) и смесь плесеней наружных (грибковые аллергены) (компания SEVAPHARMA a.s., Чехия);
- Сталораль – аллергены для сублингвального применения смеси клещей домашней пыли (компания Stallergenes, Франция);
- Сталораль – аллергены для сублингвального применения пыльцы березы (компания Stallergenes, Франция);
- Оралейр – таблетки для сублингвального применения аллергенов смеси пыльцы пяти луговых (злаковых) трав (компания Stallergenes, Франция);
- Лайс грасс – таблетки для сублингвального применения аллергенов смеси пыльцы трех злаковых трав и смеси клещей домашней пыли (компания Lofarma, Италия) [8, 9].
Методы проведения АСИТ
Существуют инъекционные (подкожные – аллерген вводится подкожно в область плеча) и неинъекционные (в основном сублингвальные – аллерген рассасывается в подъязычной области) методы АСИТ. Протоколы/схемы АСИТ не являются универсальными. Для каждого метода и препарата они свои. Различия в схемах обусловлены химическими и терапевтическими свойствами препаратов.
Клинически значимый аллерген из числа тех, к которым у больного наблюдается повышенная чувствительность, устанавливают аллергологи на основании данных аллергологического анамнеза, кожных проб, провокационных назальных и конъюнктивальных тестов. Для АСИТ отбирают аллергены, элиминация которых невозможна (пыльца растений, клещи домашней пыли, споры грибов, яд насекомых) и которые несомненно провоцируют симптомы аллергического заболевания у конкретного пациента [4].
АСИТ проводят в два этапа. Первый этап – достижение максимальной терапевтической дозы, второй – проведение поддерживающей терапии.
АСИТ может быть предсезонной, предсезонно-сезонной и круглогодичной.
В настоящее время в России применяются шесть методов АСИТ.
- Классический парентеральный метод ПКИТ с использованием отечественных ВСЭ аллергенов или аллергоидов. На первом этапе метод предусматривает введение 25–30 инъекций аллергена один или два раза в неделю.
- Ускоренный парентеральный метод с применением отечественных ВСЭ аллергенов. На первом этапе предполагается введение 25–30 инъекций аллергена по одной – три инъекции в день (с учетом индивидуальной переносимости). Данный метод проводится в стационарных условиях.
- Инъекционная АСИТ препаратами Фосталь и Алюсталь компании Stallergenes. На первом этапе терапии предполагается введение 13–17 инъекций аллергена один раз в неделю, на втором – введение поддерживающей дозы аллергена один раз в месяц или реже (интервал между инъекциями не должен превышать шесть недель). Современные лечебные аллергены (Фосталь и Алюсталь) благодаря высокой степени очистки и стандартизации позволяют увеличить интервалы между инъекциями (до шести недель) и обеспечить продолжение этапа поддерживающей иммунотерапии, несмотря на начало сезона пыления причинно-значимых аллергенов, то есть позволяют непрерывно проводить АСИТ в течение трех – пяти лет.
- СЛИТ аллергенами производства компании SEVAPHARMA a.s. проводится пациентам с повышенной чувствительностью к аллергенам клещей домашней пыли, пыльцы деревьев, злаковых (луговых) и сорных трав. При данном виде АСИТ пациент по определенной схеме самостоятельно принимает аллерген. Предусмотрены контрольные визиты к лечащему врачу. Кратность назначения препарата корректируется в зависимости от степени переносимости и состояния здоровья пациента.
- СЛИТ препаратами аллергенов Сталораль (аллерген клещей домашней пыли и аллерген пыльцы березы) производства компании Stallergenes проводится по схеме при ежедневном наращивании дозы от одного нажатия на дозатор из флакона с концентрацией 10 ИР/мл до восьми нажатий из флакона с концентрацией 300 ИР/мл и занимает 11 дней. На этапе поддержания дозы препарат вводится в концентрации 300 ИР/мл. Рекомендованная схема приема: четыре – восемь нажатий в день. Эффективность АСИТ напрямую зависит от суммарной дозы аллергена, полученной за период лечения, что обусловливает использование максимально допустимой, хорошо переносимой суточной дозы и соблюдение рекомендованной длительности курса поддерживающей терапии [8]. В случае лечения препаратом аллергенов пыльцы березы АСИТ проводится за два – четыре месяца до начала сезона поллинации, в течение всего периода пыления вплоть до его окончания, затем делается перерыв в терапии до следующего года (предсезонно-сезонная АСИТ). При лечении препаратом аллергенов клещей домашней пыли АСИТ проводится круглогодично.
- СЛИТ препаратом Оралейр (экстракт аллергенов из смеси пыльцы трав ежи сборной, колоска душистого, плевела многолетнего (райграса), мятлика лугового, тимофеевки луговой) производства компании Stallergenes начинают за четыре месяца до начала сезона пыления причинно-значимых аллергенов. Рекомендованная схема: первый день терапии – одна таблетка в дозе 100 ИР, второй день – две таблетки в дозе 100 ИР (суммарно 200 ИР), третий день – одна таблетка в дозе 300 ИР, далее по одной таблетке в дозе 300 ИР ежедневно до окончания сезона поллинации. Затем делают перерыв в терапии до следующего года (предсезонно-сезонная АСИТ).
Риск развития побочных реакций во время проведения ПКИТ, самой тяжелой из которых является анафилактический шок, необходимость частых визитов в клинику могут снижать приверженность пациентов этому виду лечения. СЛИТ характеризуется высоким профилем безопасности, сопоставимым с таковым ПКИТ, и большей приверженностью пациентов лечению. Дозы аллергена, получаемые пациентами в процессе СЛИТ, более чем в 100 раз превышают суммарные дозы при ПКИТ [3].
Механизмы АСИТ
Классические и распространенные проявления аллергии, которые подлежат купированию на фоне АСИТ, представлены заболеваниями, связанными с образованием в организме аллергических антител, принадлежащих иммуноглобулину (Ig) класса Е. Развитие IgE-опосредованных аллергических заболеваний в значительной мере обусловлено снижением контроля регуляторными Т-клетками (CD4+CD25+FOXP3 Treg, Tr1, Th3) гиперактивации иммунной системы [10]. Под влиянием АСИТ отмечается усиление регуляторной функции Tr1, Th3, CD4+CD25+Treg, которое выражается в повышении продукции интерлейкина (ИЛ) 10, трансформирующего фактора роста бета, уменьшении пролиферации аллергенспецифических Т-лимфоцитов, супрессии IgE-ответа, формировании аллергенспецифической толерантности. При проведении АСИТ под воздействием интенсивной антигенной стимуляции происходит перестройка иммунного ответа на новый тип, характеризующийся увеличением продукции интерферона гамма и ИЛ-10 Т-клетками, повышением содержания CD4+CD25+FOXP3+Т-клеток, числа клеток, продуцирующих ИЛ-12, что свидетельствует о переключении Th2-цитокинового профиля на Th1-профиль [11]. Под влиянием АСИТ наблюдается усиление экспрессии рецепторов для ИЛ-2, что способствует уменьшению дисбаланса Th1/Th2-лимфоцитов. Положительный результат АСИТ сопровождается увеличением продукции IgG-антител, повышением уровня IgG и IgA в секретах, супрессией повышения уровня специфических IgE-антител, сменяющейся при длительной АСИТ снижением их продукции, уменьшением количества медиаторов, высвобождаемых тучными клетками и базофилами при экспозиции с причинно-значимыми аллергенами, восстановлением баланса между Т-хелперами и Т-супрессорами [12]. Положительный результат АСИТ приводит к увеличению аллергенспецифических IgG1- и IgG4-антител в сыворотке крови, антител, которые могут индуцировать иммунологическую толерантность, предотвращая активацию базофилов и тучных клеток, за счет конкуренции со специфическими IgE за связь с аллергеном. Альтернативный механизм ингибиторной активности IgG1- и IgG4-антител заключается также в конкурентной связи с аллергеном, приводящей к подавлению IgE-обусловленной презентации аллергена В-клетками аллергенспецифическим Т-клеткам. Таким образом снижаются Т-клеточная активация, пролиферация и продукция Th2-цитокинов [13].
Очевидно, что ПКИТ и СЛИТ имеют общие механизмы действия в отношении переключения Тh-клеточного ответа и индукции блокирующих IgG-антител. Однако слизистая оболочка ротовой полости является особым местом в отношении индукции толерантности и имеет общий лимфатический дренаж со слизистой оболочкой носа и шейными лимфатическими узлами, что скорее всего обусловливает дополнительные локальные механизмы СЛИТ [14]. Слизистая оболочка полости рта относится к сложной сети иммунной системы слизистых оболочек, которая обеспечивает индукцию толерантности к различным антигенам из синантропных бактерий и питательных продуктов для поддержания локального иммунного баланса. Слизистая оболочка ротовой полости демонстрирует отличное заживление ран без развития серьезных рубцов и острого воспаления, несмотря на высокую бактериальную колонизацию. В отношении СЛИТ толерогенный потенциал слизистой оболочки ротовой полости выражается в отсутствии воспалительных клеток в ткани слизистой оболочки рта после приема аллергена сенсибилизированными пациентами. Кроме того, слизистая оболочка ротовой полости высокопроницаема для аллергенов, которые сохраняются в ткани ротовой полости до 20 часов [15].
Профилактическая эффективность АСИТ
Эпидемиологические исследования последовательно и убедительно демонстрируют прочные связи между ринитом и астмой. Клинические и фундаментальные научные исследования последних лет свидетельствуют, что эти два заболевания имеют общие анатомические, физиологические, иммунопатологические и терапевтические факторы [16]. Важность проблемы аллергического ринита обусловлена высокой распространенностью заболевания, существенным влиянием на качество жизни пациентов, профессиональную деятельность и способность к обучению, а также его тесной связью с БА. Среди других возможных осложнений встречаются отит среднего уха из-за обструкции евстахиевой трубы и гипертрофия аденоидной и тонзиллярной ткани из-за хронического воспаления. Подобные осложнения могут сопровождаться снижением аппетита, отставанием в росте, обструктивным апноэ во время сна, повышенной утомляемостью и перепадами настроения. Аллергический ринит и сопутствующие коморбидные состояния способны негативно влиять на качество жизни, а также на успеваемость в школе. У многих пациентов с АР отмечается повышенная бронхиальная гиперреактивность. Особенно высокий риск развития астмы имеют пациенты с тяжелыми, персистирующими симптомами ринита и синусита. В целом, как показывают результаты исследований, у пациентов с АР риск заболеть астмой в три раза выше, чем у здоровых лиц. Как правило, ринит предшествует формированию астмы (у 32–49% больных) [16].
Из-за значительного ущерба от астмы и вызываемых ею неблагоприятных воздействий на качество жизни и стоимость лечения первостепенное значение имеет профилактика БА у пациентов с АР. Взаимосвязь АР и БА определяет подходы к лечению, диктуя необходимость единой системной терапии. Наиболее полно этому принципу отвечает АСИТ – метод лечения, специфичный не для конкретной нозологии (ринит, астма или атопический дерматит), а для клинических проявлений/заболеваний, вызванных определенным аллергеном или аллергенами [17].
АСИТ эффективнее на раннем этапе болезни, предупреждает трансформацию АР в БА и расширение спектра сенсибилизации. Эффект АСИТ достигается в полной мере после повторных (трех – пяти) курсов лечения.
Клинические исследования в педиатрической популяции подтвердили иммуномодулирующий эффект АСИТ, который сохраняется по окончании лечения и способен предотвращать прогрессирование заболевания. Это особенно важно в отношении профилактики развития БА у пациентов с АР.
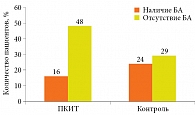
Данные одного из наиболее известных и часто цитируемых исследований показали профилактический эффект АСИТ через десять лет (спустя семь лет после окончания АСИТ) у детей и подростков с сезонным аллергическим риноконъюнктивитом (рис. 1) [18].
147 пациентов в возрасте 16–25 лет с АР, обусловленным аллергией к пыльце березы и трав, были обследованы спустя десять лет после начала трехлетнего курса ПКИТ: в группе ПКИТ у 16 (25%) пациентов отмечалось развитие БА, в контрольной группе, не получавшей ПКИТ, таких пациентов насчитывалось 24 (45%). Авторы пришли к выводу о профилактическом влиянии АСИТ на развитие БА у детей и подростков с сезонным аллергическим риноконъюнктивитом.
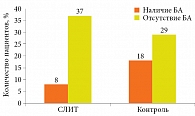
Аналогичный профилактический эффект в отношении БА был продемонстрирован на фоне СЛИТ в трехлетнем открытом исследовании с участием 113 детей в возрасте от пяти до 14 лет, страдавших аллергическим риноконъюнктивитом, обусловленным аллергией к пыльце злаковых трав. Согласно полученным данным, БА развивалась в 3,8 раза чаще в контрольной группе пациентов, не получавших СЛИТ (рис. 2) [19].
Доказано, что проведение ПКИТ уменьшает вероятность появления новой сенсибилизации у взрослых и детей [9].
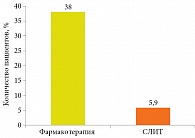
M. Marogna и соавт. (2004) изучали влияние СЛИТ на развитие сенсибилизации к новым аллергенам у 511 больных АР с интермиттирующей БА или без таковой. 319 пациентов в течение трех лет получали СЛИТ, 192 – только медикаментозную терапию. По окончании исследования было установлено, что за истекший период сенсибилизация к новым аллергенам появилась у 38% пациентов из группы симптоматической терапии и лишь у 5,9% из группы СЛИТ (p < 0,001) (рис. 3) [20].
В отличие от фармакотерапии АСИТ характеризуется пролонгированным эффектом, который продолжается по ее завершении.
В проспективном исследовании M. Marogna и соавт. [21] оценивали длительность клинического эффекта трех-, четырех- и пятилетней СЛИТ у пациентов с аллергией к клещу. У пациентов, получавших трехлетний курс СЛИТ, клинический эффект отмечался на протяжении семи лет, а у тех, кто получал четырех- и пятилетние курсы СЛИТ, длительность клинического эффекта составила восемь лет. Сенсибилизация к новым аллергенам на протяжении 15 лет наблюдалась у всех пациентов контрольной группы, не получавших СЛИТ, и менее чем у четверти пациентов, получавших ее. Авторы пришли к заключению о целесообразности четырехлетнего курса СЛИТ, который обеспечивает продолжительный клинический эффект после лечения.
Важность своевременного назначения АСИТ подтвердили результаты исследования PETRA, проведенного M. Iberoa и соавт. [22]. Исследователи проанализировали результаты диагностики и лечения детей в возрасте от пяти до 17 лет с аллергическим ринитом в Испании. Оценивалось назначенное лечение (симптоматическими препаратами или АСИТ), а также причины и последствия не проведенной вовремя АСИТ.
Анализировались данные пациентов детского возраста с аллергическим ринитом, которые обращались к специалистам по респираторным заболеваниям в Испании. Кроме того, собиралась информация о демографических характеристиках, течении заболевания (длительности, тяжести согласно классификации ARIA (Allergic Rhinitis and its Impact on Asthma – Аллергический ринит и его влияние на астму), диагностических процедурах), мнения врачей о лечении. Исследование носило наблюдательный характер и не влияло на предписание лечения практикующими клиническими специалистами.
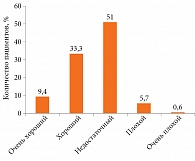
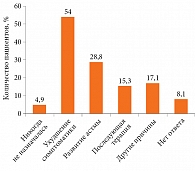
В исследование были включены 260 детей (мальчиков – 56%), средний возраст – 11,7 года. У 61,9% пациентов имела место аллергия на клещей, у 38,1% – аллергия на пыльцу трав. Среднее время от момента появления первых симптомов составило четыре года. В 85% случаев облегчение симптомов не наблюдалось с момента постановки диагноза. Согласно классификации ARIA у 180/260 (69,4%) пациентов отмечалась средняя тяжесть заболевания. Астма диагностирована у 89/161 (55%) пациентов с аллергией на клещей и у 44/99 (45%) пациентов с аллергией на пыльцу трав. Наиболее частыми терапевтическими мерами были предупреждение контакта с аллергенами (96,5%), симптоматическое лечение (98,5%) и информирование пациентов о заболевании (94,2%). Контроль заболевания при симптоматическом лечении ретроспективно оценивался как недостаточный, плохой или очень плохой у 57,3% пациентов (рис. 4).
Аллергенспецифическая иммунотерапия назначалась 56,9% пациентов. Когда исследователей спрашивали, почему они не назначали специфическую иммунотерапию определенным пациентам, 2/3 из них отвечали, что предпочли выжидательную тактику и решили наблюдать за течением болезни (54% назначили бы иммунотерапию, если бы симптоматика заболевания ухудшилась, и 28,8% – если бы у пациента развилась астма) (рис. 5).
Таким образом, в данном обсервационном исследовании у пациентов детского возраста с аллергическим ринитом, которые наблюдались у специалистов, отмечался преимущественно АР среднетяжелого течения. БА была частым сопутствующим заболеванием (у 55% пациентов с аллергией на клещей и у 45% пациентов с аллергией на пыльцу трав). У многих пациентов симптоматика заболевания или не улучшалась, или ухудшалась. Более чем у половины больных симптоматическое лечение не дало результатов. АСИТ своевременно не назначалась в связи с тем, что многие специалисты предпочли выжидательную тактику и наблюдали за течением заболевания. Несвоевременное назначение АСИТ привело к усилению симптомов АР и последующей трансформации АР в БА.
Совсем недавно были опубликованы результаты крупного немецкого ретроспективного когортного исследования, в котором оценивали влияние АСИТ на предупреждение развития астмы у пациентов с аллергическим ринитом [23].
Участниками исследования стали 118 754 пациента (средний возраст – 37 лет, женщин – 58%) с аллергическим ринитом, без астмы, которые не получали АСИТ в 2005 г. Больные были разделены на две группы. 2431 (2,0%) пациент первой группы начал получать АСИТ в 2006 г. Пациентам второй группы АСИТ в 2006 г. не проводили. У 1307 (54,5%) больных, получавших АСИТ, продолжительность лечения составила менее трех лет, а у 1091 (45,5%) пациента – три года и более. Обе группы наблюдались относительно риска возникновения астмы в 2007–2012 гг.
Как показали результаты исследования, риск развития БА у пациентов, получавших АСИТ, был значительно ниже (относительный риск 0,60; 95%-ный доверительный интервал 0,42–0,84; p = 0,003), чем у пациентов, не получавших АСИТ. Причем самые значимые результаты имели место в группе, получавшей АСИТ в течение трех лет и более.
Результаты крупного немецкого ретроспективного когортного исследования лишний раз подтверждают, что АСИТ – единственный способ лечения, позволяющий изменить естественный ход заболевания и предотвратить развитие БА у пациентов с АР в реальных клинических условиях.
Таким образом, своевременно проведенная эффективная АСИТ предупреждает переход более легких форм БА в более тяжелые и трансформацию АР в БА. Благодаря АСИТ уменьшается потребность в симптоматических препаратах. В отличие от существующих методов лечения аллергических заболеваний АСИТ характеризуется пролонгированным положительным эффектом (в течение нескольких лет). Чем в более раннем возрасте и на более ранних стадиях заболевания проведена АСИТ, тем выше лечебное действие. Наилучший клинический эффект достигается по завершении повторных (трех – пяти) курсов терапии.
Заключение
Аллергенспецифическая иммунотерапия имеет принципиальные преимущества перед другими методами лечения аллергических заболеваний, поскольку является единственным методом лечения, способным изменить естественную эволюцию аллергического заболевания, предотвратить возникновение новых сенсибилизаций и сократить риск возникновения астмы. АСИТ эффективнее на ранних стадиях заболевания. АСИТ оказывает значительный профилактический эффект. Лечебное действие АСИТ достигается в полной мере после повторных (трех – пяти) курсов лечения. Благодаря длительному и долговременному эффекту АСИТ считается терапией, способной остановить дальнейшее развитие аллергии и прогрессирование заболевания. Наличие в арсенале российских аллергологов разных препаратов для проведения АСИТ позволяет выбирать удобные и приемлемые для конкретного пациента схемы терапии.
Ye.P. Terekhova
Russian Medical Academy of Postgraduate Education
Contact person: Yekaterina Petrovna Terekhova, e.p._terekhova57@mail.ru
Allergenspecific immunotherapy (ASIT) is currently the only treatment that can change the natural evolution of allergic respiratory disease. The article describes the advantages of ASIT in front of all other methods of allergy treatment. Characteristics of therapeutic forms of allergens on the Russian market, the methods and mechanisms of ASIT. Presented clinical trials and systematic reviews that confirm the effectiveness of preventive ASIT.
