Роль иринотекана в современной химиотерапии злокачественных опухолей
- Аннотация
- Статья
- Ссылки




Результатом этих изысканий стал препарат СРТ-11 или иринотекан, представляющий собой полусинтетический растворимый дериват камптотецина, быстро гидролизующийся in vivo в активный метаболит SN-38. Этому метаболиту отводится главная роль в противоопухолевой активности камптотецина, в частности экспериментальные данные свидетельствуют о 100-1000-кратной активности SN-38 по сравнению с камптотецином (3). Механизм действия иринотекана связан с ингибированием фермента топоизомеразы-I. Топоизомераза-I представляет собой ядерный фермент с молекулярной массой 100 kDa; кодирующий ген находится в 20-ой хромосоме (4). Фермент играет ключевую роль в жизнедеятельности эукариотической клетки, а его активность связана с третичной структурой ДНК. В процессе нормальной жизнедеятельности клетки топоизомераза-I образует временный комплекс с одной из нитей ДНК, обеспечивая ее разрыв и раскручивание, необходимые в период репликации. Затем этот комплекс распадается, а разобщенные нити ДНК воссоединяются. Таким образом, ингибирование фермента топоизомеразы-I блокирует процессы репликации и транскрипции.
Иринотекан на предклинических исследованиях продемонстрировал эффективность на ряде традиционных мышиных асцитных и солидных опухолевых штаммах: лейкозе L-1210, панкреатической аденокарциноме, аденокарциноме молочной железы, саркоме Крокер, гепатоме NH-134, раке легкого Льюиса, раке толстой кишки С-38, причем эффект торможения в ряде случаев превосходил таковой при использовании цисплатина и других алкилирующих агентов. Была обнаружена также необычная активность иринотекана в отношении трансплантированных человеческих опухолей толстой кишки и шейки матки, рака легкого, рабдомиосарком, опухолей мозга, нейробластом. Препарат оказался эффективным в отношении ксенографтных линий клеток, резистентных к винбластину, доксорубицину, мелфалану, а в отношении клеточных линий колоректального рака был эффективнее топотекана, в том числе в двух случаях опухолевых трансплантатов, резистентных к иринотекану (5). Во время экспериментальных исследований было показано, что иринотекан способен in vitro и in vivo подавлять рост опухолей с высокой экспрессией гена множественной лекарственной устойчивости. Эти штаммы и линии клеток отличаются низкой чувствительностью к антрациклинам, подофиллотоксинам и таксанам. Иринотекан оказался активным в отношении мышиной культуры клеток опухолей молочной железы, желудка, легкого и толстой кишки (6).
Рассмотрим результаты клинического применения иринотекана при лечении различных форм злокачественных опухолей.
Иринотекан в лечении распространенного колоректального рака
В мире ежегодно колоректальным раком заболевает 1-1,2 млн. человек. У 60-70% пациентов из них в дальнейшем развиваются метастазы. Еще 15% больных при установке первичного диагноза имеют метастазы. В химиотерапии колоректального рака в последние годы сделаны большие успехи, связанные с применением в клинической практике новых высокоэффективных противоопухолевых препаратов – иринотекана, оксалиплатина, ралтитрексида, капецитабина. Иринотекан является одним из основных препаратов для лечения больных диссеминированным колоректальным раком, о чем свидетельствуют результаты проведенных клинических исследований. В Греческом рандомизированном исследовании комбинации оксалиплатин+5-фторурацил струйно и иринотекан+5-фторурацил струйно продемонстрировали равную эффективность в качестве первой линии химиотерапии при лечении 295 больных (7). Частота объективных эффектов составила 33% и 32%, медиана времени до прогрессирования – 8,9 и 7,6 мес. (р=0,5) и общей продолжительности жизни – 17,6 и 17,4 мес. соответственно.
В исследовании Saltz L.B. (10), больные метастатическим колоректальным раком, ранее не получавшие химиотерапию, получали либо 5-фторурацил и лейковорин, либо 5-фторурацил и лейковорин в сочетании с иринотеканом. Исследование, проведенное в Северной Америке, использовало струйное введение 5-фторурацила с лейковорином (1 исследование), тогда как в Европе назначали инфузии 5-фторурацила с лейковорином (2 исследование). Основными критериями были частота объективного ответа, время до прогрессирования, общая выживаемость и качество жизни. В Американском исследовании объективный ответ составил в группе с иринотеканом, 5-FU и лейковорином 29%, в группе с 5-фторурацилом и лейковорином – 21%, медиана времени до прогрессирования составила 7,0 и 4,3 месяца соответственно. В Европейском исследовании частота объективного ответа составила 35 и 22%, медиана времени до прогрессирования составила 6,7 и 4,4 месяца соответственно. В обоих исследованиях добавление иринотекана достоверно увеличило общую продолжительность жизни (в Американском исследовании – с 12, 6 до 14,6 месяца, в Европейском – с 14,1 до 17,6 месяцев). Если объединить данные двух исследований, то добавление иринотекана увеличило продолжительность жизни с 13,3 до 15,9 месяцев. В Американском исследовании добавление иринотекана уменьшило риск прогрессирования заболевания на 36% и риск смерти от опухолевой прогрессии на 20%, в Европейском исследовании – на 46% и 23% соответственно.
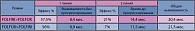
Особое значение имеют результаты исследования Tournigand C. (11), задачей которого было определить оптимальную последовательность назначения режимов иринотекан+5ФУ/Лв (FOLFIRI) и оксалиплатин + 5ФУ/Лв (FOLFOX) у нелеченных больных.
Оба режима показали приблизительно одинаковую частоту эффективности и общей выживаемости.
В другом исследовании капецитабин был использован с иринотеканом (СарIri: иринотекан 80 мг/м2 в 1, 8 дни и капецитабин 1000 мг/м2 2 раза в день внутрь 1-14 дни) и оксалиплатином (СapOx: капецитабин также, оксалиплатин 70 мг/м2 в 1, 8 дни) каждые 3 недели (8). Вновь эффективность изученных комбинаций при лечении 161 больного была одинаковой: частота объективных эффектов – 38% и 49%, медиана времени до прогрессирования – 8,2 и 6,6 мес., общей продолжительности жизни – 15,8 и 15,8 мес. для CapIri и CapOx соответственно. Эти исследования еще раз демонстрируют равную эффективность комбинаций на основе оксалиплатина и иринотекана, если второй компонент комбинации 5-фторурацил вводится в одинаковом режиме. Без сомнения, что иринотекан улучшает результаты инфузионного введения 5-фторурацила при проведении первой линии химиотерапии у больных диссеминированным колоректальным раком. Об этом еще раз свидетельствуют результаты исследования EORTC, в котором больные получали лейковорин 500 мг/м2 в течение 2 часов и 5-фторурацил 2000 мг/м2 в течение 24 часов еженедельно 6 недель отдельно или в комбинации с иринотеканом в дозе 80 мг/м2 (9). Медиана времени до прогрессирования при лечении 430 больных составила 6,3 и 8,8 мес. (р=0,0001) и общей продолжительности жизни – 16,8 и 20,1 мес. соответственно. Добавление иринотекана увеличило частоту диареи, но не сказалось существенным образом на другие проявления токсичности.
Большой интерес вызывают комбинации иринотекана с таргетными препаратами. На съезде ASCO (2003) были представлены результаты рандомизированного исследования, проведенного у 800 больных колоректальным раком, в котором одна группа получала химиотерапию комбинацией IFL (иринотекан 125 мг/м2, лейковорин 20 мг/м2 и 5-фторурацил 500 мг/м2 еженедельно 4 недели с повторением курса через 2 недели) или IFL и бевацизумаб 5 мг/кг каждые 2 недели (12). Добавление бевацизумаба привело к достоверному улучшению непосредственных и отдаленных результатов терапии (таблица 2).
Таким образом, достоверное увеличение продолжительности жизни, показанное в этом исследовании, является предпосылкой дальнейшего изучения комбинации иринотекана с бевацизумабом в лечении этих больных.
В еще одном международном рандомизированном исследовании (13) 329 больных с колоректальным раком и прогрессированием заболевания в течение 3 месяцев после химиотерапии с включением иринотекана (иринотекан-резистентные больные) получали либо моноклональные антитела к рецептору эпидермального фактора роста С225 (цетуксимаб) в дозе 400 мг/м2, затем 250 мг/м2 еженедельно до признаков прогрессирования или токсичности, либо С225 и иринотекан в тех же дозах и режиме введения, после которых было отмечено прогрессирование заболевания. Обязательным условием включения в исследование было наличие на мембране опухолевых клеток рецепторов эпидермального фактора роста. Больные, которые получали С225 только в случае прогрессирования заболевания, могли получать комбинацию С225 и иринотекана. Результаты исследования представлены в таблице 3.
Исследование убедительно продемонстрировало, что С225 обладает самостоятельной противоопухолевой активностью у этой прогностически неблагоприятной группы больных. Однако более интересным представляются данные о том, что совместное назначение С225 и иринотекана повышает чувствительность опухолевых клеток к последнему, несмотря на имеющуюся клиническую резистентность к препарату. Это приводит к достижению объективного противоопухолевого эффекта у 22% больных и медиане продолжительности жизни 8,6 мес. Эти результаты следует расценивать необычно высокими у данной группы больных. Степень экспрессии рецептора эпидермального фактора роста не коррелировала с эффективностью проводимой терапии. Было отмечено, что больные, у которых отмечено развитие кожной токсичности (сыпь) демонстрировали достоверно лучшие результаты лечения.
Иринотекан также является одним из основных препаратов для проведения второй линии химиотерапии у больных, ранее получавших 5-фторурацил или комбинацию 5-фторурацила и оксалиплатина. Авторы рандомизированного исследования поставили вопрос, как долго следует проводить терапию иринотеканом у больных с прогрессированием после лечения 5-фторурацилом (14). 333 больных получали иринотекан в дозе 350 мг/м2 в виде инфузии в течение 30 минут каждые 3 недели 8 курсов. После окончания 8 курсов больные были рандомизированы на две группы: первая прекращала терапию, а вторая продолжала получать иринотекан до признаков прогрессирования или токсичности. Из 333 больных прогрессирование процесса при проведении 8 курсов отмечено у 220. Из 113 больных с объективным эффектом или прогрессированием только 55 согласились принять участие во второй фазе исследования (25 больных продолжали принимать иринотекан и 30 больных прекратили лечение). Не отмечено объективных эффектов у больных, продолжавших введение иринотекана. Одногодичная выживаемость составила 46% в группе с продолжением введения иринотекана и 55% – в группе прекратившей лечение. Не отмечено существенной токсичности и разницы в качестве жизни больных прекративших и продолжающих лечение на 12 неделе после рандомизации. Таким образом, для большинства больных достаточно 8 курсов химиотерапии иринотеканом и продолжение лечения не приводит к улучшению результатов лечения.
Иринотекан в лечении распространенного рака поджелудочной железы
Комбинация гемцитабина с иринотеканом, при которой больные получали либо гемцитабин в 1000 мг/м2 еженедельно 7 недель, после 2-недельного перерыва в 1, 8 и 15 дни каждые 4 недели, либо гемцитабин в дозе 1000 мг/м2 и через 30 минут иринотекан в дозе 100 мг/м2 в 1 и 8 дни каждые 3 недели (15) увеличила непосредственную эффективность терапии (частота объективных эффектов составила 16% и 4%), но не улучшила отдаленные результаты (медиана времени до прогрессирования составила 2,9 и 2,7 месяца, общей выживаемости – 6,3 и 6,6 мес., 1-годичная выживаемость – 21% и 22% соответственно для комбинации и только гемцитабина).
Другие интересные результаты были получены при использовании комбинации FOLFIRINOX (оксалиплатин 80 мг/м2 1 день, иринотекан 180 мг/м2 1 день, лейковорин 400 мг/м2 1 день с последующим введением 5-фторурацила 400 мг/м2 струйно, а затем 2400 мг/м2 в виде 46-часовой инфузии каждые 2 недели), ранее продемонстрировавшую высокую эффективность при лечении больных колоректальным раком (16). Лечение получили 46 больных, частота объективного эффекта составила 22% (1 полная и 9 частичных регрессий), медиана времени до прогрессирования – 5,9 мес., общей выживаемости – 9,6 мес., одногодичная выживаемость – 39%. Это существенно лучше непосредственных и отдаленных результатов химиотерапии гемцитабином. Токсичность комбинации была умеренной и ее основными проявлениями были нейтропения 3-4 степени (18%), диарея (3%), периферическая нейропатия (3%). Авторы считают целесообразным продолжить изучение данной комбинации в рандомизированном исследовании у больных распространенным раком поджелудочной железы, сравнив ее с результатами лечения одним гемцитабином.
Иринотекан в лечении диссеминированного рака желудка
Как известно, основными комбинациями для лекарственного лечения диссеминированного рака желудка являются комбинации PF (цисплатин и 5-фторурацил), ELF (этопозид, лейковорин и 5-фторурацил) или ECF (эпидоксорубицин, цисплатин и 5-фторурацил), DCF (доцетаксел, цисплатин, 5-фторурацил). Не отмечено преимуществ какой-либо из вышеперечисленных комбинаций. Частота объективного эффекта при их применении составляет 30-40%, а медиана продолжительности жизни – 8-9 месяцев. Все это лишний раз подчеркивало актуальность поиска новых препаратов и комбинаций на их основе для лечения больных метастатическим раком желудка.
Иринотекан один из наиболее интересных препаратов, эффективность которого изучается у больных распространенным раком желудка. В исследовании II фазы сравнили эффективность трех комбинаций в первой линии у больных метастатическим раком желудка: комбинация LF (лейковорин 200 мг/м2, 5-фторурацил 400 мг/м2 струйно и затем инфузия в течение 2 суток в суточной дозе 600 мг/м2), LFP (тот же режим лейковорина и 5-фторурацила + цисплатин 50 мг/м2 в 1 и 2 дни) и LFI (то же + иринотекан 180 мг/м2 1 день) каждые 2 недели (17). Результаты исследования представлены в таблице 4.
Очевидно, что комбинация LF недостаточно эффективна у больных раком желудка и не может быть рекомендована для использования в качестве химиотерапии первой линии. Добавление цисплатина или иринотекана приводит к существенному повышению эффективности терапии при одновременном повышение токсичности терапии. Комбинация LFI продемонстрировала высокую частоту объективного эффекта (40%), увеличение медиан времени до прогрессирования (6,7 месяца) и общей продолжительности жизни (11,3 месяца). Серьезной проблемой при ее назначении остается диарея 3-4 степени, частота которой составила 22%.
В другом рандомизированном исследовании сравнивались комбинация IF (иринотекан 80 мг/м² 30-минутная инфузия, лейковорин 500 мг/м² 2-часовая инфузия, 5-фторурацил 2000 мг/м² 22-часовая инфузия, еженедельно, 6 недель) и режим цисплатин + 5-фторурацил (PF) (26). 332 больных раком желудка и пищеводно-желудочного перехода приняли участие в исследовании. Основной задачей исследования было зафиксировать увеличение времени до прогрессирования. Комбинация с иринотеканом продемонстрировала более высокую частоту объективного ответа, чем режим PF – 32% и 25%. Однако время до прогрессирования достоверно улучшить не удалось – 5 мес. и 4,2 мес (р = 0,088) соответственно. Как и следовало ожидать, в группе IF диарея наблюдалась чаще (22% и 7%). Полученные результаты свидетельствуют о возможности «безболезненной» замены цисплатина на иринотекан у больных, не подходящих по ряду причин (общее состояние, поражение почек) для терапии цисплатином.
Не менее интересным представляются результаты совместного использования иринотекана и доцетаксела (DI: доцетаксел 60 мг/м2 и иринотекан 250 мг/м2 1 день каждые 3 недели). Эта комбинация была сравнена с комбинацией доцетаксела и 5-фторурацила (DF: доцетаксел 85 мг/м2 1 день и инфузия 5-фторурацила в суточной дозе 750 мг/м2 5 суток каждые 3 недели) в качестве химиотерапии первой линии у больных метастатическим раком желудка (18). В исследование было включено 85 больных (рандомизированное исследование II фазы). Результаты исследования представлены в таблице 5.
Иринотекан в лечении немелкоклеточного рака легкого (нмрл)
В исследовании Vassilis G. больным после ранее проведенной химиотерапии таксанами и гемцитабином назначали либо цисплатин в дозе 80 мг/м2 каждые 3 недели, либо цисплатин 80 мг/м2 1 день и иринотекан 110 мг/м2 в 1, 8 дни каждые 3 недели (19). При использовании комбинации с иринотеканом частота объективных эффектов составила 24% по сравнению с 8% при назначении только цисплатина. Это, однако, не привело к увеличению продолжительности времени до прогрессирования (2,5 и 2 мес. соответственно) и продолжительности жизни (9 мес. в обеих группах). Назначение комбинации увеличило частоту нейтропении и диареи и не увеличило эффективность лечения при проведении химиотерапии второй линии у больных НМРЛ.
Японские исследователи попытались улучшить результаты лечения НМРЛ за счет использования в качестве первой линии химиотерапии трехкомпонентной комбинации: цисплатин 60 мг/м2, доцетаксел 60 мг/м2 1 день и иринотекан 60 мг/м2 2 день каждые 3 недели (20). Лечение получили 49 больных, при этом частота объективного эффекта составила 57%, медиана общей продолжительности жизни – 16,3 месяца и одногодичная выживаемость – 62%.
Иринотекан в лечении больных злокачественными опухолями гениталий
Рак шейки матки
При использовании иринотекана в режиме 100 и 150 мг/м2 с интервалом 2 недели у больных раком шейки матки частота противоопухолевых эффектов составила 24%, при этом у больных, получавших ранее лучевую терапию, эффективность лечения была примерно такой же (27%) (21, 22).
Изучается эффективность комбинаций, включающих иринотекан, в частности с производными платины. Так, при использовании иринотекана в дозе 60 мг/м2 в 1, 8 и 15 дни и цисплатина в дозе 60 мг/м2 в 1 день один раз в месяц удалось достичь объективных эффектов, в т.ч. 2 полных регрессии, у 36% больных (23).
Рак яичников
Эффективность иринотекана при раке яичников колеблется в пределах 21-23% (24). Сравнительно высокая эффективность монотерапии иринотеканом при раке яичников стимулировала изучение этого препарата в комбинациях с другими цитостатиками. При использовании иринотекана (120 мг/м2) в комбинации с митомицином С (7 мг/м2) в 1и 15 дни у больных светлоклеточной и муцинозной аденокарциномой яичников, резистентной к производным платины, у половины больных были получены объективные эффекты, среднее время до прогрессирования составило 15,3 (3,5-46,2) мес. (25).
Заключение
Таким образом, результаты проведенных исследований убедительно свидетельствуют о важнейшей роли иринотекана в химиотерапии больных колоректальным раком и в ряде случаев других опухолей. В последние годы в клиническую практику входит новый препарат иринотекана – Ирнокам компании Dr. Reddy’s, который в настоящее время успешно испытывается в отделении клинической фармакологии и химиотерапии РОНЦ им. Н.Н. Блохина РАМН в качестве 2 линии химиотерапии при диссеминированном раке желудка в комбинации с митомицином С, подтверждая ожидаемую клиническую эффективность.
