Возможности метода жидкостной цитологии в диагностике рецидивов злокачественных опухолей яичников
- Аннотация
- Статья
- Ссылки
- English
Ретроспективно проанализированы основные факторы, определяющие сроки возникновения рецидивов, у 839 больных раком яичников I–III стадий после комбинированного лечения за период 2010–2012 гг.
При изучении экссудатов и смывов брюшной полости у 33 больных раком яичников наряду с традиционным цитологическим исследованием применяли метод жидкостной цитологии с использованием питательной среды 199. Проведена оценка эффективности сравниваемых методов цитологической диагностики.
Согласно полученным результатам, точность метода жидкостной цитологии превышает таковую традиционного цитологического исследования в 1,5 раза (р < 0,05). При этом качество неудовлетворительных цитологических препаратов снижается на 23,7%.
Ретроспективно проанализированы основные факторы, определяющие сроки возникновения рецидивов, у 839 больных раком яичников I–III стадий после комбинированного лечения за период 2010–2012 гг.
При изучении экссудатов и смывов брюшной полости у 33 больных раком яичников наряду с традиционным цитологическим исследованием применяли метод жидкостной цитологии с использованием питательной среды 199. Проведена оценка эффективности сравниваемых методов цитологической диагностики.
Согласно полученным результатам, точность метода жидкостной цитологии превышает таковую традиционного цитологического исследования в 1,5 раза (р < 0,05). При этом качество неудовлетворительных цитологических препаратов снижается на 23,7%.

У большинства первично пролеченных пациенток со злокачественными опухолями яичников по окончании специального лечения диагностируются рецидивы заболевания, особенно в первые два года наблюдения [1, 2].
Согласно данным литературы [1, 3–6], рецидивы рака яичников возникают практически у каждой пятой больной с клинически установленной ранней стадией заболевания. Это свидетельствует о высокой частоте клинических ошибок при стадировании опухолевого процесса, а также в случае его агрессивного характера – о низкой эффективности лечения и т.д.
Проблема снижения числа рецидивов рака яичников, разработка и совершенствование методов их своевременной морфологической диагностики в целях повышения качества, а следовательно, увеличения продолжительности жизни больных со злокачественными новообразованиями яичников остается крайне актуальной.
Цель исследования – изучить частоту и сроки возникновения рецидивов рака яичников после проведенного лечения и оценить эффективность использования метода жидкостной цитологии в диагностике рецидивов данного заболевания.
Материал и методы исследования
Ретроспективно изучены данные 839 больных раком яичников I–III стадий, проходивших обследование и лечение в Краснодарском клиническом онкологическом диспансере № 1 министерства здравоохранения Краснодарского края с 2010 по 2012 г. Изучены частота и сроки возникновения рецидивов в течение трех лет.
Больные были разделены на группы в зависимости от стадии первичной опухоли и подгруппы – в зависимости от методов специального лечения. Всем пациенткам были выполнены хирургическое вмешательство в объеме экстирпации матки с придатками, удаление большого сальника, хирургическое стадирование опухолевого процесса. Диагноз злокачественных опухолей яичников морфологически подтвержден у всех больных. Стадирование заболевания проводилось в строгом соответствии с Международной классификацией злокачественных опухолей по системе TNM (Tumor, Nodus, Metastasis) (2009 г., 7-е издание), рубрика С56 и FIGO (International Federation of Gynecology and Obstetrics – Международная федерация акушерства и гинекологии). В каждой группе анализировались частота и сроки возникновения рецидивов в течение трех лет.
С целью улучшения цитологической диагностики абдоминальных рецидивов рака яичников в 2015–2016 гг. в онкологическом диспансере № 3 (г. Новороссийск) было обследовано 33 больных раком яичников после комбинированного лечения с использованием цитологического метода (жидкостная цитология и традиционное исследование).
При выявлении лучевыми методами (ультразвуковое исследование (УЗИ), рентгеновская компьютерная томография, магнитно-резонансная томография) асцитической жидкости больным выполняли лапароцентез. При отсутствии выпота в брюшной полости или незначительном его количестве проводилась пункция заднего свода влагалища для получения экссудата или смыва для цитологического исследования. Полученный материал разделяли на две порции. Одну исследовали традиционным цитологическим методом, другую – методом жидкостной цитологии. После отстаивания биологической жидкости в течение 20–30 минут 10 мл ее придонного слоя, обогащенного клеточными элементами, переносили в пять-шесть центрифужных пробирок и центрифугировали десять минут при скорости 2000 об/мин (центрифуга Элекон ЦЛМН-Р10-01). Надосадочную жидкость сливали, из клеточного осадка готовили препарат для традиционного цитологического исследования.
При выполнении жидкостной цитологии к клеточному осадку в объеме 100–400 мкл добавляли 4 мл питательной среды 199. Клеточную суспензию цитофугировали в CytoFuge 2 (Stat Spin, США) при скорости 1000 об/мин в течение восьми минут. Полученные монослойные препараты высушивали на воздухе. Фиксацию препарата проводили с помощью раствора по Май-Грюнвальду, окрашивание – по Романовскому – Гимзе или гематоксилин-эозином (фиксация 95%-ным этиловым спиртом) автоматизированным методом на универсальном настольном роботе Shandon Varistain Geminis ES (Англия), обеспечивающем быстрое и одновременное окрашивание большого количества цитологических препаратов. При микроскопировании цитологических препаратов использовали видеомикроскоп MC (LCD) с встроенной электронной системой, жидкокристаллическим сенсорным дисплеем, позволяющим просматривать изображения в режиме реального времени. Результаты микроскопирования фотографировались и сохранялись на CD Cart, что позволяло формировать архив микропрепаратов.
На завершающем этапе исследования на основании полученных результатов осуществлялась сравнительная оценка эффективности метода жидкостной цитологии и традиционного цитологического исследования.
Результаты исследования и их обсуждение
Возраст пациенток со злокачественными опухолями яичников колебался от 31 года до 78 лет (средний возраст 57,1 ± 0,3 года).
В первую группу вошли 179 (21,3%) больных с ранней стадией заболевания (стадия I по FIGO). Вторую группу составили 660 (78,7%) пациенток с распространенными формами опухолевого процесса (стадии II и III по FIGO).
Больных с I стадией заболевания разделили на две подгруппы. С учетом благоприятного клинического прогноза заболевания (гистологическая структура опухоли, поражение одного яичника без поражения капсулы опухоли) 38 (21,2%) пациенток первой подгруппы получали только хирургическое лечение. В этой подгруппе гистологическая структура злокачественных новообразований яичников была следующей: серозная высокодифференцированная аденокарцинома без прорастания капсулы – 32 (84,2%) случая, эпителиальные пограничные опухоли (папиллярная цистоаденома) – 6 (15,8%) случаев. Вторую подгруппу составили 141 (78,8%) больных. Всем больным этой подгруппы было проведено комбинированное лечение, включавшее выполнение на первом этапе оптимальной циторедуктивной операции. На втором этапе лечения проведена полихимиотерапия с обязательным включением препаратов платины (шесть курсов). Гистологическая структура опухолей яичников в данной подгруппе была следующей: серозные злокачественные опухоли (аденокарцинома, папиллярная аденокарцинома и папиллярная цистоаденокарцинома) – 98 (69,7%) случаев, муцинозная аденокарцинома – 26 (18,5%), эндометриоидная аденокарцинома – 13 (9,4%), злокачественная опухоль Бриннера – 4 (4,4%) случая.
660 пациенткам второй группы с распространенным опухолевым процессом (стадии II и III) было проведено комбинированное лечение, включавшее операцию и полихимиотерапию (6–8 курсов) с использованием препаратов платины.
Первую подгруппу составили 607 (92,0%) больных, которым на первом этапе лечения была выполнена циторедуктивная операция, на втором – полихимиотерапия.
Вторую подгруппу составили 53 (8,0%) пациентки с распространенным раком яичников. Комбинированное лечение этих больных начиналось с неоадъювантной химиотерапии (три-четыре курса) с целью уменьшения размера опухолевых масс, снижения операционной кровопотери, травматичности и продолжительности операции. Затем выполнялась циторедуктивная операция. В послеоперационном периоде проведены 3–6 курсов полихимиотерапии на основе препаратов платины, а в четырех случаях к схеме полихимиотерапии добавлен таргетный препарат блокатор ангиогенеза – бевацизумаб.
Гистологическая структура опухолей у пациенток второй группы была следующей: серозные злокачественные опухоли (аденокарцинома, папиллярная аденокарцинома и папиллярная цистоаденокарцинома) – 478 (72,4%) случаев, муцинозная аденокарцинома – 103 (15,6%), эндометриоидная аденокарцинома – 56 (8,5%), светлоклеточная аденокарцинома – 13 (2,0%), злокачественная опухоль Бриннера – 10 (1,5%) случаев.
Анализ полноты проведения процедуры хирургического стадирования опухолевого процесса в группе больных с I стадией заболевания показал, что стандарт этой процедуры не выполнен в полном объеме в 57 (31,8%) случаях.
В течение трех лет после окончания специального лечения диагностировано 34 рецидива у пациенток первой группы с ранней стадией заболевания и 193 рецидива – у пациенток второй группы с распространенными формами злокачественных опухолей яичников. Общая частота рецидивов рака яичников на первом году наблюдения у больных с I стадией заболевания была выше, чем среди больных с II–III стадиями (76,5 и 68,4% соответственно). Это свидетельствует об ошибках, допускаемых врачами во время проведения хирургического стадирования.
Исходя из приведенного выше анализа, учитывая высокую частоту рецидивирования рака яичников после лечения и имея собственный опыт применения метода жидкостной цитологии в диагностике рака и предраковой патологии шейки матки с использованием питательной среды 199, повышающего диагностическую точность цитологического метода исследования в 1,8 раза [7], а также в диагностике рака мочевого пузыря, улучшающей диагностику в 1,3 раза [8] по сравнению с традиционным цитологическим методом, мы предприняли попытку повышения точности цитологической диагностики рака яичников и его рецидивов с помощью метода жидкостной цитологии. В исследование были включены 33 больные раком яичников после комбинированного лечения с подозрением на рецидив заболевания. Материалом для цитологического исследования служила асцитическая жидкость, полученная у десяти пациенток при проведении лапароцентеза под контролем УЗИ. При отсутствии выпота в брюшной полости или его незначительном количестве были получены экссудат или смыв брюшной полости при выполнении пункции заднего свода влагалища у 23 больных раком яичников, находившихся на диспансерном наблюдении по окончании лечения.
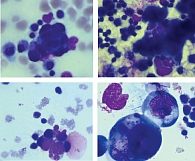
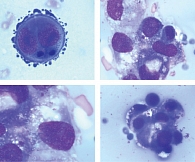
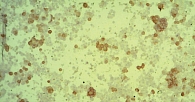
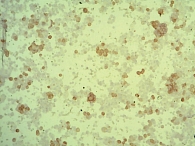
При сравнении препаратов, полученных традиционным методом и методом жидкостной цитологии, установлено следующее. При традиционном методе исследования осадок после центрифугирования образца распределяется тонким слоем по большой площади предметного стекла, при использовании цитофугирования клеточные элементы концентрируются в центре препарата в виде монослоя в пределах круга диаметром 7 мм.
Микроскопическая картина цитологических препаратов, полученных традиционным способом и методом жидкостной цитологии, представлена на рис. 1 и 2 соответственно.
В результате проведенного исследования выявлена существенная разница в диагностике рецидивов рака яичников при использовании сравниваемых методов (таблица).
Из 33 больных, находившихся на диспансерном наблюдении после проведенного лечения по поводу рака яичников, рецидив заболевания традиционным методом диагностирован у 17 (53,1%), методом жидкостной цитологии – у 21 (63,6%).
Необходимо отметить, что при исследовании смывов брюшной полости цитологическая диагностика рецидивов рака яичников методом жидкостной цитологии была выше, чем при классическом цитологическом исследовании. Это обусловлено тем, что клеточный состав экссудата или смыва брюшной полости очень скудный и клетки подвергаются частичному лизису, а метод жидкостной цитологии способствует концентрации клеток на ограниченном участке предметного стекла, что значительно улучшает результаты цитологической диагностики.
В результате применения метода жидкостной цитологии количество неудовлетворительных микроскопических препаратов снизилось на 23,7%.
Рассмотрим на клиническом примере использование метода жидкостной цитологии в диагностике рецидива рака яичников.
Клиническое наблюдение
Больная Х., 24 года, наблюдается в ГБУЗ «Онкологический диспансер № 3» (г. Новороссийск) с июля 2016 г. по поводу рака яичников.
16 октября 2014 г. была выполнена лапароскопическая операция по поводу апоплексии левого яичника.
20 мая 2015 г. в ходе УЗИ органов малого таза обнаружены кистозное образование левого яичника – 5 × 4,5 см с пристеночным компонентом, в брюшной полости – незначительное количество асцитической жидкости.
30 июня 2016 г. выполнена лапаротомия. Сальпингоофорэктомия слева. Гистологическая структура опухоли – серозная карцинома высокой степени злокачественности. От предложенного оперативного лечения и химиотерапии больная отказалась.
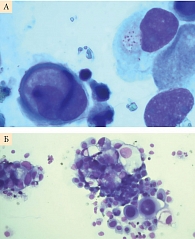
В июле 2016 г. у пациентки появилась одышка, которая усиливалась после незначительной физической нагрузки. СА 125 – 254,2 Ед/мл. 2 августа 2016 г. выполнена рентгенография органов грудной клетки. В плевральной полости справа – выпот до VI ребра. Установлен предварительный диагноз рецидива рака яичников. 3 августа 2016 г. выполнена плевральная пункция. Эвакуировано 650 мл серозного экссудата. Из клеточного осадка приготовлены морфологические препараты традиционным способом и методом жидкостной цитологии. В цитологических препаратах, полученных традиционном методом и методом жидкостной цитологии, обнаружены комплексы клеток аденокарциномы яичника и единичные клетки, похожие на перстневидноклеточный рак желудка (рис. 3).
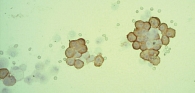
Для уточнения гистогенеза опухоли, ее органной принадлежности и проведения дифференциальной диагностики между аденокарциномой яичника и перстневидноклеточным раком желудка выполнено иммуноцитохимическое исследование с использованием панели антител: СА 125, СК 7, панцитокератин и CEAm.
В результате проведенного исследования были получены мембранные и цитоплазматические экспрессии с антителами СА 125, СК 7, панцитокератином (рис. 4–6) и отрицательные CEAm.
Иммунофенотип опухоли соответствовал аденокарциноме яичника. На основании результатов обследования у больной диагностирован рецидив рака яичника.
Заключение
Следует отметить важную закономерность: общая частота рецидивов рака яичников на первом году наблюдения у больных с I стадией заболевания была выше, чем у больных с II–III стадиями заболевания (76,5 и 68,4% соответственно). Это свидетельствует об ошибках врачей во время выполнения хирургического стадирования. Строгое следование правилам проведения данной процедуры позволяет снизить количество ошибок, связанных с определением стадии заболевания, и количество рецидивов.
Применение традиционного метода цитологического исследования экссудатов и смывов брюшной полости при получении информативного материала может оказаться достаточным для установления диагноза рецидива рака яичников. Если опухолевых клеток в мазках мало или имеют место трудности в дифференциальной цитологической диагностике, из оставшегося материала можно приготовить монослойные препараты и изучить их как при обычной окраске, так и с использованием иммуноцитохимического метода.
M.G. Leonov, V.I. Novik, S.N. Chernov, Ya.Kh.-B. Yershova
Oncology Сentre № 3, Novorossiysk
N.N. Petrov National Medical Oncology Centre, Saint-Petersburg
Contact person: Mikhail Genrikhovitch Leonov, novonko@yandex.ru
Retrospectively analyzed the main factors determining the time of recurrence in 839 patients with ovarian cancer of I–III stages after combined treatment for the period of 2010–2012.
In the study of exudates and swabs of the abdominal cavity in 33 patients with ovarian cancer along with the traditional cytological study it was applied the method of liquid-based cytology with the use of the nutrient medium 199. The efficiency of the compared methods of cytological diagnostics was evaluated.
According to the obtained results, the accuracy of the liquid cytology method exceeds that of traditional cytological research by 1.5 times (p < 0.05). The quality of unsatisfactory cytological preparations reduces by 23.7%.
