количество статей
7396
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
Адалимумаб в алгоритмах ведения пациентов с ювенильным идиопатическим артритом
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Педиатрия" № 4 (34)
- Аннотация
- Статья
- Ссылки
Современные подходы к лечению ювенильного идиопатического артрита (ЮИА) у детей включают применение генно-инженерных препаратов. Результатам последних клинических исследований, дифференцированному подходу к назначению биологических препаратов в зависимости от возраста пациента, разбору конкретных примеров из клинической практики был посвящен симпозиум компании AbbVie, прошедший в рамках ХVII Конгресса педиатров России с международным участием «Актуальные проблемы педиатрии» (Москва, 14 февраля 2014 г.). Во время симпозиума подробно освещались вопросы эффективности и безопасности адалимумаба в терапии олиго- и полиартикулярного ЮИА, ассоциированного с ЮИА увеита и юношеского серонегативного артрита.

Профессор П. Картье
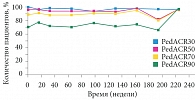
Рис. 1. Динамика критериев PedACR: открытая продленная фаза с фиксированной дозой (DEO038)
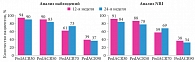
Рис. 2. PedACR 30/50/70/90 на 12-й и 24-й неделях

И.П. Никишина
Генно-инженерные биологические препараты в лечении различных форм ювенильного идиопатического артрита
В настоящее время в мировой практике для лечения ювенильного идиопатического артрита (ЮИА) применяются следующие генно-инженерные биологические препараты (ГИБП):
- ингибиторы фактора некроза опухоли альфа (ФНО-альфа): этанерцепт и адалимумаб, имеющие зарегистрированные педиатрические показания, а также применяемые в особых ситуациях off-label инфликсимаб, голимумаб и цертолизумаб пегол;
- ингибитор рецептора к интерлейкину (ИЛ) 6 тоцилизумаб (зарегистрирован при ЮИА в мире и России);
- ингибиторы ИЛ-1-бета – анакинра (препарат не зарегистрирован для применения при ЮИА), канакинумаб (в России зарегистрирован при криопирин-ассоциированном периодическом синдроме (CAPS) у взрослых и детей в возрасте четырех лет и старше с массой тела > 15 кг);
- анти-В-клеточный препарат ритуксимаб (не зарегистрирован для применения при ЮИА);
- препарат, ингибирующий активацию Т-клеток, абатацепт (зарегистрирован для терапии ЮИА в России и за рубежом).
Профессор Пьер КАРТЬЕ (Pierre CARTIER, Франция) проанализировал эффективность и безопасность терапии ГИБП при различных вариантах ЮИА с позиции доказательной медицины. Он озвучил результаты рандомизированных клинических исследований генно-инженерных биологических препаратов при основных вариантах, выделявшихся в прежней классификации ювенильного артрита. «Сегодня мы назначаем биологические препараты пациентам с ювенильным анкилозирующим спондилитом, ювенильным полиартикулярным и олигоартикулярным ЮИА, детям младшего возраста с низкой массой тела, детям с псориатическим артритом, артритом, связанным с энтезитом, и системным ЮИА», – уточнил профессор П. Картье.
Первое рандомизированное контролируемое исследование (РКИ) было посвящено оценке эффективности этанерцепта (ЭТЦ) – первого препарата, разрешенного к применению при ЮИА1. Изначально в исследование было включено 69 пациентов с полиартикулярным ЮИА в возрасте от четырех до 17 лет, не ответивших на предшествующую терапию метотрексатом (МТ).
Первая часть исследования (дизайн с выбыванием) представляла собой открытую фазу, во время которой все участники получали ЭТЦ. Во вторую плацебоконтролируемую фазу были включены пациенты, достигшие 30%-ного ответа согласно критериям ACR pedi (American College of Rheumatology – Американская коллегия ревматологов). Они были рандомизированы на две группы – плацебо (n = 26) и ЭТЦ (n = 25). Как показали результаты, в группе плацебо обострений заболевания было значительно больше, чем в группе ЭТЦ (81 против 28%). В ходе исследования была подтверждена эффективность ЭТЦ при полиартикулярном течении ювенильного артрита. Впоследствии были получены данные о поддержании эффекта ЭТЦ в продленной открытой фазе в течение восьми лет2.
В другом рандомизированном двойном слепом многоцентровом исследовании оценивали эффективность и безопасность адалимумаба (АДА) как в монотерапии, так и в комбинации с МТ3. Исходно в исследование был включен 171 пациент с полиартикулярным активным ЮИА в возрасте 4–17 лет. АДА назначали по схеме 24 мг/м2 площади поверхности тела один раз в две недели (но не более 40 мг), МТ ≥ 10 мг/м2 еженедельно. При этом пациенты были рандомизированы на две страты: в первой получали МТ (АДА + МТ), во второй МТ не принимали (АДА + плацебо). По окончании первой открытой фазы пациенты, достигшие критерия ACRpedi30, были переведены во вторую слепую фазу. При этом в первой страте (АДА + МТ) первую открытую фазу завершили 83 пациента из 85, во второй (АДА + плацебо) 77 из 86.
В двойном слепом периоде длительностью 32 недели пациенты из страты с МТ (АДА + МТ) были рандомизированы на две группы: АДА + МТ (n = 38) и МТ + плацебо (n = 37). Пациенты из страты без МТ были рандомизированы на группы плацебо (n = 28) и АДА (n = 30). Первичная конечная точка – частота обострений была достоверно ниже у пациентов, получавших АДА + МТ, по сравнению с МТ + плацебо и АДА в сравнении с плацебо. По окончании двойного слепого периода в страте с МТ процент больных, имевших улучшение показателей согласно критериям ACR на 30, 50, 70 и 90%, был выше у тех, кто получал АДА, по сравнению с пациентами, принимавшими плацебо. Затем последовала открытая фаза пролонгированного наблюдения с фиксированной дозой АДА (< 30–20 мг один раз в две недели, ≥ 30–40 мг один раз в две недели, но не более 40 мг), по завершении которой у всех пациентов, принимавших АДА, наблюдалось значительное улучшение показателей ACR (рис. 1).
Результаты исследования, проводившегося в течение шести лет4, убедительно продемонстрировали поддержание эффективности АДА, особенно выраженное в комбинации с МТ.
Профессор П. Картье ознакомил участников симпозиума с результатами РКИ по оценке эффективности и безопасности абатацепта (АБЦ) у пациентов, не ответивших в должной мере на терапию МТ и ингибиторами ФНО-альфа5, 6 (то есть во второй линии терапии ГИБП). В исследовании участвовали 190 пациентов в возрасте 6–17 лет с полиартикулярным ЮИА. Исследование включало четырехмесячную открытую вводную фазу, шестимесячную двойную слепую плацебоконтролируемую фазу и третью продленную открытую фазу.
На 113-е сутки (окончание открытого вводного периода) положительный клинический ответ (30% по критериям ACR) наблюдался у 123 больных, причем в основном у тех, кто не имел предшествующего опыта применения ингибиторов ФНО-альфа.
Профессор П. Картье остановился на недавних исследованиях, в значительной степени посвященных возможностям АДА при полиартикулярном и прогрессирующем олигоартикулярном ЮИА, ЮИА, связанном с энтезитом, и увеите, ассоциированном с ЮИА.
В одном из исследований, представленном на конгрессе ACR в 2013 г., оценивали эффективность АДА в лечении олиго- и полиартикулярного ювенильного артрита у пациентов в возрасте 2–4 лет и младше пяти лет с массой тела < 15 кг7 (в настоящее время в России адалимумаб зарегистрирован у детей с четырех лет). К концу 12-й недели у 91% детей (NRI – анализ), получавших терапию АДА в дозе 24 мг/м2, наблюдался положительный клинический ответ (30% ACRPedi), который сохранялся практически у всех пациентов (84%) к концу 24-й недели (рис. 2).
По мнению докладчика, учитывая фармакокинетические свойства препарата, АДА в дозе 24 мг/м2 (но не более 40 мг) один раз в две недели подкожно следует назначать детям в возрасте до 13 лет с последующим увеличением дозы у детей старше 13 лет (но не более 40 мг) один раз в две недели подкожно.
Как известно, увеит – одно из наиболее тяжелых осложнений ЮИА, приводящих к инвалидизации. По словам профессора П. Картье, в большинстве публикаций упоминаются хорошие результаты, относительно небольшая частота побочных реакций и целесообразность назначения биологических препаратов детям с увеитом, ассоциированным с ЮИА, при недостаточной эффективности традиционной иммуносупрессивной терапии. Несмотря на то что АДА пока не зарегистрирован для лечения увеита, данные ряда исследований демонстрируют способность препарата предупреждать развитие ЮИА-ассоциированного увеита.
В настоящее время продолжаются два РКИ – ADJUVITE8 и SYCAMORE9 – по оценке эффективности адалимумаба в лечении увеита, ассоциированного с ЮИА. Исследование ADJUVITE длительностью 12 месяцев проводится во Франции. В нем принимают участие 40 пациентов, не ответивших на лечение МТ или глюкокортикостероидами (ГКС) и рандомизированных на группу плацебо и группу АДА во время двойной слепой двухмесячной фазы. Открытая фаза составляет десять месяцев. Цель исследования – оценить возможности АДА в контроле ЮИА-ассоциированного увеита.
Говоря о трудностях ведения больных системным ювенильным идиопатическим артритом (СЮИА), профессор акцентировал внимание участников симпозиума на данных последних исследований, продемонстрировавших хорошую эффективность тоцилизумаба (ТЦЗ), анакинры, канакинумаба в лечении СЮИА. Так, результаты долгосрочного наблюдения TENDER10 показали, что на фоне терапии ТЦЗ через год 50% больных перестали принимать ГКС, через три года после постепенной отмены ТЦЗ у 25% пациентов отсутствовали рецидивы. Схожую эффективность продемонстрировал препарат анакинра в ходе контролируемого исследования, проведенного профессором П. Картье11. Однако, по словам докладчика, анакинра по эффективности несколько уступает ТЦЗ и канакинумабу.
Таким образом, биологические препараты имеют доказанную эффективность в лечении различных вариантов ЮИА. Получены также убедительные данные о безопасности этих препаратов. Однако при назначении терапии ГИБП следует не только проводить тщательное обследование больных, чтобы исключить возможную латентную или клинически стертую инфекцию, в том числе специфическую (туберкулез), но и учитывать уровень образованности пациентов и их родителей.
Профессор П. Картье перечислил показания к применению биологических препаратов при ЮИА:
- при полиартикулярном и/или прогрессирующем олигоартикулярном ЮИА:
- препараты первой линии у детей ≥ 4 лет и весом 15 кг (после неэффективности МТ) – ЭТЦ (в комбинации с МТ), АДА (+ МТ по возможности), у детей ≥ 2 лет – ТЦЗ внутривенно;
- препараты второй линии: рассматривается абатацепт внутривенно у детей ≥ 6 лет;
- при системном ЮИА:
- препараты первой линии у детей ≥ 2 лет (после неэффективности нестероидных противовоспалительных препаратов и ГКС) – ТЦЗ (внутривенно или с МТ), канакинумаб (монотерапия, дорогостоящий препарат);
- препараты второй линии – рассматривается перевод с анакинры на ТЦЗ или канакинумаб.
Между тем, по словам профессора, практикующему врачу при назначении лечения не всегда нужно строго следовать только официальным рекомендациям. «В каждом конкретном случае надо как можно раньше назначать наиболее адекватную терапию, опираясь на мнение экспертов. При этом все более популярным становится раннее назначение ГИБП – в пределах первых двух лет после установления диагноза», – подчеркнул он.
В заключение профессор П. Картье выразил надежду, что в ближайшее время результаты РКИ позволят расширить доказательную базу по применению ряда ГИБП. Тогда можно будет, например, целенаправленно назначать АДА для лечения ЮИА у детей в возрасте от двух до четырех лет и с массой тела < 15 кг.
Клинический разбор семейного случая ювенильного идиопатического артрита с увеитом: уроки прошлого и настоящего
По словам заведующей лабораторией ревматических заболеваний детского возраста ФГБУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» РАМН Ирины Петровны НИКИШИНОЙ, в структуре ювенильных артритов особое место занимает клинический вариант, не имеющий эквивалентов во взрослом возрасте и характеризующийся олигоартикулярным или лимитированным полиартикулярным поражением, РФ-негативностью, наличием антинуклеарного фактора, высоким риском и серьезными осложнениями увеита, определенным генотипом, эрозиями суставов.
«Нозологический исход АНФ-ассоциированного олиго- или полиартрита с увеитом, как правило, непредсказуем и зачастую связан с необъективным взглядом на проблему детского ревматолога, ревматолога-интерниста и офтальмолога», – пояснила докладчик. Вопреки распространенному в зарубежной литературе мнению о том, что неблагоприятный прогноз этого клинического варианта ассоциируется преимущественно с осложнениями увеита, в российской клинической практике нередко приходится сталкиваться с инвалидизацией этих пациентов и по суставному статусу, что обычно связано с недостаточной эффективностью системной терапии. Появление в арсенале педиатра-ревматолога ГИБП, в частности препарата адалимумаб, существенно расширяет терапевтические возможности в лечении ЮИА, ассоциированного с увеитом.
В качестве наглядной иллюстрации известному высказыванию лорда Байрона «лучший из пророков будущего – это прошлое» И.П. Никишина привела клиническое наблюдение семейного ЮИА, ассоциированного с увеитом у матери и дочери.
Пациентка А. 1978 г.р. (34 года) больна с трехлетнего возраста. Заболевание дебютировало с артрита правого коленного сустава. Через два года развился полиартрит с поражением голеностопных, коленных, тазобедренных суставов, отдельных мелких суставов кистей и шейного отдела позвоночника. Через три года с момента дебюта заболевания к нему присоединился увеит, быстро осложнившийся двусторонней катарактой, по поводу которой неоднократно выполнялось оперативное лечение.
С 1989 г. пациентка наблюдалась в НИИ ревматологии с диагнозом «ювенильный ревматоидный артирит с поражением глаз», АНФ+, HLA B27 негативный. Ей проводили комплексное лечение, включавшее нестероидные противовоспалительные препараты (НПВП), последовательное применение различных базисных препаратов (делагила, хлорбутина, метотрексата, азатиоприна, тауредона, сульфасалазина, циклофосфана внутривенно и внутримышечно), внутрисуставные инъекции ГКС, повторные курсы пульс-терапии ГКС.
С 18 лет пациентка перестала регулярно наблюдаться у педиатра-ревматолога. Именно тогда началось прогрессирование артрита и увеита. Развились выраженная деструкция тазобедренных суставов, потребовавшая эндопротезирования, осложнения двустороннего увеита (бельмо роговицы левого глаза, деформация зрачка правого глаза). Постепенно, уже во взрослом возрасте, манифестировала аксиальная симптоматика с болями в спине воспалительного характера, анкилоз шейного отдела позвоночника с синдесмофитозом, полный анкилоз крестцово-подвздошных сочленений. Длительное время персистировала высокая лабораторная активность, пациентка получала лечение преднизолоном (5–10 мг/сут), НПВП.
Пациентка А. родила двух здоровых девочек, однако у второй дочери в том же возрасте, что и у матери, развился суставной синдром, аналогичный по локализации и клиническим особенностям, вскоре присоединился увеит. Докладчик представила участникам симпозиума подробное описание истории болезни и схему лечения пациентки К. 2009 г.р. – младшей дочери названной больной. Маленькая пациентка с августа 2012 г. наблюдается в ФГБУ НИИР им. В.А. Насоновой РАМН по поводу обострения полиартикулярного ювенильного артрита и ассоциированного с ним увеита. Проводившаяся терапия НПВП, сульфасалазином, метотрексатом, повторными внутрисуставными инъекциями оказалась малоэффективной, и в ноябре того же года после перенесенной острой респираторно-вирусной инфекции у нее отмечено ухудшение состояния с количественным прогрессированием суставного синдрома и вовлечением шейного отдела позвоночника.
В январе 2013 г. пациентка К. поступила в стационар ФГБУ НИИР им. В.А.Насоновой РАМН с высокоактивным ярко выраженным ассиметричным полиартритом и ограничением движений в шейном отделе позвоночника с выраженным болевым синдромом. Результаты обследования: скорость оседания эритроцитов (СОЭ) 30 мм/ч, C-реактивный белок (СРБ) 52,3 мг/л, HLA B27 отрицательный, АНФ 1/320. «Наблюдая такую выраженную активность заболевания, учитывая опыт прошлого, то есть тяжелую болезнь матери на фоне недостаточно эффективной терапии, мы решили как можно раньше оптимизировать схему лечения, назначив адалимумаб в виде подкожных инъекций в дозе 30 мг каждые две недели, одновременно отменив циклоспорин для минимизации побочных эффектов. Мы считали оправданным вопреки возрастным ограничениям назначение адалимумаба ребенку, не достигшему четырехлетнего возраста, поскольку риск неконтролируемого течения болезни с перспективой инвалидизации, судя по опыту матери, был очевиден» – уточнила И.П. Никишина. По ее словам, благодаря адалимумабу был быстро достигнут отличный первоначальный эффект, выраженность которого в последующие два месяца несколько регрессировала, поскольку сохранялись умеренные проявления артрита правого коленного и левого голеностопного суставов (СОЭ 22 мм/ч). «Для того чтобы достичь цели лечения, мы увеличили дозу адалимумаба до 40 мг на введение в течение последующих десяти месяцев. Такая тактика оказалась успешной и позволила практически полностью восстановить внешний вид и функцию всех суставов, предупредить обострения увеита и достигнуть неактивного статуса болезни», – отметила докладчик. Объективизировать отсутствие активности заболевания, в том числе субклинической, помогли современные методы лучевой диагностики, показавшие регрессию признаков синовита и остеита по данным магнитно-резонансной томографии суставов.
Возможность надежного и полного подавления воспалительной активности заболевания с помощью адалимумаба позволяет с оптимизмом рассчитывать на благополучное будущее ребенка и предотвращение инвалидизации по состоянию суставов и органа зрения. Следует отметить, что обе пациентки, мать и дочь, практически одновременно начали терапию адалимумабом. И несмотря на отсрочку фактически в 30 лет от начала заболевания, у матери нашей маленькой пациентки также была достигнута определенная положительная динамика, снижение активности болезни и улучшение качества жизни. На примере представленного клинического наблюдения становится очевидно, как динамично и эффективно развивается фармакотерапия в ревматологии. Только прогресс в ревматологии ХХI в., появление и широкое внедрение в клиническую практику ГИБП как средств таргетной терапии, то есть препаратов, воздействующих точно на конкретную иммунологическую мишень в цепи патогенетических реакций, в частности ФНО-альфа, позволили избежать печальных последствий неконтролируемого заболевания, столь ярко проявившегося у матери пациентки.
***
В завершение симпозиума большое внимание слушателей привлекло выступление заведующей ревматологическим отделением ФГБУ «Научный центр здоровья детей» РАМН, д.м.н., профессора Екатерины Иосифовны АЛЕКСЕЕВОЙ. Она продемонстрировала разбор собственного клинического случая по эффективности адалимумаба в лечении юношеского серонегативного ЮИА. Результаты представленного клинического примера продемонстрировали неэффективность терапии метотрексатом, циклоспорином, инфликсимабом, этанерцептом, тоцилизумабом у пациента с серонегативным ЮИА. Только применение адалимумаба позволило добиться достоверного снижения активности заболевания, стойкой ремиссии и улучшения качества жизни пациента.
Заключение
Применение ГИБП несомненно открыло новые перспективы в лечении ЮИА, способствовало повышению качества жизни пациентов, обеспечивая их нормальный рост и развитие, радикально улучшило прогноз этого хронического заболевания, ранее трудно поддававшегося терапии. Представленные докладчиками данные РКИ и собственные клинические примеры продемонстрировали целесообразность назначения адалимумаба больным при разных вариантах ЮИА – полиартикулярном и олигоартикулярном, ЮИА, асоциированном с увеитом, артрите с энтезитом и других ювенильных спондилоартритах. Помимо значительного уменьшения суставного синдрома, лабораторной активности ревматического процесса и улучшения функциональных возможностей адалимумаб эффективно воздействует на проявления внесуставной симптоматики, в частности увеита, снижает потребность в применении сопутствующей терапии.
1. Lovell D.G., Guianini E.H., Reif A. et al. Etanercept in children with polyarticular juvenile rheumatoid arthritis. Pediatric Rheumatology Collaborative Study Group //
2. Lovell D.J. et al. Safety and efficacy of up to eight years of continuous etanercept therapy in patients with juvenile rheumatoid arthritis. Pediatric Rheumatology Collaborative Study Group // Arthritis Rheum. 2008. Vol. 58. № 5. P. 1496–1504.
3. Daniel J., Lovell D. G., Ruperto N. et al. Adalimumab with or without methotrexate in juvenile rheumatoid arthritis // N. Engl. J. Med. 2008. Vol. 359. № 8. P. 810–820.
4. Lovell Daniel J. et al. OLE DE038: Long-Term Efficacy and Safety of ADA for up to 6 years in Patients with JIA. ACR11 // Arthritis Rheum. 2011. Vol. 63. № 10. Аbstr. 265.
5. Ruperto R., Lovell D.J., Quartier P. et al. Abatacept in children with juvenile Idiopathic arthritis: a randomized, doubl –blind, placebo-controlled withdrawal triad // Lancet. 2008. Vol. 372. № 9636. P. 383–391.
6. Ruperto R., Lovell D. J., Quartier P. et al. Long-term saffety and efficacy of abatacept in children with juvenile Idiopathic arthritis // Arthritis Reum. 2010. Vol. 62. № 6. P. 1792–1802.
7. Kingsbury D.J., Bader-Meunier B., Patel G. et al. Safety, effectiveness, and pharmacokinetics of adalimumab in children with polyarticular juvenile idiopathic arthritis aged 2 to 4 years // Clin. Rheumatol. 2014. DOI 10.1007/s10067-014-2498-1.
8. http://www.clinicaltrials.gov/ct2/show/NCT01385826?term=humira&cond=%22Arthritis%2C+Juvenile+Rheumatoid%22&rank=3. Доступ от 18.12.2013.
9. http://www.sycamoretrial.org.uk/summary.html. Доступ от 18.12.2013.
10. Malattia C., Ruperto N., Palmisani E. et al. A66: assessment of radiographic progression in patients with systemic juvenile idiopathic arthritis treated with Tocilizumab: 2-year results from the TENDER trial // Arthritis Rheumatol. 2014. Vol. 66. Suppl. 11. P. S96–97.
11. Quartier P., Allantaz F., Cimaz R. et al. A multicentre, randomised, double-blind, placebo-controlled trial with the interleukin-1 receptor antagonist anakinra in patients with systemic-onset juvenile idiopathic arthritis (ANAJIS trial) // Ann. Rheum. Dis. 2011. Vol. 70. № 5. P. 747–754.
Новости на тему
09.09.2022 01:00:00
09.03.2021
02.06.2014
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.