Эффективность устекинумаба при болезни Крона после терапии блокаторами ФНО-альфа и ингибитором интегрина альфа-4-бета-7. Клиническое наблюдение
- Аннотация
- Статья
- Ссылки
- English
Введение
Болезнь Крона (БК) – многофакторное хроническое заболевание системы органов пищеварения иммуновоспалительной природы с трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных поражений [1, 2]. БК относится к воспалительным заболеваниям кишечника (ВЗК). На текущий момент процесс патогенеза ВЗК достаточно изучен [3]. Это обстоятельство позволило разработать биологическую терапию БК и язвенного колита с применением так называемых таргетных генно-инженерных биологических препаратов (ГИБП), воздействующих на ключевые элементы воспаления (цитокины). При ВЗК активно используются препараты нескольких фармакологических групп: блокаторы фактора некроза опухоли (ФНО) альфа (инфликсимаб, адалимумаб, голимумаб, цертолизумаба пэгол), ингибитор альфа-4-бета-7-интегрина (ведолизумаб), блокатор янус-киназ (тофацитиниб).
Механизмы действия перечисленных препаратов при БК не универсальны, препараты не воздействуют на все элементы воспаления [4]. У части пациентов отсутствует первичный ответ на терапию блокаторами ФНО-альфа, что расценивается как первичная неэффективность терапии – 10–20% [5, 6]. Кроме того, 17–22% пациентов, первоначально ответивших на терапию блокаторами ФНО-альфа, прекращают лечение из-за вторичной потери ответа на терапию или развития нежелательных явлений (НЯ) [5, 6]. В 19–40% случаев требуется повышение дозы препарата или уменьшение интервалов между его введениями [5]. До 26–37% пациентов прекращают лечение в течение первого года, до 28–41% – во второй год терапии блокаторами ФНО-альфа [6], что рассматривается как вторичная неэффективность терапии.
При неэффективности терапии первым анти-ФНО-альфа-препаратом пациента обычно переводят на другой блокатор ФНО-альфа. В свою очередь ответ на второй блокатор ФНО-альфа связан непосредственно с причиной, по которой врач переводит пациента с одного лекарственного средства на другой анти-ФНО-альфа-препарат [5]. Это указывает на необходимость внедрения новых лекарственных препаратов, влияющих на ключевые механизмы развития заболевания.
Установлено, что интерлейкин (ИЛ) 23 является основным регуляторным цитокином, определяющим барьерную функцию и внутренний гомеостаз, управляя Th17-типом иммунного ответа и обеспечивая связь между врожденным и приобретенным иммунитетом [7, 8]. Одновременное воздействие на ИЛ-12 и ИЛ-23 за счет направленного действия на общую субъединицу p40 приводит к блокированию последующего каскада эффекторных цитокинов, участвующих в патогенезе ВЗК. В полногеномном исследовании подтверждена ведущая роль ИЛ-23 как «главного регуляторного цитокина» при БК [9].
По данным многочисленных исследований, именно ингибирование регуляторных цитокинов ИЛ-12/23 имеет ряд преимуществ перед блокированием эффекторных цитокинов (ФНО-альфа, ИЛ-17) за счет потенциально долгосрочного, устойчивого результата терапии и более редкого режима введения препарата. Поэтому новый таргетный генно-инженерный биологический препарат (ГИБП) устекинумаб, влияющий на вновь изученные цитокиновые мишени, играющие важную роль в патогенезе БК, может быть перспективным в терапии заболевания [7–10].
Устекинумаб – полностью человеческое моноклональное антитело, относящееся к фармакотерапевтической группе иммунодепрессантов, ингибиторов ИЛ. Устекинумаб специфически связывается с субъединицей белка р40, общей для ИЛ-12 и ИЛ-23, ингибируя их связывание с рецептором ИЛ-12R1, который экспрессируется на поверхности Т-лимфоцитов. В Российской Федерации в 2019 г. зарегистрировано новое показание для данного препарата – БК. Ранее препарат был одобрен для лечения псориаза и псориатического артрита [11].
В клинических исследованиях фаз IIB и III устекинумаб, назначавшийся пациентам со среднетяжелой и тяжелой БК, продемонстрировал хорошие долгосрочные результаты в достижении клинической, бесстероидной и эндоскопической ремиссии [12–16].
Кроме того, в отличие от плацебо устекинумаб характеризуется высокой скоростью достижения симптоматической (одна-две недели) и клинической ремиссии (3–8 недель), хорошим профилем безопасности [17–19].
В 2018–2019 гг. устекинумаб вошел во все клинические рекомендации и руководства профессиональных медицинских сообществ по лечению БК. Он признан препаратом первой и второй линий терапии ГИБП при среднетяжелой и тяжелой БК Американской коллегией гастроэнтерологов (ACG) по диагностике и лечению болезни Крона у взрослых пациентов (2018 г.), Британской ассоциацией гастроэнтерологов (2019 г.), Обществом по изучению язвенного колита и болезни Крона (ECCO).
В настоящее время накоплен опыт ведения пациентов, находящихся на терапии устекинумабом, в реальной практике. Недавно опубликованный систематический обзор с метаанализом объединил результаты 13 наблюдательных исследований с участием 1450 пациентов (предшествующее применение ингибиторов ФНО отмечалось в среднем более чем у 90% пациентов). Согласно объединенным данным результатов наблюдательных исследований, в индукционном периоде терапии устекинумабом (8–16 недель) достижение клинического ответа и клинической ремиссии составило 56% (95%-ный доверительный интервал (ДИ) 43–68; диапазон 16–94%; I2 = 94%) и 34% (95% ДИ 25–45; диапазон 15–58%; I2 = 90%) соответственно. Комбинированная оценка результатов поддерживающей терапии, которая проводилась в зависимости от исследования в период 24–52 недели, показала достижение клинического ответа, клинической ремиссии, эндоскопического ответа и ремиссии – 62, 40, 56 и 19% соответственно. Отмечался низкий уровень потери ответа у пациентов, ответивших на индукционное введение препарата, – 13% (95% ДИ 8–20; диапазон: 4–27%; I2 = 83%). Эти данные коррелируют с результатами клинических исследований программы UNITI [15, 20].
Показан хороший профиль безопасности устекинумаба в реальной практике с низким уровнем НЯ, инфекций/инфузионных реакций. Уровень инфекционных осложнений был низким и сопоставимым с уровнем, зарегистрированным в проспективном наблюдательном регистре PSOLAR (12 000 пациентов с псориазом). Профиль безопасности устекинумаба превосходит таковой инфликсимаба, адалимумаба, этанерцепта и иммуносупрессоров. По данным регистра PSOLAR, частота серьезных инфекций самая низкая на фоне терапии устекинумабом по сравнению с другими ГИБП: 0,93 на 100 пациенто-лет [19, 20]. Аналогичная тенденция прослеживалась при анализе подгруппы пациентов с сочетанием псориаза и ВЗК в данном регистре. Тем не менее нужно учитывать, что данные о безопасности у пациентов с псориазом необязательно экстраполируются на пациентов с БК, поскольку в первом случае обычно используется терапия в более низких дозах.
Недавний метаанализ был посвящен сравнению частоты реактивации туберкулеза при использовании устекинумаба и различных анти-ФНО-препаратов в клинических испытаниях II и III фазы с участием пациентов с ревматоидным артритом, анкилозирующим спондилитом, псориазом, псориатическим артритом, БК и язвенным колитом. Частота осложнений была значительно ниже у пациентов, получавших устекинумаб [21]. Объединенные данные пяти клинических исследований устекинумаба у пациентов с псориазом показали отсутствие реактивации латентного туберкулеза при использовании устекинумаба [22].
Таким образом, устекинумаб продемонстрировал высокую эффективность и безопасность в качестве препарата для индукции и поддержания ремиссии у пациентов с БК среднетяжелого и тяжелого течения после неэффективности терапии блокаторами ФНО-альфа или традиционными иммуносупрессорами. В нашей стране до настоящего времени эффективность устекинумаба во второй линии терапии БК не описана. Наше клиническое наблюдение – одно из первых в отечественной практике, демонстрирующее возможности применения устекинумаба при неэффективности других ГИБП.
Клиническое наблюдение
Пациентка В., 1998 г.р., в декабре 2013 г. отметила повышение температуры тела до 39 °С в отсутствие катаральных явлений. По поводу неясного генеза лихорадки проходила обследование и лечение в Детской городской клинической больнице № 13 им. Н.Ф. Филатова. При обследовании инфекционный генез лихорадки исключен. Однако больную стал беспокоить жидкий стул с примесью крови и слизи до 6–8 раз в сутки. В январе 2014 г. пациентка поступила в Измайловскую детскую городскую клиническую больницу для дообследования. При проведении колоноскопии выявлены эрозивно-геморрагические изменения со стороны толстой кишки. Установлен диагноз язвенного колита и назначена терапия месалазином 3 г/сут. На фоне проводимой терапии отмечалась положительная динамика – регулярный стул, два-три раза в сутки, без крови и слизи. Однако в связи с изменениями в клиническом и биохимическом анализах крови (гемоглобин – 101 г/л, лейкоциты – 14,2 × 109/л, палочкоядерные нейтрофилы – 12%, скорость оседания эритроцитов (СОЭ) – 35 мм/ч, С-реактивный белок (СРБ) – 101,9 мг/л, сывороточное железо – 1,6 мкм/л, ферритин – 6 мкг/л, общий белок – 58 г/л, альбумин – 28,5 г/л) в сентябре 2014 г. пациентка госпитализирована в 12-е гастроэнтерологическое отделение Морозовской детской городской клинической больницы Департамента здравоохранения г. Москвы для проведения видеокапсульной эндоскопии.
В ходе исследования выявлены множественные язвенно-геморрагические изменения тощей, подвздошной и толстой кишок, что позволило диагностировать БК с поражением тощей, подвздошной и толстой кишок, хроническое рецидивирующее течение тяжелой степени высокой активности. Гипопротеинемия, гипоальбуминемия, железодефицитная анемия.
В соответствии с общепринятыми рекомендациями, проведена терапия: преднизолон 60 мг/сут, азатиоприн 100 мг/сут, сульфасалазин 3 г/сут, местная терапия (микроклизмы с дексаметазоном 4 мг). На фоне проводимой терапии отмечался регулярный стул – один раз в сутки без крови и слизи. Через три месяца после отмены преднизолона вновь имело место обострение заболевания – жидкий стул до десяти раз в сутки с примесью крови. Заболевание вновь осложнилось гипоальбуминемией, железодефицитной анемией.
Выполнена КТ-энтерография: КТ-картина соответствует БК тонкой и подвздошной кишок I–II стадий. Лимфаденопатия брыжейки. Возобновлена терапия глюкокортикостероидами, продолжена терапия иммуносупрессорами, проведена коррекция водно-электролитных и белково-энергетических нарушений.
Из-за высокой активности и формирования гормонозависимости с 2015 г. начата антицитокиновая терапия ГИБП инфликсимабом по стандартной схеме 5 мг/кг. Пациентка продолжала прием азатиоприна 100 мг/сут. На фоне терапии достигнута клинико-эндоскопическая ремиссия заболевания.
В июле 2015 г. выполнена контрольная колоноскопия: слизистая оболочка слепой, восходящей, поперечно-ободочной и дистального отдела сигмовидной кишки очагово гиперемирована. Сосудистый рисунок сглажен. Складки нормальной высоты. Слизистая остальных отделов розовая, гладкая, блестящая. Сосудистый рисунок усилен, перестроен. Определяются единичные псевдполипозные разрастания до 0,3 см в диаметре. Контактная кровоточивость отсутствует.
С 2015 по 2017 г. пациентка чувствовала себя удовлетворительно на фоне проводимой терапии инфликсимабом в комбинации с иммуносупрессорами. Однако в декабре 2017 г. появился жидкий стул до 4–6 раз в сутки с примесью крови и слизи. Проведена оптимизация терапии инфликсимабом – введение препарата в дозе 5 мг/кг массы тела каждые четыре недели. Несмотря на оптимизированную терапию, в течение шести месяцев сохранялся жидкий стул до четырех раз в сутки с примесью крови и слизи. Ввиду вторичной неэффективности инфликсимаба пациентка переведена на другой ГИБП – цертолизумаба пэгол. На фоне лечения отмечалась положительная динамика: боль в животе уменьшилась, стул три-четыре раза в сутки, снизилось количество крови в стуле.
Контрольная илеоколоноскопия от 28 января 2018 г.: слизистая оболочка подвздошной, поперечно-ободочной и сигмовидной кишок ярко гиперемирована, резко отечна. Сосудистый рисунок отсутствует. В просвете гноевидная слизь и кровь. Определяются множественные сливные язвенные дефекты полигональной формы, некоторые из них занимают 1/3 окружности кишки. Отмечается выраженная контактная кровоточивость. Просвет этих отделов сужен за счет отека. Слизистая оболочка остальных отделов толстой кишки розовая, гладкая, блестящая с умеренной гиперемией и отеком на высоте складок в восходящей кишке. Сосудистый рисунок отчетливый. Циркулярные складки слизистой оболочки средней величины. Стенки кишки эластичные. Тонус кишки сохранен. Заключение: БК, высокая активность воспалительного процесса.
Обзорная рентгенография брюшной полости показала тонкокишечные уровни жидкости. Тонкокишечная непроходимость.
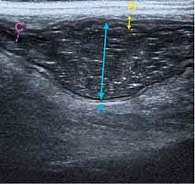
Ультразвуковое исследование (УЗИ) от 2 февраля 2018 г. выявило эхопризнаки тонкокишечной непроходимости, воспалительных изменений со стороны тощей и подвздошной кишок, воспалительную инфильтрацию клетчатки, незначительное количество свободной жидкости в межпетельном пространстве (рис. 1).
В связи с выявленной острой кишечной непроходимостью больная госпитализирована в отделение колопроктологии, где на фоне консервативной терапии удалось разрешить явления тонкокишечной непроходимости.
На фоне продолжавшегося лечения препаратом цертолизумаба пэгол без существенной динамики сохранялись умеренная боль в животе перед стулом, жидкий стул до 4–6 раз в сутки с прожилками крови. С учетом сохранявшейся активности БК и неэффективности двух ингибиторов ФНО-альфа начата терапия глюкокортикостероидами 120 мг/кг внутривенно, продолжена терапия иммуносупрессорами и принято решение о назначении ГИБП с другим механизмом действия ведолизумаба по утвержденной схеме.
На фоне терапии (2018–2019 гг.) отмечалась слабоположительная динамика: сохранялись умеренная боль в животе перед стулом, жидкий стул до четырех-пяти раз в сутки с прожилками крови. В анализах крови до начала терапии ведолизумабом выявлены следующие изменения. Общеклинический анализ крови (ОАК): гемоглобин – 98 г/г, лейкоциты – 14,2 × 109/л, палочкоядерные нейтрофилы – 12%, СОЭ – 45 мм/ч. Биохимический анализ крови: СРБ – 51,8 мг/л, сывороточное железо – 3,6 мкм/л, ферритин – 18 мкг/л, общий белок – 60 г/л, альбумин – 29,5 г/л. Уровень фекального кальпротектина более 1800 мкг/г. В динамике на фоне проводимой терапии ведолизумабом (после оптимизации терапии) ОАК показал: гемоглобин – 104–108 г/л, лейкоциты – 9,9–8,3 × 109/л, палочкоядерные нейтрофилы – 8–10%, СОЭ – 25–35 мм/ч. Биохимический анализ крови: СРБ – 22,0–14,9 мг/л, сывороточное железо – 6,5–7,3 мкм/л, ферритин – 23–44 мкг/л, общий белок – 60–62 г/л, альбумин – 30,0–31,5 г/л. Уровень фекального кальпротектина – 1200–900 мкг/г.
В феврале 2020 г. пациентка госпитализирована в отделение лечения воспалительных заболеваний кишечника Московского клинического научно-практического центра им. А.С. Логинова с жалобами на жидкий стул с примесью слизи до пяти раз в сутки, вздутие живота, общую слабость, повышение температуры в вечерние часы до 37,4 °С. ОАК: гемоглобин – 98 г/л, лейкоциты – 18,3 × 109/л, палочкоядерные нейтрофилы – 13%, СОЭ – 45 мм/ч. Биохимический анализ крови: СРБ – 94,9 мг/л, сывороточное железо – 1,3 мкм/л, ферритин – 4 мкг/л, общий белок – 52 г/л, альбумин – 24,5 г/л. Уровень фекального кальпротектина более 1800 мкг/г.
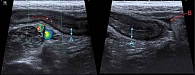
УЗИ от 7 февраля 2020 г.: в терминальном отделе подвздошной кишки визуализируются отечные стенки толщиной до 8 мм (норма до 2–4 мм), дифференцировка на слои отсутствует (выраженный отек), в толще стенки – гиперэхогенные включения (язвенные дефекты). Васкуляризация стенки кишки при цветовом допплеровском картировании усилена. Просвет сужен. Вокруг кишки – воспалительная инфильтрация клетчатки с небольшим количеством жидкости межпетельно (рис. 2).
Проведена медикаментозная терапия: коррекция белково-энергетических и водно-электролитных нарушений, спазмолитическая терапия, инфузия препарата устекинумаб 390 мг внутривенно. Ранних и поздних осложнений не выявлено.
Контрольное обследование выполнено через восемь недель. Субъективно пациентка отмечала значительное улучшение общего самочувствия: купирование болевого синдрома, нормализацию температуры, уменьшение слабости. ОАК: лейкоциты – 8,0 × 109/л, палочкоядерные нейтрофилы – 4%, СОЭ – 15 мм/ч. Биохимический анализ крови: СРБ – 6,9 мг/л, сывороточное железо – 10,3 мкм/л, ферритин – 44 мкг/л, общий белок – 66 г/л, альбумин – 33,5 г/л. Уровень фекального кальпротектина – 200 мкг/г.
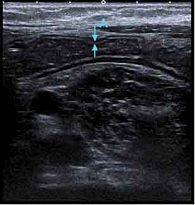
УЗИ 7 апреля 2020 г.: стенки тонкой кишки не утолщены (2 мм), дифференцировка на слои четкая, структура не изменена (рис. 3).
Заключение
Приведенное клиническое наблюдение демонстрирует сложности ведения пациентов с БК, а также перспективные возможности иммунобиологической терапии современными лекарственными препаратами. Несмотря на полный объем медикаментозной терапии, проводимой в соответствии с рекомендуемым алгоритмом [2], эффективность некоторых ГИБП может со временем снижаться. Повторное назначение ГИБП с аналогичным (анти-ФНО-альфа) и даже иным (анти-альфа-4-бета-7-интегрин) механизмом действия менее эффективно, чем первое назначение препарата. Тем не менее в данном клиническом случае при прогрессирующем и трудно контролируемом течении БК применение устекинумаба было эффективным, что подтвердило возможность его использования при резистентности к препаратам анти-ФНО-альфа и анти-альфа-4-бета-7-интегрина.
Подход, основанный на современной концепции лечения БК [15], позволяет считать устекинумаб препаратом, который может быть использован при неэффективности альтернативного лечения заболевания. В то же время с учетом данных клинических и наблюдательных исследований и накопленного опыта применения препарата в других терапевтических областях устекинумаб может быть многообещающей альтернативой для лечения пациентов со среднетяжелым течением БК в случае неэффективности или непереносимости базисной терапии. Особенно привлекательным представляется использование препарата для достижения долгосрочной эффективности и устойчивого результата терапии у пациентов с высоким риском инфекционных осложнений, со значимыми коморбидными заболеваниями (III–IV класс сердечной недостаточности, диабет, демиелинизирующие заболевания), с внекишечными проявлениями БК, у молодых пациентов и пациентов с сочетанными иммуновоспалительными заболеваниями [23–25]. Вместе с тем отечественные исследования, направленные на расширение применения устекинумаба при БК как в первой, так и во второй линии терапии ГИБП, должны быть продолжены, а результаты опубликованы и использованы при принятии решений о тактике лечения заболевания.
O.V. Knyazev, MD, PhD, A.V. Kagramanova, PhD, T.V. Shkurko, PhD, A.A. Lishchinskaya, PhD, N.G. Samsonova, PhD, M.Yu. Zvyaglova, I.A. Li, MD, PhD, A.I. Parfyonov, MD, PhD, Prof.
A.S. Loginov Moscow Clinical Research Center
Research Institute of Health Organization and Medical Management
Contact person: Oleg V. Knyazev, oleg7@bk.ru
Despite the full scope of drug therapy performed in accordance with the recommended algorithm, the effectiveness of some genetically engineered biologic drugs (GEBD) may decrease over time. Repeated administration of GEBD with the same (anti-TNF-alpha) and even different (anti-alpha-4-beta-7-integrin) mechanism of action is less effective than the first administration of the drug. The clinical example shows the effectiveness of Ustekinumab in the progressive and difficult to control course of Crohn’s disease. The drug can be used in the case of the resistance to drugs of anti-TNF-alpha and anti-alpha-4-beta-7-integrin.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.