Алгоритм терапии и профилактики простого герпеса генитальной локализации препаратом Виферон
- Аннотация
- Статья
- Ссылки

В 1957 г. A. Jsaacs и G. Lindenmann при изучении интерференции вирусов сделали важное открытие, быстро привлекшее к себе внимание ученых всего мира. Авторы обнаружили, что в результате взаимодействия клеток перевиваемых хорион-аллантоисных оболочек куриного эмбриона с инактивированным вирусом гриппа в окружающей среде обнаруживается особое вещество, обладающее способностью обусловливать невосприимчивость других перевиваемых хорион-аллантоисных оболочек к вирусной инфекции. Это вещество, ответственное за феномен интерференции вирусов, было названо авторами интерфероном (ИФН). Проведенные затем многочисленные экспериментальные исследования ИФН как у нас в стране, так и за рубежом дали основания считать его «естественным противовирусным антибиотиком», вырабатывающимся в организме и обладающим широким спектром иммунного действия. Это в свою очередь привело к постепенному терапевтическому внедрению ИФН для лечения и профилактики вирусных заболеваний человека, в том числе герпес-вирусной инфекции. Первый опыт использования человеческого ИФН в терапии простого герпеса (ПГ) был сделан офтальмологом V. Tommila в 1963 г. При инстилляциях ИФН в конъюнктивальный мешок он наблюдал сокращение в 2 раза сроков лечения герпетического древовидного кератита у 17 больных.
В 1965 г. Н.С. Потекаев и соавт. (4), а также З.В. Ермольева и соавт. (1) независимо друг от друга сообщили об эффективности ИФН у больных с герпетическим поражением кожи и слизистых. Авторы отмечали значительное уменьшение рецидива заболевания и быстрое стихание субъективной симптоматики при его местном применении.
Позже препараты человеческого ИФН при ПГ стали применять системно в виде внутримышечных инъекций. Было отмечено, что при этом значительно быстрее наступает регресс высыпаний, а курс из 5 инъекций в ряде случаев обеспечивал длительное отсутствие клинических манифестаций заболевания. Однако кратковременность действия природного ИФН, часто наблюдаемое угасание клинического эффекта в зависимости от частоты его применения, а также сложность и дороговизна получения человеческого лейкоцитарного ИФН со временем заставили отказаться от его широкого применения в терапии больных герпесом (1).
Существенным прогрессом в дальнейшей разработке данного метода лечения ПГ явилось создание путем генной инженерии рекомбинантного a2-ИФН, эффективность которого оказалась близка к таковой одного из естественных ИФН (a-ИФН). Именно он послужил основой для создания препаратов, используемых сегодня в клинической практике при терапии многих вирусных заболеваний человека. Однако, как отмечают Ф.И. Ершов и соавт., «пока рекомбинантные интерфероны – это лишь воспроизведенные отдельные субтипы ИФН (альфа, бета или гамма), а идеальный препарат должен, подобно натуральному, иметь их физиологически сбалансированное состояние» (2).
После создания в начале 80-х гг. прошлого века первого препарата рекомбинантного ИФН Реаферона прошло более 20 лет. За это время были синтезированы Реальдерон, Интрон А, Роферон, Велферон и др. Однако при применении этих средств часто возникали определенные препятствия, ограничивающие их использование для лечения больных. Данные препараты дают клинический эффект в больших дозах (3-10 ME в сутки) и вводятся парентерально, что нередко приводит к существенным побочным реакциям и осложнениям (гриппоподобный синдром, головная боль, артралгии, депрессивное состояние, галлюцинации и ряд других) (5).
В результате фундаментальных исследований, проведенных в отделе интерферонов НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи РАМН, была найдена реальная возможность обойти сложности, возникающие при применении препаратов ИФН. В процессе углубленного изучения функционирования системы ИФН в онтогенезе был создан препарат Виферон (рекомбинантный ИФН a-2 в комбинации с антиоксидантами – витаминами Е и С в суппозиториях), который прочно занял свое место в терапии больных ПГ (5, 6).
Более чем 10-летний собственный опыт работы с этим препаратом и исследования его влияния на иммунный статус пациентов дают нам основания констатировать, что основное противогерпетическое действие Виферона связано с активацией им мононуклеарно-фагоцитарной системы и Т-клеточного звена иммунитета, а также повышением уровня эндогенного ИФН (3, 7, 8).
В качестве примера его клинической эффективности и алгоритма применения можно привести одно из последних наших исследований.
Под наблюдением находились 110 больных ПГ в возрасте от 20 до 62 лет, из них 67 женщин и 43 мужчины в возрасте от 20 до 62 лет. Продолжительность заболевания составляла от 1 года до 7 лет. Течение вирусного процесса, в основном генитальной локализации, характеризовалось частыми, не менее 6 раз в год, обострениями, длительность которых в среднем составляла 14 дней. Для определения оптимальной лечебной дозы препарата при ПГ пациенты были разделены на 3 группы: 73 больным 1-й группы Виферон назначали по 500 000 ME, 15 пациентам 2-й группы – по 1 000 000 ME и 22 больным 3-й группы – по 1 500 000 ME. Независимо от дозы препарат назначали по одному ректальному суппозиторию 2 раза в сутки через день (для исключения развития рефрактерности) в течение 6 мес. Во всех случаях лечение начиналось в начале очередного рецидива. На фоне проводимой терапии отмечалось быстрое купирование клинических проявлений обострения. Сроки регресса высыпаний в среднем сокращались на 5-7 дней (рисунок 1). Этот эффект был несколько более выражен при применении Виферона в дозах 1 000 000 и 1 500 000 ME.
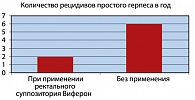
При клиническом наблюдении больных в течение года после окончания терапии отмечено, что Виферон при длительном применении оказывает также и профилактическое действие. Уменьшение частоты рецидивов в 3-4 раза констатировано у 41,6% пациентов, получавших препарат по 500 000 ME, и у 69% – в дозах 1 000 000 и 1 500 000 ME (рисунок 2). В случае развития очередного обострения оно не сопровождалось общими продромальными явлениями, высыпания обычно занимали меньшую площадь, а продолжительность рецидива значительно сокращалась. Клинические данные в целом соответствовали результатам исследований в динамике иммунного статуса больных, при которых отмечалась его нормализация. При этом более выраженная динамика была в случаях, когда Виферон назначали по 1 000 000 и 1 500 000 ME, однако и при дозе 500 000 ME через 3-4 мес. от начала лечения достигался примерно тот же результат. Полученные данные еще раз подтверждают, что Виферон наиболее эффективен в период обострения ПГ благодаря способности быстро купировать клинические проявления болезни. Профилактическое же действие препарата достигается при его длительном (не менее 6 мес.) применении.
Таким образом, мы считаем обоснованным следующий подход к назначению Виферона: лечение следует начинать в период обострения генитального герпеса с дозы 1 000 000 или 1 500 000 ME по 1 ректальному суппозиторию 2 раза в сутки через день в течение 1 мес. Затем дозу препарата можно снизить до 500 000 ME, однако применение его по той же схеме следует продолжить еще в течение 5 мес., а иногда и дольше.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.