Безопасность и эффективность использования филлеров на основе гиалуроновой кислоты с точки зрения доказательной медицины
- Аннотация
- Статья
- Ссылки
- English





Введение
Контурная пластика в виде инъекций тканевых наполнителей на основе гиалуроновой кислоты (ГК) – современный безоперационный метод, позволяющий корректировать недостатки кожи, связанные с процессом старения, чем и объясняется неуклонный рост популярности данного вида косметологических процедур. Инъекции филлеров доступны по цене, не требуют больших временных затрат, для них характерен минимальный реабилитационный период [1, 2].
В настоящее время доступно большое количество дермальных наполнителей с разной концентрацией ГК, плотностью сшивки, обладающих различной гидратационной способностью. Коррекция ГК полностью обратима с помощью инъекций гиалуронидазы [3, 4]. Однако наполнители на основе ГК все же являются инородными телами в нашем организме, поэтому могут вызвать множество осложнений как сразу после инъекции, так и через несколько месяцев или лет.
ГК представляет собой биополимер, состоящий из повторяющихся единиц дисахаридов, которые включают молекулы D-глюкуроновой кислоты и молекулы N-ацетилглюкозамина, связанные β-гликозидами. ГК относится к группе мукополисахаридов, принадлежащих к семейству гликозаминогликанов (ГАГ) [5, 6].
ГК в филлерах находится в связанном состоянии во избежание быстрой деградации вследствие воздействия гиалуронидазы, температуры или свободных радикалов. Наполнители на основе ГК различаются плотностью сшивки и жесткостью. Без перекрестного связывания экзогенная ГК расщепляется за один – три дня [7–9].
Наполнители ГК с более высокой плотностью сшивки могут использоваться для коррекции глубоких морщин, а с более низкой плотностью предпочтительны для коррекции мелких морщин. Сшивание ГК может быть монофазным (один из способов сшивания) или двухфазным (поперечно-сшитая дважды) [10–12].
Вязкоупругость и когезивность играют важную роль в выборе наполнителя на основе ГК и, соответственно, клинических результатах. Эти свойства относятся к способности наполнителя выдерживать различные виды деформации и нагрузки при имплантации в различные области лица [13, 14].
Таким образом, биологические процессы, связанные с введением ГК, зависят от многих составляющих. Исследования в области гистохимических процессов продолжаются, но также необходимо оценивать клинические результаты проведенного лечения пациента, длительность сохранения результата.
Материал и методы
Проведено исследование биодеградации филлера на основе ГК у 12 женщин в возрасте от 21 года до 65 лет с инволютивными изменениями кожи.
Общий срок наблюдения за участниками исследования составил один год. Из 12 участниц исследования трем филлер ввели в область подбородка и углов нижней челюсти, трем – в скулы, четырем – в область носогубных складок, двум – в область губоподбородочных складок. Также всем участницам исследования были сделаны инъекции в заушную область.
Панч-биопсии кожи за ушами были взяты на седьмой день, через один, три и шесть месяцев после процедуры. Обработку и подготовку срезов проводили по общепринятойw методике – материал фиксировали в 10%-ном нейтральном формалине, затем биоптаты заливали в парафин. Серийные парафиновые срезы окрашивали гематоксилином и эозином.
На седьмой день после инъекции судебно-медицинским экспертом была оценена морфологическая картина взятых препаратов кожи.
Критерии включения:
- подписанное добровольное информированное согласие;
- возраст старше 18 лет;
- отсутствие беременности и лактации;
- отсутствие злокачественных новообразований, острых инфекций и аутоиммунных заболеваний;
- отсутствие лечения гормональными препаратами и цитостатиками в течение последних шести месяцев;
- отсутствие участия в других исследованиях.
Все участники были тщательно обследованы, собран подробный анамнез их жизни и заболеваний, а также проведены гистологическое, иммуногистохимическое (ИГХ) исследования до начала исследования и в нескольких контрольных точках.
В ходе исследования женщинам вводили препарат на основе ГК с концентрацией 20 мг/мл в области проблемных зон лица для коррекции возрастных изменений. Также препарат был введен болюсно в две точки заушного пространства. На седьмой день, затем в первый и третий месяцы исследования проводили гистологическое исследование с окраской гематоксилин-эозином. Через три месяца проводили ИГХ-исследование.
Результаты
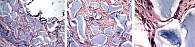
По данным гистологии, сделанной на седьмой день после инъекции, в гиподерме было отмечено присутствие очагового, четко отграниченного образования из множества лакун различного размера, заполненных ГК и окруженных тонкими тяжами фиброзной ткани с очагами кровоизлияния и мелкими очагами инфильтрации макрофагами, эозинофилами, лимфоцитами и редкими нейтрофилами (рис. 1).
Через 30 дней после введения в глубоком слое дермы и в гиподерме прослеживалась крупная псевдокистозная полость со скоплениями базофильного вещества в просвете (ГК). В окружающей полость дерме и гиподерме – большое количество разных по размеру лакун, заполненных ГК. Они окружены тонкими тяжами рыхлой фиброзной ткани с хорошей сосудистой сетью и множественными очагами инфильтрации – эозинофилами с примесью немногочисленных лимфоцитов и макрофагов (рис. 2).
Через три месяца в глубоком слое дермы и гиподерме обнаружено множество мелких лакунарных образований, плотно или рыхло расположенных. Они заполнены ГК, окружены тонкими тяжами умеренно васкуляризированной фиброзной ткани. Эозинофилы и макрофаги обнаруживаются в незначительном количестве (рис. 3).
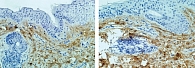
По данным ИГХ-исследования, через три месяца после введения филлера отмечено резкое усиление экспрессии эластина, а также коллагена первого и третьего типов, что говорит об активации процессов неоколлагеногенеза в месте введения филлера. При статистической обработке результатов по критерию Манна – Уитни различия оказались достоверны (р < 0,05) (рис. 4–7).
Результаты гистологического исследования показывают отсутствие воспалительного ответа на введение филлера на всех сроках наблюдения. Обращает на себя внимание выраженная активация фибробластов.
Через семь дней после введения филлера отмечается равномерное распределение вещества в тканях с дальнейшим образованием васкуляризированной фиброзной ткани в месте введения, которая препятствует миграции введенного препарата, что обеспечивает длительное сохранение эстетического результата. Через три месяца филлер по-прежнему обнаруживался в мягких тканях в достаточном количестве.
Таким образом, можно сделать вывод, что использование филлера на основе ГК является безопасным методом с отсутствием воспалительной реакции в тканях. Кроме того, происходит активизация коллагеногенеза и эластиногенеза, что подтверждено данными гистологического и ИГХ-исследования.
N.V. Gryazeva, PhD, S.N. Gres, L.S. Kruglova, PhD, Prof.
Central State Medical Academy of Department of Presidential Affairs, Moscow
People’s Friendship University of Russia, Moscow
Contact person: Natalya V. Gryazeva, tynrik@yandex.ru
The introduction of fillers based on hyaluronic acid is a non-surgical method that allows you to correct skin imperfections associated with the aging process. Hyaluronic acid in fillers is in a bound state to avoid rapid degradation by hyaluronidase, temperature or free radicals. We conducted a study of the biodegradation of a filler based on hyaluronic acid in 12 women aged 21 to 65 years with involutive skin changes. A detailed history of life and diseases was collected from them, as well as a histological, immunohistochemical study was carried out before the start of the study and at several control points. It can be concluded that the use of a hyaluronic acid-based filler is a safe method, with no inflammatory reaction in the tissues. In addition, there is an activation of collagenogenesis and elastogenesis, which is confirmed by the data of histological and immunohistochemical studies.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.