Болевой синдром в общей врачебной практике. XXI Давиденковские чтения. Сателлитный симпозиум компании «Верофарм»
- Аннотация
- Статья
- Ссылки


Мультидисциплинарный подход в лечении болевого синдрома при заболеваниях опорно-двигательного аппарата
Как напомнил к.м.н. Ярослав Николаевич КУШНИРЕНКО (кафедра нейрохирургии и неврологии медицинского факультета СПбГУ), боль – самая частая причина обращения пациентов за медицинской помощью.
Различают острую и хроническую боль. Острый болевой синдром возникает как защитная реакция в результате повреждения тканей, разрешается по мере их заживления и, как правило, хорошо купируется анальгетиками. Хроническая боль продолжается сверх нормального периода заживления тканей (дольше трех месяцев), уже не имеет первоначального сигнального защитного значения и считается не симптомом какого-либо заболевания, а самостоятельной болезнью, требующей особого внимания и адекватной терапии1.
В основе формирования боли могут лежать различные патофизиологические механизмы, определяющие ее тип. Ноцицептивная боль, как правило, острая, связана с активацией болевых рецепторов, соответствует степени тканевого повреждения и длительности действия повреждающих факторов. Невропатическая боль обычно вызвана поражением корешков при формировании грыжи межпозвоночного диска. В свою очередь психогенная боль в большей степени определяется психологическими и социальными факторами.
При заболеваниях опорно-двигательного аппарата, сопровождающихся болевым синдромом, используют такие методы инструментальной диагностики, как рентгенография, электронейромиография, магнитно-резонансная томография. В ряде случаев возникает необходимость в дополнительных методах: рентгенографии органов грудной клетки, ультразвуковом исследовании органов брюшной полости и малого таза, лабораторных методах исследования.
Ведение пациентов с болевым синдромом подразумевает использование хирургических и фармакологических методов лечения. Возможная схема консервативного лечения хронического болевого синдрома включает:
- нестероидные противовоспалительные препараты (НПВП);
- витамины группы В;
- миорелаксанты (толперизон, тизанидин, баклофен) при мышечно-тоническом синдроме;
- антиконвульсанты (габапентин, прегабалин) при невропатической боли;
- препараты для местного применения (например, содержащие лидокаин);
- антидепрессанты при психогенной боли.
Не подлежит сомнению, что НПВП – основное патогенетическое средство лечения острой и хронической боли, связанной с тканевым повреждением и воспалением. Только для НПВП характерно сочетание противовоспалительных, анальгетических, жаропонижающих свойств, что перекрывает весь спектр основных симптомов заболеваний позвоночника и суставов.
При выборе НПВП необходимо учитывать безопасность и переносимость конкретных препаратов. Хорошо известно, что препараты, вектор которых смещен в максимальное ингибирование циклооксигеназы первого типа, небезопасны в отношении слизистой оболочки желудочно-кишечного тракта, тогда как на фоне приема селективных ингибиторов циклооксигеназы второго типа может повышаться риск развития кардиотоксических или кардиоэмболических осложнений.
В российских современных клинических рекомендациях по рациональному использованию НПВП подчеркивается, что все НПВП в адекватных дозах при длительном курсе лечения имеют равный обезболивающий потенциал. По скорости наступления обезболивающего эффекта преимущество может иметь применение инъекционных форм, а также быстрорастворимых препаратов для приема внутрь2.
Я.Н. Кушниренко выделил неселективный ингибитор циклооксигеназы 1 и 2 ибупрофен, который при высокой эффективности редко вызывает осложнения со стороны желудочно-кишечного тракта и сердечно-сосудистой системы. Ибупрофен с пролонгированным высвобождением (Бруфен СР) обладает потенциально улучшенным профилем безопасности и переносимости. Его основное преимущество по сравнению с традиционным ибупрофеном – режим приема. Так, Бруфен СР принимают всего один раз в день по две таблетки, как правило, в раннее вечернее время (около 20:00). Терапия препаратом Бруфен СР позволяет улучшить качество сна, снижает выраженность утренней скованности и обеспечивает возможность активной повседневной жизни. Бруфен СР рекомендован для лечения воспалительных и дегенеративных заболеваний, заболеваний околосуставных тканей, включая ревматические, повреждений мягких тканей, а также для ослабления болевого синдрома. В исследованиях показано, что при остеоартрозе коленного и/или тазобедренного сустава ибупрофен с пролонгированным высвобождением продемонстрировал более значимый эффект в отношении ослабления дневной и ночной боли, повышения качества сна и восстановления повседневной активности по сравнению с диклофенаком – золотым стандартом среди неселективных НПВП3.
Надо отметить, что есть ситуации, когда НПВП абсолютно противопоказаны. Например, после аортокоронарного шунтирования, стентирования или других чрескожных вмешательств, реконструктивных операций на сонных, мозговых и позвоночных артериях. Кроме того, в список абсолютных противопоказаний входят фибрилляция предсердий, дестабилизированная хроническая сердечная недостаточность, прием ацетилсалициловой кислоты и клопидогрела, прямых оральных антикоагулянтов. Для пациентов, которые страдают от хронической боли в суставах и/или спине, не связанной с онкопатологией, инфекционными заболеваниями и коллагенозами, и имеют противопоказания к НПВП, была предложена терапия, предусматривающая:
- компенсацию всех коморбидных состояний;
- когнитивную терапию;
- двигательную активность;
- фармакологическое и хирургическое снижение веса;
- парентеральное введение хондроитина сульфата и глюкозамина до достижения эффективного обезболивания;
- дальнейшее длительное применение пероральных форм хондроитина сульфата и глюкозамина сульфата.
Что касается хирургических методов лечения хронической боли в спине, то абсолютными показаниями для оперативного вмешательства считаются изменения в двигательной сфере и тазовых органах, приводящие к невозможности удерживать мочу и кал, сильная выраженная боль, которую нельзя купировать другими методами. Среди относительных показаний следует выделить частичное нарушение двигательной активности конечностей, слабость в мышцах конечностей, приводящую к атрофии на фоне нарушения иннервации, отсутствие положительных сдвигов после трех месяцев лечения консервативными методами. К современным хирургическим методам относятся дискэктомия (микродискэктомия), эндоскопическое хирургическое вмешательство и лазерное облучение.
В заключение Я.Н. Кушниренко отметил, что врачебная тактика при заболеваниях опорно-двигательного аппарата должна быть направлена на выявление причины возникновения боли, максимально быстрое купирование болевого синдрома и принятие совместно с нейрохирургом решения о необходимости оперативного лечения. Мультидисциплинарный подход к проблеме исключит риск хронизации болевого синдрома и улучшит качество жизни пациентов с заболеваниями опорно-двигательного аппарата.
Головная боль и инсульт: до, во время и после
В начале выступления профессор кафедры нервных болезней СПбГПМУ, д.м.н. Дмитрий Анатольевич ИСКРА отметил, что к числу самых распространенных видов боли относится головная боль. Различают первичные и вторичные головные боли. Первичная (не связанная с другими причинами) головная боль встречается в 95% случаев у людей в возрасте до 50 лет. Оставшиеся 5% случаев приходятся на вторичную головную боль, которая развивается как следствие или симптом какого-либо заболевания. С возрастом (у людей старше 50 лет) представленность вторичных головных болей возрастает, достигая 19%4.
Чаще всего встречаются такие первичные головные боли, как головная боль напряжения и мигрень. В последнее время активно обсуждается их связь с инсультом. С одной стороны, мигрень и головная боль напряжения повышают риск развития инсульта, причем наиболее высок риск у женщин 45–64 лет с частыми и хроническими головными болями5. С другой стороны, взаимосвязь мигрени и инсульта неоднозначна, поскольку не опосредована общими сосудистыми факторами риска6. Предполагается, что их связь может быть обусловлена микроэмболией, провоспалительным статусом, прокоагулянтным состоянием, приемом триптанов, ишемией при распространяющейся корковой депрессии, эндоваскулярной дисфункцией, вазоконстрикцией, общими генетическими дефектами и диссекцией артерий шеи. Ассоциация головной боли напряжения и инсульта может объясняться гиперинтенсивностью белого вещества мозга, развившейся вследствие артериосклероза, поражения малых сосудов, окислительного стресса, дисфункции эндотелия или нарушения сосудистой регуляции.
Головные боли, связанные с транзиторной ишемической атакой и инсультом, относятся к вторичным головным болям. Первую определяют как головную боль, которая развилась одновременно с другими симптомами и/или клиническими признаками транзиторной ишемической атаки длительностью менее 24 часов. Вторую – как цефалгию, которая появляется во временной связи с очаговыми неврологическими симптомами, но не коррелирует с их выраженностью, как правило, имеет признаки головной боли напряжения, легкую или умеренную интенсивность и длится до трех месяцев (а в среднем три-четыре дня).
Есть несколько этиологических вариантов инсульта, которые почти в 100% случаев сопровождаются головной болью: диссекция экстракраниальных артерий шеи, внутримозговая нетравматическая геморрагия, церебральный тромбоз венозных синусов и синдром церебральной обратимой вазоконстрикции. Таким образом, выявление головной боли и уточнение ее характеристик могут помочь верифицировать диагноз.
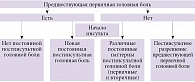
Различают несколько вариантов развития головной боли после инсульта (рис. 1). По мнению профессора Д.А. Искры, наибольшую проблему представляет постоянная, или персистирующая, головная боль при цереброваскулярных заболеваниях, которая возникает примерно у пятой части пациентов с инсультом. Это цефалгия, которая появляется после острого сосудистого события и сохраняется от трех месяцев до нескольких лет. Она характеризуется умеренной или значительной выраженностью (иногда ежедневно), приступами, подобными головной боли напряжения (50%) или мигрени (30%), отсутствием связи с тяжестью поражения7, 8.
Для купирования легких или умеренно выраженных приступов головной боли напряжения применяют ацетилсалициловую кислоту и ацетаминофен. В случае тяжелых приступов головной боли напряжения и на первом этапе купирования мигрени используют НПВП (ибупрофен, кетопрофен, напроксен, диклофенак и др.). Выбор НПВП основывается на показателях селективности и безопасности. Кроме того, необходимо учитывать индивидуальные особенности пациента и степень тяжести заболевания. Еще один немаловажный фактор – влияние формы препарата на профиль фармакокинетики. Слишком высокое пиковое значение повышает вероятность негативного воздействия на здоровье, слишком низкое свидетельствует о возможном отсутствии терапевтического эффекта. Еще важно, чтобы концентрация препарата в крови перед сном и во время сна была на достаточном уровне, обеспечивающем адекватное обезболивание, поскольку недостаток сна может снизить болевой порог.
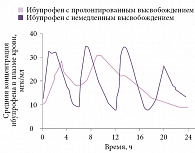
В этом отношении интересен препарат Бруфен СР – пролонгированная форма ибупрофена, который отличается удобством применения, оптимальной фармакокинетикой и хорошим профилем безопасности. Благодаря пролонгированному высвобождению происходит более плавное повышение кривой соотношения концентрации препарата в плазме и времени с более низким значением соотношения максимума и минимума (рис. 2)9. Профиль концентрации плазмы с двумя пиками может обеспечивать преимущество пациентам, страдающим от боли с суточным ритмом нарастания.
Второй этап купирования мигрени в обязательном порядке должен включать специфическую терапию, в частности назначение триптанов. Сегодня на фармацевтическом рынке представлено много препаратов этой группы. Выбор триптана для лечения мигрени должен осуществляться с учетом переносимости и эффективности препарата, степени изученности и ценового диапазона. Суматриптан (Амигренин) – самый изученный препарат этой группы. Установлено, что более 60% пациентов, ранее принимавших другие препараты для купирования приступов мигрени, оценили эффективность терапии Амигренином как высокую или очень высокую и выразили желание принимать этот препарат далее10. Амигренин в дозе 50 и 100 мг продемонстрировал эффективность в купировании не только приступов мигрени, но и сопутствующей симптоматики (тошноты, фото- и фонофобии)11.
Еще одна проблема в лечении мигрени – частое рецидивирование. По данным наблюдений, у 40% пациентов в течение 48 часов отмечается рецидив приступа мигрени12 – атака, которая возникает через четыре часа после купирования первого приступа. Стратегия терапии рецидива атаки мигрени подразумевает повторный прием триптана (в перспективе неэффективный триптан необходимо сменить) и НПВП. Для профилактики рецидива мигрени или мигренеподобных приступов используют следующую схему: комбинация «триптан + НПВП» при дебюте первой атаки, а далее НПВП через 6–12 часов после первого приема триптана.
Профессор Д.А. Искра отметил, что патогенетическая терапия головной боли прежде всего направлена на устранение структурно-функционального дефекта головного мозга, в частности нейромедиаторного дисбаланса. Он возникает при нарушениях мозгового кровообращения и затрагивает зоны мозга, отвечающие за когнитивные функции и эмоциональное состояние. Иначе говоря, боль, депрессия, астения и когнитивные расстройства взаимосвязаны общими звеньями патогенеза.
В настоящее время активно используются препараты, которые влияют на дофаминергическую, глутаматергическую, ГАМКергическую и холинергическую систему и тем самым восстанавливают нейромедиаторный баланс. В частности, холина альфосцерат (препарат Церепро), будучи предшественником ацетилхолина, стимулирует его синтез, повышая холинергическую активность в головном мозге. Препарат Церепро способствует восстановлению структуры и функции нейронов. В исследовании на фоне применения холина альфосцерата у пациентов с ишемией мозга отмечались снижение выраженности мнестических нарушений (памяти и речи) и проявлений астении (утомляемости и ухудшения работоспособности) ко второму месяцу приема препарата. Кроме того, наблюдался эффект в отношении купирования приступов головной боли и головокружения13.
Подводя итог, профессор Д.А. Искра подчеркнул необходимость повышения качества медицинской помощи и индивидуального подхода к лечению каждого конкретного пациента с болевым синдромом.
Заключение
Проблема лечения боли является ведущей в неврологической практике. При ведении пациентов с болевым синдромом наиболее эффективным считается комплексный мультидисциплинарный подход, включающий фармакологическую терапию препаратами различного механизма действия с доказанной эффективностью. К основным целям лечения относятся уменьшение интенсивности болевого синдрома, повышение функциональной активности и улучшение качества жизни пациентов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.