Длительное использование нестероидных противовоспалительных препаратов у больных аксиальным спондилоартритом для подавления острого костномозгового воспаления в крестцово-подвздошных суставах
- Аннотация
- Статья
- Ссылки
- English
В статье представлены клинические случаи приема разных нестероидных противовоспалительных препаратов в течение трех месяцев и более. На фоне многомесячного непрерывного использования отмечены не только хорошая клиническая эффективность, но и отсутствие нежелательных явлений.
В статье представлены клинические случаи приема разных нестероидных противовоспалительных препаратов в течение трех месяцев и более. На фоне многомесячного непрерывного использования отмечены не только хорошая клиническая эффективность, но и отсутствие нежелательных явлений.

Введение
Нестероидные противовоспалительные препараты (НПВП) основной массой пациентов, да и нередко врачами воспринимаются в качестве анальгетических средств, реже – в качестве жаропонижающих, то есть в первую очередь в качестве симптоматических средств. При этом на подсознательном уровне необходимость их длительного приема часто вызывает отторжение и у пациентов, и у врачей.
Однако существуют заболевания, при которых НПВП играют более важную роль. К таковым прежде всего относятся аксиальные спондилоартриты (аксСпА).
Аксиальные спондилоартриты – спондилоартриты с преимущественным поражением позвоночника и крестцово-подвздошных суставов (КПС) [1], наиболее известным представителем которых является анкилозирующий спондилит (АС), известный как болезнь Бехтерева. В свою очередь спондилоартриты представляют собой группу хронических воспалительных заболеваний позвоночника, суставов и энтезисов, характеризующуюся общими клиническими, рентгенологическими/магнитно-резонансно-томографическими (МРТ) и генетическими особенностями.
В настоящее время НПВП при аксСпА рассматриваются в качестве патогенетических, иногда даже в качестве базисных препаратов [2], которые помимо уменьшения боли и воспаления могут тормозить прогрессирование болезни. Именно поэтому при данном проградиентно текущем хроническом заболевании лечение обязательно должно проводиться длительно, то есть его сроки должны быть на порядок больше, чем указано в инструкциях по применению НПВП. Это подчеркивается во всех клинических рекомендациях по ведению больных аксСпА, как отечественных [2], так и зарубежных [3, 4]. Как следствие, остро встает вопрос, связанный с вызываемыми НПВП нежелательными явлениями. Однако нежелательные явления обычно преодолимы и не столь ужасны, как это принято считать.
При длительном применении НПВП можно не только достичь клинической ремиссии, но и подавить внутрикостное воспаление (остеит) в КПС [5, 6] и замедлить рентгенологическое прогрессирование сакроилиита, то есть прогрессирование аксСпА.
Ниже приведены пять примеров из клинической практики, подтверждающие эффективность очень длительного использования НПВП для лечения аксСпА и АС, а также для подавления активного (неинфекционного) остеита КПС.
Клиническая практика
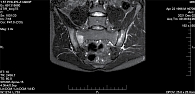
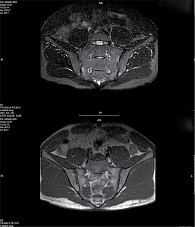
Клинический случай 1. Пациент К., 26 лет. Впервые обратился в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» (НИИР им. В.А. Насоновой) в декабре 2021 г. с жалобами на боли воспалительного характера в поясничном отеле позвоночника, перемежающие боли в ягодицах, боли в нижнечелюстных суставах при жевании. Боли в пояснице появились два года назад и постепенно нарастали по интенсивности. Боли в ягодицах пациент отмечает последние полгода. Скорость оседания эритроцитов (СОЭ) и уровень С-реактивного белка (СРБ) всегда были нормальными. Выявлен антиген HLA-B27. На МРТ КПС определялись обширные очаги костномозгового воспаления (остеит) с обеих сторон (рис. 1). Исходя из анализа семейного анамнеза установлено, что у отца и брата имеет место анкилозирующий спондилит.
При осмотре состояние пациента было расценено как относительно удовлетворительное, кожные покровы чистые, подвижность всех отделов позвоночника и суставов в пределах возрастной нормы, пальпация суставов безболезненная. Индекс активности АС (Bath AS Disease Activity Index – BASDAI) – 3,9 балла.
Установлен диагноз: анкилозирующий спондилит, HLA-B27-ассоциированный, ранняя стадия, умеренная активность.
Был назначен эторикоксиб (препарат Аркоксиа) в дозе 90 мг/сут длительно.
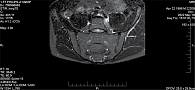
При повторном осмотре через полгода (май 2022 г.) пациент не предъявлял жалоб. Боли нивелировались уже через неделю постоянного приема назначенного препарата и в дальнейшем не возобновились. СОЭ и уровень СРБ были в пределах нормы. На МРТ КПС признаки острого воспаления в области суставов отсутствовали (рис. 2). С момента предыдущего приема больной постоянно принимал эторикоксиб в назначенной дозе. Проведенная через месяц от начала лечения фиброгастродуоденоскопия не выявила патологических изменений в желудочно-кишечном тракте. Показатели печеночных проб были в пределах нормы.
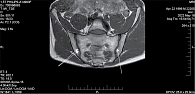
Следует также отметить, что на фоне постоянного приема НПВП в течение полугода в КПС не развилась и жировая дистрофия, хотя появились первые мелкие эрозии суставов (рис. 3).
В результате осмотра диагноз остался без изменений, однако было констатировано развитие полной (клинико-лабораторно-МРТ) лекарственной ремиссии.
Клинический случай 2. Пациентка Б., 31 год. Считает себя больной с 2006 г. (с 17 лет), когда впервые появились боли воспалительного характера в пояснично-крестцовом отделе позвоночника с иррадиацией в правую ногу до колена. Получала терапию НПВП по требованию, то есть при усилении боли. В 2019 г. отмечено значимое обострение: усилились боли в спине, увеличилась скованность, появились боли в правом плечевом суставе. Выявлен HLA-B27-антиген, на обзорном снимке таза обнаружен левосторонний сакроилиит I и II стадий, по описанию МРТ крестцово-подвздошных суставов – двусторонний активный сакроилиит. СРБ – 40 мг/л.
По месту жительства был установлен диагноз: анкилозирующий спондилит, HLA-B27-ассоциированный, ранняя стадия, высокая активность.
Назначена терапия сульфасалазином в дозе 2 г/сут и этодолаком (препаратом Нобедолак) в постоянном режиме.
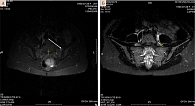
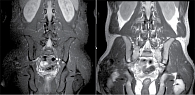
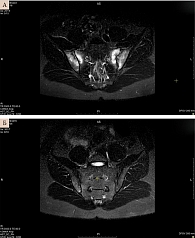
Пациентка получала указанную выше терапию до весны 2020 г. В июне 2021 г. развился OS-увеит, передний активный с гипопионом. В декабре того же года отмечено усиление боли в пояснично-крестцовом и грудном отделах позвоночника. Лабораторное исследование от 1 декабря 2021 г.: СРБ – 4,8 мг/л, СОЭ по Вестергрену – 34 мм/ч, аспартатаминотрансфераза – 26 ед/л, аланинаминотрансфераза – 21 ед/л. По данным МРТ КПС от марта 2021 г., признаки активного левостороннего сакроилиита (рис. 4А).
Назначена терапия эторикоксибом (препаратом Аркоксиа) в дозе 90 мг/сут и сульфасалазином в дозе 2 г/сут.
В марте 2022 г. в связи с обострением больная Б. была госпитализирована в НИИР им. В.А. Насоновой. При поступлении жаловалась на боль в правом тазобедренном суставе, боль в шейном и грудном отделах позвоночника, утреннюю скованность в позвоночнике в течение двух часов.
При осмотре состояние расценено как относительно удовлетворительное. Артритов нет. Болезненность при пальпации в области КПС с двух сторон. Позвоночные индексы: расстояние «подбородок – грудина» – 3 см, подвижность шейного отдела – 45º с двух сторон, экскурсия грудной клетки – 2,5 см, проба Шобера – 2,0 см, расстояние между лодыжками – 100 см, BASDAI – 4,6 балла, индекс активности анкилозирующего спондилита (Ankylosing Spondylitis Disease Activity Score – ASDAS) – 1,5 балла. Ширина глазных щелей D = S. Величина зрачков D = S, симметричные. Зрачковые рефлексы на свет, на аккомодацию, на конвергенцию живые. СОЭ – 10 мм/ч, СРБ – 0,8 мг/л. По данным фиброгастродуоденоскопии, признаков поражения желудка и двенадцатиперстной кишки не обнаружено. На МРТ КПС признаков активного сакроилиита не выявлено (рис. 4Б), однако на месте предшествующего воспаления отмечены признаки хронического сакроилиита (рис. 5).
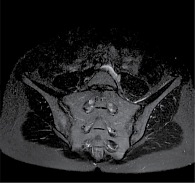
Клинический случай 3. Пациент И., 31 год. Дебют заболевания произошел в 2017 г. с боли в грудном и поясничном отделах позвоночника. В 2020 г. наблюдалось усиление боли и появление скованности. При обследовании выявлена позитивность по HLA-B27, на МРТ – признаки двустороннего активного сакроилиита (рис. 6), повышение СРБ – до 11 мг/л, BASDAI – 5,4 балла, ASDAS-СРБ – 2,6 балла.
Установлен диагноз: анкилозирующий спондилит.
Начата терапия целекоксибом (препаратом Целебрекс) в дозе 400 мг/сут.
В течение недели на фоне терапии пациент И. отметил значительное уменьшение выраженности боли и скованности. Через три месяца, по данным МРТ, наблюдалась положительная динамика в виде уменьшения и регресса очагов остеита (рис. 7).
Клинический случай 4. Пациентка П., 23 года. Дебют заболевания отмечен в 2016 г. (в 16 лет). Именно тогда после длительной сидячей работы впервые появилась боль в области крестцово-подвздошных суставов. На фоне упражнений на растяжку и других физических упражнений боль купировалась. Зимой 2019 г. зафиксирован эпизод переднего увеита. В 2020 г. находилась в ремиссии. Летом 2021 г. снова возникла боль в области ягодиц.
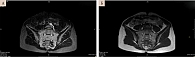
При обследовании обнаружен HLA-B27-антиген. На МРТ КПС в августе 2021 г. выявлены признаки активного правостороннего сакроилиита (рис. 8).
В январе 2022 г. получила консультацию в НИИР им. В.А. Насоновой. Заподозрен анкилозирующий спондилит. Рекомендован постоянный прием целекоксиба (препарата Дилакса) в дозе 400 мг/сут с хорошим клиническим эффектом в виде уменьшения боли в течение месяца.
В марте 2022 г. повторный эпизод OS-увеита. Назначена местная терапия с недостаточным эффектом. Через две недели произошел рецидив увеита. Назначен сульфасалазин в дозе 2 г/сут. После этого рецидивы не были отмечены.
На фоне пятимесячного постоянного приема целекоксиба в дозе 400 мг/сут в мае 2022 г. при повторной МРТ выявлена положительная динамика в виде регресса активного остеита без формирования жировой дегенерации КПС (рис. 9). В анализах крови отклонений не обнаружено. Переносимость терапии расценена как удовлетворительная.
Клинический случай 5. Пациент М., 22 года. Дебют заболевания в 2018 г. (в 17 лет) с острой боли в поясничном отделе позвоночника, которая в течение месяца купировалась на фоне физических упражнений. В феврале 2021 г. наблюдался эпизод энтероколита, через неделю – присоединение боли воспалительного характера в нижней части спины, перемежающаяся боль в области ягодиц, боль и ограничение движений в тазобедренных суставах.
При обследовании: СРБ – 96 мг/л, СОЭ – 37 мм/ч, HLA-B27-позитивный, на МРТ признаки активного двустороннего сакроилиита (рис. 10А), по данным ультразвукового исследования – двусторонний коксит, BASDAI – 6,3 балла, ASDAS-СРБ – 4,2 балла.
Установлен диагноз: анкилозирующий спондилит.
Начата терапия нимесулидом (препаратом Нимесил) в дозе 200 мг/сут. На фоне ежедневного приема нимесулида в течение двух месяцев отмечено значительное уменьшение боли, уровня СРБ – до 7 мг/л, нормализация СОЭ – до 10 мм/ч, снижение активности процесса по BASDAI (2,8 балла) и ASDAS-СРБ (2,0 балла). На контрольном МРТ-исследовании крестцово-подвздошных сочленений через семь месяцев наблюдалась положительная динамика в виде регресса распространенных очагов активного воспаления (остеита) (рис. 10Б). Кроме того, по данным ультразвукового исследования, наметилась положительная динамика и в отношении коксита – шеечно-капсулярное пространство уменьшилось с 14,3 до 8,1 мм.
Обсуждение
Во всех рекомендациях по лечению аксСпА, в том числе в рекомендациях экспертов Американской коллегии ревматологов 2019 и 2022 гг., лидирующую позицию занимают НПВП, при этом подчеркивается преимущество постоянного приема перед приемом по требованию [7, 8]. Кроме того, не указан конкретный НПВП в качестве предпочтительного. Действительно, в практике ревматолога НПВП являются эффективными средствами контроля острой и хронической боли.
Вызываемые НПВП нежелательные явления не столь часты, страшны и тяжелы, как это обычно считается. Это убедительно иллюстрируют результаты всех клинических испытаний генно-инженерных биологических препаратов при АС. В данных исследованиях пациенты, формирующие группы плацебо, всегда получают НПВП, причем длительно – от трех до шести месяцев. Кроме того, при обсуждении результатов в отношении безопасности исследуемого препарата приводятся данные и по выявленным нежелательным явлениям, которые встречались и в группе сравнения. Практически во всех этих исследованиях было показано, что постоянное использование НПВП в течение нескольких месяцев очень редко приводило к развитию серьезных осложнений со стороны желудочно-кишечного тракта [9–11]. Следует подчеркнуть, что в этих исследованиях НПВП назначались на сроки, значительно превосходящие те, которые рекомендованы в инструкциях по их применению.
Известно, что НПВП при аксСпА используются не только как симптоматические, анальгетические и противовоспалительные, но и как базисные средства, которые могут модифицировать течение болезни. Было показано, что, например, напроксен способствует устойчивой частичной клинической ремиссии у трети пациентов с ранним аксСпА [12]. Установлено также, что при регулярном использовании в течение двух лет целекоксиба по сравнению с его применением по требованию в два раза замедляется рентгенологическое прогрессирование АС [8].
Безусловно, с появлением генно-инженерных биологических препаратов достигнут значительный прогресс в лечении акСпА, однако НПВП не уступают им по эффективности. Так, в одном из последних исследований оценивались эффективность (в отношении активного воспаления по данным МРТ) и безопасность монотерапии целекоксибом и этанерцептом, а также их комбинации у 150 больных АС из трех медицинских центров Китая. Средний возраст пациентов составил 32,4 года, средняя продолжительность заболевания – 109 месяцев. Завершили 52-недельное исследование 133 (88,6%) участника. Частота ответа по шкале ASAS 20 (индексу эффективности лечения Международного общества по изучению спондилоартрита, 20%-ное улучшение) составила 44% для целекоксиба, 58% для этанерцепта и 84% для комбинации целекоксиба с этанерцептом [13].
Представленные нами клинические случаи активного и длительного использования НПВП подтверждают, что такая тактика способствовала не только быстрому уменьшению выраженности боли, достижению медикаментозной ремиссии болезни, но и исчезновению очагов активного воспаления (остеита) в костной ткани. Такой результат был ожидаем, поскольку отмечен именно у больных аксСпА [5, 14]. Кроме того, предполагаемые при длительном использовании НПВП нежелательные явления наблюдались редко. В наших клинических примерах не было зарегистрировано случаев развития нежелательных эффектов как со стороны желудочно-кишечного тракта, так и со стороны сердечно-сосудистой системы и печени. Однако следует подчеркнуть, что развившаяся фобия у врачей в отношении небезопасного длительного применения НПВП, конечно, имеет под собой определенные основания. Поэтому такую тактику следует использовать только при уверенности в правильной постановке диагноза, учете всех факторов риска развития желудочно-кишечных осложнений и возможности постоянного мониторинга состояния пациента, что особенно подчеркнуто в последних клинических рекомендациях по использованию НПВП [2, 15].
Заключение
Приведенные данные позволяют сделать следующие выводы:
- длительное использование НПВП при активном аксСпА является одной из обязательных терапевтических опций;
- длительное непрерывное использование НПВП при аксСпА в ряде случаев позволяет нейтрализовать воспаление в костной ткани и добиться клинической ремиссии;
- при длительном использовании НПВП у больных аксСпА требуется постоянный мониторинг состояния для предотвращения развития нежелательных явлений;
- длительное использование эторикоксиба, целекоксиба и нимесулида при аксСпА безопасно при учете факторов риска развития желудочно-кишечных и сердечно-сосудистых осложнений и своевременном мониторинге состояния пациентов;
- нерациональное назначение НПВП может быть причиной необоснованной замены потенциально эффективных (клинически и экономически) препаратов на более дорогостоящие средства.
M.K. Kurbanmagomedov, A.S. Starkova, Sh.F. Erdes, MD, PhD, Prof.
V.A. Nasonova Research Institute of Rheumatology
Contact person: Magomed K. Kurbanmagomedov, kmk05st@mail.ru
Long-term use of nonsteroidal anti-inflammatory drugs in daily therapeutic practice is not welcome and often causes rejection due to the potential for the development of a variety of adverse events. However, in axial spondyloarthritis, these drugs play the role of not only symptomatic therapy, but also modify the course of the disease. Therefore, they should be prescribed for a long period, much longer than that described in the instructions for the drug.
A brief description of clinical cases of the use of various non-steroidal anti-inflammatory drugs lasting 3 or more months is presented. Against the background of good clinical efficacy, adverse events did not develop during many months of continuous use.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.