Синдром избыточного бактериального роста (СИБР) характеризуется изменением количественного и качественного состава микрофлоры в биоптатах тонкого кишечника; появлением факультативных условно-патогенных штаммов, не входящих в состав резидентной микрофлоры. СИБР – состояние, которым очень часто сопровождаются заболевания ЖКТ, при различных гастроэнтерологических патологических состояниях частота СИБР может достигать 70–97%, отметила в начале своего выступления А.П. БАЛАБАНЦЕВА (Крымский ГМУ им. С.И. Георгиевского, кафедра госпитальной терапии и семейной медицины, Симферополь, Украина).
Диагностика СИБР проводится при помощи прямого теста (тонкокишечной аспирации или посева биоптата) или непрямых исследований, к которым относятся индикановый (феноловый) тест, 13С-D-ксилозный или холиглициновый дыхательный тест и водородный дыхательный тест (ВДТ), глюкозный или лактулозный. Последняя методика использовалась в целом ряде исследований, посвященных поискам связи между приемом ингибиторов протонной помпы (ИПП) и развитием СИБР. Наличие данной корреляции было выявлено только в тех исследованиях, в которых субстратом служила глюкоза, при использовании же лактулозного водородного дыхательного теста или посева аспирата тонкой кишки связи между приемом ИПП и нарушениями состава микробиоты кишечника выявлено не было (табл. 1), однако была отмечена более высокая степень обсеменения микрофлоры в начальных отделах тонкого кишечника.
С целью оценки распространенности СИБР при гастроэзофагеальной рефлюксной болезни (ГЭРБ), выявления прогностических факторов возникновения СИБР при длительном приеме ИПП у больных ГЭРБ и сравнения эффективности различных пороговых значений водородного дыхательного теста (12 и 20 ppm) при СИБР специалистами Крымского ГМУ им. С.И. Георгиевского было проведено собственное исследование. В работе приняли участие 143 больных ГЭРБ (63 мужчины и 80 женщин), возраст пациентов составил 36–38 лет. У 58% включенных в работу больных была диагностирована неэрозивная рефлюксная болезнь (НЭРБ), у остальных – ГЭРБ, преимущественно степени А (по Лос-Анджелесской классификации).
Длительность курса лечения ИПП у пациентов не превышала шести месяцев, а средняя его продолжительность составила 21,94 недели. В работу не включались пациенты, перенесшие оперативные вмешательства по поводу заболеваний желудка или кишечника, страдающие воспалительными заболеваниями кишечника, хроническим панкреатитом с внешнесекреторной недостаточностью поджелудочной железы (ВНПЖ), пациенты, получавшие в течение 4 недель до проведения ВДТ антибактериальные или пробиотические препараты, а также перенесшие в этот период колоноскопию или ирригоскопию. Участникам работы были проведены следующие диагностические исследования:
- эзофагогастродуоденоскопия (ЭГДС) с биопсией;
- диагностический тест на Нelico-bacter pylori;
- определение уровня пепсиногена;
- ВДТ с лактулозой;
- суточная pH-метрия (на фоне терапии ИПП).
Пациентов разделили на 3 группы: в первой группе принимали ИПП «по требованию»; во второй группе получали препараты данной группы 1 раз в день, в третьей группе – 2 раза в день. Существенных отличий по полу, возрасту или продолжительности лечения между группами не было. Распространенность выявления H. pylori в первой группе составила 28%, во второй группе – 36%, в третьей группе – 34%. Для проведения ВДТ пациентам давали выпить раствор 20 г лактулозы в 200 мл воды. Затем определялся базальный уровень водорода. Если в течение 90 минут концентрация Н2 увеличивалась на 12 или 20 ppm или исходный уровень повышался более чем на 20 ppm, результат теста интерпретировался как положительный.
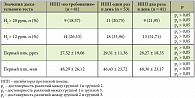
Результаты ВДТ несколько разнились в зависимости от того, какое значение было установлено в качестве порогового (табл. 2), не достигая, однако, статистически достоверного различия. Не было выявлено достоверных отличий по распространенности СИБР у пациентов с различными режимами приема ИПП, уточнила А.П. Балабанцева. Что касается выраженности таких клинических симптомов, как диарея или метеоризм, то она напрямую зависела от степени атрофии слизистой желудка. А вот уровень пепсиногена-1 (ПГ-1) коррелировал с результатами ВДТ: он оказался более низким у тех больных, у кого результаты теста были положительными.
Если пороговое значение ВДТ составляло 12 ppm, среднее значение ПГ-1 у пациентов с положительным ВДТ было равно 45,34 ± 24,09, а у пациентов с отрицательным ВДТ – 109,72 ± 46,09, p < 0,001. В исследовании с использованием порогового значения ВДТ 20 ppm аналогичные показатели составили 35,12 ± 14,01 и 104,412 ± 46,35 соответственно. Анализируя итоги работы, исследователи сделали следующие выводы:
- СИБР у больных ГЭРБ крымской популяции, получающих терапию ИПП, имеет важное клиническое значение, оказывает влияние на течение основного заболевания и формируется в присутствии предрасполагающих факторов.
- Отсутствуют достоверные различия распространенности СИБР у больных ГЭРБ при различных режимах терапии ИПП (прерывистый, постоянный) продолжительностью до 6 месяцев.
- Хронический атрофический гастрит с поражением тела желудка является важным прогностическим фактором развития СИБР у больных ГЭРБ при длительной терапии ИПП независимо от выбранного режима лечения.
- Определение ПГ-1 в сыворотке крови с пограничным значением 40 мг/л позволяет успешно выявлять пациентов группы риска развития СИБР перед назначением ИПП больным ГЭРБ.
- Требуется дальнейшее уточнение чувствительности и специфичности пороговых значений ВДТ.
- Необходимо дальнейшее изучение эффективности ВДТ в диагностике СИБР при сочетанной гастроэнтерологической патологии.
Характеристика диагностических методов выявления и роль вирулентных штаммов Нelicobacter pylori при хронической патологии гастродуоденальной области у детей г. Казани
Профессор кафедры пропедевтики детских болезней Казанского государственного медицинского университета, д.м.н. Р.А. ФАЙЗУЛЛИНА ознакомила участников симпозиума с результатами исследования, посвященного заболеваниям желудочно-кишечного тракта (ЖКТ), которое было проведено специалистами Казанского государственного медицинского университета. В последние годы учеными разных стран была проделана огромная работа по изучению H. pylori, однако этот труд еще далек от завершения: сегодня продолжают появляться новые схемы лечения заболеваний, ассоциированных с H. pylori, а значит, растет необходимость в новых методах, которые позволили бы идентифицировать микроорганизм и оценить его свойства.
Как известно, вызываемые H. pylori заболевания протекают у пациентов по-разному: патология может только затронуть слизистую оболочку желудка, а может обернуться эрозивно-язвенными процессами. Чтобы установить причины такого разнообразия вариантов течения, казанские специалисты решили провести отдельное исследование. Целями работы стало сравнение диагностической значимости методов для первичной диагностики H. pylori у детей с заболеваниями желудка и двенадцатиперстной кишки (ДПК) и выявление роли вирулентных штаммов H. pylori при хронической патологии гастродуоденальной области у детей. Для достижения этих целей были поставлены следующие задачи:
- провести сравнительную оценку диагностической значимости дыхательного ХЕЛИК®-теста (ООО «АМА»), полимеразной цепной реакции (ПЦР) и цитологического метода исследования биоптатов слизистой оболочки антрального отдела желудка для первичной верификации H. pylori-инфекции у детей с заболеваниями желудка и ДПК;
- выявить распространенность CagA-позитивных штаммов H. pylori у детей с хроническими заболеваниями гастродуоденальной области;
- оценить морфологические особенности хронических H. pylori-ассоциированных заболеваний гастродуоденальной области в зависимости от генетических особенностей микроорганизма.
В исследование были включены 117 детей в возрасте от 7 до 17 лет, 17 из них страдали язвенной болезнью ДПК (ЯБДПК) 3-й стадии, остальные – различными формами хронического гастродуоденита (ХГД): поверхностный гастродуоденит был зарегистрирован у 76% детей, гипертрофический – у 19%, эрозивный – у 5% детей. Критериями включения стало, среди прочего, наличие клинических, анамнестических и диагностических признаков, соответствующих проявлениям заболеваний верхнего отдела ЖКТ. Для получения истинного результата экспресс-диагностики хеликобактерных инфекций с помощью дыхательного ХЕЛИК®-теста в работу включались исключительно пациенты, в течение 5 дней перед исследованием не получавшие средств, снижающих кислотность желудочного сока, а также обезболивающих и противовоспалительных препаратов; и не принимавшие антибиотики в течение 2 недель.
В начале исследования все дети прошли скрининговое исследование: дыхательный ХЕЛИК®-тест на оборудовании компании «АМА». Положительный результат был получен у 103 детей (в том числе у 86 с ХГД и 17 с ЯБДПК). Затем детям с положительными результатами ХЕЛИК®-теста была проведена ЭГДС с визуальной оценкой гастродуоденальной области с прицельной биопсией из двух точек антрального отдела желудка. В дальнейшем эти биоптаты использовались для цитологического исследования по стандартной методике оценки степени обсеменения слизистой оболочки H. pylori. Кроме того, биоптат применялся для проведения ПЦР с детекцией ureC гена островка патогенности H. pylori.
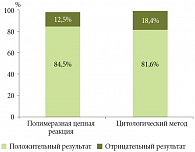
При сравнительной характеристике результатов методов диагностики H. pylori выяснилось, что положительный результат ХЕЛИК®-теста подтверждался при использовании ПЦР в 84,5% случаев. Результаты цитологического исследования совпали с результатом ХЕЛИК®-теста в 81,6% случаев (рис. 1). Для второго этапа исследования ученые отобрали детей, у которых инфицирование H. pylori было подтверждено не менее чем 2 различными тестами. С помощью цитологического метода ложноотрицательный результат был выявлен почти в 11%, а с помощью ПЦР-диагностики – в 7,8%. В 6,8% случаев на ошибку ХЕЛИК®-теста указывали как данные цитологического исследования, так и результаты проведенной ПЦР. Всего в дальнейшую работу было включено 96 детей с подтвержденными H. pylori-ассоциированными гастродуоденальными заболеваниями: 80 детей страдали ХГД, остальные 16 – ЯБДПК.
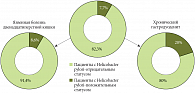
При сравнении диагностической значимости методов выявления хеликобактерной инфекции было установлено, что все тесты отличаются высокой чувствительностью (табл. 3). В ходе дальнейшего исследования было установлено, что H. pylori в среднем регистрируется у 82,3% детей, страдающих хроническими заболеваниями желудка и двенадцатиперстной кишки, причем у пациентов с ЯБДПК хеликобактерная инфекция встречается несколько чаще (рис. 2). По результатам цитологического исследования у большинства (68,8–72,5%) детей вне зависимости от диагноза регистрировалась слабая степень обсеменения слизистой оболочки H. pylori. Однако при изучении результатов анализов детей, страдающих различными формами гастродуоденита, были выявлены существенные различия: при гипертрофическом и эрозивном ХГД наблюдалась достаточно высокая степень обсеменения слизистой оболочки (табл. 4).
Кроме того, при помощи цитологического исследования удалось оценить различные изменения слизистой оболочки: как характерные для острой фазы воспалительного процесса, так и те, что возникают в результате хронического течения инфекции. Оказалось, что у многих детей, особенно у тех, кто страдал эрозивным ХГД, присутствует лимфоцитарная инфильтрация, а у детей с гипертрофической или эрозивной формами ХГД имеются маркеры острого воспалительного процесса в виде нейтрофильной инфильтрации. У 13% детей были выявлены признаки атрофического гастрита, указывающие на необходимость коррекции лечения и длительного наблюдения. Степень обсеменения слизистой оболочки антрального отдела желудка оказалась напрямую связана с выраженностью лимфоцитарной и нейтрофильной инфильтрации, однако со степенью прироста дыхательного теста корреляции установлено не было.
Другой применявшийся в ходе работы способ исследования – ПЦР-диагностика – дал возможность проанализировать не только количество H. pylori, но и генетические свойства этого микроорганизма, в частности, определить распространенность CagA-позитивных штаммов у детей с хроническими H. pylori-ассоциированными заболеваниями желудка и двенадцатиперстной кишки. Выяснилось, что эта разновидность H. pylori встречается приблизительно у 40% детей с подтвержденными H. pylori-ассоциированными хроническими заболеваниями. Чаще всего CagA-позитивные штаммы выявлялись у детей с эрозивными и язвенными поражениями, но достоверных различий в клинической картине в зависимости от того, положительным штаммом инфицирован пациент или отрицательным, обнаружено не было. На основании полученных данных исследователи смогли прийти к следующим выводам:
- При помощи комплексной диагностики было установлено, что у детей хронические заболевания желудка и двенадцатиперстной кишки более чем в 74% случаев ассоциированы с H. pylori.
- Выявлена высокая чувствительность таких методов, как микроскопия мазков-отпечатков слизистой оболочки антрального отдела желудка и ПЦР-диагностика, – при положительном результате данных исследований можно с большой долей уверенности говорить о наличии у пациента хеликобактерной инфекции.
- Дыхательный ХЕЛИК®-тест также показал высокую чувствительность в выявлении инфекции, однако по его результатам судить о степени обсемененности слизистой оболочки желудка H. pylori не представляется возможным.
- Распространенность H. pylori CagA+ у детей с хронической патологией гастродуоденальной области составляла от 28,6 до 48,4%.
- При инфицировании CagA-позитивными штаммами H. pylori риск заболевания ЯБДПК выше в 3,3 раза, а риск развития кишечной метаплазии выше в 7,5 раз, чем при инфицировании
H. рylori CagA-.
Роль и место дыхательных тестов в оптимизации лечения больных целиакией
Дыхательные тесты могут применяться не только для диагностики инфицирования H. pylori и СИБР, но и для повышения эффективности лечения целиакии, наиболее изученного на сегодняшний день заболевания тонкой кишки, распространенность которого составляет в среднем 1% общей популяции. Проблеме лечения целиакии было посвящено выступление д.м.н., профессора кафедры внутренней медицины Национального медицинского университета им. А.А. Богомольца (Киев, Украина) Е.Ю. ГУБСКОЙ. В настоящее время единственным методом лечения целиакии является безглютеновая диета (БГД), позволяющая достигать отличных результатов при высокой приверженности пациентов к лечению. Однако накопленный клинический опыт ведения пациентов с целиакией указывает на то, что достигнуть полной ремиссии удается не всегда, а значит, в ряде случаев пациенты нуждаются в дополнительном обследовании и после выявления причин – в обоснованной коррекции терапии.
Различные дыхательные тесты (лактулозные, ксилозные, сорбитоловые и др.) на протяжении многих лет применялись для диагностики целиакии. Исследователи из НМУ им. А.А. Богомольца поставили перед собой цель изучить причины персистенции клинической симптоматики у больных, находящихся на БГД в течение 6 месяцев. В исследование был включен 41 пациент в возрасте около 35 лет, женщины преобладали над мужчинами в соотношении 1,6:1. У всех включенных в работу пациентов так или иначе наблюдалась позитивная динамика после назначения БГД. Клинически это проявлялось в улучшении общего самочувствия, уменьшении частоты дефекации, тенденции к нормализации стула, стабилизации массы тела, повышении индекса массы тела (ИМТ), однако у 30% больных сохранились рецидивирующая боль в животе, вздутие, метеоризм. Наблюдалось у включенных в исследование пациентов и улучшение лабораторных показателей: нормализация или снижение титров антител к тканевой трансглутаминазе и дезаминированным пептидам глиадина.
Участники исследования были разделены на 2 группы. В первую группу вошли 17 больных, у которых наблюдалось субъективное улучшение в отсутствие клинической ремиссии, во вторую – 24 пациента с неудовлетворительными результатами лечения, отсутствием клинического эффекта от лечения или слабой позитивной динамикой на фоне БГД. В ходе подготовительной работы оценивалась приверженность пациентов лечению посредством пищевых дневников и опросников, целью данных мероприятий было выявление нарушений БГД как основной причины персистенции клинической симптоматики. Выявлялись и другие причины сохранения симптомов: внешнесекреторная недостаточность поджелудочной железы, лактазная недостаточность, СИБР (для диагностики использовались 13С-углеродные и водородные дыхательные тесты). В частности, для выявления лактазной недостаточности использовался водородный тест на анализаторе Micro H2-meter с пороговым значением 20 ppm.
В процессе предварительного исследования пациентов с персистирующими симптомами целиакии было установлено, что 26 пациентов (63,4%) в обеих группах нарушали БГД, что и стало причиной персистирования клинической симптоматики. 34,6% пациентов после коррекции диеты достигли полной ремиссии, однако 65,4% по-прежнему страдали от симптомов целиакии, то есть нарушение диеты оказалось первой, но не единственной причиной персистирования клинической симптоматики у больных целиакией. Для решения этой проблемы была сформирована новая группа из 32 серонегативных пациентов, в которую вошли больные первого и второго этапа исследования. Всем пациентам вновь сформированной группы выполнялись 13С-ТДТ и Н2-тесты с лактозой и D-ксилозой. В результате лактазная недостаточность была выявлена у 15 больных. У 6 пациентов при помощи углеродного теста была обнаружена внешнесекреторная недостаточность поджелудочной железы, а пятерым на основании теста с D-ксилозой был поставлен диагноз СИБР.
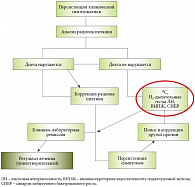
В завершение своего выступления Е.Ю. Губская ознакомила собравшихся с алгоритмом курации больных целиакией с персистенцией клинической симптоматики на фоне БГД (рис. 3). Говоря о результатах проведенной работы, докладчик отметила, что основной причиной недостаточной эффективности лечения оказались нарушения БГД, которые были выявлены у 63,4% обследованных. Персистенция клинической симптоматики также вызывалась лактазной недостаточностью (47%), внешнесекреторной недостаточностью поджелудочной железы (19%), СИБР (16%) и комбинацией внешнесекреторной недостаточности и СИБР (6,3%). По мнению авторов работы, включение в комплексное обследование больных целиакией дыхательных тестов может значительно улучшить результаты лечения и сократить сроки наступления клинической ремиссии.
Болезни ЖКТ занимают одно из лидирующих мест в общей структуре заболеваемости, и вряд ли эта ситуация изменится в обозримом будущем, скорее наоборот, роль гастроэнтерологии будет становиться все более важной. Именно поэтому вопросы неинвазивной диагностики гастроэнтерологических заболеваний, например, с использованием дыхательных тестов, сегодня стоят так остро. Водородный, лактулозный, углеродный и другие разновидности дыхательных тестов хорошо зарекомендовали себя в клинической практике: уже собрана обширная доказательная база, показывающая высокую чувствительность данных методов. Более того, имеются данные, указывающие на то, что в дальнейшем область применения дыхательных тестов будет расширяться, а сами тесты – становиться еще точнее и эффективнее. В этой связи тема следующего IV Международного конкурса научно-исследовательских работ на 2012–2013 гг. остается неизменной: «Диагностика заболеваний желудочно-кишечного тракта по выдыхаемому воздуху».