Географическая атрофия на фоне возрастной макулярной дегенерации: клиническое значение, патогенез и современные возможности терапии
- Аннотация
- Статья
- Ссылки
- English
Введение
Возрастная макулярная дегенерация (ВМД) занимает четвертое место среди причин тяжелой потери зрения у лиц старше 50 лет [1]. Распространенность географической атрофии (ГА) в мире составляет 0,44% среди населения в возрасте от 30 лет и старше [2]; экстраполяция этих данных на возрастную структуру Российской Федерации позволяет оценить количество пациентов с ГА примерно в 370 тыс. человек. Почти у 50% пациентов с ГА в течение семи лет после постановки диагноза наблюдается двустороннее прогрессирование заболевания [3].
Несмотря на высокую глобальную распространенность ГА, возможности ее патогенетической терапии до недавнего времени оставались крайне ограниченными. В отличие от неоваскулярной (влажной) формы ВМД, для лечения которой применяются ингибиторы ангиогенеза (анти-VEGF-препараты), эффективные методы предотвращения прогрессирования сухой формы ВМД до стадии ГА отсутствовали [4].
В настоящее время активно изучаются препараты, действие которых направлено на модуляцию системы комплемента. К ним относятся ингибиторы факторов комплемента C1q, B, D, C3 и C5, средства, повышающие уровень эндогенных факторов комплемента H и I, а также препараты, препятствующие формированию мембраноатакующего комплекса. Помимо этого, изучаются методы, направленные на коррекцию окислительного стресса, и способы клеточной терапии при ГА. Результаты клинических испытаний различных терапевтических подходов остаются неоднозначными [5–14].
Цель – систематизировать и проанализировать современные данные о патогенетическом обосновании, механизме действия, клинической эффективности и профиле безопасности препарата авацинкаптад пегол – первого селективного ингибитора компонента комплемента С5 для лечения ГА у пациентов с ВМД. Обобщение указанных сведений призвано способствовать принятию практикующими офтальмологами обоснованных решений при выборе тактики ведения пациентов с поздней стадией сухой формы ВМД.
Материал и методы
Был проведен анализ научных работ, опубликованных за последние десять лет в базах данных PubMed, Scopus, The Lancet Public Health и Российском офтальмологическом журнале, по ключевым словам, соответствующим тематике исследования. Дополнительно изучены материалы регуляторных органов США (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, FDA), касающиеся применения авацинкаптада пегола при ГА. Основными критериями отбора статей были: соответствие тематике патогенеза сухой формы ВМД; наличие подтвержденных данных о динамике морфологических изменений сетчатки на фоне ингибирования С5; описание нежелательных явлений. Полученная информация систематизирована и обобщена с целью определения клинической значимости препарата для современной офтальмологической практики.
Результаты
ВМД в своем развитии проходит несколько стадий. Поздняя стадия ВМД подразделяется на влажную (неоваскулярную) форму, характеризующуюся хориоидальной неоваскуляризацией, и сухую форму, при которой формируются очаги ГА. Выделяют также смешанный тип, сочетающий признаки обоих патологических процессов [2].
Ключевую роль в патогенезе ГА играют активация системы комплемента и последующее хроническое воспаление. Система комплемента, являющаяся компонентом врожденного иммунитета, представляет собой каскад из более чем 30 белков. Она обеспечивает связь между врожденным и адаптивным иммунитетом, участвует в защите от инфекционных агентов, а также способствует элиминации иммунных комплексов и апоптотических клеток [15]. В связи с этим терапевтическая стратегия должна быть направлена на предотвращение повреждающих эффектов гиперактивации системы комплемента при одновременном сохранении его физиологических функций [16, 17].
В данном аспекте предпочтительным представляется подход, направленный на дистальные (конечные) звенья каскада комплемента. На фоне лечения должны подавляться последствия чрезмерной активации системы, но при этом сохраняться ее физиологические функции. Ингибирование компонента С3 характеризуется широким спектром действия и затрагивает множественные пути активации комплемента. В отличие от этого блокада С5 ограничивается ингибированием анафилатоксина С5а и мембраноатакующего комплекса (МАС) на фоне частичного сохранения активности С3 [16]. Однако ингибирование С3 может оказаться нежелательным в долгосрочной перспективе [17]. Так, в экспериментальных исследованиях на мышах генетическая абляция С3 приводила к снижению клиренса апоптотических клеток и ускорению дегенерации фоторецепторов [18].
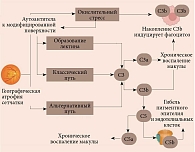
Участие компонентов комплемента в патогенезе заболевания подтверждается накоплением друз между пигментным эпителием сетчатки и мембраной Бруха. Друзы, представляющие собой продукт окислительного повреждения, при избыточном накоплении инициируют хроническое воспаление опосредованно через систему комплемента. Длительно персистирующее воспаление оказывает повреждающее действие на фоторецепторы, пигментный эпителий и хориокапилляры, индуцируя их дегенерацию и последующую атрофию. Ключевую роль в описанных патологических процессах играют фрагменты С3 и С5, обнаруженные в составе друз [19] (рисунок).
Следствием описанных патоморфологических изменений становятся клинические проявления, включающие возникновение скотом и снижение зрительных функций, хотя первоначально патологический процесс затрагивает экстрафовеолярную область желтого пятна. На ранних стадиях ГА проявляется минимальными симптомами: метаморфопсиями, нечеткостью изображения вблизи, снижением контрастной чувствительности и центральной скотомой. По мере прогрессирования заболевания атрофический процесс распространяется на фовеальный центр, что приводит к полной и необратимой потере зрения [19–21].
Одобрение FDA препарата авацинкаптад пегол (Изервей) в августе 2023 г. стало важной вехой в лечении ГА, предоставив первую таргетную терапию, способную замедлять прогрессирование заболевания [22].
Авацинкаптад пегол представляет собой пегилированный РНК-аптамер, фармакологическое действие которого направлено на селективное ингибирование компонента комплемента С5. Препарат связывается с С5, блокируя его расщепление на биологически активные фрагменты С5а и С5b. Это в свою очередь предотвращает образование МАС (C5b-9) – ключевого цитотоксического фактора, повреждающего клетки пигментного эпителия сетчатки. Таким образом, ингибирование С5 замедляет прогрессирование дегенерации клеток сетчатки при ВМД [23].
Препарат Изервей вводится интравитреально, что обеспечивает высокую локальную концентрацию действующего вещества в стекловидном теле и макулярной области. Пегилирование молекулы способствует увеличению периода ее полувыведения, обусловливая пролонгированный терапевтический эффект [24].
Результаты клинических исследований (программа GATHER).
Эффективность и безопасность авацинкаптада пегола оценивали в двух ключевых многоцентровых рандомизированных двойных слепых плацебо-контролируемых исследованиях фазы III – GATHER1 (NCT02686658) и GATHER2 (NCT04435366) [8, 25].
В обоих исследованиях пациенты с ГА получали интравитреальные инъекции препарата авацинкаптад пегол (2 мг) ежемесячно или каждые два месяца либо плацебо (имитацию инъекции). На 12-м месяце оценивали скорость роста площади ГА, измеренной с помощью фундус-аутофлуоресценции.
В исследовании GATHER1 к 12-му месяцу отмечалось снижение скорости роста ГА на 27,4% при ежемесячном введении препарата и на 27,8% – при введении каждые два месяца по сравнению с плацебо [8].
Исследование GATHER2 подтвердило эти результаты, показав снижение к 12-му месяцу скорости роста ГА на 17,7% при ежемесячном введении авацинкаптада пегола по сравнению с плацебо [25].
Объединенные данные исследований GATHER1 и GATHER2 показали устойчивое снижение скорости роста ГА в среднем на 18–20% в течение 12 месяцев терапии с тенденцией к увеличению эффекта в последующие периоды наблюдения [3].
Общая переносимость была сопоставима с таковой при других интравитреальных вмешательствах. Наиболее частыми неблагоприятными явлениями были конъюнктивальные кровоизлияния, повышение внутриглазного давления, нечеткость зрения, развитие неоваскулярной ВМД.
Частота серьезных внутриглазных осложнений оставалась низкой; сообщения о васкулитах или окклюзионной васкулопатии отсутствуют в рамках данных, доступных за период до трех с половиной лет [4, 5].
Важным аспектом безопасности является риск развития неоваскулярной ВМД. В исследованиях GATHER частота конверсии в неоваскулярную ВМД была выше в группах, получавших авацинкаптад пегол, по сравнению с плацебо (6,5–7,2 против 2,4–3,2%) [5, 20]. Этот риск требует тщательного мониторинга пациентов, получающих терапию.
Серьезные офтальмологические побочные эффекты, такие как эндофтальмит, наблюдались редко и соответствовали ожидаемым показателям при интравитреальных инъекциях [4, 5].
Долгосрочные результаты и данные расширенных исследований
Данные открытого расширенного исследования GATHER2 OLE продемонстрировали дальнейшее замедление роста очагов ГА на фоне продолжения терапии до трех с половиной лет по сравнению с плацебо с сохранением благоприятного профиля безопасности.
У пациентов, получавших непрерывное лечение авацинкаптадом пеголом, скорость роста очагов ГА снизилась на 40,5% по сравнению с плацебо. У пациентов, переведенных с плацебо на авацинкаптад пегол, рост очагов уменьшился на 37,1%; терапевтический эффект проявлялся на ранних этапах и нарастал со временем. В целом более раннее начало лечения обеспечивало более выраженное и устойчивое замедление прогрессирования ГА [5].
Профиль безопасности соответствовал ранее полученным данным. В открытом продленном исследовании не выявлено новых сигналов безопасности по сравнению с двухлетним исследованием GATHER2. Препарат хорошо переносился; случаев ретинального васкулита или окклюзионного ретинального васкулита не зарегистрировано.
С клинической точки зрения максимальная эффективность наблюдалась при раннем и непрерывном применении терапии. Позднее начало лечения также способствовало замедлению прогрессирования заболевания, но выраженность эффекта была ниже по сравнению с ранним началом [5].
Данные реальной клинической практики дополнительно подтверждают благоприятный профиль безопасности препарата авацинкаптад пегол и отсутствие новых нежелательных сигналов.
Следует учитывать, что терапия ГА направлена преимущественно на замедление прогрессирования заболевания, а не на быстрое улучшение зрительных функций. Хотя функциональные изменения на поздних стадиях могут быть менее заметны, сохранение структуры сетчатки имеет большое клиническое значение, поскольку способствует защите фоторецепторов. Более раннее начало терапии ассоциировано с большей сохранностью ретинальной ткани.
Заключение
Авацинкаптад пегол зарекомендовал себя как важный терапевтический инструмент в лечении ГА при ВМД. Для пациентов с ГА, подверженных риску необратимой утраты зрения, применение данного препарата имеет жизненно важное значение, поскольку позволяет замедлять прогрессирование атрофических изменений сетчатки на протяжении длительного периода времени. Терапия должна назначаться строго при наличии подтвержденных зон атрофии, но в максимально ранние сроки для достижения наибольшего сохранения зрительных функций. С учетом повышенного риска развития неоваскулярной ВМД пациенты, получающие авацинкаптад пегол, требуют регулярного наблюдения офтальмолога, включая динамический контроль методом оптической когерентной томографии для своевременного выявления признаков неоваскуляризации.
Появление инновационной терапевтической опции знаменует важный этап в развитии патогенетической терапии ГА. Накопленная доказательная база, данные реальной клинической практики и благоприятный профиль безопасности свидетельствуют о высокой научной и практической значимости препарата. Регистрация и последующее внедрение авацинкаптада пегола в Российской Федерации позволят существенно расширить арсенал патогенетически обоснованных методов лечения и улучшить прогноз у пациентов с данной тяжелой патологией, предоставив им возможность сохранить зрение и вести полноценную самостоятельную жизнь.
В условиях появления первых патогенетически ориентированных методов лечения ГА особую значимость приобретают своевременная диагностика заболевания и повышение его выявляемости в клинической практике. В настоящее время ГА нередко диагностируется на поздних стадиях, что ограничивает возможности раннего начала терапии. Рутинное применение современных методов визуализации, прежде всего спектральной оптической когерентной томографии, фундус-аутофлуоресценции и цветной фотографии глазного дна, позволяет надежно выявлять и объективно оценивать зоны атрофии и динамику их прогрессирования.
Перспективным направлением считается создание региональных и федеральных регистров пациентов с ГА, с помощью которых можно будет уточнять эпидемиологические показатели, стандартизировать клиническое наблюдение и оптимизировать планирование терапии. Формирование соответствующей диагностической и организационной инфраструктуры создаст условия для оперативного внедрения современных методов лечения в российскую офтальмологическую практику и обеспечит своевременный доступ пациентов к патогенетической терапии, способной замедлить прогрессирование ГА и сохранить зрительные функции.
I.A. Loskutov, PhD, M.P. Yugay, PhD, A.R. Zotova, A.I. Sibikina
Moscow Regional Research and Clinical Institute
Contact person: Igor A. Loskutov, loskoutigor@mail.ru
The incidence of age-related macular degeneration (AMD) increases as the population ages. Geographic atrophy is the terminal stage of the non-exudative form of AMD and, until recently, lacked effective pathogenetic treatment methods. This article emphasizes the importance of shifting from a strategy of symptomatic observation to active therapy for the late stages of dry AMD.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.