Гипотироксинемия и синдром поликистозных яичников: современный взгляд на проблему. Конгресс «Эндокринология Северо-Запада Роcсии – 2015». Сателлитный симпозиум компании Merck Serono
- Аннотация
- Статья
- Ссылки



Гипотироксинемия: биохимический, клинический и лабораторный феномен
Заведующий кафедрой эндокринологии лечебного факультета Первого Московского государственного медицинского университета им. И.М. Сеченова, председатель Московской ассоциации эндокринологов, председатель секции по заболеваниям щитовидной железы Российской ассоциации эндокринологов, д.м.н., профессор Валентин Викторович ФАДЕЕВ в своем докладе затронул вопросы диагностики и лечения гипотироксинемии. Выступающий отметил, что 180 лет назад была опубликована статья Роберта Джеймса Грейвса (Robert James Graves) о системном аутоиммунном заболевании, которое развивалось вследствие выработки антител к рецептору тиреотропного гормона (ТТГ) и клинически проявлялось поражением щитовидной железы. 100 лет назад Эдвард Кендалл (Edward Kendall) в процессе эксперимента выделил чистый гормон щитовидной железы в кристаллическом виде, получив препарат, который с тех пор активно используется в клинической практике для лечения нарушений функции щитовидной железы.
Гипотироксинемию можно рассматривать с нескольких позиций – биологической, клинической и лабораторной. С биологической точки зрения гипотироксинемия – состояние, развивающееся вследствие дефицита тиреоидных гормонов. Тироксин (тетрайодтиронин – Т4) – универсальный тиреоидный гормон, регулирующий процесс потребления клеткой кислорода. Однако при дефиците этого гормона в организме уменьшается не только потребление кислорода. Снижаются также скорость окислительного процесса, синтез аденозинтрифосфата. Как следствие, наступает гипоэнергетическое состояние организма, нарушается функциональная и пролиферативная активность клетки. Гормон влияет на все виды обмена веществ и функцию всех органов и систем организма.
Диагностика гипотироксинемии основывается на клинических лабораторных исследованиях, предполагающих прямое определение уровня Т4 (общий и свободный Т4) и непрямую оценку тканевых эффектов Т4 (ТТГ, периферические маркеры эффектов тиреоидных гормонов). Однако доступные иммунометрические методы определения уровня свободного Т4 не всегда точны, поскольку не предусматривают физического разделения свободного гормона и связанного и зависят от изменений уровня связывающих белков. При избытке белков уровень свободного Т4 понижается, при дефиците – повышается.
Часто выявляется существенная вариабельность результатов оценки уровня свободного Т4 разными методами в период беременности. В исследовании, в котором уровень свободного Т4 оценивали с помощью девяти различных иммунометрических тестов, а также равновесного диализа, показано, что у части женщин без каких-либо признаков патологии щитовидной железы и при нормальном значении ТТГ уровень свободного Т4 на поздних сроках гестации был значительно снижен1.
Следует отметить, что с несовершенством рутинных методов определения свободного Т4 связано такое состояние беременных, как изолированная гестационная гипотироксинемия. Это означает, что во время беременности при нормальном значении ТТГ выявляют сниженный уровень свободного Т4.
Согласно клиническим рекомендациям Американской тиреоидной ассоциации лечение при изолированной гипотироксинемии в период беременности нецелесообразно2.
Определение в сыворотке крови уровня ТТГ высокочувствительными методами признано самым распространенным способом оценки тиреоидной функции. ТТГ вырабатывается гипофизом и регулирует выработку гормонов щитовидной железы (Т4 и трийодтиронина – Т3) по системе обратной связи, которая позволяет поддерживать стабильную концентрацию этих гормонов в крови. Особое значение имеет референсный диапазон, поскольку от него зависят точность и надежность анализа уровня ТТГ как диагностического инструмента. Сегодня референсный диапазон для ТТГ в разных группах больных обсуждают многие специалисты. Эта дискуссия началась в середине 1990-х гг., когда были опубликованы результаты британского популяционного исследования, продемонстрировавшие, что у лиц с ТТГ более 2 мЕд/л увеличивается риск развития гипотиреоза.
В американском исследовании уровень ТТГ 2,5–4 мЕд/л выявлен у 5% взрослых обследованных лиц. У большинства пациентов (95%) зафиксирован относительно низкий уровень ТТГ – 0,45–2,5 мЕд/л3.
Таким образом, необходимо интерпретировать итоги гормональных исследований с учетом факторов, влияющих на результаты.
Периферический дефицит тиреоидных гормонов может играть важную роль в расхождении между клинической картиной гипотиреоза и нормальным уровнем ТТГ.
Еще один метод диагностики гипотироксинемии заключается в определении периферических маркеров эффектов тиреоидных гормонов на ткани. Один из них – уровень холестерина, отражающий реакцию печени на циркулирующие тиреоидные гормоны. В недавних американских рекомендациях был затронут вопрос об использовании периферических тканевых маркеров действия тиреоидных гормонов для оценки адекватности заместительной терапии первичного гипотиреоза. Эксперты не рекомендуют в этом случае применять тканевые маркеры эффектов тиреоидных гормонов, за исключением научных исследований, поскольку подобные параметры обладают низкой специфичностью. Однако у больных с вторичным гипотиреозом, у которых единственным контрольным параметром является уровень самих тиреоидных гормонов, в качестве дополнительных методов оценки адекватности заместительной терапии можно использовать периферические маркеры уровня тиреоидных гормонов4.
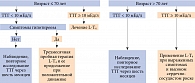
Европейская тиреоидная ассоциация в 2013 г. предложила рекомендации по субклиническому гипотиреозу. Субклинический гипотиреоз – состояние, характеризующееся повышением уровня сывороточного ТТГ и нормальными показателями циркулирующих в крови Т4 и Т3. Согласно рекомендациям, повышение уровня ТТГ может иметь две степени: среднюю – 4,0–10,0 мЕд/л (90% популяции) и высокую – более 10,0 мЕд/л. Схемы лечения субклинического гипотиреоза зависят от уровня ТТГ и возраста пациента. Алгоритм лечения субклинического гипотиреоза Европейской тиреоидной ассоциации представлен на рис. 1.
По мнению экспертов, для большинства взрослых пациентов целью лечения субклинического гипотиреоза является стойкое поддержание уровня ТТГ в нижней половине референсного диапазона – 0,4–2,5 мЕд/л5.
В заключение профессор В.В. Фадеев отметил, что эффективным средством лечения гипотиреоза является Эутирокс® (левотироксин натрия) – синтетический левовращающий изомер тироксина, выпускаемый компанией Merck.
Метформин. Синдром поликистозных яичников
Синдром поликистозных яичников (СПКЯ) считается распространенной эндокринной патологией и одной из наиболее частых причин бесплодия у женщин репродуктивного возраста. Он включает в себя гетерогенную группу гинекологических расстройств с различной степенью яичниковой и надпочечниковой гиперандрогенемии. О применении метформина в терапии пациентов с СПКЯ рассказала директор Института эндокринологии ФГБУ «Федеральный медицинский исследовательский центр им. В.А. Алмазова» Минздрава России (Санкт-Петербург), главный внештатный специалист эндокринолог по Северо-Западному федеральному округу, д.м.н., профессор Елена Николаевна ГРИНЕВА. Она отметила, что СПКЯ характеризуется сочетанием хронической ановуляции и гиперандрогенемии. В последние десятилетия эксперты разных стран предложили несколько подходов к диагностике СПКЯ.
В 1990 г. Национальным институтом здоровья США были утверждены критерии для диагностики СПКЯ – хроническая ановуляция, клинические и/или биохимические признаки гиперандрогении. В 2003 г. Роттердамский консенсус утвердил рекомендации для диагностики СПКЯ, предусматривающие наличие хотя бы двух из трех признаков: олигоменорея и/или ановуляция, гиперандрогения (клинические или биохимические признаки), ультразвуковые (УЗ) признаки поликистозных яичников6. В 2006 г. эти рекомендации были дополнены Ассоциацией по изучению избытка андрогенов и синдрома поликистозных яичников. Согласно рекомендациям, критерии диагностики СПКЯ основаны на выраженности и сочетании таких симптомов, как гиперандрогенизм (андрогензависимая дермопатия, гирсутизм), повышение андрогенов в крови, дисфункция яичников (олиго- и/или ановуляция), УЗ-картина поликистозных яичников7.
Наряду с сочетанием хронической ановуляции и гиперандрогенемии важным критерием диагностики СПКЯ признаны морфологические изменения в яичниках, выявляемые с помощью УЗ-исследования. Определение УЗ-признаков поликистоза яичников сформулировано Роттердамским консенсусом. Это 12 или более фолликулов диаметром 2–9 мм либо увеличенные в объеме яичники (более 10 см3)8.
Со временем понятие СПКЯ стало мультидисциплинарным. Сегодня СПКЯ включает не только гинекологические, но и метаболические нарушения. После того как в 1980 г. была доказана связь между СПКЯ и гиперинсулинемией, внимание исследователей привлекла роль инсулинорезистентности и гиперинсулинемии в развитии СПКЯ.
В ходе исследований установлены общие характеристики для СПКЯ и метаболического синдрома. Можно сказать, что СПКЯ – метаболический синдром женщин репродуктивного возраста.
В ходе исследований отмечена прямая зависимость между наследственностью, образом жизни, гормональными изменениями, ожирением и уровнями инсулина и андрогенов9.
Кроме того, по мнению ряда исследователей, существует тесная связь между индексом массы тела (ИМТ) и инсулинорезистентностью, причем как при избыточной, так и нормальной массе тела. В случае СПКЯ инсулинорезистентность реализуется не столько в жировой ткани, особенно в отсутствие ожирения, сколько на уровне мышечной ткани. Безусловно, избыточный вес, в большей степени у женщин с СПКЯ, усиливает инсулинорезистентность, которая имеет патогенетическое значение в развитии не только метаболических, но и гинекологических заболеваний10. Таким образом, взаимосвязь СПКЯ и метаболических нарушений очевидна.
Изучение роли гиперинсулинемии и инсулинорезистентности при СПКЯ способствовало внедрению новых терапевтических схем на основе препаратов, улучшающих чувствительность к инсулину, прежде всего метформина (Глюкофаж® Лонг, компания-производитель Merck). Терапевтический эффект препарата при СПКЯ – положительное влияние на такие метаболические параметры, как избыточная масса тела, окружность талии, нарушения углеводного и липидного обмена. Кроме того, метформин оказывает действие на гинекологические нарушения, характерные для СПКЯ, такие как гиперандрогенемия, гирсутизм, гиперплазия эндометрия, нарушение фертильности.
Данные клинических исследований продемонстрировали, что эффект метформина при СПКЯ сопровождается снижением избыточной массы тела, уровня глюкозы и инсулина (рис. 2)11.
На фоне применения метформина у больных СПКЯ снижается активность секреции андрогенов яичниками. Доказан эффект метформина (непрямой механизм) в отношении уменьшения уровня тестостерона и выраженности гирсутизма12.
В ряде исследований показано, что комбинированное применение метформина и кломифена цитрата является эффективным способом индукции овуляции у женщин с СПКЯ. Метформин не продемонстрировал значительного преимущества перед кломифеном. Однако его использование у больных СПКЯ и ИМТ более 32 кг/м2 способствовало большему числу овуляций, беременностей и родоразрешений по сравнению с плацебо13.
Получены положительные результаты назначения метформина в программах вспомогательной репродукции. Важным преимуществом стало снижение риска развития синдрома гиперстимуляции яичников14.
На сегодняшний день для лечения бесплодия у женщин с СПКЯ может быть использован кломифен (при нормальной массе тела) и комбинированная терапия кломифеном и метформином (при избыточной массе тела).
Профессор Е.Н. Гринева подчеркнула, что недостаток многих исследований заключается в том, что метформин назначали коротким курсом, максимально шесть месяцев. Необходимо более длительное применение препарата – в течение 9–12 месяцев с возможным добавлением после шести месяцев кломифена. Женщинам с СПКЯ и нарушениями углеводного обмена, не планирующим беременность, показано применение метформина, а также изменение образа жизни. Отметим, что ожирение или наличие поликистозных яичников не является показанием к назначению метформина. Назначать терапию метформином необходимо после рассмотрения индивидуальных особенностей пациенток.
Таким образом, применение метформина при лечении СПКЯ является эффективным патогенетическим средством терапии, направленным на коррекцию гиперинсулинемии и инсулинорезистентности.
Заключение
Эутирокс® – препарат гормонов щитовидной железы. Он представляет собой синтетический левовращающий изомер тироксина, влияющий на развитие и рост тканей, обмен веществ. Эутирокс® стимулирует рост и развитие, повышает потребность тканей в кислороде, активирует метаболизм белков, жиров и углеводов, повышает функциональную активность сердечно-сосудистой и нервной систем. Показаниями к применению Эутирокса являются гипотиреоз, эутиреоидный зоб, заместительная терапия и профилактика рецидива зоба после оперативных вмешательств на щитовидной железе, рак щитовидной железы (после оперативного лечения), диффузный токсический зоб (после достижения эутиреоидного состояния на фоне антитиреоидной терапии) в виде комбинированной или монотерапии.
Глюкофаж® Лонг (метформина гидрохлорид) относится к группе бигуанидов. Он является препаратом первой линии в лечении сахарного диабета типа 2. Глюкофаж® Лонг показан для применения у взрослых больных в качестве монотерапии или в сочетании с другими пероральными гипогликемическими препаратами либо с инсулином.
Глюкофаж® Лонг повышает чувствительность периферических рецепторов к инсулину и утилизацию глюкозы клетками, оказывает благоприятный эффект на метаболизм липидов. Применение препарата способствует торможению глюконеогенеза в печени и снижению всасывания углеводов в кишечнике.
По данным исследований, Глюкофаж® Лонг уменьшает уровень глюкозы в крови без увеличения массы тела, приводит к снижению риска сердечно-сосудистых осложнений. Кроме того, препарат не стимулирует секрецию инсулина и не оказывает гипогликемического действия у здоровых лиц.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.