Клодронат в онкологической практике
- Аннотация
- Статья
- Ссылки
Развитие метастазов в костях резко снижает качество жизни этих больных, и если на ранних этапах противоопухолевое лечение может эффективно контролировать развитие скелетных осложнений и болевой синдром, то с течением заболевания проблема поддержания качества жизни усложняется.
В качестве средств, активно подавляющих остеолиз, уменьшая тем самым проявления метастазов в костях, в клинической практике успешно применяются бисфосфонаты.
Клодронат является одним из первых бисфосфонатов, клинические исследования которого открыли новые возможности лечения метастазов в костях. Клодронат сохранил до настоящего времени передовые позиции.
Структура, механизм действия и фармакокинетические параметры
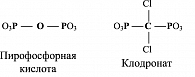
По структуре клодронат, как и остальные бисфосфонаты, представляет собой производное пирофосфорной кислоты с замещением на атом углерода атома кислорода (рисунок).
Исследования фармакокинетики клодроната, вводимого однократной инфузией в дозе 300 мг в течение 2 часов, проведенные у 20 пациентов, показали, что общий клиренс препарата составил 86,6 ± 7,4 мл/мин., почечный клиренс -41 ± 4,3 мл/мин., непочечный клиренс -45,6 + 5,2 мл/мин. Различия в почечном клиренсе были обусловлены в основном показателями почечной функции (клиренс креатинина). Из общего количества препарата около 20% связывается с костной тканью и около 80% выводится с почками в неизмененном виде.
Биодоступность перорального клодроната, как и остальных бисфосфонатов, составляет около 2%, в связи с низкой липофильностью. В системный кровоток препарат попадает путем пассивной диффузии через межклеточные пространства в желудке и тонкой кишке. Чем выше принятая доза, тем большее количество препарата поступает в системный кровоток, однако повышение стандартной дозы в 1600 мг до 3200 дозы не выявило преимуществ. Процент препарата, попавшего в системный кровоток, значительно ниже, если он принимается после еды, особенно содержащей молочные продукты, т.к. происходит связывание препарата в кишечнике с кальцием и другими двухвалентными ионами. Для клодроната суточная доза составляет 1600 мг в день в 2 приема.
Клодронат при метастатическом раке молочной железы и в адъювантном режиме
Первыми клиническими исследованиями, показавшими эффективность клодроната, была серия исследований по лечению гиперкальциемии у больных с метастазами в костях (проведены в 1982-1995 гг.). Одним из них было исследование G.H. Urwin и соавт., 1987 году (2). Препарат вводился в дозе 300 мг внутривенно в течение 5 дней и показал 60-70% эффективность, в зависимости от степени гиперкальциемии, ее типа и т.д.
N.P. O’Rourke и соавт. (1993 г.) сравнили пятидневный режим лечения гиперкальциемии клодронатом по 300 мг в сутки и однократное введение 1500 мг препарата, в котором были показаны преимущества однократной инфузии как по времени достижения нормокальциемии, так и длительности нормализации (3).
В настоящее время при гиперкальциемии можно применять клодронат по 300 мг в течение 5 дней или в дозе 1500 мг одной инфузией. Показано, что нормокальциемия удерживается дольше, если далее проводится терапия пероральной формой клодроната по 1600 мг в день в 2 приема.
A.H.G. Paterson, B. Kristensen и M. Tubiana-Hulin и соавт. провели исследования активности клодроната при метастазах в кости рака молочной железы в общей сложности у 317 больных (4, 5, 6). Больные рандомизированно принимали клодронат 1600 мг в день, перорально, длительно (в течение 18 мес., 24 мес. и 12 мес. соответственно) или плацебо, в которых было показано уменьшение частоты патологических переломов, частоты развития гиперкальциемии, снижение болевого синдрома у пациентов, получавших клодронат. При мета-анализе этих исследований было показано достоверное снижение риска скелетных осложнений на 16% (ОР 0,84; 95% ДИ 0,72-0,98) (р = 0,03) (7).
В 1996 году J. Kanis опубликовал результаты исследования, в котором оценивалась частота появления костных метастазов у больных только с внекостными метастазами рака молочной железы (8). В исследование было включено 133 пациента, получавших клодронат 1600 мг в сутки в течение 3 лет или плацебо. Количество пациентов, у которых развились костные метастазы, было меньше в группе, получавшей клодронат, но различия не были статистически значимы. В то же время количество костных метастазов у пациентов в группе с клодронатом было значительно меньше, чем в контроле. Количество скелетных осложнений при развитии метастазов в костях в группе плацебо было выше на 26%, количество патологических переломов позвоночника было выше на 29%, внепозвоночных патологических переломов на 75%. Было отмечено преимущество (22%) в группе клодроната в отношении числа курсов лучевой терапии и частоты гиперкальциемии (39%).
Несмотря на положительные в целом результаты исследования, дальнейшего развития это не получило.
Тем не менее возможности профилактики развития костных метастазов, показанные в работе J. Kanis, позволили начать сразу три рандомизированных исследования у больных с ранним раком молочной железы.
I.J. Diel и соавт. проведено рандомизированное исследование по адъювантному применению клодроната у женщин с высоким риском развития метастазов в отношении частоты и выраженности метастазов в кости (9). В исследование были включены 302 пациентки, оперированные по поводу рака молочной железы, у которых в аспирате костного мозга иммуноцитохимически были обнаружены во время операции клетки рака. Пациенты получали клодронат 1600 мг ежедневно внутрь в течение 2 лет (157 больных) или плацебо (145 больных).
При наблюдении через 36 и 55 месяцев было установлено преимущество в отношении развития костных и висцеральных метастазов у больных, получавших клодронат, которое при анализе через 103 мес. нивелировалось. Однако, что более важно, в этот период отмечено значительное улучшение общей выживаемости (79,6% против 59,3% соответственно, р = 0,049).
Аналогичное исследование T. Powles и соавт., в котором не проводилась специальная селекция больных, выявил преимущество в отношении частоты развития метастазов в костях по сравнению с контролем (10). 1069 больных ранним раком молочной железы также получали клодронат 1600 мг/день в течение 2 лет или плацебо. При анализе через 2 года и 5 лет было показано, что на фоне приема клодроната значимо реже развивались метастазы в костях (снижение риска на 45,4% и на 30,8% соответственно). Более важно и то, что, как и в исследовании I.J. Diel, увеличивалась общая выживаемость у больных, получавших клодронат (снижение риска на 23,2%, р = 0,048). Это преимущество увеличивалось при исключении больных с I стадией рака молочной железы. При дальнейшей оценке больных, у которых развились костные метастазы (51 клодронат и 73 плацебо) ,было отмечено более частое развитие скелетных осложнений у больных, получавших плацебо.
Однако в исследовании T. Saarto и соавт. 299 пациенток с N+-операбельным раком молочной железы, которые в течение 3 лет получали клодронат 1600 мг внутрь или плацебо, были получены обратные результаты, не показавшие преимуществ адъювантного применения клодроната.
Тем не менее в настоящее время проводится несколько обширных исследований с клодронатом, золедроновой кислотой и ибандронатом (NSABP B-34, AZURE, ICE, GAIN, S0307), призванное дать окончательную оценку адъювантному применению бисфосфонатов, а также выделить группы больных, которым данная терапия будет особенно полезна.
Наиболее обширным в этой связи можно назвать исследование S0307, в которое планируется включить 6000 пациенток ранним раком молочной железы, распределенным в 3 ветви: клодронат 1600 мг/день, в течение 3 лет; бондронат 50 мг/день внутрь в течение 3 лет и золедроновая кислота 4 мг в/в в течение 6 мес., далее 4 мг каждые 3 мес. до 3 лет.
Все исследования, приведенные выше, показали незначительную токсичность, связанную с пероральным приемом клодроната. В связи со специальным интересом к развитию, на фоне бисфосфонатов, остеонекроза челюсти, G.R. Jones опубликовал отчет, из которого следует, что побочные эффекты, связанные с клодронатом, отмечаются у 6 на 10 000/год (12). Тем не менее, ни одного сообщения об остеонекрозе, остеомиелите или аваскулярном некрозе не отмечено.
Клодронат при раке предстательной железы
При раке предстательной железы было проведено 3 исследования, из которых одно адъювантное и 2 при метастазах.
D.S. Ernst и соавт. оценили анальгезирующий эффект клодроната 1500 мг в/в каждые 3 недели или плацебо у больных с гормонорезистентным раком предстательной железы с болевым синдромом на фоне химиотерапии митоксантрон + преднизолон (13). В исследование было включено 209 больных. Различий как в снижении боли, использовании анальгетиков, продолжительности противоболевого эффекта выявлено не было.
В исследовании D.P. Dearnaley оценено время до появления болевого синдрома у 311 больных гормоночувствительным раком предстательной железы с метастазами в костях (14). Больные получали клодронат 2080 мг/день или плацебо. В результате было показано, что снижение риска развития симптомных метастазов в костях составило 21%, однако различия были недостоверными (р = 0,066). Это же касалось и общей выживаемости (37,1 против 28,4 месяцев, р = 0,082). В то же время отмечено значительно меньшее число больных, у которых диагностировалось ухудшение общего состояния (р = 0,008).
В исследовании M.D. Mason было включено 508 больных, у которых в течение 3 лет после установления рака предстательной железы не было признаков костных метастазов (15). Больные получали клодронат 2080 мг/день или плацебо максимально до 5 лет. При медиане наблюдения 10 лет различий в частоте развития костных метастазов или общей выживаемости не было отмечено.
Клодронат при миеломной болезни
При множественной миеломе было проведено 2 плацебо-контролируемых исследования.
R. Lahtinen оценил 350 больных, получавших клодронат 2400 мг/день или плацебо в течение 24 месяцев (16). При оценке установлено, что в группе больных, получавших клодронат, значительно реже отмечалось прогрессирование костных метастазов (24 vs 12%, p = 0,026), вертебральных переломов (30% против 40%, различие не значимо). Значительно увеличилось число больных без болевого синдрома (с 24% до 54%, p < 0,001) в группе с клодронатом против 29% до 44%, p < 0,01 в группе плацебо.
Другое исследование, проведенное E.V. McCloskey и соавт., включало в себя 535 больных множественной миеломой (17). Пациенты получали клодронат 1600 мг/день. При медиане наблюдения 8,6 лет в общей группе различия в общей выживаемости не было отмечено (р = 0,38). Однако в группе больных, не имевших патологических переломов, преимущество в общей выживаемости было значительным (59 и 37 мес., р = 0,006), а 5-летняя выживаемость составила 46% и 35% соответственно.
Таким образом, можно отметить достаточную эффективность клодроната при метастазах в костях рака молочной железы и множественной миеломой, выражающейся в предупреждении скелетных осложнений и увеличении времени до их наступления у этих больных. Исследования у больных раком предстательной железы не показали пользы от применения клодроната.
Наиболее интересным являются результаты исследований по предупреждению развития метастазов в костях у больных ранним раком молочной железы, а также у больных с внекостными метастазами.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.