Комбинированная терапия больных доброкачественной гиперплазией простаты: анализ результатов 4-летнего исследования CombAT
- Аннотация
- Статья
- Ссылки


Наличие у пациента одного или нескольких упомянутых факторов риска значительно увеличивает вероятность прогрессирования заболевания. В связи с этим, особенную актуальность приобрела оценка эффективности медикаментозной терапии не только по влиянию на симптомы нижних мочевых путей (СНМП), но и по способности снижать риск таких последствий прогрессирования ДГПЖ, как острая задержка мочеиспускания (ОЗМ) и/или возникновение необходимости в оперативном вмешательстве.
В настоящее время установлено, что из препаратов, применяемых для терапии больных гиперплазией простаты, только ингибиторы 5α-редуктазы обладают способностью предотвращать прогрессирование заболевания (7). Опубликованное в 2003 г. исследование MTOPS (Medical Treatment оf Prostatic Symptoms) со средним периодом наблюдения за больными 4,5 года показало, что монотерапия ингибитором 5α-редуктазы финастеридом снижает риск клинического прогрессирования ДГПЖ на 34% по сравнению с плацебо, а при лечении в комбинации с α1-адреноблокатором риск клинического прогрессирования заболевания уменьшается на 66% по сравнению с плацебо (р < 0,001). Значимое снижение риска клинического прогрессирования на фоне комбинированной терапии отмечалось также и при сравнении с монотерапией финастеридом или доксазозином (р < 0,001 для обоих). Результаты исследования также продемонстрировали, что комбинированная терапия и монотерапия финастеридом, но не монотерапия доксазозином значительно снижала риск ОЗМ и необходимости оперативного вмешательства по поводу ДГПЖ (р < 0,001 для обоих) (7). Таким образом, было доказано, что комбинированное лечение ингибитором 5α-редуктазы и α1-адреноблокатором может быть целесообразным не только с точки зрения быстрого уменьшения расстройств мочеиспускания, но и для предотвращения развития осложнений ДГПЖ. Следует, однако, отметить, что при наборе больных в исследование MTOPS не устанавливались допустимые нижние границы для объема простаты и уровня ПСА, то есть для основных показателей, связанных с риском прогрессирования ДГПЖ. В результате, средний объем простаты в исследовании составил 36,3 см3, а средний уровень ПСА – 2,4 нг/мл, т.е. очевидно, что в исследование попали как пациенты с высоким, так и с низким риском прогрессирования заболевания.
В то же время, чрезвычайно востребованным представлялся сравнительный анализ возможностей комбинированной и монотерапии в отношении отдаленных исходов заболевания (ОЗМ, необходимость оперативного лечения) именно у пациентов с высоким риском прогрессирования ДГПЖ:
- с объемом простаты не менее 30 см3;
- ПСА не менее 1,5 нг/мл;
- с умеренными и выраженными СНМП по данным IPSS (не менее 12 баллов в исследовании CombAt) (8).
Именно такая когорта пациентов была рандомизирована в крупномасштабное двойное слепое 4-летнее исследование CombAT (Сombination of Avodart and Tamsulosin) с комбинацией Аводарта и тамсулозина. Заключительный анализ результатов данного исследования был представлен в конце 2009 г. на сайте журнала European Urology, а затем, уже в начале 2010 г., в основной, печатной версии этого издания (8).
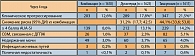
В исследовании приняли участие 4844 пациента, страдающих доброкачественной гиперплазией простаты и имеющих высокий риск прогрессирования заболевания (см. исходные характеристики пациентов в группах в таблице 1). Больные были рандомизированы в 3 группы:
- группа комбинированной терапии (дутастерид 0,5 мг/сут. + тамсулозин 0,4 мг/сут., n = 1610);
- группа лечения дутастеридом (0,5 мг/сут., n = 1623); группа лечения тамсулозином (0,4 мг/сут., n = 1611).
Лечение в группах продолжалось в течение 48 месяцев (8).
Основной целью исследования стало проведение сравнительной оценки эффективности 4-летнего комбинированного лечения (дутастеридом + тамсулозином) и монотерапии каждым из препаратов в отношении рисков развития ОЗМ или оперативного лечения, а также клинического прогрессирования ДГПЖ у мужчин, имеющих повышенный риск прогрессирования заболевания.
Анализ результатов через 2 года с начала терапии убедительно показал, что комбинированная терапия дутастеридом и тамсулозином (ДУТ+ТАМ) статистически значимо снижает суммарный балл IPSS, чем любой из монорежимов (в каждом из сравнений p < 0,001). Так, средние снижения IPSS, по сравнению с исходным значением, составили 6,2 балла для комбинированного лечения по сравнению с 4,9 и 4,3 для дутастерида и тамсулозина, соответственно. Было отмечено, что большее статистически значимое снижение балла IPSS от исходного наблюдалось для комбинированной терапии по сравнению с дутастеридом с 3-го месяца, а для комбинированной терапии по сравнению с тамсулозином – с 9-го месяца лечения. Немаловажно, что данное достоверное преимущество группы комбинированной терапии в сравнении с группой монотерапии тамсулозином в период от 24 до 48 месяцев продолжало увеличиваться (от 1,8 до 2,5 баллов), а по сравнению с монотерапией дутастеридом поддерживалось (от 1,3 до 0,96 баллов) (8).
Аналогичная тенденция через два года лечения наблюдалась и при оценке динамики изменения пиковой скорости мочеиспускания Qmax. Так, к 24-му месяцу в группе комбинированной терапии отмечено увеличение Qmax на 2,4 мл/с, что статистически значимо (p < 0,006) превосходило таковое в группе дутастерида и группе тамсулозина, где рост Qmax составил соответственно 1,9 и 0,9 мл/с. Достоверное преимущество комбинированной терапии по данному показателю отмечалось с 6 месяца лечения и сохранялось до конца периода лечения, до 48 месяцев.
К 48-му месяцу скорректированное среднее увеличение Qmax по сравнению с исходным значением составило 2,4 мл/с для группы комбинированной терапии по сравнению с 2,0 мл/с (p = 0,05) для группы дутастерида и 0,7 мл/с (p < 0,001) для группы тамсулозина.
Как уже отмечалось ранее, основной целью исследования было провести сравнительную оценку эффективности 4-летнего комбинированного лечения дутастеридом с тамсулозином и монотерапии каждым из препаратов в отношении рисков развития ОЗМ или оперативного лечения у больных ДГПЖ с высокой возможностью прогрессирования.
Для этого, в первую очередь, в группах анализировались время до события/доля пациентов с ОЗМ или оперативным вмешательством, обусловленными ДГПЖ. Установлено, что время до первого эпизода ОЗМ или до операции по поводу ДГПЖ было статистически значимо меньше в группе комбинированной терапии по сравнению с группой тамсулозина (p < 0,001). В то же время существенного различия между группой комбинированной терапии и группой дутастерида не отмечалось (p = 0,18). Когда ОЗМ и хирургическое вмешательство по поводу ДГПЖ были рассмотрены отдельно, время до первого события было значительно меньше на фоне комбинированной терапии по сравнению с группой терапии тамсулозином (p < 0,001).
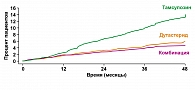
Весьма существенным результатом явилось то, что, уже начиная с 8-го месяца, в группе тамсулозина по сравнению с группой комбинированной терапии и дутастерида отмечалась значительно более высокая частота ОЗМ и/или операций по поводу ДГПЖ. Степень этого различия со временем, вплоть до 48-го месяца терапии, увеличивалась (рисунок 1, таблица 2).
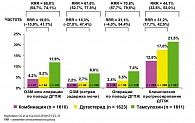
По состоянию на 48 месяц лечения комбинированная терапия снижала относительный риск развития ОЗМ или операции по поводу ДГПЖ на 65,8% по сравнению с тамсулозином и на 19,6% по сравнению с дутастеридом (р – статистически не значимо). При раздельном сравнительном анализе групп комбинированной терапии и тамсулозина в первой относительный риск ОЗМ снижался на 67,6%, а риск операции по поводу ДГПЖ уменьшался на 70,6%. При сравнении же с группой монотерапии дутастеридом, снижение относительного риска на фоне комбинированной терапии составило 18,3% для ОЗМ и 31,1% для операции по поводу ДГПЖ. Однако различие по времени до события между группами лечения было статистически не значимым (p = 0,37 и p = 0,074, соответственно) (рисунок 2).
Также, в ходе анализа оценивалось влияние терапии на общее клиническое прогрессирование ДГПЖ. Данное понятие применялось не только к больным с развившейся ОЗМ, но и к пациентам с увеличением степени выраженности симптомов по шкале IPSS на 4 и более баллов, с появившимися недержанием мочи, рецидивирующими инфекциями мочевых путей/уросепсисом или почечной недостаточностью, связанными с ДГПЖ. Время до первого эпизода клинического прогрессирования ДГПЖ значительно различалось в пользу комбинированной терапии по сравнению с тамсулозином и дутастеридом (p < 0,001 для обоих сравнений) (8).
Комбинированная терапия снижала относительный риск клинического прогрессирования ДГПЖ на 44,1% по сравнению с тамсулозином и 31,2% по сравнению с дутастеридом. Прогрессирование симптомов на 4 и более баллов по шкале IPSS было самым частым проявлением клинического прогрессирования в каждой группе лечения (таблица 3). Время до первого эпизода клинического прогрессирования ДГПЖ значительно различалось в пользу комбинированной терапии по сравнению с тамсулозином и дутастеридом (p < 0,001 для обоих сравнений) (8).
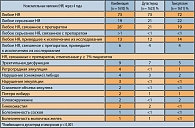
Таким образом, приведенные данные свидетельствуют о том, что у пациентов с высоким риском прогрессирования ДГПЖ комбинированная терапия дутастеридом и тамсулозином имеет ряд преимуществ перед каждым из монорежимов. При этом немаловажно, что хотя в группе комбинированного лечения частота препарат-ассоциированных нежелательных явлений была выше, это не оказало существенного влияния на переносимость терапии. В конечном итоге, частота отмены терапии по причине связанных с препаратом нежелательных событий была сходной во всех группах лечения (таблица 4).
Отличий в общей частоте сердечно-сосудистых явлений во всех группах лечения не отмечалось, несмотря на то, что частота диагноза «сердечная недостаточность» была выше в группах комбинированной терапии (14 из 1610; 0,9%) и монотерапии тамсулозином (10 из 1611; 0,6%), чем в группе монотерапии дутастеридом (4 из 1623; 0,2%). Следует отметить, что частота сердечной недостаточности (≤ 1%) во всех трех группах лечения в исследовании CombAT была ниже, чем частота событий в группе плацебо через 2 года в ключевых исследованиях 3-й фазы по ДГПЖ (1,3%).
Подводя итог можно заключить, что профиль наиболее часто отмечавшихся НЯ при применении комбинированной терапии соответствовал ранее выявленному при монотерапии каждым из препаратов, и в целом, комбинированная терапия хорошо переносилась в течение 4 лет исследования (8).
Заключение
С момента появления и развития медикаментозного направления в лечении больных с расстройствами мочеиспускания, обусловленными ДГПЖ, наиболее часто назначаемыми препаратами были α1-адреноблокаторы. Ингибиторы 5α-редуктазы применялись не так широко, что, по всей видимости, было связано с не столь быстрым и, возможно, не таким очевидным, как у α1-адреноблокаторов, эффектом от терапии. Однако опубликованные в последние годы результаты больших и долгосрочных исследований показали уникальную на сегодняшний день способность ингибиторов 5α-редуктазы существенно снижать риски прогрессирования заболевания.
Данные 4-летнего исследования CombAT свидетельствуют о высокой эффективности и изученной безопасности долгосрочного использования комбинированной терапии дутастеридом и тамсулозином у больных ДГПЖ с умеренными и выраженными СНМП, имеющих повышенный риск прогрессирования заболевания. Полученные результаты 4-летнего исследования CombAT поддерживают необходимость длительного использования комбинированной терапии дутастеридом и тамсулозином у мужчин со среднетяжелыми и тяжелыми СНМП вследствие ДГПЖ, имеющих повышенный риск прогрессирования заболевания (с объемом простаты не менее 30 см3, ПСА не менее 1,5 нг/мл).
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.