Мастер-класс по ведению коморбидных больных: внимание от общего к частному. XI Всероссийский съезд неврологов. Сателлитный симпозиум компании «Берлин-Хеми/А. Менарини»
- Аннотация
- Статья
- Ссылки




Ранняя диагностика и терапия болезни малых сосудов головного мозга
Профессор, д.м.н. Игорь Алексеевич ВОЗНЮК (Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе, Военно-медицинская академия им. С.М. Кирова) напомнил, что к цереброваскулярным болезням относится группа заболеваний головного мозга, обусловленных патологическими изменениями церебральных сосудов с нарушением мозгового кровообращения. Это может быть как поражение крупных магистральных и внутричерепных сосудов по типу стеноза при развитости и сохранности коллатеральных путей кровообращения, так и патология более мелких ветвей сосудистой системы головного мозга. Причины и механизмы развития и прогрессирования болезни мелких (малых) сосудов (БМС) в значительной степени не ясны. Считается, что повреждение вещества головного мозга при этом состоянии, вероятно, обусловлено не только поражением артериол и артерий малого калибра, но и вовлечением в патологический процесс капилляров и мелких вен.
Выделяют шесть основных типов БМС (при этом все типы взаимосвязаны):
- артериолосклероз;
- церебральная амилоидная ангиопатия;
- воспалительные и аутоиммунные БМС (васкулиты, инфекции);
- другие дегенеративные БМС (посттрадиционная ангиопатия, неамилоидная дегенерация микрососудов при болезни Альцгеймера);
- врожденная или наследственная БМС (болезнь Фабри, церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией, церебральная аутосомно-рецессивная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией);
- венозный коллагеноз.
Показано, что артериальная гипертензия, один из основных факторов развития БМС, не только изменяет структуру церебральных сосудов, вызывая гипертрофию и ремоделирование сосудистой стенки, способствует развитию атеросклероза крупных сосудов и липогиалиноза мелких сосудов, но и может блокировать феномен функциональной гиперемии (увеличение перфузии активированного участка мозга). Результатом нарушения функционирования пенетрирующих артерий и артериол становится расстройство механизмов ауторегуляции мозгового кровообращения и нарушение целостности гематоэнцефалического барьера1. Повышение проницаемости гематоэнцефалического барьера сопровождается экстравазацией компонентов плазмы как непосредственно в артериальную стенку (что ведет к ее утолщению и дезинтеграции), так и в прилегающие области мозга с развитием периваскулярного отека (что может быть одним из механизмов поражения белого вещества), а кроме того, процессами асептического воспаления. В белом веществе появляются обширные зоны неполных инфарктов с демиелинизацией, утратой олигодендроцитов и аксонов2. Ввиду более неблагоприятных условий кровоснабжения подкорковое и перивентрикулярное белое вещество полушарий головного мозга страдает в большей степени, чем серое вещество мозга, что обусловливает клиническую картину хронической ишемии мозга.
Следствием БМС может стать острое сосудистое (лакунарные инсульты, кровоизлияния) и хроническое диффузное поражение мозга с нарушением когнитивных функций, ходьбы, тазовыми расстройствами и другими симптомами. Их выраженность (негрубые изменения, изменения средней степени или тяжелые) зависит от степени поражения белого вещества. Один из заметных симптомов – изменение походки: неустойчивость, мелкий шаг, синдром «астазии – абазии», синдром «прилипших ног» (трудности с инициацией движения). Со временем снижается интеллект, нарушается оперативное мышление (синдром дезорганизации), что проявляется психомоторной замедленностью, потерей инициативности, нарушением функции планирования, ослаблением памяти. При прогрессировании заболевания когнитивный дефицит усугубляется, вплоть до деменции. Как правило, превалирует деменция альцгеймеровского типа (42%), несколько реже встречаются сосудистая деменция на фоне недостаточности мозгового кровообращения (24%) и смешанная деменция (22%). Кроме того, развиваются депрессия, апатия, психотические расстройства. Часто наблюдается недержание мочи. Все это в совокупности ведет к утрате пациентом независимости, инвалидизации и окончательно выключает его из социальной жизни.
В последние годы определены стандартизированные подходы к диагностике и интерпретации маркеров болезни мелких сосудов: множественных лакунарных инфарктов в глубинных отделах мозга, видимых расширений периваскулярных пространств (криблюр), диффузного поражения белого вещества (лейкоареоза), микроинфарктов, церебральных микрокровоизлияний, церебральной атрофии (таблица). Диагноз также может быть подкреплен данными лабораторных исследований. Выделяют несколько типов лабораторных маркеров: нейрональные (глутамат, гомоцистеин, тау-белок, нейроспецифическая энолаза, NR2-пептиды и NR2-антитела, N-ацетиласпартат), глиальные (белок S-100b, основной белок миелина, глиальный фибриллярный белок) и неспецифические (интерлейкины 1-бета, 6, 10, фактор некроза опухоли альфа, амилоидные пептиды, С-реактивный белок). Обнаружение маркеров позволяет предположить причину повреждения. Например, белок S-100b свидетельствует об ишемии на фоне артериальной гипертензии, гомоцистеин – о микроповреждении сосудов, основной белок миелина – о нарушении белого вещества, NR2-пептиды и NR2-антитела – о гипоксическом повреждении и т.д.
БМС имеет прогредиентный характер течения. Как правило, пациенты плохо отвечают на лечение даже в период стабильности симптомов, тем не менее в качестве терапевтических мишеней при БМС потенциально могут выступать гематоэнцефалический барьер, эндотелий и микрососудистая функция. «И безусловно, особое значение в лечебном процессе имеет адекватная гипотензивная терапия, поскольку артериальная гипертензия – наиболее важный модифицируемый фактор риска развития БМС», – подчеркнул профессор И.А. Вознюк.
Известно, что патологические процессы в мелких сосудах приводят к нарушению гематоэнцефалического барьера с миграцией протеинов плазмы через поврежденную сосудистую стенку, провоцируя нарушение циркуляции межклеточной жидкости в периваскулярных пространствах и активации макрофагов с развитием местного воспаления.
С учетом значения системного воспаления, можно предположить эффект от применения нестероидных противовоспалительных препаратов (НПВП). Однако высокая частота нежелательных явлений (гипертензия, гипергликемия, остеопороз, повышение риска сердечно-сосудистых событий, патология желудочно-кишечного тракта) при длительном использовании делает их назначение нецелесообразным.
«Есть средство, которое способно влиять на воспаление в эндотелии сосудов и микроциркуляцию. Это дипиридамол (Курантил)», – отметил профессор И.А. Вознюк. Препарат оказывает прямое антитромбоцитарное действие, тормозит экспрессию провоспалительных цитокинов и фактора некроза опухоли альфа. Дипиридамол ингибирует фермент, участвующий в разрушении аденозина, в результате чего повышается концентрация аденозина в тромбоцитах и эндотелии с развитием вазодилатирующего и антиагрегантного эффекта. Изменение динамики тромбоцитарной активности и васкулярной реактивности способствует улучшению церебральной перфузии. Следовательно, можно говорить о нейропротективном действии препарата, которое клинически выражается в виде улучшения когнитивных функций3. Еще одна важная особенность дипиридамола – способность стимулировать развитие капиллярной сети за счет действия аденозина на аденозиновые рецепторы в капиллярах. Таким образом, препарат способствует восстановлению поврежденного микроциркуляторного русла и активизирует процессы ангиогенеза4.
Благодаря тому что Курантил оказывает выраженное антиагрегантное, антиадгезивное, ангиопротективное, кардиопротективное, вазодилатирующее, противовоспалительное, антиоксидантное и иммуномодулирующее действие, его применение позволяет улучшить состояние пациентов при нарушениях микроциркуляции любого типа.
Персонализированный подход к ведению коморбидного пациента с диабетической полиневропатией и сопутствующей хронической ишемией мозга
По данным Всемирной организации здравоохранения, сейчас в мире насчитывается больше 500 млн человек с установленным сахарным диабетом (СД), больше 200 млн – с недиагностированным СД, больше 300 млн – со скрытым СД. Как отметил профессор, д.м.н. Евгений Робертович БАРАНЦЕВИЧ (Первый Санкт-Петербургский государственный медицинский университет), ввиду таких факторов, как постарение населения и высокая распространенность ожирения, число больных СД будет только расти. Еще одна важная проблема заключается в том, что, по данным Европейской ассоциации по изучению диабета, у 67% больных СД 2 типа в мире показатели гликированного гемоглобина выше целевых (6%) и не смогут опуститься до нормальных значений по целому ряду причин. Одна из них – отсутствие приверженности терапии и несоблюдение рекомендаций врача из-за когнитивных нарушений.
В мире каждые 10 секунд у трех человек развивается СД, а каждые 6 секунд один человек умирает от его осложнений – поражений сердечно-сосудистой, пищеварительной, нервной, мочеполовой, дыхательной систем, органов зрения. Закономерно, что еще в 2006 г. Всемирная организация здравоохранения признала СД неинфекционной эпидемией, представляющей для человечества не меньшую угрозу, чем вирус иммунодефицита человека/синдром приобретенного иммунодефицита.
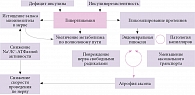
Более подробно профессор Е.Б. Баранцевич разобрал причины поражения нервной системы при СД, в частности диабетической полиневропатии (ДПН) – комплекса клинических и субклинических синдромов, каждый из которых характеризуется диффузным или очаговым поражением периферических нервных волокон и/или волокон автономной нервной системы в результате СД. Основными факторами в развитии патогенеза ДПН считаются нарушения в утилизации глюкозы (рисунок). Гипергликемия запускает каскад биохимических реакций, приводящих к дегенерации и демиелинизации нервного волокна. Избыток глюкозы также способствует повышенному образованию активных форм кислорода и последующему формированию окислительного стресса.
Долгое время поражение нервной системы считалось поздним осложнением СД, однако более широкое использование нейрофизиологических исследований показало, что практически все пациенты с СД и первого, и второго типа имеют клинические или субклинические неврологические нарушения. Если при СД первого типа ДПН возникает через несколько лет от дебюта заболевания, то при СД второго типа может быть его первым симптомом.
Выделяют разные варианты ДПН, отличающиеся по клиническим проявлениям, патогенезу, гистологическим изменениям, течению, реакции на лечение, прогнозу. Чаще всего в популяции встречается симметричная дистальная сенсорная полиневропатия. Клинические симптомы ДПН многообразны и могут включать сенсорную дисфункцию, двигательные и вегетативные нарушения в различных сочетаниях. К наиболее распространенным сенсорным симптомам относятся ощущение жжения, покалывания, режущая, колющая, стреляющая боль, аллодиния, онемение и парестезии в пораженных конечностях (покалывание, жжение), возникновение болей в ногах, усиливающихся по ночам.
Еще одно серьезное неврологическое осложнение СД – дисциркуляторная (диабетическая) энцефалопатия. Это медленно прогрессирующее многоочаговое или диффузное сосудистое поражение головного мозга, а также их сочетание. Клинически диабетическая энцефалопатия проявляется когнитивными расстройствами, органической неврологической симптоматикой, нарушениями сна, тревогой и депрессией. Развитие нарушений со стороны центральной нервной системы значимо ухудшает качество жизни этих пациентов и укорачивает их жизнь.
По данным магнитно-резонансной томографии, у пациентов с СД второго типа достоверно чаще, чем у лиц того же возраста без диабета, встречаются такие проявления дисциркуляторной энцефалопатии, как церебральная атрофия, лейкоареоз, «немые инфаркты». При этом выраженность этих нарушений со стороны центральной нервной системы коррелирует с тяжестью когнитивной дисфункции.
Далее профессор Е.Р. Баранцевич проанализировал подходы к терапии неврологических осложнений СД, отметив необходимость нормализации уровня гликемии. Однако достижение адекватного метаболического контроля не всегда приводит к регрессу неврологических нарушений, особенно при СД второго типа. В качестве патогенетической терапии ДПН отечественные эксперты рекомендуют назначать антиоксиданты, в частности альфа-липоевую кислоту (АЛК) и современные формы витаминов группы B5, 6. Надо отметить, что АЛК включена в Европейские рекомендации по лечению ДПН как единственное средство для патогенетически обоснованной терапии ДПН с подтвержденной эффективностью в нескольких рандомизированных контролируемых исследованиях и метаанализе (уровень рекомендаций А)7.
АЛК обладает двойным механизмом действия: прямым (связывание свободных радикалов) и непрямым (повышение содержания естественного антиоксиданта – глутатиона). Целесообразность назначения АЛК больным с недостаточной или плохой компенсацией СД подтверждена в большом количестве экспериментальных и клинических исследований. Было показано, что АЛК способствует уменьшению уровня глюкозы в крови, повышению синтеза гликогена и снижению инсулинорезистентности8, благоприятно воздействует на нервные волокна при ДПН, позволяет достичь долговременного улучшения функций нервов, особенно в нижних конечностях. Так, применение АЛК 600 мг/сут в таблетках в течение четырех лет предупреждало прогрессирование ДПН и развитие синдрома диабетической стопы9. Даже кратковременная терапия уменьшает основные симптомы ДПН, но показано, что длительный прием АЛК (в течение четырех – семи месяцев) более эффективен9–13. Кроме того, АЛК проявляет анальгетические свойства за счет улучшения состояния периферических нервных волокон, относящихся к соматосенсорной системе. Установлено, что инфузии АЛК 600 мг/сут в течение трех недель позволили быстро снизить выраженность болевого синдрома при ДПН14.
Один из наиболее часто назначаемых препаратов АЛК – Берлитион, который производится в Германии в соответствии со стандартами GMP. Результатом 74-дневной терапии Берлитионом стало уменьшение выраженности симптомов и улучшение биохимических показателей крови: глюкозы, гликированного гемоглобина, общего холестерина у пациентов с ДПН8. Рекомендуется следующая схема назначения Берлитиона: 600 мг/сут внутривенно капельно от двух до трех недель с дальнейшим переходом на 600 мг/сут перорально, длительность терапии на усмотрение врача (обычно два-четыре месяца).
Что можно использовать для профилактики и лечения диабетической энцефалопатии и нарушений микроциркуляции на фоне СД? По мнению докладчика, патогенетическая терапия диабетической энцефалопатии должна включать коррекцию эндотелиальной дисфункции, лежащей в основе микроангиопатии при СД, в том числе с помощью приема эндотелио- и ангиопротекторов, улучшающих реологические свойства и текучесть крови за счет снижения адгезии и агрегации тромбоцитов. Одним из таких препаратов является дипиридамол (Курантил).
Благодаря целому ряду эффектов Курантил может успешно использоваться при дисциркуляторной энцефалопатии на фоне СД. Он уменьшает окислительный стресс, тем самым вызывает обратное развитие периферической ишемии, снижает воспаление в эндотелии сосудов, улучшая микроциркуляцию. Кроме того, препарат расширяет сосуды, благоприятно влияет на реологию крови, нормализует венозный отток, стимулируя ангиогенез и коллатеральное кровообращение. Курантил также увеличивает образование и биодоступность оксида азота в тканях, что улучшает кровоток в периферических артериях.
«Курантил обладает плейотропными эффектами, а потому имеет преимущества в лечении коморбидных пациентов, в частности с СД и развившимися неврологическими осложнениями», – отметил профессор Е.Р. Баранцевич, завершая выступление.
Персонализированный подход к ведению коморбидного пациента с болью. Внимание к деталям
Как отметила профессор, д.м.н. Марина Викторовна ПУТИЛИНА (Российский национальный исследовательский медицинский университет им. Н.И. Пирогова), при назначении лечения врач апеллирует к стандартам (протоколам, клиническим рекомендациям и т.п.). Однако подход, основанный на применении единообразных правил ко всем пациентам, не учитывает индивидуальность конкретного больного. В клинической практике можно столкнуться с повышенной чувствительностью пациента к лекарству, похожей на передозировку, хотя доза соответствует возрасту и полу, частичной или полной толерантностью, несмотря на увеличение дозы, или парадоксальными реакциями, включающими совсем другие осложнения, чем те, которые могли бы быть вызваны механизмами действия препарата. Все эти проявления обусловлены индивидуальностью фармакологического ответа, который зависит от возраста, тяжести основного заболевания и сопутствующих заболеваний (особенно печени и почек). Однако основным фактором, в 50% случаев определяющим неэффективность лекарственных средств или нежелательные реакции, является генетика. В этой связи трудно переоценить значение фармакогенетики, которая изучает аллельные варианты генов, обусловливающих индивидуальные особенности фармакокинетических и фармакодинамических характеристик организма.
Генетический полиморфизм определяет три главных фенотипа метаболизаторов (лиц, принимающих лекарства): экстенсивные, медленные и быстрые. У экстенсивных метаболизаторов (их большинство среди населения) нормальная скорость метаболизма. У медленных метаболизаторов снижена скорость метаболизма, поэтому лекарственное средство может накапливаться в высоких концентрациях и приводить к развитию нежелательных реакций. Следовательно, в таких случаях нужно уменьшать дозу. Быстрые, или сверхактивные, метаболизаторы характеризуются повышенной скоростью метаболизма, которая не позволяет при стандартных дозах достичь терапевтической концентрации в крови. Им необходимо принимать лекарство в более высокой, чем экстенсивным метаболизаторам, дозе.
В настоящее время выделены гены-кандидаты, полиморфизмы в которых влияют на фармакологический ответ. В частности для оценки эффективности и безопасности НПВП клинически значимо изучение гена-кандидата CYP2C9, поскольку большинство НПВП метаболизируются ферментной системой цитохрома Р450 – изоформой CYP2C9. Полиморфизм гена CYP2C9 может влиять на фармакокинетику многих НПВП, например целекоксиба, флурбипрофена, ибупрофена, лорноксикама, диклофенака15. Сравнительный хемореактомный анализ таких популярных НПВП, как декскетопрофен, кетопрофен и диклофенак, выявил существенное различие профилей взаимодействия этих НПВП с ферментами цитохрома Р45016. Оказалось, что декскетопрофен снижает активность только четырех цитохромов: CYP17A1, CYP3A5, CYP4B1 (метаболизм стероидов) и CYP2D6 (метаболизм антиаритмиков, антагонистов адренорецепторов, антидепрессантов). А кетопрофен и диклофенак воздействуют на гораздо более широкий диапазон цитохромов Р450, что негативно сказывается на метаболизме омега-3 полиненасыщенных жирных кислот и витамина D.
«Всем пациентам проводить фармакогенетические исследования невозможно, да и не нужно, но в определенных ситуациях они необходимы, например при длительном применении лекарственных средств (сердечно-сосудистых, психотропных, гормональных) или высоком риске развития нежелательных лекарственных реакций», – отметила профессор М.В. Путилина.
Персонализированная терапия может рассматриваться шире, чем основанный на генетическом анализе прогноз лечебного эффекта. Еще один способ индивидуализировать лечение – учитывать фенотип заболевания. Например, известны три фенотипа болевого синдрома – метаболический, диспластический и воспалительный, каждый из которых требует различной диагностики и лечения. Более подробно докладчик рассмотрела метаболический фенотип, для которого характерны ожирение, высокая коморбидность (СД второго типа, артериальная гипертензия, ишемическая болезнь сердца), выраженная боль, наличие суставного синдрома. Таким пациентам показано выполнение ряда лабораторных анализов, в частности на обнаружение маркеров воспаления. Ожирение само по себе рассматривают как состояние хронического воспаления, поскольку адипоциты являются источником воспалительных цитокинов (фактора некроза опухоли альфа, интерлейкина 6, С-реактивного белка, ингибитора активатора плазминогена I типа). Адипоцит висцерального жира синтезирует фактор некроза опухоли альфа, который стимулирует интерлейкин 6, мощный регулятор продукции веществ острой фазы воспаления, таких как С-реактивный белок, ингибитор активатора плазминогена 1 и фибриноген.
Российские исследователи провели дифференциальный хемореактомный анализ глюкозамина сульфата и семи различных НПВП, что позволило выделить наиболее перспективные комбинации, в которых оба действующих начала максимально эффективно дополняют друг друга. Оказалось, что при метаболическом фенотипе для быстрого обезболивания более эффективной будет комбинация «глюкозамина сульфат + декскетопрофен (Дексалгин)», которая продемонстрировала высокий синергизм в отношении основных маркеров воспаления (фактора некроза опухоли альфа, матриксной металлопротеиназы 17, NF-κB, интерлейкина 6)17. Кроме того, декскетопрофен проявил дополнительные свойства, не обнаруженные у препаратов сравнения. Так, он наиболее выраженно ингибировал циклооксигеназу 2 (при концентрации 10 мкМ 90,9 ± 31% против 35–77 ± 31% для остальных НПВП) и конкурентно ингибировал D2-рецептор простагландина, который непосредственно опосредует эффекты провоспалительного простагландина D218. Для декскетопрофена также была наиболее характерна модуляция метаболизма провоспалительных лейкотриенов посредством ингибирования арахидонат-5-липоксигеназы (на 64% при концентрации 10 мкМ, остальные НПВП – 0–55%) и рецептора лейкотриена 1 (на 24% при 10 мкМ, остальные НПВП – 0–23%). Наконец, среди исследованных НПВП декскетопрофен проявлял наиболее выраженные ингибирующие свойства по отношению к различным матриксным металлопротеиназам (он ингибировал металлопротеиназы 1, 2, 3, 12, 13 в среднем на 46%). Помимо этого он высокоэффективно угнетал NF-κB и интерлейкин 6. Наконец, было показано, что декскетопрофен обладает наиболее благоприятным профилем лекарственного взаимодействия по сравнению с другими часто используемыми НПВП.
Профессор М.В. Путилина отметила, что после купирования острого болевого синдрома с помощью Дексалгина при необходимости дальнейшего лечения целесообразно назначать нимесулид (Нимесил), который воздействует на воспалительный и медиаторный компоненты ноцицептивной боли, а также центральную сенситизацию, характеризуется быстрым эффектом, устойчивым и благоприятным фармакокинетическим профилем и минимальными нежелательными явлениями. В комментарии экспертов, опубликованном в 2015 г., отмечается, что нимесулид хорошо переносится, при этом общий профиль его безопасности аналогичен другим НПВП, а риск развития желудочно-кишечных осложнений гораздо ниже. Установлено, что у пациентов с эрозивно-язвенными поражениями желудочно-кишечного тракта, получавших нимесулид в комбинации с противоязвенной терапией по поводу остеоартроза, не только не появлялись новые эрозии и язвы, но и исчезали имевшиеся эрозии слизистой оболочки желудка, а у трех больных произошла эпителизация язвы желудка. Это позволило сделать вывод о высокой анальгетической и противовоспалительной эффективности и безопасности препарата даже при сопутствующей патологии желудочно-кишечного тракта19.
Таким образом, для эффективного и быстрого устранения метаболического болевого синдрома на первой неделе лечения рекомендуется назначать Дексалгин в комбинации с глюкозамина сульфатом, после чего переходить на Нимесил в сочетании с хондроитина сульфатом.
Заключение
В рамках симпозиума обсуждались плейотропные фармакологические эффекты дипиридамола (препарат Курантил), перспективного средства, которое с успехом используется в лечении и профилактике нарушений мозгового кровообращения по ишемическому типу, дисциркуляторной энцефалопатии на фоне артериальной гипертензии и СД, а также в составе комплексной терапии при нарушениях микроциркуляции любого генеза.
Кроме того, анализировались перспективы применения АЛК (препарат Берлитион), универсального эндогенного антиоксиданта, который способствует уменьшению клинических проявлений ДПН, восстановлению температурной и тактильной чувствительности. При наличии у больного сочетанной цереброваскулярной патологии, например артериальной гипертензии и СД, АЛК может оказать дополнительный эффект ввиду положительного влияния на состояние микроциркуляции.
На примере болевого синдрома рассматривались возможности персонализированной терапии, в частности выбора того или иного НПВП с учетом результатов фармакогенетического тестирования чувствительности к конкретному препарату и фенотипа боли. Так, при метаболическом типе боли продемонстрирована эффективность декскетопрофена (препарат Дексалгин) в комбинации с глюкозамина сульфатом с дальнейшим переходом на нимесулид (препарат Нимесил) в сочетании с хондроитина сульфатом.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.