Никотинзаместительная терапия: возможности и ограничения
- Аннотация
- Статья
- Ссылки
- English
Введение
Употребление табака – одна из основных проблем общественного здравоохранения и предотвратимая причина заболеваемости и смертности в мире. По оценкам Всемирной организации здравоохранения, из 1,3 млрд курильщиков в мире 80% – жители стран с низким и средним уровнем дохода. В 2020 г. табак употребляли 22,3% населения планеты: 36,7% мужчин и 7,8% женщин. Несмотря на значительное снижение распространенности ежедневного курения, число курильщиков сигарет в мире увеличилось с 721 млн в 1980 г. до 967 млн в 2012 г. В 2020 г. этот показатель достиг 1,3 млрд [1, 2].
Продолжительность жизни курильщиков в среднем на 10–15 лет меньше, чем некурящих [3]. Курение ассоциируется с повышением бремени мутаций и риска развития злокачественных новообразований различной локализации, прежде всего рака легкого, вероятность летального исхода при котором может достигать 37% [4, 5]. Помимо участия в патофизиологии злокачественных новообразований курение является главной причиной хронических респираторных заболеваний, таких как хроническая обструктивная болезнь легких (ХОБЛ) [6, 7], а также основной детерминантой сердечно-сосудистых заболеваний – инфаркта миокарда, инсульта и заболеваний периферических артерий. У пациентов, страдающих артериальной гипертензией, даже при достижении оптимального контроля артериального давления курение служит независимым провокатором развития раннего атеросклероза [8]. Доказано, что 10–30% всех смертей от сердечно-сосудистых заболеваний (ССЗ) в мире связаны с курением. Экспериментальные, эпидемиологические и клинические исследования продемонстрировали нелинейную зависимость между дозой вдыхаемого сигаретного дыма и сердечно-сосудистым повреждением. Поэтому даже небольшая концентрация сигаретного дыма во вдыхаемом воздухе способна обусловить непропорционально высокий риск ССЗ [9]. Эта нелинейная тенденция объясняет, почему некурящие, но подвергающиеся пассивному курению люди имеют повышенный на 25–30% риск ССЗ. Крайне важно предупреждать всех пациентов с ССЗ избегать пассивного курения [3].
На сегодняшний день уточнены многие патофизиологические механизмы, инициированные курением. Курение увеличивает адгезию тромбоцитов и макрофагов и создает так называемую прокоагулянтную и воспалительную среду, в которой ускоряется развитие ССЗ. При этом повышается выработка провоспалительных цитокинов (фактора некроза опухоли альфа, интерлейкинов 1, 6, 8 и гранулоцитарно-макрофагального колониестимулирующего фактора). В то же время на фоне курения снижаются уровни противовоспалительных цитокинов, таких как интерлейкин 10. Курение приводит к повышению концентрации иммуноглобулина Е и предрасполагает к последующему развитию атопических заболеваний и бронхиальной астмы тяжелого течения. Курение снижает активность действия ингаляционных глюкокортикостероидов [10], стимулирует выработку протеаз и оксидантов альвеолярными макрофагами и нейтрофилами, что приводит к повреждению тканей и способствует развитию ХОБЛ [11]. Согласно метаанализу, курение практически в два раза повышает риск инфицирования туберкулезом (95%-ный доверительный интервал 1,46–2,04) [12]. Курение также увеличивает риск развития ряда интерстициальных заболеваний легких [13]. Давно доказана связь между курением и желудочно-кишечными заболеваниями (например, язвенной болезнью, воспалительными заболеваниями кишечника) [14–16].
Курение обусловливает более высокую восприимчивость к легочным бактериальным и вирусным инфекциям, вызывая структурные изменения в дыхательных путях и снижая активность иммунного ответа. Многочисленные исследования показали, что курильщики в два раза чаще заболевают гриппом и имеют более тяжелые симптомы по сравнению с некурящими [17, 18]. Кроме того, в эпоху пандемии COVID-19, вызванной коронавирусом SARS-CoV-2, получены данные, указывающие на то, что курение, возможно, утяжеляет прогноз при этой инфекции. Недавно проведенное исследование продемонстрировало, что у постоянно курящих людей или бывших курильщиков усилена экспрессия гена легочного ангиотензинпревращающего фермента 2, что приводит к повышенному риску связывания вируса и проникновения его в легкие [19]. Таким образом, курение представляет собой серьезную угрозу общественному здоровью и экономике всего мира. Отказ от курения представляется наиболее эффективной контрмерой.
Механизмы никотиновой зависимости
Как правило, курильщики не могут бросить курить самостоятельно вследствие развития у них никотиновой зависимости (НЗ), проявляющейся чрезвычайно сильным стремлением ощутить на себе фармакологические эффекты никотина. Подобное состояние представляет собой отдельную нозологическую единицу и не является просто вредной привычкой. Никотин – основная детерминанта табачной НЗ. Как и другие хронические заболевания, НЗ – хроническая рецидивирующая патология, требующая длительного комплексного лечения. НЗ имеет два компонента – физический и психологический [20].
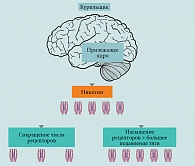
Механизм, ответственный за развитие зависимости и последующее хроническое и повторное употребление, основан на фармакодинамике никотина (рисунок). Никотин растворим в липидах, имеет скорость связывания с белками плазмы около 5% и легко проходит через гематоэнцефалический барьер. Он связывает специфические ацетилхолиновые рецепторы подтипов альфа-4-бета-2. При связывании с этими рецепторами открываются ионные каналы и высвобождается дофамин. Он вызывает кратковременное чувство удовольствия и вознаграждения. Затем никотин быстро метаболизируется в печени в котинин и выводится с мочой. В течение часа концентрация никотина снижается, рецептор инактивируется, и у курильщика вновь возникает сильная потребность в никотине [21]. При повторном курении развивается физическая НЗ. Никотин также участвует в высвобождении нейротрансмиттеров, таких как норадреналин, серотонин и гамма-аминомасляная кислота [22].
Степень НЗ оценивается количественно с помощью простых и проверенных временем инструментов скрининга – теста Фагерстрема [23] и индекса тяжести курения [24]. Баллы, полученные в результате этих тестов, могут предсказать как вероятность возобновления употребления табака после прекращения курения (рецидив), так и выбор наиболее благоприятной терапевтической стратегии для отказа от курения.
Как и другие синдромы патологической зависимости, НЗ характеризуется специфическим синдромом отмены. Синдром отмены никотина развивается в первые 4–12 часов после прекращения курения. Основные симптомы включают тягу к курению, раздражительность/агрессивность/ярость, тревогу, беспокойство, утомляемость, повышенный аппетит, трудности с концентрацией внимания, депрессию, головную боль, бессонницу, головокружение. Спектр симптомов у людей может быть разным. Все проявления носят временный характер и достигают наибольшей интенсивности в первые 24–72 часа, постепенно уменьшаясь в последующие три-четыре недели. У 40% пациентов симптомы обычно сохраняются свыше трех-четырех недель [25].
Эпидемиологические данные показывают, что НЗ является не только хроническим, но и рецидивирующим заболеванием. Рецидив означает возобновление регулярного курения после его прекращения. Рецидив считается распространенным явлением и возникает чаще всего в первые дни после попытки бросить курить, когда симптомы отмены обычно сильно выражены. Более чем у 75% людей, пытающихся бросить курить самостоятельно, в течение первой недели возникает рецидив, что делает этот период критическим [26]. Тем не менее риск рецидива распространен даже у курильщиков, которые отказались от курения в течение более длительного периода. У пациентов, воздерживающихся от курения не менее 12 месяцев, вероятность рецидива в течение жизни составляет 35% [25].
Принципы отказа от табакокурения
Для отказа от курения разработан алгоритм, известный как модель «5А» (спросите, посоветуйте, оцените, помогите и организуйте) [27]. Курильщикам, желающим бросить курить, рекомендуется оказать немедленную комплексную поддержку (фармакологическую и поведенческую). Пациентов, не желающих бросить курить, необходимо мотивировать.
НЗ предполагает самостоятельную титрацию. Поэтому, если пациент уменьшит количество выкуриваемых сигарет, он будет непроизвольно делать глубокие и частые затяжки сигаретой во время курения. Следовательно, уменьшение количества сигарет не является эффективным средством отказа от курения, и врачи не должны рекомендовать уменьшение количества сигарет пациентам, которые не могут самостоятельно бросить курить.
Лечение НЗ должно быть комплексным и включать как немедикаментозные стратегии (поведенческое консультирование), представляющие собой проверенные подходы к содействию процесса отказа от курения, так и фармакотерапевтические вмешательства.
Фармакотерапевтические вмешательства для прекращения курения
Для лечения НЗ разработан ряд фармакологических стратегий [28]. В общем виде фармакологические методы лечения для прекращения курения предусматривают применение никотинзаместительной терапии (НЗТ), варениклина, бупропиона и др.
Никотинзаместительные препараты – основа базовой терапии. Назначая препарат, врач определяет его дозу исходя из степени НЗ пациента, соблюдая принцип ступенчатой терапии. НЗТ основана на контролируемом введении никотина, что облегчает воздержание от курения за счет частичной замены поступления никотина. НЗТ направлена как на стимуляцию никотиновых рецепторов, что устраняет тягу к курению и симптомы отмены (эффект проявляется немедленно), так и на уменьшение количества никотиновых рецепторов (эффект проявляется медленнее и продолжается в течение нескольких недель, постепенно снижая табачную зависимость).
Контролируемое введение никотина при НЗТ мягко снижает эффекты, вызванные курением, благодаря более низкой дозировке и более медленной фармакокинетике. Никотин поглощается медленнее, вызывая более низкие, но продолжительные пиковые концентрации в крови по сравнению с сигаретами, что снижает симптомы отмены, включая раздражительность, беспокойство, трудности с концентрацией внимания, дисфорию, повышенный аппетит, увеличение веса и нарушения сна [25].
Каждый отдельный продукт НЗТ продемонстрировал одинаковую эффективность в достижении прекращения курения. Благодаря более благоприятному фармакокинетическому профилю комбинированная НЗТ (использование препаратов короткого и длительного действия) эффективнее монотерапии. Так, исследование комбинации никотинового пластыря и жевательной резинки показало, что комбинированный подход превосходит монотерапию [29]. Показатель отказа от курения на фоне комбинированной терапии составляет 34%, при использовании никотинового пластыря в режиме 12-недельной монотерапии – 24% (таблица).
Трансдермальные никотиновые пластыри доставляют никотин с относительно постоянной скоростью (контролирующие НЗТ), поэтому они считаются наиболее оправданным выбором для пролонгированного уменьшения симптомов отмены. В то же время жевательные резинки, пастилки, ингаляторы и назальные спреи (облегчающие НЗТ) ликвидируют симптомы быстрее, чем пластыри, но не обеспечивают долгосрочного эффекта [25].
Неконтролируемое использование никотиновых ингаляторов или спреев приводит к высоким пикам никотина в крови, сопровождающимся ощущениями, аналогичными традиционному курению, что замедляет процесс отказа.
Пероральные препараты НЗТ содержат никотин, который всасывается в слизистой оболочке полости рта. Основным недостатком НЗТ этого класса является необходимость следования строгой схеме дозирования, иногда с фиксированным коротким интервалом один-два часа. Кроме того, никотин всасывается слизистой оболочкой полости рта только при нейтральном значении рН во рту. В связи с этим пациенту следует избегать приема пищи или напитков во время или за 15 минут до приема препарата, а также исключить из рациона кислые продукты и напитки. К преимуществам ингаляторов относят имитацию курения сигарет – сохранение привычного при курении положения «руки во рту» [2, 25].
Продолжительность НЗТ индивидуальна. Терапия должна проводиться до тех пор, пока пациент не почувствует себя уверенно, чтобы избежать рецидива. Обычно продолжительность НЗТ составляет 12 недель. Доказано, что длительная НЗТ не связана с повышенным риском возникновения нежелательных лекарственных реакций. Пролонгированные курсы НЗТ особенно показаны пациентам с психическими расстройствами.
Хорошая переносимость НЗТ подтверждена клиническими исследованиями. Они не выявили повышенного риска нежелательных побочных явлений по сравнению с плацебо у пациентов с сопутствующей сердечно-сосудистой патологией. Исследователи отмечали некоторое учащение сердечно-сосудистых симптомов, таких как тахикардия, обусловленных, по всей видимости, действием никотина на симпатическую нервную систему [9].
Для всех продуктов НЗТ типичны такие нежелательные явления, как желудочно-кишечные симптомы (тошнота, рвота, боль в животе, диарея), головокружение, головная боль, местное раздражение в зависимости от способа введения препарата. Выраженность побочного эффекта, связанного с НЗТ, можно контролировать, регулируя дозу.
Пациенты часто интерпретируют симптомы как нежелательные явления НЗТ, а не как синдром отмены. Например, депрессия и нарушения сна – наиболее распространенные симптомы отмены, ошибочно принимаемые за побочные эффекты лечения.
Стандартная схема назначения НЗТ зависит от мотивации пациентов. Так, при наличии мотивации совместно с пациентом выбирается дата отказа, начиная с которой полностью прекращается потребление табачной продукции. Выбор начальных доз никотинсодержащих препаратов проводится с учетом степени НЗ и/или числа ежедневно выкуриваемых сигарет, а также выбора формы никотинсодержащего препарата.
Стандартная схема назначения жевательной резинки следующая. При полном отказе от табака количество жевательных резинок в сутки определяется степенью зависимости от никотина и обычно составляет 8–12 штук, но не более 15. Основной критерий – максимальное снижение симптомов отмены. Применять жевательную резинку в указанном количестве следует до трех месяцев. После этого ежедневное число резинок следует постепенно снижать до полной отмены. Жевательную резинку отменяют тогда, когда ее суточная доза составляет одну-две штуки в сутки. Регулярное использование жевательной резинки более 12 месяцев обычно не рекомендуется, однако в некоторых случаях требуется более длительная терапия, чтобы не возобновить потребление табака. Если при использовании максимальной дозы жевательной резинки симптомы отмены не удается контролировать, следует перейти на комбинированную НЗТ [2]
Длительность применения трансдермального пластыря составляет 12 недель. При выкуривании более 20 сигарет в день или степени никотиновой зависимости свыше 8 лечение проходит в три этапа, начиная с использования пластыря с максимальной дозой 25 мг, а затем доза постепенно снижается. Если пациент выкуривает 20 и менее сигарет в день или степень никотиновой зависимости более 6–8, лечение проводят в два этапа, начиная с пластыря в дозе 15 мг с последующим снижением дозы до 10 мг. При сохранении симптомов отмены применение пластыря продолжают или переходят на использование комбинированной терапии с применением других форм никотинсодержащих препаратов. В большинстве случаев применение трансдермального пластыря свыше шести месяцев не рекомендуется. Однако может потребоваться и более длительная терапия во избежание возобновления потребления табачных продуктов. Пациента необходимо предупредить о невозможности потребления табака и никотина при использовании трансдермального пластыря.
Спрей используют в период, когда обычно пациент потреблял табачные продукты, а также в случае появления тяги к их приему. В таких случаях необходимо сделать одно-два впрыскивания из спрея. Если после однократного впрыскивания тяга к табаку в течение нескольких минут не снижается, необходимо выполнить второе впрыскивание. При необходимости использования двух доз применение спрея может состоять из двух последовательных впрыскиваний. Большинству пациентов требуются одна-две дозы спрея каждые 30 минут или один час. Каждый час разрешается принимать не более четырех дозированных впрыскиваний спрея. Не следует впрыскивать более двух доз спрея одномоментно или применять более 64 доз в течение суток (или четыре дозы в час в течение 16 часов) [2].
Если в процессе оценки статуса курения выявлена средняя мотивация к отказу от табака и/или никотина, пациенту можно рекомендовать отсроченный полный отказ от табака с периодом предварительного снижения числа потребляемой табачной или никотинсодержащей продукции в день на фоне дискретного приема дозированного препарата. Пациент должен осознавать, что данная схема лечения направлена на полный отказ от табака/никотина, а предварительное снижение количества употребляемой продукции только подготовительный период, в процессе которого проводятся беседы по усилению мотивации к отказу от табака. Таким образом, сразу же с пациентом оговаривается дата полного отказа от табака/никотина, лечение разбивается на два этапа. Этап снижения количества употребляемой продукции не должен продолжаться более шести недель, но желательно его максимально сократить. Дозированный препарат выбирается по желанию пациента. Одновременное проведение мотивационного консультирования повышает эффективность терапии. После назначенной даты отказа от табака/никотина пациенту следует полностью прекратить употребление продукции и перейти только на прием НЗТ. На этапе полного отказа от табака/никотина можно использовать любую схему назначения НЗТ, включая комбинированную терапию, как и для мотивированных пациентов. При выборе любой схемы необходимо учитывать, что доза никотинсодержащих препаратов должна быть повышена по сравнению с дозой, которую пациент принимал в конце этапа снижения количества употребляемого продукта.
Заключение
Табакокурение – уникальное социально значимое общественное явление с доказанным патогенным действием на здоровье человека, многократно повышающее риск развития сердечно-сосудистых, легочных, злокачественных заболеваний и достоверно приводящее к преждевременной смерти курящего человека. Быстрое привыкание к потреблению табака и высокий уровень курения определяются выраженной никотиновой зависимостью – связыванию никотина с ацетилхолинергическими рецепторами головного мозга, активация которых приводит к выделению дофамина и норадреналина, изменению в психоэмоциональной сфере, ощущению удовольствия, возбуждению. Эти эффекты определяют статус комфортного самочувствия, формируют психическую и физическую зависимость, что относит потребление никотина при курении табака к классическим типам наркотического пристрастия. Стратегии отказа от курения следует применять в каждом клиническом контексте. Согласно результатам исследований, НЗТ может помочь людям, которые пытаются бросить курить, и увеличить их шансы на успешное прекращение курения. Никотинзаместительные препараты являются основой базовой терапии. НЗТ повышает частоту отказа от курения на 50–60%. Фармакологический подход к прекращению курения, основанный на НЗТ, безопасен и эффективен.
Ye.A. Leonova, O.V. Fesenko, PhD, Prof., A.S. Belousov, M.N. Agaragimova, Ye.A. Zolotova, Yu.A. Persova
Russian Medical Academy of Continuing Professional Education
City Clinical Hospital named after V.P. Demikhov
Contact person: Yelena A. Leonova, irileonova@yandex.ru
Tobacco consumption causes many diseases and poses a serious threat to public health around the world. Smoking is a chronic disease characterized by the development of addiction, mainly due to nicotine. Promoting smoking cessation is the most important intervention contributing to the maintenance of health for both smokers and non-smokers and saving financial costs. Nicotine replacement drugs are the basis of basic therapy. When prescribing the drug, the doctor determines the dose of the drug based on the degree of nicotine dependence of the patient, observing the principle of step therapy. Nicotine replacement therapy is aimed both at stimulating nicotine receptors, which eliminates cravings for smoking and withdrawal symptoms (the effect manifests itself immediately), and at reducing the number of nicotine receptors (the effect manifests itself more slowly and lasts for several weeks, gradually reducing tobacco dependence). The review provides data on the prevalence and consequences of smoking, analyzes the molecular basis of nicotine addiction, and evaluates the effectiveness and safety of nicotine replacement therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.