количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Новые возможности применения корректоров метаболизма в клинической практике
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Кардиология и Ангиология" №1
- Аннотация
- Статья
- Ссылки
В настоящее время в России высокая смертность населения является одной из наиболее сложных медико-демографических проблем. Это обусловлено не только высокой распространенностью, прежде всего, сердечно-сосудистых заболеваний (ССЗ), но и увеличением доли пожилых лиц и ассоциированных с возрастом сопутствующих состояний
(Верткин А.Л. и соавт., 2009).
(Верткин А.Л. и соавт., 2009).
В настоящее время в России высокая смертность населения является одной из наиболее сложных медико-демографических проблем. Это обусловлено не только высокой распространенностью, прежде всего, сердечно-сосудистых заболеваний (ССЗ), но и увеличением доли пожилых лиц и ассоциированных с возрастом сопутствующих состояний
(Верткин А.Л. и соавт., 2009).
(Верткин А.Л. и соавт., 2009).
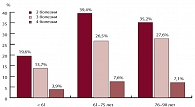
Рис. 1. Полиморбидность у пациентов в многопрофильном стационаре скорой медицинской помощи
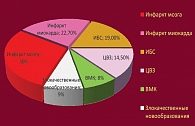
Рис. 2. Основные причины летальных исходов при полиморбидности

Таблица 1. Индекс полиморбидности (по Чарльсон)

Таблица 2. Степени риска послеоперационных венозных тромбоэмболических осложнений (по C. Samama и M. Samama, 1999)

Таблица 3. Риск сердечно-сосудистых осложнений (по Гольдману)
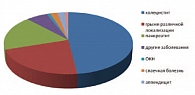
Рис. 3. Причины госпитализации в хирургический стационар
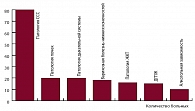
Рис. 4. Коморбидная патология у пациентов хирургического стационара

Таблица 4. Риски осложнений
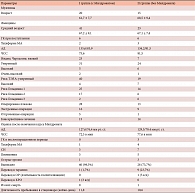
Таблица 5. Характеристика больных, получавших Милдронат
В настоящее время в России высокая смертность населения является одной из наиболее сложных медико-демографических проблем. Это обусловлено не только высокой распространенностью, прежде всего, сердечно-сосудистых заболеваний (ССЗ), но и увеличением доли пожилых лиц и ассоциированных с возрастом сопутствующих состояний (Верткин А.Л. и соавт., 2009).
Этот тезис наглядно иллюстрируется в структуре больных, поступающих в стационар с острыми хирургическими заболеваниями (ОХЗ) органов брюшной полости, доля которых в Москве ежегодно увеличивается на 3–5%. Справедливости ради следует отметить, что несмотря на сохраняющуюся тенденцию к росту этих заболеваний, летальность при этом продолжает снижаться, что, безусловно, связано с современными возможностями диагностики и лечения, внедрением малоинвазивных оперативных вмешательств и специализации хирургической помощи.
В то же время летальность от сопутствующей патологии и прежде всего у пожилых пациентов с кардиоваскулярными заболеваниями сохраняется высокой. Ситуация осложняется еще и тем, что у пожилых больных имеет место сочетание сразу двух или более сопутствующих заболеваний (рис. 1).
Для описания этого феномена предложен термин полиморбидность – состояние, обусловленное множеством патологических процессов (патоморфологических и патофизиологических), которые могут квалифицироваться как нозологические формы, синдромы, клинико-диагностические признаки и симптомы (Feinstein A.R., 1970; Akker M., Buntinx F., Knottnerus A., 1996; Yancik R., Ershler W., Satariano W., 2007). При ретроспективном анализе 3500 протоколов вскрытий умерших больных в многопрофильном стационаре в 2005–2007 гг. у 2751 (78,6%) была коморбидная патология. При этом несмотря на заболевания, составляющие коморбидность, причинами летальных исходов у них более чем в 90% случаях были острые и хронические сердечно-сосудистые заболевания (рис. 2).
Роль полиморбидности всегда отрицательная, как с клинической, так и с социальной точки зрения. Она утяжеляет течение ОХЗ, видоизменяет привычную клинику, осложняет и удлиняет по времени диагностику и лечение больных, способствует развитию послеоперационных и смертельных нехирургических осложнений (тромбозы и эмболии, острые эрозии и язвы слизистой оболочки верхних отделов ЖКТ, декомпенсация сердечной недостаточности, гнойно-септические процессы и др.). По нашим данным, 44,5% больных умирают от сочетания ОХЗ и ССЗ, 62,3% – от сердечной декомпенсации, каждый четвертый – от пневмонии, а каждый пятый – от острых эрозивно-язвенных повреждений слизистой верхних отделов пищеварительного тракта, осложненных желудочно-кишечными кровотечениями (ЖКК).
Полиморбидность нередко является причиной непрофильной госпитализации больных, низкой оперативной активности, увеличения затрат на диагностику и лечение заболеваний, длительности пребывания больных в стационаре. Так, в США примерно 80% расходов на медицинское обслуживание тратится на больных с четырьмя и более хроническими заболеваниями, а затраты на здравоохранение увеличиваются в геометрической прогрессии при увеличении количеств заболеваний (Wolff J.L., Starfield B., Anderson G., 2002; Valderas J.M., 2009).
Итак, пожилой возраст больных с ОХЗ, наличие полиморбидной патологии и, прежде всего, кардиоваскулярной с полиорганными нарушениями обусловливает необходимость оптимизации фармакотерапии этих пациентов на всех этапах ведения.
Как хорошо известно, концепция ведения хирургического больного, поступающего в приемное отделение многопрофильного стационара, определяется тяжестью состояния и наличием показаний к экстренному или плановому оперативному пособию.
Задачи врача в пред- и послеоперационный периоды различны. Так, в предоперационный период терапевт с учетом полиморбидной патологии должен:
Итоговый балл показывает, во сколько раз риск развития госпитальных осложнений и неблагоприятный исход заболевания выше у больных с полиморбидной отягощенностью. Так, при сумме до 3 баллов индекс полиморбидности (ИП) определяется как низкий, 3–6 баллов – умеренный, 7–9 баллов – высокий и более 9 баллов – очень высокий.
Затем на основании подсчитанного ИП совместно с хирургом определяется тактика ведения больного (оперативное лечение или консервативное ведение). У больных, которым показано оперативное лечение, терапевт, используя общепринятые шкалы, определяет прогноз возможных нехирургических осложнений в послеоперационном периоде. Среди них главное – риски сердечно-сосудистых и тромбоэболических осложнений (табл. 2, 3).
Этот тезис наглядно иллюстрируется в структуре больных, поступающих в стационар с острыми хирургическими заболеваниями (ОХЗ) органов брюшной полости, доля которых в Москве ежегодно увеличивается на 3–5%. Справедливости ради следует отметить, что несмотря на сохраняющуюся тенденцию к росту этих заболеваний, летальность при этом продолжает снижаться, что, безусловно, связано с современными возможностями диагностики и лечения, внедрением малоинвазивных оперативных вмешательств и специализации хирургической помощи.
В то же время летальность от сопутствующей патологии и прежде всего у пожилых пациентов с кардиоваскулярными заболеваниями сохраняется высокой. Ситуация осложняется еще и тем, что у пожилых больных имеет место сочетание сразу двух или более сопутствующих заболеваний (рис. 1).
Для описания этого феномена предложен термин полиморбидность – состояние, обусловленное множеством патологических процессов (патоморфологических и патофизиологических), которые могут квалифицироваться как нозологические формы, синдромы, клинико-диагностические признаки и симптомы (Feinstein A.R., 1970; Akker M., Buntinx F., Knottnerus A., 1996; Yancik R., Ershler W., Satariano W., 2007). При ретроспективном анализе 3500 протоколов вскрытий умерших больных в многопрофильном стационаре в 2005–2007 гг. у 2751 (78,6%) была коморбидная патология. При этом несмотря на заболевания, составляющие коморбидность, причинами летальных исходов у них более чем в 90% случаях были острые и хронические сердечно-сосудистые заболевания (рис. 2).
Роль полиморбидности всегда отрицательная, как с клинической, так и с социальной точки зрения. Она утяжеляет течение ОХЗ, видоизменяет привычную клинику, осложняет и удлиняет по времени диагностику и лечение больных, способствует развитию послеоперационных и смертельных нехирургических осложнений (тромбозы и эмболии, острые эрозии и язвы слизистой оболочки верхних отделов ЖКТ, декомпенсация сердечной недостаточности, гнойно-септические процессы и др.). По нашим данным, 44,5% больных умирают от сочетания ОХЗ и ССЗ, 62,3% – от сердечной декомпенсации, каждый четвертый – от пневмонии, а каждый пятый – от острых эрозивно-язвенных повреждений слизистой верхних отделов пищеварительного тракта, осложненных желудочно-кишечными кровотечениями (ЖКК).
Полиморбидность нередко является причиной непрофильной госпитализации больных, низкой оперативной активности, увеличения затрат на диагностику и лечение заболеваний, длительности пребывания больных в стационаре. Так, в США примерно 80% расходов на медицинское обслуживание тратится на больных с четырьмя и более хроническими заболеваниями, а затраты на здравоохранение увеличиваются в геометрической прогрессии при увеличении количеств заболеваний (Wolff J.L., Starfield B., Anderson G., 2002; Valderas J.M., 2009).
Итак, пожилой возраст больных с ОХЗ, наличие полиморбидной патологии и, прежде всего, кардиоваскулярной с полиорганными нарушениями обусловливает необходимость оптимизации фармакотерапии этих пациентов на всех этапах ведения.
Как хорошо известно, концепция ведения хирургического больного, поступающего в приемное отделение многопрофильного стационара, определяется тяжестью состояния и наличием показаний к экстренному или плановому оперативному пособию.
Задачи врача в пред- и послеоперационный периоды различны. Так, в предоперационный период терапевт с учетом полиморбидной патологии должен:
- определить степень компенсации имеющихся полиорганных нарушений с акцентом на кардиоваскулярную патологию;
- определить риск госпитальных и послеоперационных нехирургических осложнений;
- своевременно назначить адекватную терапию или провести ее коррекцию в рамках предоперационной подготовки;
- совместно с анестезиологом определить метод обезболивания.
- при отклонениях в привычном течении послеоперационного периода (одышка, боли в области сердца, аритмия и др.) проведение дифференциального диагноза и терапии возникших осложнений;
- оценка возникшей декомпенсации сердечно-сосудистой патологии;
- определение общих рекомендации (режим, диета, объем физических нагрузок) и лекарственной терапии, в том числе и при выписке пациента.
Итоговый балл показывает, во сколько раз риск развития госпитальных осложнений и неблагоприятный исход заболевания выше у больных с полиморбидной отягощенностью. Так, при сумме до 3 баллов индекс полиморбидности (ИП) определяется как низкий, 3–6 баллов – умеренный, 7–9 баллов – высокий и более 9 баллов – очень высокий.
Затем на основании подсчитанного ИП совместно с хирургом определяется тактика ведения больного (оперативное лечение или консервативное ведение). У больных, которым показано оперативное лечение, терапевт, используя общепринятые шкалы, определяет прогноз возможных нехирургических осложнений в послеоперационном периоде. Среди них главное – риски сердечно-сосудистых и тромбоэболических осложнений (табл. 2, 3).
После определения прогноза становится ясной и обоснованной необходимость профилактики этих осложнений по общепринятым позициям. Вместе с тем, современная клиническая особенность больных – полиморбидность – требует поиска лекарственных препаратов, влияющих не прицельно на один орган, а системно, на каждую клетку организма, испытывающую оперативный стресс. В настоящее время такие препараты существуют. Это корректоры метаболизма, способные предотвратить негативное воздействие кислородного голодания на жизнеспособность клеток. Наиболее изученным в этом плане является Милдронат, который предотвращает накопление токсических продуктов обмена веществ в клетке путем переключения метаболизма для образования АТФ со свободных жирных кислот на использование глюкозы. Сегодня имеются убедительные доказательства эффективности Милдроната при ИБС, сердечной недостаточности, периферического атеросклероза, острых ишемических повреждений мозга.
В связи с такими теоретическими предпосылками мы решили посмотреть эффективность Милдроната у хирургических больных с сердечно-сосудистыми заболеваниями в реальной клинической практике.
Цель исследования – определить эффективность Милдроната в условиях оперативного стресса у хирургических больных с коморбидной, прежде всего карлиоваскулярной патологией для снижения частоты послеоперационных нехирургических осложнений.
Материалы и методы
В исследование были включены 99 больных, госпитализированных в отделение общей хирургии многопрофильной больницы скорой медицинской помощи города Москвы. Среди пациентов было 64 женщин и 35 мужчин, в возрасте 64,4 ± 8,4 лет, из них 39 были госпитализированы в плановом порядке, 60 – по экстренным показаниям. Основными причинами госпитализации в хирургический стационар были острый холецистит и панкреатит, соответственно в 47% и 18%, а также в 22% грыжа различной локализации (рис. 3).
В течение 1–2 суток все пациенты были консультированы терапевтом, который диагностировал сопутствующую коморбидную патологию (рис. 4). Так, у большинства хирургических больных была диагностирована сердечно-сосудистая патология: у 81 больного – АГ, у 27 – хронические формы ИБС и у 10 – последствия перенесенного ОНМК. Среди пациентов с АГ 51 длительно страдают повышением АД, а 30 (37,03%) болели менее 5 лет. При этом постоянную терапию амбулаторно получали только 45 пациентов, а нерегулярно лечились 36 больных. 15 человек ранее переносили инфаркт миокарда, что доказывалось анамнестическими данными и рубцовыми изменениями на ЭКГ, в том числе у 7, по данным ЭхоКГ, были выявлены зоны гипо- и акинеза различной локализации. Клинические признаки сердечной недостаточности (СН) имели место у 17 больных, в том числе у 12 – IIА, у 3 – IIБ и у 2 – III стадии. 12 человек имели мерцательную аритмию. Амбулаторно только каждый второй больной с хроническими формами ИБС получал препараты ацетилсалициловой кислоты, а каждый пятый – статины, несмотря на современные клинические рекомендации.
Фоном для ССЗ у большей половины были атеросклероз аорты и ее ветвей (53,5%), абдоминальное ожирение (56,6%) и в 23,2% – СД типа 2, причем у 15 больных в стадии субкомпенсации и у 5 – декомпенсации, в 3 случаях диабет был выявлен впервые в жизни.
Помимо ССЗ у 20 больных была ХОБЛ, у 19 – варикозная болезнь ног, у 14 – язвенная болезнь желудка и 12-перстной кишки, у 21 – мочекаменная болезнь. Злоупотребляли алкоголем 10 больных, курили – 23. Инвалидность имели 44 пациента, в том числе 5 – по онкологическому заболеванию, 39 – по сердечно-сосудистой патологии.
В анамнезе 71 пациент ранее уже переносил какое-либо оперативное вмешательство, из них 36,6% – более двух операций: аппендэктомия (34 больных), холецистэктомия (12), грыжесечение (11), резекция или экстирпация щитовидной железы (9), флебэктомия (5), гинекологические операции (11) и др.
27 больных поступило в хирургический стационар в удовлетворительном состоянии, 71 – средней тяжести и 1 – в тяжелом. Примерно в половине случаев тяжесть состояния была обусловлена сопутствующей коморбидной патологией. Из поступивших больных 70 (70,7%) были прооперированы, в том числе в плановом порядке – 41, в экстренном – 26 и отсрочено – 3. Среди оперативных пособий на первом месте по частоте была выполнена холецистэктомия – 33 больных, 21 случай – грыжесечение, в 6 – операции по поводу кишечной непроходимости и спаечной болезни, в единичных наблюдениях ушивание перфоративной язвы желудка (2 случая), аппендэктомия (1), дренирование сальниковой сумки по поводу деструктивных форм панкреатита (3), панкреатодуоденальная резекция (1) и диагностическая лапаротомия (4). Большая часть оперативных вмешательств (51) выполнялась под эндотрахеальным наркозом, эпидуральная анестезия использовалась у 11 больных, местное обезболивание – у 8.
У всех больных были посчитаны риски:
- коморбидной отягощенности по Чарльсон – низкий индекс коморбидности имели 30 больных (30,3%), умеренный 55 (55,6%), высокий 11 (11,1%) и очень высокий 3 (3%);
- тромбоэмболических осложнений в послеоперационном периоде – 84,3% оперированных больных имели умеренный риск и только 15,7% больных – высокий;
- сердечно-сосудистых осложнений в послеоперационном периоде.
Результаты
По окончанию наблюдения в группе Милдроната показатели гемодинамики (АД, ЧСС) оказались в пределах референтных значений, но ниже, чем при поступлении больных. В этой группе не было зарегистрировано ни одного гипертонического криза, в отличие от группы контроля, где были зарегистрированы гипертонические кризы у 3 больных, в том числе у 2 – при экстренной и отсроченной операциях у пациентов с умеренным и высоким индексом коморбидности и у 1 больного с низким индексом по Чарльсон при плановом оперативном лечении.
На фоне приема Милдроната в послеоперационном периоде у больных с умеренным и высоким риском в 4 раза реже наблюдалась тахиситолическая форма мерцательной аритмии, симптомы СН и развитие острых эрозивно-язвенных повреждений слизистой верхних отделов ЖКТ.
В группе Милдроната в 1,7 раз реже встречалась пневмония, причем это осложнение фиксировалось только после операций, выполненных в экстренном порядке, и у неоперированных больных с очень высоким риском при наличии СН.
Мы констатировали развитие осложнений преимущественно у больных с умеренным и высоким коморбидным индексом. Однако в основной группе кардиоваскулярные осложнения (гипертонический криз, СН, тахисистолия) встречались реже, чем в группе контроля. С учетом того, что в обеих группах проводилась одинаковая предоперационная подготовка и разница между группами состояла только в добавлении Милдроната, можно сделать вывод, что кардиопротекция была обеспечена именно Милдронатом.
У больных обеих групп с очень высоким риском несмотря на терапию Милдронатом мы не получили положительных результатов, что может объясняться очень маленькой выборкой больных, изначальной тяжестью их состояния в связи с тяжелой декомпенсацией основной и сопутствующей патологии.
Заключение
Таким образом, терапевтическая коморбидность у лиц хирургического стационара составляет более 50%. Среди больных, имеющих коморбидную отягощенность, преобладают пожилые пациенты с 4–5 заболеваниями, а лидером по частоте коморбидной патологии является патология сердца и сосудов – риск госпитальных осложнений, связанный с коморбидностью, увеличивается с возрастом, пропорционально количеству нозологических форм.
Возникновение нехирургических осложнений в послеоперационном периоде определяет более тяжелое течение послеоперационного периода, что удлиняет пребывание больного в хирургическом отделении (увеличение койко-дня и снижение оборота койки), а подчас и перевод в отделения реанимации и интенсивной терапии или профильные отделения терапевтического профиля. Так, при низком и умеренном индексе коморбидности 94% пациентов были выписаны из хирургического отделения, 6% были переведены в терапевтическое отделение. Тогда как при высоком индексе только 43% больных выписаны и 50% больных этой группы были переведены в терапевтическое отделение для продолжения лечения в связи с развитием нехирургических осложнений в послеоперационном периоде.
Проведение предоперационной подготовки больных способствовало уменьшению частоты обострений ССЗ в послеоперационном периоде. Применение Милдроната рекомендовано в качестве дополнительной цитопротективной и кардиометаболической терапии у хирургических больных с низким, умеренным и высоким рисками полиморбидной отягощенности, подвергшихся оперативному вмешательству. Это позволяет снизить число нехирургических осложнений, и прежде всего сердечно-сосудистых.
Новости на тему
13.02.2025
14.05.2024
Отправить статью по электронной почте
Ваш адрес электронной почты:
В настоящее время в России высокая смертность населения является одной из наиболее сложных медико-демографических проблем. Это обусловлено не только высокой распространенностью, прежде всего, сердечно-сосудистых заболеваний (ССЗ), но и увеличением доли пожилых лиц и ассоциированных с возрастом сопутствующих состояний (Верткин А.Л. и соавт., 2009).
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
