Опыт применения иммуномодулятора Полиоксидоний для лечения ОРИ у детей
- Аннотация
- Статья
- Ссылки
- English
Учитывая особенности строения слизистой оболочки ротоглотки, а также процессы активации и миграции лимфоцитов в детском организме, обоснована целесообразность сублингвального применения препарата Полиоксидоний® для лечения инфекционно-воспалительных заболеваний верхних дыхательных путей.
Учитывая особенности строения слизистой оболочки ротоглотки, а также процессы активации и миграции лимфоцитов в детском организме, обоснована целесообразность сублингвального применения препарата Полиоксидоний® для лечения инфекционно-воспалительных заболеваний верхних дыхательных путей.





Острые респираторные инфекции (ОРИ) занимают лидирующее место среди инфекционных заболеваний у детей. Гриппом и острыми респираторными вирусными инфекциями (ОРВИ) ежегодно болеют от 65 до 72 тысяч детей в возрасте до 17 лет. В группе часто болеющих детей (ЧБД), составляющих от 15 до 75% в детской популяции, на долю ОРИ приходится 47–75% [1]. Известно, что группа ЧБД формирутся обычно в последние месяцы первого года и на втором году жизни, когда начинается переориентация иммунного ответа на инфекционные агенты со свойственного плодам и детям первого полугодия жизни Th2-ответа на Th1-ответ, типичный для инфекционного процесса у взрослых. Такие особенности иммунной системы ребенка обусловливают более высокую чувствительность его организма к инфекциям и менее дифференцированный ответ (по сравнению со взрослыми) иммунной системы на инфекцию.
Высокая восприимчивость к возбудителям ОРИ в раннем детском возрасте объясняется отсутствием иммунологической памяти предыдущих контактов с патогенами. При этом не происходит адекватного восстановления функциональных характеристик иммунной системы в случае повторяющихся ОРИ. Детей с повышенной заболеваемостью ОРИ, повторными ЛОР-инфекциями предложено рассматривать как иммунокомпрометированных и считать, что реального иммунодефицитного состояния у них, как правило, не бывает, но может выявляться преходящая функциональная нестабильность иммунитета, повышающая их восприимчивость к инфекции. Уровни интерлейкина (ИЛ) 10 в крови ЧБД как при ОРИ, так и без ОРИ достоверно значимо повышены в 10 раз по сравнению с редко болеющими детьми и нормальными показателями.
Вирусы, повреждая барьерную функцию мукоцилиарной системы респираторного тракта, нередко способствуют наслоению бактериальной инфекции с формированием вирусно-бактериальных ассоциаций, осложняющих клиническую картину и исход заболевания. У детей при первичной вирусной инфекции часто активируется эндогенная условно-патогенная микрофлора. Около 70% ОРИ поражают верхние дыхательные пути и область среднего уха. Одно из частых проявлений ОРИ у детей первых лет жизни – острый обструктивный ларинготрахеобронхит, развивающийся на фоне гиперчувствительности дыхательных путей, обычно в случае отягощенного аллергоанамнеза.
По нашим данным, этот синдром чаще встречается у детей второго и третьего года жизни с функциональной несостоятельностью иммунокомпетентных клеток, требующих повышения эффективности диагностики и лечения. Доказано, что при первичном и в большей степени рецидивирующем остром обструктивном ларинготрахеобронхите выражена гиперпродукция IgE и провоспалительных цитокинов (фактор некроза опухоли альфа, ИЛ-4, ИЛ-6, ИЛ-8) на фоне патологии Т- и В-клеточного звеньев иммунитета, а также клеток системы мононуклеарных фагоцитов и интерфероногенеза в сочетании с нарушениями микроциркуляторного гемостаза.
Острый обструктивный ларинготрахеобронхит при ОРИ сопровождается выраженными воспалительными изменениями в дыхательных путях, преимущественно в подсвязочном пространстве и области голосовых связок. Воспалительная реакция в респираторном тракте развивается с эффектами гиперчувствительности немедленного или замедленного типа. Появляется выраженный отек, обусловленный аллергическими реакциями при избыточной продукции лейкотриенов, провоспалительных цитокинов, накопления иммунного комплекса «IgE – антиген», индуцирующих выброс биологически активных веществ (гистамина, серотонина и др.) и запускающих аллергическое воспаление в верхних и нижних дыхательных путях по экссудативно-деструктивному варианту.
Для эффективной терапии необходимо применять средства, способные неспецифически стимулировать иммунную систему для повышения резистентности организма к любым патогенам и обладающие мембранопротекторными, антиоксидантными и противовоспалительными свойствами. Такими средствами в настоящее время являются иммуномодуляторы [2]. К препаратам, стимулирующим неспецифическую защиту организма, предъявляются такие требования, как эффективность, доступность, отсутствие токсичности и соответствие условиям неинъекционного применения. Перечисленным требованиям отвечает иммуномодулятор Полиоксидоний®.
Полиоксидоний® – высокомолекулярный, химически чистый иммуномодулятор, полученный с помощью направленного химического синтеза. Он представляет собой N-оксидированное производное полиэтиленпиперазина с молекулярной массой около 100 кДа. По своему химическому строению близок к соединениям природного происхождения. Оказывает иммуномодулирующее, дезинтоксикационное, антиоксидантное и мембранопротекторное действие. В основе механизма иммуномодулирующего эффекта препарата Полиоксидоний® лежит прямая активация фагоцитирующих клеток и естественных киллеров, а также стимуляция антителообразования. Препарат оказывает корригирующее влияние только на исходно измененные параметры иммунитета и не влияет на показатели, находящиеся в пределах нормальных значений.
Полиоксидоний® не нарушает естественных механизмов торможения иммунных реакций, не истощает резервных возможностей кроветворной системы. Его можно назначать больным как с выявленными, так и с невыявленными нарушениями иммунного статуса, то есть основанием для назначения является клиническая картина острого инфекционного заболевания. Наряду с иммуномодулирующим действием Полиоксидоний® характеризуется выраженной дезинтоксикационной активностью, которая определяется высокомолекулярной природой препарата. Полиоксидоний® – водорастворимый полимер, молекула которого состоит из 1000 элементарных звеньев. В длинной полимерной цепи препарата большое количество слабо заряженных групп (N-оксидные группы), обеспечивающих высокую адсорбционную способность полимера. Каждая молекула образует комплекс с молекулами эндо- и экзотоксинов и выводит их из организма.
Особенность препарата Полиоксидоний®, принципиально отличающая его от других иммуномодуляторов, в том, что его можно применять для лечения не только хронических, но и острых инфекционных заболеваний вирусной, бактериальной и грибковой этиологии. Полиоксидоний®, кроме иммуномодулирующих, имеет еще детоксикационные и антиоксидантные свойства, которые проявляются при лечении токсико-септических состояний. Применение Полиоксидония быстро уменьшает интоксикацию. Наряду с нормализацией иммунологических параметров снижается уровень общего и связанного билирубина, трансаминаз, креатинина, мочевины, повышается уровень гемоглобина, общего белка и альбумина, вероятнее всего, за счет детоксицирующего и антиоксидантного действия препарата. Применение Полиоксидония значительно повышает эффективность этиотропной терапии. По возбудителю наносится двойной удар: с одной стороны, бактерицидно или бактериостатически действующий антибиотик, с другой – Полиоксидоний®, повышающий киллерную способность фагоцитов и способствующий элиминации возбудителя из организма. В результате сокращается количество потребляемых антибиотиков и период госпитализации.
Полиоксидоний® значительно снижает чувствительность клеток к повреждающему действию лекарственных средств (антибиотиков, цитостатиков, противовирусных, гормональных препаратов и др.). Препарат хорошо переносится, не дает побочных эффектов, не обладает митогенной, поликлональной активностью, антигенными свойствами, не оказывает аллергизирующего, мутагенного, тератогенного и канцерогенного действия. Полиоксидоний® принимается один раз в сутки и позволяет достигать высокой приверженности пациента к лечению, оптимальный препарат для использования в педиатрии. Полиоксидоний® выпускается в трех лекарственных формах: лиофилизат для приготовления раствора для инъекций 3 мг и 6 мг (рег. номер 002935/02), суппозитории 6 мг и 12 мг (рег. номер 002935/03), таблетки 12 мг (рег. номер 002935/04).
Таблетированная форма более удобна, поскольку таблетки можно применять двумя способами – сублингвально и перорально. При сублингвальном применении Полиоксидоний® активирует лимфоидные клетки, находящиеся в бронхах, носовой полости, евстахиевых трубах, то есть в областях, которые являются входными воротами для любой инфекции. Как следствие, повышается устойчивость этих органов к инфекционным агентам. При пероральном применении Полиоксидоний® активирует лимфоидные клетки кишечника, а именно В-клетки, продуцирующие секреторные IgA, отвечающие за местный иммунитет. В результате повышается устойчивость дыхательного и желудочно-кишечного тракта к инфекционным агентам. Одна таблетка препарата Полиоксидоний® содержит 12 мг активного вещества. Полиоксидоний® с 1996 г. широко применяется в медицинской практике для лечения заболеваний различной этиологии с сопутствующими нарушениями иммунитета у взрослых и детей.
Иммуномодулирующие свойства препарата Полиоксидоний® связаны со способностью значительно повышать поглощение и разрушение бактерий фагоцитами, прежде всего за счет активации кислороднезависимых механизмов киллинга. Это способствует быстрому снижению количества бактерий в воспалительном очаге и их элиминации из организма. При развитии воспаления и избыточной продукции фагоцитарными клетками свободных радикалов (супероксид-анион-радикала, перекисных и гидроперекисных радикалов) Полиоксидоний® понижает их уровень. Как известно, активные формы кислорода, образуемые лейкоцитами, играют ведущую роль в деструкции клеток, органов и тканей при воспалении. Полиоксидоний® усиливает цитотоксические свойства естественных киллеров, тем самым активируя процессы элиминации из организма инфицированных и других модифицированных клеток организма. Усиливая функциональную активность тканевых макрофагов и дендритных клеток, расположенных под эпителием слизистых оболочек, препарат активирует развитие адаптивного иммунитета, осуществляющего завершение процесса борьбы организма с инфекцией. Полиоксидоний® является также активатором синтеза антител к инфекционным агентам. Он увеличивает эффективность кооперативного взаимодействия Т- и В-лимфоцитов в реакциях антителообразования в ответ на чужеродные антигены. Полиоксидоний® не нарушает естественных механизмов торможения иммунных реакций. В присутствии препарата происходит как формирование СD8+ клеток, так и функционирование уже сформировавшихся клеток. Стимуляция иммунитета с помощью препарата Полиоксидоний® не истощает резервных возможностей кроветворной системы.
Антиоксидантные свойства препарата Полиоксидоний® обусловлены его способностью уменьшать концентрацию каталитически активного двухвалентного железа в клетках в воспалительном очаге, что приводит к ингибированию перекисного окисления липидов и образованию активных форм кислорода. Детоксицирующие свойства препарата Полиоксидоний® связаны с особенностью его химической структуры и наличием в основной цепи макромолекулы множества активных N-оксидных групп, взаимодействующих с различными токсическими веществами. Полиоксидоний®, как губка, сорбирует на своей поверхности токсины, удаляет их из организма и делает работу иммунной системы более эффективной. Полиоксидоний® повышает устойчивость мембран клеток к цитотоксическому действию, снижает токсичность лекарственных препаратов и химических веществ. Сочетание иммуномодулирующих, антиоксидантных и детоксицирующих свойств делает препарат Полиоксидоний® одним из наиболее эффективных иммуномодулирующих средств с противовоспалительной активностью. Опыт применения в медицинской практике препарата Полиоксидоний® в течение 15 лет у взрослых и детей от 6 месяцев внутривенно, внутримышечно, перорально, сублингвально и интраназально свидетельствует о его высокой эффективности и безопасности при лечении больных с первичными и вторичными иммунодефицитными состояниями, аллергическими заболеваниями, аутоиммунными процессами. Применение Полиоксидония в комплексной терапии позволяет повысить эффективность действия антибактериальных, противогрибковых и противовирусных лекарственных средств, сократить сроки лечения и уменьшить количество потребляемых противоинфекционных средств.
Цель исследования
Оценить безопасность, переносимость и эффективность препарата Полиоксидоний® в таблетках 12 мг для лечения острых респираторных инфекций у детей в возрасте от 3 до 14 лет в качестве иммуномодулирующего и противовоспалительного средства при сублингвальном применении в течение 7 дней и последующего 6-месячного периода наблюдения в рандомизированном двойном слепом плацебоконтролируемом исследовании.
Материалы и методы
Для исследования были выбраны 100 пациентов в возрасте от 3 до 14 лет, страдающих острыми респираторными заболеваниями с явлениями острого обструктивного ларинготрахеобронхита средней степени тяжести на фоне ОРИ. Обязательным критерием включения в исследование являлось отсутствие в схемах терапии больных в течение последних 3 месяцев иммуномодулирующих препаратов. Мы не включали в исследование пациентов, имеющих какие-либо заболевания в стадии декомпенсации, которые могли повлиять на проведение исследования (органические поражения центральной нервной системы, декомпенсированная патология сердечно-сосудистой системы, больные с любыми проявлениями почечной или острой печеночной недостаточности, онкологические заболевания), а также с индивидуальной непереносимостью препарата Полиоксидоний®. Из 100 наблюдавшихся пациентов двое выбыли через 2 и 3 дня от начала исследования в связи с выпиской и отсутствием контакта с клиникой со стороны родителей.
Дизайн исследования строился следующим образом. Формировались основная группа, в которую вошли пациенты, получавшие Полиоксидоний®, и контрольная – получавших плацебо. Исследование состояло из периода скрининга, стартовой оценки в течение трех дней, семидневного периода терапии и последующего наблюдения в течение шести месяцев. Рандомизация – простая по методу случайных чисел (таблица генерировалась при помощи стандартной функции пакета статистических программ Statistica 6,0). Стадия скрининга начиналась за 3 дня до приема первой дозы исследуемого препарата. Проводимое обследование должно было установить, удовлетворяет ли пациент критериям включения/исключения. После включения в исследование больные начинали прием препарата Полиоксидоний® по схеме: таблетки 12 мг сублингвально за 20 минут до еды в дозе 6 мг детям от 3 до 9 лет и по 12 мг детям от 10 до14 лет два раза в день ежедневно в течение 7 дней. Завершал исследование контрольный осмотр пациента через 6 месяцев после проведения курса лечения препаратом Полиоксидоний®. Оставшиеся 98 пациентов были распределены случайным образом на 2 группы, сопоставимые по основным прогностическим признакам: основную (52 чел.) и контрольную (46 чел.). В основной группе 28 детей были в возрасте от 3 до 9 лет и 24 ребенка – от 10 до 14 лет, в контрольной группе – 24 и 22 соответственно.
Пациенты в возрасте от 3 до 9 лет получали Полиоксидоний® по 6 мг (1/2 таблетки), а в возрасте от 10 до 14 лет – 12 мг (1 таблетку) 2 раза в день (утро – вечер с интервалом 12 часов). Больные контрольной группы в возрасте от 3 до 9 лет получали плацебо по 1/2 таблетки, а в возрасте от 10 до 14 лет – 1 таблетку 2 раза в день (утро – вечер с интервалом 12 часов). Препарат и плацебо назначались всем пациентам за 20 минут до еды сублингвально ежедневно в течение 7 дней. В процессе наблюдения проводили ежедневный физикальный осмотр. Контроль лабораторных показателей общего анализа крови, биохимического анализа крови, общего анализа мочи, иммунологического исследования крови проводили до назначения и через 2–3 дня после отмены (перед выпиской) препарата; РНИФ-определение (реакция непрямой иммунофлюоресценции) IgM к респираторным вирусам выполняли до назначения и после отмены препарата. Эффективность препарата оценивалась на основании сравнительного анализа динамики купирования основных клинических симптомов заболевания и клинико-иммунологических показателей пациентов в основной и контрольной группах. В испытании применялся препарат Полиоксидоний® таблетки 12 мг производства ООО «НПО Петровакс Фарм».
Фармакологическая группа: иммуномодулирующие средства.
Способ применения: сублингвально детям от 3 до 9 лет (включительно) в дозе 6 мг (1/2 таблетки), детям от 10 до 14 лет в дозе 12 мг.
Безопасность применения Полиоксидония оценивалась по частоте и тяжести возникновения нежелательных явлений, лабораторным параметрам безопасности, а также по числу исключенных из исследования пациентов вследствие нежелательных явлений. Ни в одном случае при назначении препарата Полиоксидоний® не было зарегистрировано каких-либо нежелательных явлений. Статистический анализ данных по критериям эффективности проводился с использованием дисперсионного анализа. Различия по качественным показателям оценивались с помощью непараметрического критерия хи-квадрат. Различия по количественным показателям оценивались с помощью непараметрических методов (критерия Уилкоксона – Манна – Уитни) и/или t-критерия (параметрический метод). В качестве критерия статистической значимости принималась вероятность ошибки р < 0,05.
Результаты исследования
В соответствии с критериями включения для исследования были отобраны 98 детей в возрасте от 3 до 14 лет, у которых на момент поступления в больницу были клинические признаки острой респираторной вирусной инфекции в форме стенозирующего ларинготрахеита со стенозом гортани первой степени (51 чел.) и второй степени (25 чел.) и ларинготрахеобронхита без стеноза (18 детей, из них 4 – с признаками бронхообструкции). Пациенты были случайным образом распределены на 2 группы: основная группа – 52 и контрольная группа – 46 детей. Дети в обеих группах были сопоставимы по возрасту, полу и клиническим проявлениям ОРИ. В основной группе было 28 детей в возрасте от 3 до 9 лет и 24 – от 10 до 14 лет; 23 девочки и 29 мальчиков. В контрольной группе было 24 ребенка в возрасте от 3 до 9 лет и 22 – от 10 до 14 лет; 21 девочка и 25 мальчиков. Распределение больных по полу и возрасту представлено в табл. 1. В основной группе ларинготрахеит со стенозом гортани первой степени выявлен у 25 больных, второй степени – у 14 больных; у 13 детей наблюдали только симптомы ларинготрахеобронхита без стеноза, из них у 2 детей с признаками бронхообструкции. В контрольной группе проявления стеноза гортани первой степени на фоне ларинготрахеита диагностированы у 26 больных, второй степени – у 11 детей; у 9 пациентов был ларинготрахеобронхит без стеноза, из них у 2 с признаками бронхообструкции (табл. 2). В группе детей, получавших Полиоксидоний®, выявили следующие сопутствующие заболевания: хронический тонзиллит – в 36 случаях, аденоидит – 12, хронический отит – 6, хронический пиелонефрит – 2; атопический дерматит – 4; гипотонусную дисфонию – у 1 больного. У детей с атопическим дерматитом выявлена бытовая и сезонная пыльцевая сенсибилизация на злаки и сложноцветные (1 и 3 детей соответственно).
В группе детей, получавших плацебо, хроническим тонзиллитом страдали 23 ребенка, аденоидитом – 16, хроническим отитом – 4, хроническим пиелонефритом – 4, атопическим дерматитом – 5 больных. У больных с атопическим дерматитом в 1 случае выявлена бытовая и в 3 – сезонная пыльцевая сенсибилизация на деревья и злаковые травы. В целом из сопутствующих заболеваний наиболее часто наблюдалась патология ЛОР-органов (хронический тонзиллит, аденоидит). У 9 детей основной группы и у 8 контрольной ОРВИ осложнилась бактериальной инфекцией в виде отита и аденосинусита. У одного больного была диагностирована острая внебольничная полисегментарная пневмония. Диагноз пневмонии был установлен клинически и подтвержден в первые сутки поступления ребенка в больницу. Наблюдаемые больные находились в отделении боксированного режима обслуживания.
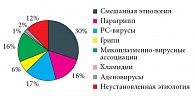
Больные поступали в первые 2 суток от начала заболевания с лихорадкой (интоксикация была умеренной или выраженной); у 100% больных воспалительные явления в носо-ротоглотке сопровождались ринитом, выраженной гиперемией, отеком миндалин, у старших детей при этом отмечались жалобы на боль в горле при глотании и/или в ухе при наличии острого среднего отита; у всех детей отмечался сухой грубый кашель без (или при слабой) продукции мокроты. В этиологической структуре ОРИ преобладала моноинфекция – выявлена у 59 (59%) больных. Микст-инфекция регистрировалась у 28 (28%) больных, инфекция неустановленной этиологии была у 12 (12%) детей. В микст-инфекции преобладали РС-вирусно-вирусные ассоциации и микоплазменно-вирусные ассоциации респираторных патогенов (рис. 1). Все больные независимо от группы наблюдения получали базисную терапию, которая включала:
- лечебно-охранительный режим (постельный – в период лихорадки и интоксикации с переходом на полупостельный – до выздоровления);
- диету (молочно-растительную), фруктовые соки, кисели; обильное питье в виде щелочных минеральных вод («Боржоми» с молоком и др.);
- противовоспалительные (Эреспал, Нурофен) и жаропонижающие средства при температуре 38,5 °С и выше (Нурофен или парацетамол в возрастной дозировке);
- муколитические средства (ацетилцистеин – АЦЦ, карбоцистеин) или отхаркивающие средства (Бронхикум, Амбробене, бромгексин, микстура с иодидом калия, мукалтин, термопсис, алтей и др.);
- бронходилататоры при обструктивном синдроме (Беродуал, Вентолин);
- при стенозе гортани – щелочные, с Беродуалом или Пульмикортом ингаляции, щелочные капли в нос, парокислородную палатку;
- антигистаминные препараты детям с аллергическими проявлениями: препараты 1-го поколения (Тавегил, Супрастин, Фенкарол, Димедрол и др.) или 2-го поколения (Кларитин, Зиртек).
- хорошая – при значительном клиническом улучшении общего состояния, исчезновении симптомов интоксикации и катаральных явлений в течение 2–3 дней лечения с последующим полным исчезновением признаков и симптомов инфекции;
- удовлетворительная – при улучшении общего состояния и исчезновении симптомов респираторного заболевания в течение первых 3 дней с неполным исчезновением признаков инфекции в течение периода последующего наблюдения, но без необходимости дополнительного лечения антибиотиками;
- нет эффекта – неудовлетворительный результат – при усилении симптомов инфекции как минимум после 72 часов лечения.
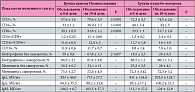
Сухой кашель исчезал быстрее с эффектом разжижения мокроты у детей основной группы – со 2-х суток, а с 3-х суток достоверных различий в его исчезновении и появлении влажного продуктивного кашля у детей обеих групп не выявили. Начало продукции мокроты в среднем составило у получавших Полиоксидоний® 2,6 ± 0,1 дня, а в группе плацебо – 2,9 ± 0,2 дня (табл. 3). В основной группе по сравнению с группой контроля сокращалось количество койко-дней, составив 6,6 ± 0,8 против 7,8 ± 1,5 дня (табл. 3). У больных, получавших Полиоксидоний® на фоне антибиотикотерапии, отмечено достоверное сокращение продолжительности ларинготрахеобронхита в сравнении с таковой в контрольной группе, что в среднем составило 6,0 ± 0,2 дня против 7,5 ± 0,5 дней (р < 0,001) соответственно. Также в основной группе статистически значимо сокращались сроки аденоидита, лихорадки и интоксикации (р < 0,05). Кроме того, у получавших Полиоксидоний® на фоне антибиотикотерапии, в отличие от детей, получавших только антибиотики, статистически достоверно быстрее исчезал сухой кашель со сменой на влажный – в течение 3,0 ± 0,1 против 4,2 ± 0,4 дня (р < 0,001) (табл. 4).
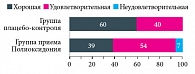
В динамике наблюдения у детей на фоне терапии препаратом Полиоксидоний® в сравнении с больными из контрольной группы не выявлено достоверных различий (то есть патологических изменений) в показателях периферической крови (общий анализ крови) (табл. 5), биохимии крови (табл. 6) и общего анализа мочи, что свидетельствовало о высоком профиле безопасности препарата Полиоксидоний®. Таким образом, в группе детей, получавших Полиоксидоний®, у 31 больного (60%) отмечен хороший эффект, у 21 (40%) – удовлетворительный эффект терапии. Ни у одного ребенка не отмечалось отсутствия эффекта. В контрольной группе хороший эффект наблюдался у 18 (39%) детей, удовлетворительный эффект – у 25 (54%) детей, отсутствие эффекта отмечалось у 3 (7%) пациентов (рис. 2). Отмечено значимое отличие (p < 0,05) между долями пациентов с хорошим эффектом терапии в обеих возрастных группах. Наблюдение за детьми в течение 6 месяцев после окончания терапии показало, что ни у одного ребенка, получавшего лечение препаратом Полиоксидоний®, не было выявлено отрицательной динамики в состоянии здоровья. После прекращения лечения (с марта до сентября) среди детей основной группы заболело 11 (22%) детей (25 случаев ОРИ, из которых 21 – повторный), в то же время среди детей, получавших плацебо, заболел 21 (42%) ребенок (40 случаев ОРИ, из них 28 повторных). Отмечается значимое отличие (p < 0,05) между долями пациентов, перенесших ОРИ, в обеих возрастных группах. При динамическом наблюдении оценивались показатели иммунного статуса до назначения терапии препаратом Полиоксидоний® или плацебо и спустя 10 дней от начала терапии. Отмечено достоверное улучшение показателей Т-клеточного звена (СD3+, СD4+, СD8+); фагоцитарной активности (нейтрофилов, моноцитов). В группе плацебо-контроля достоверного изменения указанных выше показателей в динамике наблюдения за больными не отмечено (табл. 7).
Обсуждение результатов
К группам риска по развитию стенозирующего (обструктивного) ларингита – крупа и/или бронхообструкции – относят ЧБД. На фоне частых ОРИ рецепторы поврежденного эпителия респираторного тракта приобретают гиперчувствительность к внешним воздействиям. В иммунном статусе у таких детей нередко транзиторно формируется ответ по Th2-типу с гиперпродукцией ИЛ-4 и ИЛ-5, стимулирующих высокую продукцию В-лимфоцитами IgE на фоне снижения синтеза IgA, ИЛ-2 и гамма-интерферона, выражена депрессия фагоцитарной активности макрофагов. На фоне указанных нарушений развивается аллергическое воспаление в верхних и нижних дыхательных путях по экссудативно-деструктивному варианту, что клинически сопровождается ларинго- и/или бронхообструкцией [1, 3, 4]. Первоочередной задачей в реабилитации таких детей является направленность терапии на снижение интенсивности антигенного воздействия (санацию очагов хронической инфекции, восстановление целостности эпителиального покрова респираторного тракта и повышение эффективности иммунных факторов защиты) [2, 3, 4]. На основании проведенных исследований можно утверждать, что Полиоксидоний® обладает иммуномодулирующей и противовоспалительной активностью, которая опосредуется через стимуляцию Т-клеточного ответа, фагоцитоза и антителообразования. Препарат нетоксичен и хорошо переносится детьми с 3-летнего возраста, что подтверждено отсутствием побочных и аллергических реакций в их состоянии, а также показателями периферической крови, биохимических тестов и общего анализа мочи.
Выводы
Основываясь на данных, полученных в ходе проведенного исследования по изучению безопасности, переносимости и эффективности препарата Полиоксидоний® в таблетках 12 мг для лечения острых респираторных инфекций у детей в возрасте от 3 до 14 лет, можно сделать следующие выводы.
- Применение препарата Полиоксидоний® в комплексной терапии ОРИ у детей позволяет быстрее добиться положительной динамики клинических симптомов ОРИ.
- Включение препарата Полиоксидоний® в комплексную терапию ОРИ у детей позволяет уменьшить потребность в длительной антибактериальной терапии.
- Полиоксидоний® способствует нормализации показателей Т-клеточного звена (СD3+, СD4+, СD8+) и фагоцитарной активности (нейтрофилов, моноцитов), в связи с чем представляется, что его использование в качестве иммуномодулятора у детей начиная с трех лет перспективно.
- В течение 6-месячного наблюдения за пациентами основной группы не было выявлено негативных изменений в состоянии здоровья, что свидетельствует о высоком профиле безопасности препарата Полиоксидоний® (таблетки по 12 мг).
- Через 6 месяцев после окончания лечения было отмечено сокращение в два раза частоты ОРИ среди детей, получавших Полиоксидоний®, по сравнению с группой, получавшей плацебо.
- Учитывая высокий профиль безопасности и клинико-иммунологическую эффективность, препарат Полиоксидоний® (таблетки по 12 мг) можно рекомендовать для применения в педиатрической практике у часто и длительно болеющих детей с 3-летнего возраста по схеме: детям от 3 до 9 лет по 6 мг и детям от 10 до 14 лет по 12 мг два раза в день сублингвально в течение 7 дней.
Immunomodulatory agent Polyoxidonium for treatment of acute respiratory infections in children
F.S. Kharlamova, Pirogov Russian State Medical University
V.F. Uchaykin, Pirogov Russian State Medical University
L.V. Kuzmenko, Peoples’ Friendship University of Russia
N.V. Chirun, LLC ‘NPO Petrovax Pharm’
T.P. Legkov, Morozovskaya Children’ s Clinical Hospital, Moscow
L.V. Feldfix, Morozovskaya Children’ s Clinical Hospital, Moscow
Contact person: Flora Semyonovna Kharlamova, kharlamova47@bk.ru
Sublingual Polyoxidonium® was administrated to 98 children with prolonged and recurrent respiratory infections (age 3-14 years old), chronic inflammation of pharyngeal lymphoid tissue ring (chronic adenoiditis, chronic tonsillitis, hypertrophy of palatine tonsils).
Treatment with Polyoxidonium® was associated with reduced hypertrophy of palatine tonsils and lower bacterial colonization of upper airway mucosa, improvement of local humoral immunity, activation of non-specific protective factors of the mucosa (lysozyme), decreased incidence and severity of URTI (upper respiratory tract infection). Any systemic and local adverse reactions were not reported.
Taking into account special characteristics of oropharyngeal mucosa and lymphocytes activation/migration in children, sublingual administration of Polyoxidonium® is advisable for treatment of infectious/inflammatory disorders of the upper airways.
Key words: children with recurrent respiratory infections, acute respiratory infections, acute obstructive laryngotracheobronchitis, Polyoxidonium
Учитывая особенности строения слизистой оболочки ротоглотки, а также процессы активации и миграции лимфоцитов в детском организме, обоснована целесообразность сублингвального применения препарата Полиоксидоний® для лечения инфекционно-воспалительных заболеваний верхних дыхательных путей.
