Оценка экспрессии генов – регуляторов созревания ооцитов в кумулюсных клетках у пациенток с повторными неудачами имплантации в анамнезе
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. Проведено сравнительное пилотное проспективное исследование. В основную группу вошли 19 пациенток в возрасте 18–40 лет с повторными неудачами имплантации и уровнем антимюллерова гормона в крови в диапазоне от 0,8 до 3,5 нг/мл. Группу сравнения составили девять доноров ооцитов.
В кумулюсных клетках полученных ооцитов определяли экспрессию генов AREG, STAR, PTGS2, HAS2 и SCD5 (метод количественной полимеразной цепной реакции) с использованием CFX96 Real-Time System (Bio-Rad, США).
Результаты. Выявлена достоверная корреляция между количеством бластоцист пятого дня развития и уровнем экспрессии гена амфирегулина в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов. Проведенный множественный регрессионный анализ показал зависимость количества полученных бластоцист пятого дня от экспрессии генов AREG, SCD5 в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов.
Заключение. Предположительно уровень экспрессии генов AREG и SCD5 в кумулюсных клетках фолликулов женщин можно использовать в качестве перспективного неинвазивного показателя компетентности полученных ооцитов. Ограничениями данного исследования являются малая выборка и группа пациенток с неудачами имплантации в анамнезе.
Необходимы более репрезентативные исследования с оценкой экспрессии генов AREG и SCD5 в кумулюсных клетках получаемых ооциткумулюсных комплексов у большего количества женщин с различными факторами бесплодия.
Материал и методы. Проведено сравнительное пилотное проспективное исследование. В основную группу вошли 19 пациенток в возрасте 18–40 лет с повторными неудачами имплантации и уровнем антимюллерова гормона в крови в диапазоне от 0,8 до 3,5 нг/мл. Группу сравнения составили девять доноров ооцитов.
В кумулюсных клетках полученных ооцитов определяли экспрессию генов AREG, STAR, PTGS2, HAS2 и SCD5 (метод количественной полимеразной цепной реакции) с использованием CFX96 Real-Time System (Bio-Rad, США).
Результаты. Выявлена достоверная корреляция между количеством бластоцист пятого дня развития и уровнем экспрессии гена амфирегулина в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов. Проведенный множественный регрессионный анализ показал зависимость количества полученных бластоцист пятого дня от экспрессии генов AREG, SCD5 в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов.
Заключение. Предположительно уровень экспрессии генов AREG и SCD5 в кумулюсных клетках фолликулов женщин можно использовать в качестве перспективного неинвазивного показателя компетентности полученных ооцитов. Ограничениями данного исследования являются малая выборка и группа пациенток с неудачами имплантации в анамнезе.
Необходимы более репрезентативные исследования с оценкой экспрессии генов AREG и SCD5 в кумулюсных клетках получаемых ооциткумулюсных комплексов у большего количества женщин с различными факторами бесплодия.





Введение
Бесплодие представляет собой состояние, характеризующееся нарушением репродуктивной функции у мужчин и женщин и проявляющееся в невозможности достижения беременности при регулярной половой жизни без применения методов контрацепции в течение 12 месяцев. Согласно последним данным Всемирной организации здравоохранения, проблема бесплодия затрагивает 17,5% взрослого населения.
Вспомогательные репродуктивные технологии (ВРТ) признаны самыми эффективными методами лечения бесплодия. Главные задачи преодоления бесплодия с помощью ВРТ – наступление беременности и рождение здорового ребенка. Основной путь достижения повышения частоты наступления беременности и живорождений – отбор эмбриона лучшего качества для переноса в матку, то есть эмбриона с высоким потенциалом имплантации и развития.
В клинической практике для снижения риска возникновения многоплодной беременности рекомендуется проводить селективный перенос только одного эмбриона в соответствии с клиническими рекомендациями Минздрава России [1]. Для выбора эмбриона используют как морфологические критерии (классификация бластоцист по Гарднеру), так и дополнительные инвазивные и неинвазивные методы (морфокинетика, преимплантационное генетическое тестирование на анеуплоидии). Предпочтительны неинвазивные методы, не требующие биопсии эмбриона. Оценка качества ооцита, из которого получен эмбрион, представляется дополнительным высокоинформативным инструментом для выбора эмбриона с максимальным потенциалом имплантации.
Качество эмбрионов во многом определяется качеством гамет, использованных для оплодотворения, – ооцитов и сперматозоидов. Именно поэтому возможность оценки ооцита, использованного для получения эмбриона, может стать дополнительным инструментом выбора при селективном переносе. Для определения пригодности ооцитов к использованию в программах экстракорпорального оплодотворения (ЭКО)/криоконсервации выполняют морфологическую оценку, включающую установление степени мейотической зрелости, а также выявление и фиксацию в протоколе морфологических дисморфизмов различных структур ооцита, которые существенно влияют на клинические исходы [1].
Во время фолликуло- и оогенеза между клетками ооциткумулюсного комплекса (ОКК) формируются тесные взаимосвязи посредством щелевых контактов [2]. В результате между ооцитом и кумулюсом происходит перенос питательных веществ и сигнальных молекул, что обеспечивает взаимное влияние при созревании ооцита. Избыточные кумулюсные клетки, окружающие ооцит, часто удаляют непосредственно при получении ОКК. Несколько слоев клеток вокруг ооцита оставляют для удобства дальнейших манипуляций.
В настоящее время появляется все больше исследований, в которых кумулюсные клетки используются в качестве дополнительного неинвазивного маркера качества яйцеклеток, поскольку можно контролировать, от какого ооцита получены кумулюсные клетки. Предлагаемые методы позволяют получить данные достаточно быстро. Таким образом, кумулюсные клетки служат мощным инструментом для получения информации о компетентности ооцита.
Хорионический гонадотропин человека (ХГЧ) и лютеинизирующий гормон (ЛГ) индуцируют быструю кратковременную экспрессию факторов, подобных эпидермальному фактору роста (EGF), – амфирегулина (AREG) и эпирегулина (EREG) – в пристеночных гранулезных и кумулюсных клетках. AREG и EREG индуцируют экспрессию простагландинсинтазы 2 (PTGS2, также называемой COX2) и HAS2, которые необходимы для синтеза и стабилизации внеклеточного матрикса кумулюсных клеток, экспансии кумулюса и последующей овуляции. Эти гены в исследованиях методом полимеразной цепной реакции в режиме реального времени (рПЦР) рассматривались как потенциальные биомаркеры для анализа транскриптома кумулюсных и гранулезных клеток [3, 4].
L.J. McKenzie и соавт., изучая связь между экспрессией генов в кумулюсных клетках и развитием эмбрионов in vitro, проанализировали уровень экспрессии HAS2, PTGS2 и GREM1 в ооцитах человека в зависимости от их зрелости, оплодотворения и качества эмбрионов [5]. P. Feuerstein и соавт. оценили транскрипцию генов, активность которых повышается в кумулюсных клетках в ответ на предовуляторный всплеск ЛГ, предшествующий экспансии кумулюса, – стероидогенный острый регуляторный белок STAR, PTGS2, AREG, две стеароил-коэнзим А-десатуразы SCD1 и SCD5 [4]. Уровни экспрессии всех изученных генов повышались после возобновления мейоза. Установлено, что созревание ядра связано с повышенной экспрессией STAR, PTGS2, AREG, SCD1 и SCD5 кумулюсными клетками.
Основываясь на данных литературы, для исследования мы отобрали гены AREG, STAR, PTGS2, HAS2 и SCD5. К сожалению, в указанных выше исследованиях детально не сопоставляли данные об экспрессии генов интереса с анамнезом пациенток. Однако исследование взаимосвязи данных анамнеза и молекулярных маркеров качества ооцита позволит скорректировать применяемый протокол с учетом индивидуальных особенностей и тем самым повысить эффективность применения ВРТ.
Цель данного исследования – оценить уровни экспрессии генов AREG, STAR, PTGS2, HAS2 и SCD5 в кумулюсных клетках здоровых доноров и пациенток с повторными неудачами имплантации в анамнезе.
Материал и методы
В основную группу вошли 19 пациенток с повторными неудачами имплантации.
Критерии включения:
- наличие двух и более неудач имплантации после программы ЭКО;
- возраст 18–40 лет;
- нормальные показатели овариального резерва, уровень антимюллерова гормона (АМГ) – 0,8–3,5 нг/мл, уровень фолликулостимулирующего гормона (ФСГ) в сыворотке крови на третий день ниже 12 МЕ/л;
- информированное согласие на участие в исследовании.
Критерии исключения:
- хронические соматические заболевания, препятствующие имплантации эмбрионов;
- получение сперматозоидов для оплодотворения оперативным доступом.
Группу сравнения представляли девять доноров ооцитов.
Получение клеток кумулюса
Всем участницам исследования осуществлялась контролируемая овариальная стимуляция препаратами ФСГ с антагонистами гонадотропин-рилизинг-гормона (ГнРГ). В качестве триггера финального созревания ооцитов использовался рекомбинантный ХГЧ 250 мкг (Овитрель, Merck Serono, S.p.A., Италия) или агонист ГнРГ 0,1 мг (Декапептил, FERRING, GmbH, Германия) по стандартному протоколу. Через 36 часов проводили трансвагинальную пункцию фолликулов. Фолликулярная жидкость с кумулюсными клетками от 1–4 фолликулов каждой пациентки поступала эмбриологу, который часть кумулюсных клеток отделял с помощью препарационных игл. Полученные клетки помещали в культуральную среду Flushing Medium (Origio, США). В день забора клетки кумулюса помещались в питательную среду при температуре 37 °С и доставлялись в лабораторию для выделения РНК.
Выделение РНК и получение кумулюсной ДНК
РНК из кумулюсных клеток выделяли с помощью набора RNA Solo («Евроген», Россия). Для получения кумулюсной ДНК (кДНК) осуществляли реакцию обратной транскрипции с помощью набора MMLV RT kit («Евроген», Россия) праймерами олиго(dT)16. Затем полученную однонитевую кДНК использовали в качестве матрицы для проведения рПЦР.
Олигонуклеотиды
Для определения кДНК применяли следующие пары праймеров: STAR, AREG, SCD5, PTGS2, HAS2 [3, 4].
кПЦР
Количественную ПЦР (кПЦР) выполняли с использованием CFX96 Real-Time System (Bio-Rad, США). В реакционную смесь 5X qPCRmix-HS SYBR («Евроген», Россия) добавляли 5 нг кДНК, а также праймеры до конечной концентрации 2 мкм.
При амплификации использовали следующий протокол: 95 °С в течение трех минут, затем 39 циклов при 95 °С в течение десяти секунд, 58 °С в течение 35 секунд. Детекцию флюоресцентного анализа проводили после стадии отжига (двухэтапный протокол). Уровни экспрессии мРНК рассчитывали методом 2-ΔΔCt.
Экспрессию генов нормализовали к двум референсным генам GAPdH и B2M.
Все эксперименты выполняли в трех технических и трех биологических повторностях. Эффективность рПЦР оценивали методом серийных разведений.
Статистическая обработка
Статистический анализ выполняли с помощью программы StatTech v. 4.8.11 (разработчик – ООО «Статтех», Россия). Статистический анализ результатов рПЦР проводили с использованием GraphPad Prism 8.0.
Количественные показатели оценивали на соответствие нормальному распределению на основании критерия Шапиро – Уилка.
Количественные показатели, выборочное распределение которых соответствовало нормальному, описывали с помощью средних арифметических величин (M) и стандартных отклонений (SD). В качестве меры репрезентативности для средних значений указывали границы 95%-ного доверительного интервала (95% ДИ).
В отсутствие нормального распределения количественные данные описывали с помощью медианы (Me) и нижнего и верхнего квартилей (Q1–Q3).
Категориальные данные представлены в виде абсолютных значений и процентных долей. 95% ДИ для процентных долей рассчитывали методом Клоппера – Пирсона.
Прогностическая модель, характеризующая зависимость количественной переменной от факторов, разработана методом линейной регрессии.
Различия считались статистически значимыми при p < 0,05.
Результаты
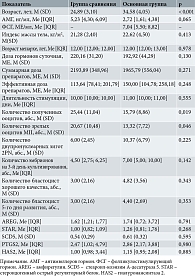
В таблице 1 представлены данные сравнительного анализа исследованных показателей у доноров ооцитов и пациенток с повторными неудачами имплантации.
Выявлена достоверная разница в общем числе полученных ооцитов, а также зрелых ооцитов в группе доноров ооцитов. Зафиксирована также существенная разница в возрасте участниц обеих групп. Остальные показатели, включая средние показатели экспрессии изучаемых генов в клетках кумулюса, достоверно не отличались. Отсутствовала и разница в группах по частоте наступления беременности. Наряду со сравнительным статистическим анализом был проведен корреляционный анализ зависимости выбранных показателей эффективности стимуляции от показателей овариального резерва и экспрессии изучаемых генов в клетках полученных ОКК.
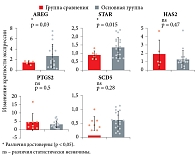
При количественной оценке уровня матричной РНК (мРНК) генов интереса в клетках кумулюса здоровых доноров и пациенток с повторными неудачами имплантации выявлены достоверные различия в экспрессии генов AREG и STAR (рисунок). Количество мРНК AREG (2,26 ± 1,8) и STAR (1,3 ± 0,5) в клетках кумулюса в основной группе было достоверно выше, чем в группе сравнения (1,45 ± 0,31 и 0,89 ± 0,24 соответственно). По остальным проанализированным генам достоверных различий не зарегистрировано.
При выполнении корреляционного анализа установлена прямая связь умеренной тесноты между АМГ и AREG. В свою очередь уровень экспрессии AREG отрицательно коррелировал с уровнем экспрессии SCD5 (табл. 2).
Зависимость количества полученных зрелых ооцитов от количественных факторов оценивали методом линейной регрессии (табл. 3). Число наблюдений – 25.
Зависимость количества зрелых ооцитов от эффективной дозы препаратов гонадотропина описывается уравнением линейной регрессии:
Yзр. ооцит = 18,689 - 0,016Xэфф. доза,
где Yзр. ооцит – величина зрелого ооцита;
Xэфф. доза – эффективная доза препаратов гонадотропина.
При увеличении эффективной дозы на 1 следует ожидать уменьшения количества зрелых ооцитов на 0,016.
Полученная регрессионная модель характеризуется коэффициентом корреляции rxy = 0,530, что соответствует заметной тесноте связи по шкале Чеддока. Модель статистически значима (p = 0,006). Полученная модель объясняет 28,1% наблюдаемой дисперсии количества зрелых ооцитов.
Зависимость количества бластоцист пятого дня от количественных факторов оценивали методом линейной регрессии (табл. 4). Число наблюдений – 17.
Зависимость количества бластоцист пятого дня от уровней антимюллерова гормона (АМГ), SCD5 описывается уравнением линейной регрессии:
Yбласт. 5 = -0,371 + 0,518XАМГ + 3,420XSCD5,
где Yбласт. 5 – количество бластоцист пятого дня;
XАМГ – уровень АМГ;
XSCD5 – экспрессия SCD5.
При увеличении АМГ на 1 следует ожидать увеличения количества бластоцист пятого дня на 0,518, при увеличении SCD5 на 1 – увеличения на 3,420.
Полученная регрессионная модель характеризуется коэффициентом корреляции rxy = 0,862, что соответствует высокой тесноте связи по шкале Чеддока. Модель статистически значима (p < 0,001). Полученная модель объясняет 74,4% наблюдаемой дисперсии пятого дня.
Зависимость количества полученных бластоцист пятого дня от экспрессии генов кумулюсных клеток оценивали методом линейной регрессии (табл. 5). Число наблюдений – 18.
Зависимость количества бластоцист пятого дня от экспрессии AREG и SCD5 описывается уравнением линейной регрессии:
Yбласт. 5 = -0,801 + 1,185XAREG + 3,943XSCD5,
где Yбласт. 5 – количество бластоцист пятого дня;
XAREG – экспрессия AREG;
XSCD5 – экспрессия SCD5.
При увеличении AREG на 1 следует ожидать увеличения количества бластоцист пятого дня развития на 1,185, при увеличении SCD5 на 1 – увеличения количества бластоцист пятого дня на 3,943.
Полученная регрессионная модель характеризуется коэффициентом корреляции rxy = 0,824, что соответствует высокой тесноте связи по шкале Чеддока. Модель статистически значима (p < 0,001). Полученная модель объясняет 67,9% наблюдаемой дисперсии пятого дня.
Зависимость экспрессии AREG от количественных факторов оценивали методом линейной регрессии (табл. 6). Число наблюдений – 17.
Зависимость AREG от количества бластоцист хорошего качества, экспрессии STAR, SCD5 описывается уравнением линейной регрессии:
YAREG = 2,634 + 0,456Xбласт. хор. кач. - 1,057XSTAR - 2,278XSCD5,
где YAREG – уровень AREG;
Xбласт. хор. кач. – количество бластоцист хорошего качества;
XSTAR – уровень STAR;
XSCD5 – уровень SCD5.
При увеличении бластоцист хорошего качества на 1 следует ожидать увеличения уровня AREG на 0,456, при увеличении STAR на 1 – уменьшения экспрессии AREG на 1,057, при увеличении SCD5 на 1 – уменьшения уровня AREG на 2,278.
Полученная регрессионная модель характеризуется коэффициентом корреляции rxy = 0,882, что соответствует высокой тесноте связи по шкале Чеддока. Модель статистически значима (p < 0,001). Полученная модель объясняет 77,7% наблюдаемой дисперсии AREG.
Обсуждение
В нашем исследовании показана корреляционная связь между уровнем АМГ и экспрессией гена в кумулюсных клетках. На основании оценки корреляционных связей и построения статистических моделей можно предположить, что экспрессия генов AREG и SCD5 в кумулюсных клетках полученных ооцитов существенно влияет на формирование качественных эмбрионов в процессе культивирования. Полученные данные позволяют рассматривать AREG в качестве одного из кандидатов для создания панели маркеров прогнозирования качества ооцита на основе молекулярно-биологического исследования кумулюсных клеток. При этом необходимо отметить, что проведенное исследование было пилотным.
Для подтверждения полученных результатов необходимы исследования на большей выборке пациенток. Кроме того, необходимо уточнить влияние исследуемых генов на общую эффективность программ ВРТ, оцениваемую по частоте наступления беременности и кумулятивной частоте живорождений.
Выводы
На основании полученных результатов можно сделать несколько важных выводов.
- Выявлена достоверная корреляционная зависимость между количеством бластоцист пятого дня развития и уровнем экспрессии гена амфирегулина в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов.
- Построена множественная регрессионная модель зависимости количества бластоцист пятого дня развития от экспрессии генов AREG, STAR, SCD5, PTGS2, HAS2 в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов. Зависимость количества полученных бластоцист пятого дня от экспрессии AREG, SCD5 описывается уравнением линейной регрессии: Yбласт.5 = -0,801 + 1,185XAREG + 3,943XSCD5 (p < 0,001).
- Многофакторный регрессионный анализ зависимости количества бластоцист пятого дня развития от уровня АМГ и экспрессии генов AREG, STAR, SCD5, PTGS2, HAS2 в клетках кумулюса выявил зависимость количества бластоцист пятого дня от уровня АМГ в крови и экспрессии гена SCD5 в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов.
- Установлена достоверная отрицательная зависимость количества полученных зрелых ооцитов от эффективной дозы препаратов гонадотропина в отсутствие связи с экспрессией изучаемых генов в кумулюсных клетках женщин с повторными неудачами имплантации и у доноров ооцитов.
Предположительно определение экспрессии генов AREG и SCD5 в кумулюсных клетках фолликулов женщин можно использовать в качестве перспективного неинвазивного показателя компетентности полученных ооцитов.
Ограничениями данного исследования были малая выборка и группа пациенток с неудачами имплантации в анамнезе.
Необходимы более репрезентативные исследования с оценкой экспрессии генов AREG и SCD5 в кумулюсных клетках получаемых ОКК у большего количества женщин с различными факторами бесплодия.
Работа выполнена при поддержке Российского научного фонда (грант № 24-24-00533).
I.A. Babenchuk, N.V. Ponomartsev, V.A. Gallyamova, A.R. Smolyaninova, Yu.A. Tatishcheva, PhD, N.A. Slominskaya, PhD, N.A. Kuzminykh, D.A. Gerculov, PhD, N.I. Yenukashvili, PhD, A.S. Kalugina, PhD, Prof.
Skaifert Clinic, St. Petersburg
Institute of Cytology of RAS, St. Petersburg
Academician I.P. Pavlov First St. Petersburg State Medical University
Contact person: Irina A. Babenchuk, babenchuk69@gmail.com
The aim was to evaluate the expression level of the AREG, STAR, PTGS2, HAS2, and SCD5 genes in the cumulus cells of healthy donors and patients with a history of repeated implantation failures.
Material and methods. A comparative pilot prospective study was conducted. The main group included 19 patients aged 18–40 years with repeated implantation failures and blood levels of anti-Mullerian hormone ranging from 0.8 to 3.5 ng/ml. The comparison group consisted of nine oocyte donors. The expression of the AREG, STAR, PTGS2, HAS2, and SCD5 genes (quantitative polymerase chain reaction method) in the cumulus cells of the obtained oocytes was determined using the CFX96 Real-Time System (Bio-Rad, USA).
Results. A significant correlation was found between the number of blastocysts on the fifth day of development and the level of amphiregulin gene expression in cumulus cells of women with repeated implantation failures and in oocyte donors. A multiple regression analysis showed the dependence of the number of blastocysts obtained on the fifth day on the expression of the AREG and SCD5 genes in the cumulus cells of women with repeated implantation failures and in oocyte donors.
Conclusion. Presumably, the expression level of the AREG and SCD5 genes in the cumulus cells of female follicles can be used as a promising noninvasive indicator of the competence of the obtained oocytes. The limitations of this study are a small sample and a group of patients with a history of implantation failures. More presentative studies are needed to evaluate the expression of the AREG and SCD5 genes in the cumulus cells of the resulting oocyte cumulus complexes in a larger number of women with various infertility factors.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.