Оценка клинической эффективности альгинатсодержащего препарата Гевискон (суспензия) у детей с различными эндоскопическими вариантами ГЭРБ
- Аннотация
- Статья
- Ссылки
Изжога – один из наиболее часто испытываемых и описываемых желудочно-кишечных симптомов – является основным симптомом гастроэзофагеальной рефлюксной болезни (ГЭРБ). Актуальность проблемы ГЭРБ определяется целым рядом обстоятельств. Эпидемиологические исследования последних лет показали, что по своей частоте и распространенности ГЭРБ выходит на лидирующие позиции в ряду других гастроэнтерологических заболеваний. Изжога, по разным данным, выявляется у 10–40% населения [1–3]. У детей заболевания пищевода составляют, по данным разных авторов, от 18 до 25% от всех заболеваний органов пищеварения [4]. Актуальность проблемы ГЭРБ для педиатрической практики определяется не только высокой ее частотой среди заболеваний желудочно-кишечного тракта (ЖКТ), но и частыми внепищеводными проявлениями ГЭРБ [4–6].
Хронические заболевания верхних отделов пищеварительного тракта в большинстве случаев тесно взаимосвязаны с продукцией соляной кислоты в желудке. При развитии хронических воспалительных заболеваний органов пищеварения в той или иной степени страдает механизм кислотообразования. В то же время изменение продукции соляной кислоты в желудке может служить пусковым моментом в развитии различных патологических изменений органов ЖКТ. Нарушение механизмов кислотообразования влияет на развитие воспалительных процессов не только в желудке, но и в пищеводе. Этим можно объяснить тот факт, что в спектре хронических воспалительных заболеваний органов пищеварения изолированные эзофагиты занимают чуть меньше 1,5%, при гастритах сочетанное поражение пищевода определяется у 15% детей, при гастродуоденитах – у 38,1%, а при язвенной болезни двенадцатиперстной кишки эзофагит встречается практически у всех детей [7]. При наличии некоторых предрасполагающих факторов, таких как врожденный короткий пищевод, грыжа пищеводного отверстия диафрагмы, нарушение моторной активности желудка, повышение внутрибрюшного давления, гастроэзофагеальный пролапс, кислое желудочное содержимое может забрасываться в пищевод, вызывая раздражение и приводя к воспалительному процессу. Если агрессивные факторы действуют продолжительное время, может развиться ГЭРБ, часто с появлением эрозий и даже язв пищевода.
Рефлюксная болезнь может развиться и после проведенной эрадикационной терапии [8–13]. Как показали проведенные исследования, H. pylori, находясь на поверхности слизистой оболочки, стимулируют перистальтическую активность желудка. После эрадикации отмечается исчезновение алкилирующего эффекта аммония, получаемого из мочевины с помощью уреазы H. pylori, возрастает секреция соляной кислоты [14]. Накопление кислого содержимого в желудке создает предпосылки для развития рефлюкс-эзофагита, особенно после отмены кислотоподавляющих препаратов. Кроме того, кларитромицин, входящий во многие схемы лечения хеликобактериоза, стимулирует моторику желудка. После окончания курса эрадикационной терапии перистальтическая активность, уже не поддерживаемая ни H. pylori, ни кларитромицином, значительно снижается, что создает дополнительные условия для заброса кислого желудочного содержимого в пищевод. Этому способствует также снижение уровня сывороточного гастрина после эрадикации, который, как известно, повышает тонус нижнего пищеводного сфинктера.
В настоящее время существуют различные группы препаратов, направленные на регуляцию кислотообразования. Это в первую очередь антисекреторные препараты (Н2-гистаминоблокаторы и ингибиторы протонной помпы (ИПП)) и антациды. Известно, что фармакологическое действие антисекреторных препаратов и антацидов различается принципиально. И если первые более или менее стойко и на длительный период (в зависимости от групповой принадлежности и свойств конкретного препарата) угнетают процесс кислотообразования в желудке, который тесно скоординирован с моторикой верхних отделов пищеварительного тракта, то вторые нейтрализуют уже секретированную в просвет желудка хлористоводородную кислоту на короткое время. Вместе с тем преимуществами современных антацидов перед препаратами других фармакологических групп, используемых для лечения кислотозависимых заболеваний, являются быстрое купирование боли и диспепсии, способность адсорбировать желчные кислоты и лизолецитин, положительное влияние на скорость эвакуации из желудка, возможность коррекции нарушений кишечной моторики.
Многообразные свойства антацидов и широкий спектр показаний к их применению привели к созданию большого количества лекарственных средств, которые неоднородны по своим свойствам и механизму действия. В настоящее время в клинической практике показаны к применению лишь нерастворимые (невсасывающиеся) антациды, поскольку растворимые (всасывающиеся) антациды (натрия гидрокарбонат и др.) действуют быстро, но кратковременно, часто обусловливают синдром рикошета, иногда алкалоз, увеличение объема циркулирующей крови, в связи с чем их практически не применяют [15–18].
Однако терапия антацидными препаратами не может использоваться как основной метод лечения кислотозависимых заболеваний, так как не контролирует выработку соляной кислоты. Длительное применение антацидов, в том числе и невсасывающихся, может приводить к нарушению стула, минерального баланса, развитию алкалоза [15].
Применение Н2-блокаторов гистамина ограничено подавлением секреции, воздействием всего лишь на один тип рецепторов. При этом при стимуляции других рецепторов (гастрин, ацетилхолин) вновь может возникнуть гиперсекреция кислоты. Кроме того, терапевтическая эффективность Н2-блокаторов гистамина обеспечивается высоким уровнем препарата в крови, что иногда требует его многократного приема. Длительное применение этой группы препаратов и затем резкая их отмена могут приводить к развитию толерантности и синдрома рикошета. Толерантность может развиться уже через два дня после начала лечения [19, 20]. Н2-блокаторы гистамина в последнее время все реже используются в качестве основного средства для лечения кислотозависимых заболеваний органов пищеварения, в том числе и в педиатрической практике.
Изучение молекулярных механизмов образования соляной кислоты желудочного сока позволило выявить его ключевое звено – активную секрецию протонов, сопряженную с транспортом К+, реализуемую специальным мембранным комплексом – протонной помпой. В то время как образование протонов в ходе различных внутриклеточных реакций контролируется различными регуляторными факторами (ацетилхолином, гистамином, гастрином, простагландинами, гастроинтестинальными тканевыми факторами и др.), работа этого механизма практически не связана с физиологическими регуляторными механизмами. Поэтому разработка лекарственных средств, способных снижать активность АТФазы протонной помпы, является важной задачей фармакологии.
В настоящее время ИПП применяют для лечения ГЭРБ наиболее часто, поскольку они эффективнее контролируют симптомы и способствуют заживлению эрозий при рефлюкс-эзофагите, чем все другие перечисленные выше группы препаратов. Вместе с тем для ИПП характерен отсроченный эффект первой дозы, не всегда позволяющий использовать их для быстрого устранения изжоги. Так, недавно опубликованный метаанализ клинических исследований показал, что первый прием ИПП полностью купировал изжогу лишь у 30% больных, при этом у большинства из них в течение первых двух дней лечения изжога не уменьшалась [21].
Трудности лечения выделяют ГЭРБ среди других заболеваний органов пищеварения. Тем не менее в настоящее время существуют достаточно четкие алгоритмы тактики терапии этой группы взрослых пациентов. При лечении детей с ГЭРБ возникают сложности, связанные прежде всего с ограничениями применения основных групп препаратов в педиатрии. Так, до сих пор нет официально разрешенных к применению ИПП у детей младше 12 лет, соответственно, использование этой группы препаратов у детей связано с проведением этого решения через соглашение с этическим и фармакологическим комитетами ЛПУ, составлением и подписанием информированного согласия родителей или опекунов ребенка. Все это ограничивает широкое использование ИПП в качестве первого и основного средства лечения, в том числе и осложненных форм ГЭРБ у детей.
Как показали скрининговые мониторинговые исследования частоты и предпочтения назначения различных препаратов для лечения ГЭРБ среди терапевтов и педиатров, на первом месте находятся прокинетики, второе и последующие места среди терапевтов делят между собой кислоторегулирующие препараты различных групп. Частота назначения антацидных препаратов среди педиатров занимает лишь пятую позицию, уступая лидирующие места ферментам, пробиотикам и адсорбентам [22].
Таким образом, несмотря на высокую терапевтическую активность, основные группы препаратов, традиционно применяемых для лечения ГЭРБ (антисекреторные препараты, антациды), имеют определенные побочные эффекты и ограничения в использовании, особенно в педиатрии. Следовательно, сохраняет свою актуальность поиск новых способов медикаментозного лечения данного заболевания. В связи с этим своевременным следует признать внедрение в схемы лечения больных ГЭРБ альгинатов – группы препаратов на основе альгиновой кислоты, получаемой из морских бурых водорослей.
Альгинатные препараты формируют механический барьер, который предупреждает заброс содержимого желудка в пищевод. Альгинат натрия и гидрокарбонат натрия/калия взаимодействуют с соляной кислотой в желудке с образованием пузырьков углекислого газа, удерживающих барьерный гелеобразный значительной толщины слой альгинатов «на плаву» на поверхности слизи желудка. Карбонат кальция, входящий в состав альгинатов, является источником кальция, который связывает друг с другом длинные молекулы альгината и таким образом укрепляет барьер. Образующийся прочный, вязкий, близкий к нейтральному (pH ~ 7) барьер, вступая в контакт с желудочной кислотой, располагается (плавает) на поверхности содержимого желудка. При возникновении гастроэзофагеального рефлюкса, пролабировании слизистой оболочки желудка в пищевод при антиперистальтических волнах первым в пищевод попадает именно гелеобразный значительной толщины слой альгинатов, предотвращая раздражающее действие соляной кислоты и пепсинов на слизистую оболочку пищевода.
Следует отметить, что альгинаты не всасываются в ЖКТ, а следовательно, не оказывают системного воздействия на организм. Механизм их действия имеет только физическую природу, с сохранением нормального, физиологичного для пищеварения pH в желудке под барьерным гелеобразным значительной толщины слоем альгинатов. При этом не отмечается какого-либо нарушения процессов пищеварения или лекарственных взаимодействий. Эти свойства дают преимущества для использования препарата у детей.
В настоящее время в мире накоплен достаточно большой клинический опыт применения альгинатов у взрослых и детей, в частности препарата Гевискон при ГЭРБ и диспепсиях, сопровождающихся изжогой [23–34]. Однако в России Гевискон стал использоваться для лечения изжоги и других проявлений ГЭРБ у детей недавно, в связи с чем требуются дополнительные исследования.
Цель: оценить клиническую эффективности и безопасность суспензии Гевискон у детей c различными эндоскопическими вариантами ГЭРБ.
Материалы и методы
В исследование были включены 60 детей в возрасте от 6 до 18 лет (12,7 ± 2,51 лет), 18 девочек и 42 мальчика. Критерием включения было наличие диспептических жалоб, характерных для ГЭРБ (изжога и отрыжка). Все дети находились на стационарном обследовании в гастроэнтерологическом отделении УДКБ Первого МГМУ им. И.М. Сеченова и Морозовской ДГКБ г. Москвы по поводу воспалительных заболеваний верхних отделов пищеварительного тракта.
С целью диагностики, а также для оценки эффективности проводимой терапии детям проводился сбор анамнеза с помощью специально разработанной индивидуальной регистрационной карты пациента, инструментальная диагностика. Проводились следующие исследования:
- эзофагогастродуоденоскопия (ЭГДС) (исходно всем детям);
- суточный мониторинг рН в пищеводе и желудке (факультативно).
ЭГДС проводилась всем пациентам до лечения с целью оценки степени выраженности воспалительных изменений слизистой оболочки верхних отделов пищеварительного тракта. Для оценки степени повреждения слизистой оболочки пищевода использовалась классификация рефлюкс-эзофагита у детей по G. Tytgat в модификации В.Ф. Приворотского и соавт.
10 детям факультативно проводилось 24-часовое мониторирование рН при помощи аппарата «Гастроскан 24» («Исток-Система», Россия). Исследование выполнялось дважды: до назначения лечения Гевисконом и на 7–10-й день приема препарата. Для оценки результатов рН-метрии в пищеводе использовали критерии T.R. DeMeester. Патологически кислый ГЭР диагностировали в тех случаях, когда общая продолжительность снижения внутрипищеводного рН ниже 4,0 составляла более 4,5% времени исследования, а индекс DeMeester превышал 14,7.
После сбора анамнеза и проведения первичной диагностики всем пациентам назначалось лечение препаратом Гевискон. Продолжительность лечения составляла 10–14 дней. Дозы препарата назначали в соответствии с инструкцией к препарату в зависимости от возраста ребенка: от 6 до 12 лет – по 10 мл, от 7 до 18 лет – по 15 мл суспензии Гевискон 4 раза в день (3 раза через 15–20 минут после еды и 1 раз на ночь).
Оценка влияния Гевискона проводилась по следующим критериям:
- исчезновение изжоги;
- наличие или отсутствие других клинических проявлений воспалительных заболеваний верхних отделов ЖКТ.
Проводилась статистическая обработка результатов исследования. Количественные и порядковые показатели представлялись как среднее значение ± стандартное отклонение. Качественные показатели представлялись в виде абсолютного числа наблюдений и доли (в процентах) от общего числа больных по выборке в целом или в соответствующей группе. Достоверность различий сравниваемых величин определяли по критерию Стьюдента, различия считали достоверными при р < 0,05.
Результаты
Основными жалобами у детей с ГЭРБ были изжога и отрыжка. Так, изжогу испытывали 43 ребенка (72%), отрыжку – 48 детей (80%), причем 14 детей (23%) кроме отрыжки воздухом испытывали также и кислую отрыжку. Достаточно часто у детей имели место такие неспецифические жалобы, как боль, тяжесть и ощущение дискомфорта в животе: у 32 (53%), 29 (48%) и 12 (20%) детей соответственно. Часть пациентов жаловались на регургитацию (срыгивания) – 4 ребенка (7%), тошноту – 8 детей (13%) и горечь во рту – 1 ребенок (2%). Эти жалобы также являются признаками нарушения моторики верхних отделов пищеварительного тракта и ГЭРБ.
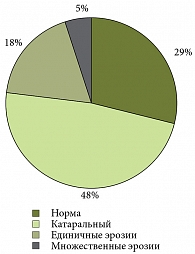
По результатам ЭГДС был проведен анализ эндоскопических изменений слизистой оболочки верхних отделов ЖКТ у детей, включенных в исследование. У всех детей были выявлены воспалительные изменения разной степени выраженности в пищеводе, желудке и двенадцатиперстной кишке. Воспалительные изменения слизистой оболочки пищевода у большинства больных были представлены катаральным эзофагитом (эзофагит 1-й степени) – у 29 детей (48%). У 14 детей (23%) выявлялись эрозивные поражения слизистой пищевода: единичные эрозии (эзофагит 2-й степени) – у 11 детей (18%), множественные эрозии (эзофагит 3-й степени) – у 3 детей (5%) (рис. 1). У двух детей с эзофагитом 2-й степени морфологически был подтвержден диагноз «пищевод Барретта, желудочная метаплазия».
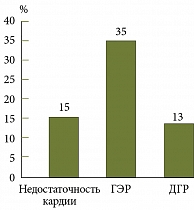
Нарушения моторики в области кардиоэзофагеального перехода в виде недостаточности кардии и гастроэзофагеального рефлюкса выявлялись по данным ЭГДС у 9 (15%) и 21 (35%) детей соответственно. Нарушения моторики в пилородуоденальной зоне в виде дуоденогастрального рефлюкса по данным ЭГДС отмечались у 8 (13%) обследованных детей (рис. 2).
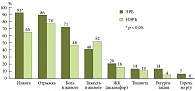
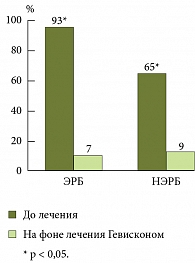
Учитывая, что интенсивность жалоб у детей с эрозивной и неэрозивной формой ГЭРБ может различаться, все пациенты были разделены на две группы в зависимости от степени выраженности воспалительных изменений в пищеводе по данным ЭГДС. В группу детей с неэрозивной формой ГЭРБ (НЭРБ) вошли 46 детей. Эрозивная форма (ЭРБ) была выявлена у 14 детей. При сравнении частоты основных жалоб оказалось, что дети с эрозивным эзофагитом жалуются на изжогу достоверно чаще – 93% против 65% (p ≤ 0,005). При этом частота других жалоб, таких как боль в животе, отрыжка, регургитация, также была больше в группе детей с эрозивной формой ГЭРБ (рис. 3).
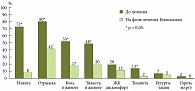
При оценке основных клинических проявлений ГЭРБ у обследованных детей в динамике на фоне лечения суспензией Гевискон было отмечено статистически достоверное уменьшение выраженности следующих жалоб: изжоги (с 72% до 8%), отрыжки (с 80% до 42%), болей в животе (с 53% до 17%), ощущения тяжести в животе (с 48% до 20%) и тошноты (с 13% до 2%) (рис. 4). Причем кислая отрыжка и ощущение горечи во рту были купированы у всех детей, принимавших Гевискон. Жалобы на регургитацию (срыгивание), отмечавшиеся у 4 пациентов, на фоне приема Гевискона сохранялись у 3, однако, по ощущениям самих детей, беспокоили реже.
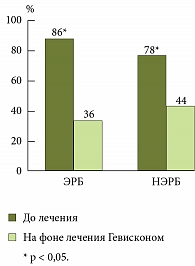
При сравнительной оценке динамики жалоб у детей с ЭРБ и НЭРБ было показано, что Гевискон одинаково эффективен для купирования основных симптомов ГЭРБ, таких как изжога и отрыжка (рис. 6, 7). Так, на фоне терапии Гевисконом у детей с ЭРБ достоверно уменьшилась частота жалоб на изжогу (с 93% до 7%, p ≤ 0,001), на отрыжку (с 86% до 36%, p ≤ 0,05). Также отмечалось уменьшение болей в животе (с 71% до 21%, p ≤ 0,005). У детей с НЭРБ на фоне терапии Гевисконом отмечалась более выраженная положительная динамика. Так, зарегистрировано достоверное снижение частоты не только изжоги (с 65% до 9%, p ≤ 0,001), отрыжки (с 78% до 44%, p ≤ 0,001) и боли в животе (с 48% до 15%, p ≤ 0,001), но и тяжести в животе (с 52% до 20%, p ≤ 0,001) и тошноты (с 13% до 0%, p ≤ 0,005).
Следует отметить, что ни у одного ребенка из вошедших в исследование нежелательных явлений или побочных реакций при приеме суспензии Гевискон не отмечалось.
10 детям с жалобами на изжогу факультативно была проведена суточная рН-метрия с использованием трехэлектродного трансназального зонда (положение зонда «пищевод – кардия – тело желудка»). У большинства детей (8 из 10), которым дважды была проведена суточная рН-метрия, по данным ЭГДС был выявлен эрозивный эзофагит.
Оценка исходных данных суточной рН-метрии показала отсутствие признаков гиперацидности в теле желудка у обследованных больных. Патологически кислые ГЭР по критериям DeMeester определялись у 2 из 10 обследованных больных. На фоне приема Гевискона отмечалось повышение среднего значения рН в теле желудка за сутки с 2,7 ± 0,51 до 5,4 ± 3,17, что может говорить о буферном действии суспензии Гевискон. Средний общий процент времени с рН < 4 в пищеводе за сутки был в норме и не менялся (2,9 ± 1,88% исходно против 3 ± 2,67% на фоне приема Гевискона). В то же время при приеме Гевискона уменьшалось количество ГЭР с рН < 4 за сутки с 24 ± 15,85 до 19 ± 14,44. У большинства детей эти показатели были в норме и до назначения Гевискона, но в целом уменьшение числа кислых ГЭР может свидетельствовать об антирефлюксном действии препарата. Средний показатель индекса DeMeester на фоне лечения не менялся и составил 7,7 (7,7 ± 4,95 до лечения и 7,7 ± 6,61 на фоне терапии Гевисконом). У двоих больных отмечалось ухудшение суточных показателей рН-метрии, что связано с тяжелым течением ГЭРБ. В дальнейшем этим больным терапия была усилена антисекреторными препаратами.
Выводы
Прием Гевискона при ГЭРБ у детей уменьшает частоту основных жалоб, таких как изжога, отрыжка, в том числе кислым, боль и тяжесть в животе, тошнота.
Гевискон эффективен для уменьшения изжоги, отрыжки и болей в животе при ГЭРБ у детей вне зависимости от эндоскопической формы заболевания. У детей с неэрозивной формой ГЭРБ на фоне приема Гевискона достоверно чаще купировались также тошнота и тяжесть в животе. Таким образом, можно думать о более выраженном симптоматическом эффекте Гевискона у детей с неэрозивной формой ГЭРБ.
У обследованных детей с ГЭРБ на фоне приема Гевискона статистически значимых изменений показателей суточного рН-мониторинга не отмечалось, однако отмечалась тенденция к повышению среднесуточных значений рН в теле желудка и уменьшению числа кислых ГЭР, что свидетельствует об антацидном и антирефлюксном действии суспензии Гевискон.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.