Патогенетическая терапия хронической диареи у пациентов с резекцией тонкой кишки
- Аннотация
- Статья
- Ссылки
- English
Введение
За последние десятилетия получены новые данные, в свете которых пересмотрено и расширено представление о значении желчных кислот (ЖК) в организме человека. В процессе эволюции животного мира сложились условия, обеспечивающие экономное использование их посредством печеночно-кишечной циркуляции. Этот процесс осуществляется с помощью транспортных систем тонкой кишки [1–3].
У здорового человека 95% ЖК реабсорбируется в подвздошной кишке (ПК) и вновь поступает в печень, а 5% выделяется с фекалиями в виде бактериальных метаболитов. Последние способствуют формированию кала путем торможения всасывания воды и их дегидратации. Реабсорбция ЖК осуществляется в результате активного транспортного механизма в терминальном отделе ПК. Пассивная транспортная диффузия ионов не имеет существенного значения, однако может играть компенсаторную роль при резекции ПК [3–8].
Исследования механизмов диареи у пациентов, перенесших резекцию ПК, особенно терминального отдела, позволили выделить два типа диареи: диарею, связанную с мальабсорбцией ЖК (хологенная диарея), и диарею, связанную с нарушением всасывания жирных кислот (стеаторейная диарея). Также при резекциях кишки подобного объема может наблюдаться мальабсорбция витаминов В12 и D. У пациентов с небольшими резекциями всасывание ЖК незначительно снижено и компенсаторного увеличения их синтеза в печени достаточно для восстановления их пула. Однако даже незначительное увеличение поступления ЖК в толстую кишку может вызывать хологенную диарею. У пациентов с обширными резекциями мальабсорбция ЖК выражена сильно, а увеличение их синтеза недостаточно для поддержания нормального их количества в желчи. В результате нарушаются мицеллярная дисперсия липолитических продуктов и всасывание жиров [9–11].
Клиническое наблюдение
Приведенное клиническое наблюдение демонстрирует успешную диагностику и лечение хологенной диареи, основанные на анализе патогенетических факторов ее развития, у пациентки, перенесшей резекцию ПК.
Пациентка Б., 1949 г.р., в 2018 г. перенесла резекцию тонкой кишки в объеме 1,8 м в связи с развитием некроза тонкой кишки вследствие тромбоза одной из ветвей верхней брыжеечной артерии. После операции появился водянистый не обильный стул зеленого цвета с частотой до семи-восьми раз в день, преимущественно в первой половине дня, а также инконтиненция (недержание) жидкого кишечного содержимого и чувство жжения в аноректальной зоне. Больная наблюдалась в поликлинике по месту жительства, около двух лет получала лечение антисептиками и панкреатическими ферментами. Улучшения не наступило. Обратилась в отделение патологии кишечника Московского клинического научного центра им. А.С. Логинова.
При поступлении состояние удовлетворительное, индекс массы тела – 21,5 кг/м2. Кожные покровы и видимые слизистые чистые, обычной окраски, на коже передней поверхности живота виден послеоперационный рубец после верхней срединной лапаротомии длиной 15 см. В легких дыхание везикулярное, частота дыхательных движений – 16 в минуту. Тоны сердца ритмичные, систолический шум над аортой. Артериальное давление – 130/80 мм рт. ст., пульс – 74 в минуту. Язык влажный, не обложен. Живот мягкий, болезненный в мезогастрии. Печень не выступает из-под края реберной дуги. Размеры по Курлову – 9–8–7 см. Селезенка не пальпируется. Мочеиспускание свободное, безболезненное. Стул жидкий до восьми раз в день ярко-желтого/зеленоватого цвета.
Клинический анализ крови: гемоглобин – 130 г/л, эритроциты – 4,37 × 106, тромбоциты – 332 × 103, лейкоциты – 7,56 × 103, палочкоядерные – 1,5%, сегментоядерные – 65,1%, эозинофилы – 4,4%, лимфоциты – 22,8%, моноциты – 5,6%, скорость оседания эритроцитов – 24 мм/ч, признаков гиперхромии не выявлено.
Биохимическое исследование крови: общий белок – 76,8 г/л, альбумин – 39 г/л, холестерин – 4,5 ммоль/л, щелочная фосфатаза – 120 Ед/л, гамма-глутамилтранспептидаза – 25,2 ед/л, К+ – 4,86 ммоль/л, Na+ – 138 ммоль/л, Са2+ – 2,31 ммоль/л, железо – 13,6 мкмоль/л, аланинаминотрансфераза – 31,9 ед/л, аспартатаминотрансфераза – 24,4 ед/л, амилаза – 68,35 ед/л, глюкоза – 5,1 ммоль/л, мочевина – 7 ммоль/л, креатинин – 75,3 мкмоль/л. Общий анализ мочи – без особенностей.
Суточный вес кала – 980 г, экскреция ЖК с калом – 2000 мг в сутки (50–200 мг в сутки). Копрограмма: консистенция мягкая, цвет ярко-желтый, запах обычный, дрожжевые грибы, жирные кислоты, крахмал – в незначительном количестве. Панкреатическая эластаза кала – более 500 мкг/г.
Ультразвуковое исследование органов брюшной полости – без особенностей.
Эндоскопическое исследование с биопсией слизистой оболочки желудка и двенадцатиперстной кишки: картина хронического гастрита с фовеолярной гиперплазией, хронического дуоденита.
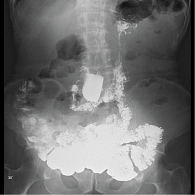
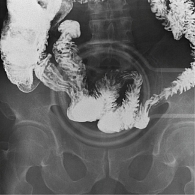
Рентгенологическое исследование тонкой кишки: картина оперированной тонкой кишки с удовлетворительной функцией анастомоза и косвенными признаками спаечного процесса в брюшной полости (рис. 1, 2).
Ректороманоскопия: органической патологии прямой кишки не выявлено.
Дуплексное сканирование брюшной части аорты и ее непарных висцеральных ветвей: признаки атеросклероза брюшной аорты и гемодинамически значимого стенозирования устья чревного ствола.
Для уточнения характера изменений брюшного отдела аорты проведена компьютерная ангиография с внутривенным контрастированием, при которой выявлена картина стеноза чревного ствола до 40% вследствие экстравазальной компрессии ножками диафрагмы. Больная консультирована сосудистым хирургом, который рекомендовал динамическое наблюдение.
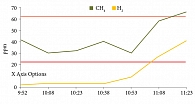
Пациентке проведен дыхательный водородно-метановый тест с лактулозой: повышение Н2, СН4 на 20 ррм по сравнению с исходным уровнем, характерное для избыточного бактериального роста в тонкой кишке (рис. 3).
На основании жалоб, анамнеза заболевания и данных обследования сформулирован окончательный диагноз: синдром резецированного кишечника (резекция 1,8 м тонкой кишки от июня 2018 г. по поводу сегментарного мезентериального тромбоза). Осложнения: синдром нарушенного всасывания первой степени. Хологенная диарея. Синдром избыточного бактериального роста в тонкой кишке. Сопутствующие заболевания: хроническая ишемическая болезнь органов пищеварения. Субкомпенсированный стеноз чревного ствола. Во время госпитализации пациентке проведено комплексное лечение. Немедикаментозная терапия включала дробное питание щадящей диетой пять-шесть раз в день (подверженной механической, термической и химической обработке), восполнение водно-электролитного баланса. Медикаментозная терапия включала невсасывающиеся кишечные антисептики, адсорбенты – секвестранты ЖК, мультиштаммовые пробиотики. В результате проведенного лечения наступило улучшение состояния: прекратилась диарея, улучшилось качество жизни.
Обсуждение
Выраженность клинических проявлений у пациентов, перенесших резекцию тонкой кишки, связана как с длиной резецированной кишки, так и с адаптивными способностями желудочно-кишечного тракта. Отсутствие терминального отдела ПК у таких пациентов является причиной мальабсорбции витамина B12, жирорастворимых витаминов и ЖК [12].
С учетом особенностей энтерогепатической циркуляции ЖК в организме человека резекция любого участка ПК может привести к нарушению их всасывания. Резекция менее 100 см ПК приводит к умеренному нарушению, а резекция более 100 см – к тяжелому синдрому мальабсорбции ЖК и стеаторее [13, 14].
У пациентов с резекцией менее 100 см тонкой кишки клинические симптомы обычно ограничиваются диареей без стеатореи.
После обширной резекции ПК клиническая картина более яркая и характеризуется водянистой диареей, как правило плохо поддающейся лечению. Связано это со снижением способности печени компенсировать значимые потери ЖК. Дефицит ЖК в составе образуемой желчи приводит к перенасыщению желчи холестерином, чем объясняется высокая частота образования холестериновых камней в желчном пузыре у пациентов с синдромом резецированного кишечника.
Обширная резекция ПК может также сопровождаться образованием оксалатных камней в почках. В норме избыток пищевых оксалатов связывается с кальцием и выделяется с калом. При стеаторее, обусловленной обширной резекцией ПК, жирные кислоты захватывают соли кальция и выделяются с калом в виде кальциевых мыл, в то время как пищевые оксалаты всасываются в кровь, вызывая гипероксалурию, а затем образование в почках оксалатных камней [1, 15, 16].
Количественное исследование суточного кала на содержание жиров и ЖК позволяет оценить полноценность процессов энтерогепатической циркуляции ЖК у больных после резекции тонкой кишки и более точно понять причину диарейного синдрома.
В комплексной терапии, проводимой пациентам с резекцией ПК, необходимо учитывать патогенетическую составляющую диарейного синдрома и применять дифференцированное назначение препаратов [17, 18], к которым относятся лекарственные средства, связывающие избыток неабсорбированных ЖК, препараты, подавляющие избыточный бактериальный рост, пробиотики. Назначение каждого препарата должно подтверждаться данными лабораторных и инструментальных исследований (суточного анализа кала на содержание ЖК, дыхательного водородного теста с лактулозой, рентгенологического исследования пассажа бария по тонкой кишке и т.п.). Подобный подход позволит предотвратить полипрагмазию и повысить эффективность лечения больных с синдромом резецированного кишечника.
Заключение
В представленном клиническом наблюдении показано, что выявление отдельных патогенетически значимых факторов развития хронической диареи и назначение комплексной дифференцированной терапии дают возможность стабилизировать состояние больной и избавить ее от изнуряющей хронической диареи.
L.Kh. Indeykina, PhD, E.A. Sabelnikova, PhD, Prof., T.N. Kuzmina, PhD, S.Yu. Silvestrova, PhD, A.A. Makarova, M.B. Pavlov, A.I. Parfenov, PhD, Prof.
A.S. Loginov Moscow Clinical Scientific Center, Moscow
Research Institute of Healthcare Organization and Medical Management of the Moscow Health Department
Russian University of Medicine, Moscow
Contact person: Liliya Kh. Indeykina, l.indeykina@mknc
A clinical case of the observation of a patient with chronic diarrhea, occurred after a resection of the small intestine with an ileoileal anastomosis, is described further.
The resection of the small intestine, including the ileum, where the conversion and reabsorption of bile acids (BA) usually occur, leads to their excessive influx into the large intestine, causing chologenic diarrhea. The increased amount of BA has a detrimental effect on the activity of the intestinal microbiota in the anatomically altered intestine and can cause the biliary insufficiency. The exclusion of the ileocecal zone, especially the Bauhinia valve, from the passage of chyme, disrupts the motor activity of the large intestine, reduces water and ion absorption, and promotes regurgitation of intestinal contents from the cecum into the small intestine. Difficulties in identifying the chologenic factor in the development of diarrhea are exacerbated by the lack of available diagnostic methods. Identification of individual pathogenetically significant factors contributing to the development of diarrhea syndrome and their adequate therapeutic correction is the key to successful rehabilitation of patients with post-resection short bowel syndrome.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.