Перспектива применения противовоспалительного препарата аммония глицирризината в лечении пациентов с обострением хронической обструктивной болезни легких
- Аннотация
- Статья
- Ссылки
- English
Цель. Оценить переносимость и эффективность применения противовоспалительного препарата аммония глицирризината (Реглисам, ЗАО «ВИФИТЕХ», Россия) в комплексном лечении пациентов с обострением ХОБЛ.
Материал и методы. В открытой проспективной наблюдательной программе приняли участие 60 пациентов старше 18 лет с обострением ХОБЛ, 30 из которых составили основную группу и в дополнение к стандартной терапии получали аммония глицирризинат в течение 14 дней; группу контроля составили оставшиеся 30 пациентов, не принимавших исследуемый препарат. На 1-й и 14-й дни наблюдения в группах фиксировались клинико-лабораторные и инструментальные показатели пациентов, случаи нежелательных реакций.
Результаты. У пациентов, получавших аммония глицирризинат, на 14-й день лечения в сравнении с группой контроля фиксировалось стойкое преимущество в снижении интенсивности кашля на 42,2%, одышки – на 22,1%, балльной оценки качества жизни по шкале COPD Assessment Test – на 22,6%, повышении теста шестиминутной ходьбы (ТШМХ) на 9,6% и объема форсированного выдоха за одну секунду (ОФВ1) – на 12,2%; в контрольной группе данные показатели в динамике менялись менее значимо: на 32,7; 19,2; 18,7; 7,5 и 0,3% соответственно.
При прицельном анализе состояния пациентов на II и III стадиях ХОБЛ в основной группе на фоне терапии аммония глицирризинатом в сравнении с группой контроля отмечена более значимая достоверная положительная динамика как среди большего количества исследуемых клинико-функциональных параметров (5 против 2 и 11 против 9 параметров соответственно), так и в отношении их выраженности.
Заключение. Показана высокая терапевтическая эффективность схем терапии обострений ХОБЛ с включением аммония глицирризината в виде эффективного снижения выраженности важных клинических симптомов (кашель, одышка, мокрота) и улучшения функциональных показателей (ТШМХ, ОФВ1), а также параметров качества жизни пациентов. Полученные данные позволяют рекомендовать аммония глицирризинат в качестве дополнительного противовоспалительного средства в лечении пациентов с обострением ХОБЛ.
Цель. Оценить переносимость и эффективность применения противовоспалительного препарата аммония глицирризината (Реглисам, ЗАО «ВИФИТЕХ», Россия) в комплексном лечении пациентов с обострением ХОБЛ.
Материал и методы. В открытой проспективной наблюдательной программе приняли участие 60 пациентов старше 18 лет с обострением ХОБЛ, 30 из которых составили основную группу и в дополнение к стандартной терапии получали аммония глицирризинат в течение 14 дней; группу контроля составили оставшиеся 30 пациентов, не принимавших исследуемый препарат. На 1-й и 14-й дни наблюдения в группах фиксировались клинико-лабораторные и инструментальные показатели пациентов, случаи нежелательных реакций.
Результаты. У пациентов, получавших аммония глицирризинат, на 14-й день лечения в сравнении с группой контроля фиксировалось стойкое преимущество в снижении интенсивности кашля на 42,2%, одышки – на 22,1%, балльной оценки качества жизни по шкале COPD Assessment Test – на 22,6%, повышении теста шестиминутной ходьбы (ТШМХ) на 9,6% и объема форсированного выдоха за одну секунду (ОФВ1) – на 12,2%; в контрольной группе данные показатели в динамике менялись менее значимо: на 32,7; 19,2; 18,7; 7,5 и 0,3% соответственно.
При прицельном анализе состояния пациентов на II и III стадиях ХОБЛ в основной группе на фоне терапии аммония глицирризинатом в сравнении с группой контроля отмечена более значимая достоверная положительная динамика как среди большего количества исследуемых клинико-функциональных параметров (5 против 2 и 11 против 9 параметров соответственно), так и в отношении их выраженности.
Заключение. Показана высокая терапевтическая эффективность схем терапии обострений ХОБЛ с включением аммония глицирризината в виде эффективного снижения выраженности важных клинических симптомов (кашель, одышка, мокрота) и улучшения функциональных показателей (ТШМХ, ОФВ1), а также параметров качества жизни пациентов. Полученные данные позволяют рекомендовать аммония глицирризинат в качестве дополнительного противовоспалительного средства в лечении пациентов с обострением ХОБЛ.







Введение
В настоящее время хроническая обструктивная болезнь легких (ХОБЛ) относится к наиболее распространенным заболеваниям человека, что обусловлено непрекращающимся загрязнением окружающей среды, усиливающимся табакокурением и повторяющимися респираторными инфекционными заболеваниями [1, 2]. Характерной чертой течения ХОБЛ является развитие обострений [3, 4]. Частые обострения приводят к длительному ухудшению показателей функции внешнего дыхания, более быстрому прогрессированию болезни, значимому снижению качества жизни пациентов и сопряжены с существенными экономическими затратами на лечение [5, 6]. Кроме этого, ХОБЛ является третьей лидирующей причиной смерти в мире, ежегодно от ХОБЛ умирает около 2,8 млн человек, что составляет 4,8% всех причин смерти, при этом около 50–80% больных ХОБЛ умирают именно от респираторных причин во время обострений ХОБЛ [7].
Одним из значимых патогенетических факторов ХОБЛ служит хроническое воспаление нижних отделов респираторного тракта, которое индуцировано воздействием повреждающих веществ. Воспалительная реакция при ХОБЛ многогранна, так как в ее развитии задействовано большое количество различных провоспалительных медиаторов, таких как фактор некроза опухоли-α (ФНО-α), интерлейкины 6 и 8 (ИЛ-6, ИЛ-8), лейкотриен B4 и др., что вносит определенные сложности в ведение данной группы пациентов и поддержание контроля заболевания [8]. В этой связи, наряду с утвержденными в клинических рекомендациях группами препаратов для терапии обострений ХОБЛ, продолжается поиск дополнительных потенциальных биологически активных молекул, способных повысить терапевтические возможности в лечении ХОБЛ. В частности, одной из таких молекул является глицирризиновая кислота. Эффективность включения противовоспалительных препаратов на основе глицирризиновой кислоты в терапию острых инфекций дыхательных путей, пневмонии, бронхита и аллергических заболеваний респираторного тракта продемонстрирована в большом количестве исследовательских работ и активно обсуждается в отечественной и международной медицинской литературе [9]. Вместе с тем наличие большого спектра патогенетически значимых эффектов глицирризиновой кислоты: противовоспалительное, противоаллергическое, мукоактивное и противовирусное действия – позволяет использовать ее и при ХОБЛ.
Противовоспалительный эффект глицирризиновой кислоты основан на ингибирующем влиянии на группу ферментов протеинкиназ и фермент 11-β-оксистероид-дегидрогеназы, что приводит к снижению активности фосфолипазы А2 и уменьшению образования и выбросов ключевых медиаторов воспаления (лейкотриенов, простагландинов и тромбоксанов). Глицирризиновая кислота способна ингибировать продукцию провоспалительных цитокинов, таких как ФНО-α, ИЛ-6, ИЛ-8. Более того, на сегодняшний день имеются данные экспериментальных зарубежных работ, в которых показано, что глицирризиновая кислота способна воздействовать на ключевые критические биомаркеры ХОБЛ, тесно коррелирующие со степенью тяжести и прогнозом заболевания [10, 11]. В этом свете препараты на основе глицирризиновой кислоты являются интересной и перспективной патогенетической противовоспалительной терапией при обострении ХОБЛ, что заслуживает прицельного изучения.
Цель наблюдательной программы – оценить переносимость и эффективность применения противовоспалительного препарата аммония глицирризината (АГ) (Реглисам, ЗАО «ВИФИТЕХ», Россия) в комплексном лечении пациентов с обострением ХОБЛ.
Материал и методы
Открытая проспективная наблюдательная программа по изучению опыта применения АГ в комплексном лечении пациентов с обострением ХОБЛ проводилась на базе Областного пульмонологического центра ГБУЗ «Областная клиническая больница № 3» в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации.
Критерии включения пациентов в наблюдательную программу:
- пациенты обоего пола в возрасте от 18 лет;
- диагноз: ХОБЛ, фаза обострения легкой/средней степени;
- возможность соблюдения процедур протокола;
- подписанное добровольное информированное согласие.
Критерии невключения пациентов в наблюдательную программу:
- возраст младше 18 лет;
- отсутствие диагноза ХОБЛ;
- сопутствующие или нестабильные соматические заболевания или состояния, которые, по мнению исследователей, затрудняют интерпретацию результатов лечения и приводят к невозможности проведения процедур согласно протоколу;
- индивидуальная непереносимость и повышенная чувствительность к компонентам, входящим в состав препарата;
- отказ от участия в наблюдательной программе и проведения процедур в рамках настоящего протокола;
- беременность, кормление грудью.
Набор пациентов осуществлялся в амбулаторных условиях методом сплошного отбора. Длительность наблюдения за пациентами составила 14 дней. В клиническое наблюдение были включены 60 пациентов:
- 30 пациентов (основная группа), получавших дополнительно к основной терапии заболевания в течение 14 дней ежедневно перорально АГ (Реглисам);
- 30 пациентов (контрольная группа), получавших только основную лекарственную терапию заболевания, без перорального приема АГ.
Медикаментозную терапию при обострении основного заболевания назначали согласно клиническим рекомендациям «Хроническая обструктивная болезнь легких» 2024 г. [1].
Среди исследуемых групп было 53 мужчины и 7 женщин: 27 мужчин (90%) и 3 женщины (10%) в основной группе, 26 мужчин (86,7%) и 4 женщины (13,3%) в группе контроля. Средний возраст – 67,62 ± 8,8 года и 66,5 ± 7,1 года соответственно, достоверного различия по полу и возрасту в группах не отмечено.
На протяжении всего периода наблюдения лечащий врач вел индивидуальную регистрационную карту (ИРК), где на 1-й и 14-й дни наблюдения фиксировал данные: балльная оценка симптомов (кашель, с помощью визуально-аналоговой шкалы (ВАШ), где 0 – отсутствие симптома, 10 – максимальные проявления симптома), одышка (по шкале Modified Medical Research Council Dyspnea Scale [12]), объем и характер мокроты (слизистая, слизисто-гнойная, гнойная; количество, мл/сут), слабость (по ВАШ), повышение температуры тела, оценка качества жизни (по шкале COPD Assessment Test, САТ [13]). В ИРК также фиксировали показатели спирометрии, данные теста шестиминутной ходьбы (ТШМХ), все случаи нежелательной реакции, предположительно связанные с приемом исследуемого препарата.
Статистическая обработка полученного материала осуществлялась с использованием пакета статистических программ – Statistica for Windows 12.0. Данные представлены в виде медианы и межквартильных интервалов (Ме, 25%; 75%) или % от общего числа пациентов. Вероятность р < 0,05 считали достаточной для вывода о статистически значимых различиях между вариационными рядами [14].
Результаты
Согласно спирометрической классификации GOLD 2025 г., у 1 (1,7%) пациента из 60 зарегистрирована I стадия ХОБЛ, у 20 (33,3%) – II стадия, у 33 (55%) – III стадия, и 6 пациентов (10%) имели IV стадию ХОБЛ. Распределение пациентов по группам в зависимости от стадии ХОБЛ представлено в таблице 1.
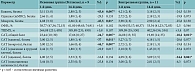
Средний объем форсированного выдоха за одну секунду (ОФВ1) у пациентов с различной тяжестью ХОБЛ составил 45,3 ± 9,2% (81,1 ± 7,3%, 59,6 ± 6,2%, 40,5 ± 3,2% и 27,6 ± 4,2% соответственно по стадиям). Средний стаж курения составил 44,6 ± 17,2 года. Характеристики клинико-функциональных параметров пациентов при динамическом наблюдении представлены в таблице 2.
Исходно основные контролируемые показатели в исследуемых группах статистически значимо не различались, что свидетельствует об их однородности. При первичной сравнительной оценке контрольных точек на 14-й день наблюдения статистически значимых различий между группами не выявлено, однако при анализе показателей в динамике внутри каждой из групп зафиксировано стойкое и достоверное преимущество в основной группе в сравнении с группой контроля (табл. 2). Так, среди пациентов, получавших АГ, на 14-й день лечения отмечено статистически значимое снижение интенсивности кашля на 42,2%, мокроты – на 44,6%, одышки – на 22,1% и балльной оценки САТ на 22,6%, в контрольной группе показатели в динамике менялись менее значимо (32,7; 42,2; 19,2 и 18,7% соответственно).
При оценке физического статуса пациентов в динамике с помощью ТШМХ выявлено, что в основной группе дистанция, проходимая пациентами, увеличилась в среднем на 9,6%, в контрольной группе – лишь на 7,5%. При сравнении объективных спирометрических показателей уровень ОФВ1 у пациентов, получавших АГ, увеличился на 12,2%, тогда как в контрольной группе данный показатель практически не изменился (+0,3%), см. табл. 2.
Для большей наглядности динамика клинико-функциональных параметров пациентов основной группы представлена на рис. 1.
С учетом присутствия в исследуемых группах пациентов с различной стадией ХОБЛ в рамках настоящей работы дополнительно была проанализирована динамика контрольных точек до и после лечения в основной и контрольных группах отдельно для II и III стадии заболевания. Поскольку пациентов с I и IV стадиями ХОБЛ было немного, в анализ данные пациенты не были включены.
Среди пациентов со II стадией ХОБЛ выявлена статистически значимая положительная динамика в основной группе в виде уменьшения выраженности кашля на 43,6%, количества отделяемой мокроты – на 45,5%, общий балл по шкале САТ снизился на 24,7%, балльные оценки вопросов шкалы САТ, оценивающих кашель и мокроту, уменьшились на 37% и 44,7% соответственно (табл. 3, рис. 2). В группе контроля достоверная, но не столь значительная положительная динамика зарегистрирована лишь относительно общего балла шкалы САТ и только в отношении уровня одышки, при этом к 14-му дню лечения зафиксирована отрицательная динамика ОФВ1 в виде снижения показателя на 2,5%.
Анализ III стадии ХОБЛ (табл. 4, рис. 3) показал положительную динамику большинства исследуемых клинико-функциональных показателей в обеих группах, однако среди пациентов основной группы отмечена более выраженная в сравнении с группой контроля степень снижения кашля (39,3% против 34,2%), одышки (21,2% против 20,5%), общего балла CAT (21,9% против 18,3%), повышения ТШМХ (18,7% против 11,7%) и ОФВ1 (16,1% против 2,1%). Достоверная позитивная динамика у пациентов основной группы, в отличие от пациентов группы контроля, прослеживалась при оценке по шкале CАТ не только в отношении кашля, мокроты и одышки, но и чувства сдавления в грудной клетке и повседневной активности (рис. 4).
За период проведения наблюдательной программы отклонений от нормы показателей общеклинических и биохимических анализов крови в обеих группах не отмечено. Нежелательные явления в основной и контрольной группах не зарегистрированы. Все пациенты отметили хорошую переносимость АГ.
Обсуждение и заключение
Глицирризиновая кислота, являющаяся фармакологической основой препарата АГ, по данным отечественных и зарубежных исследований, обладает комплексом эффектов: противовоспалительным, мукорегуляторным, противоаллергическим, противовирусным и прочими, большинство которых высоко потенциальны в лечении ХОБЛ [15–17], так как практически все эти механизмы лежат в основе обострений и неуклонного прогрессирования заболевания [18–23].
Именно по этой причине в ходе настоящей наблюдательной программы была показана более высокая терапевтическая эффективность схем терапии обострений ХОБЛ с включением АГ в сравнении с использованием исключительно стандартного лечения. Пациенты с обострением ХОБЛ, получавшие дополнительно АГ курсом 14 дней, демонстрировали стойкое и значимое снижение выраженности важных клинических симптомов заболевания (кашля – на 42,2%, мокроты – на 44,6%, одышки – на 22,1%) и улучшение объективных функциональных показателей (ТШМХ – на 9,6%, ОФВ1 – на 12,2%), в том числе параметров качества жизни больных. В контрольной группе данные показатели в динамике менялись менее значимо, в частности результаты спирометрических показателей оставались практически на исходном уровне. Важно отметить, что преимущества перечисленных позитивных эффектов сохранялись в том числе при прицельном анализе пациентов со II и III стадиями ХОБЛ. Так, на фоне терапии АГ в сравнении с группой контроля отмечена достоверная положительная динамика среди большего количества исследуемых клинико-функциональных параметров и в отношении их выраженности.
Результаты проведенной работы также показали высокий уровень безопасности и хорошую переносимость препарата АГ. Нежелательных явлений, в том числе аллергических реакций, не зарегистрировано.
Таким образом, полученные результаты позволяют рекомендовать АГ в качестве дополнительного средства для лечения пациентов с обострением ХОБЛ. Кроме того, перспективным направлением в рамках лечения ХОБЛ представляется назначение АГ на более пролонгированный период, который, согласно инструкции препарата, может составлять до 3–6 месяцев.
Авторы заявляют об отсутствии конфликта интересов.
Статья написана без финансовой поддержки.
G.L. Ignatova, PhD, Prof., V.N. Antonov, PhD, I.A. Zakharova, PhD, E.A. Makarova, E.V. Tikhonova
South-Ural State Medical University, Chelyabinsk
Regional Clinical Hospital No. 3, Chelyabinsk
Contact person: Inna A. Zakharova, zaharowa.inna2012@yandex.ru
The search for additional mechanisms for more effective control and relief of exacerbations of COPD remains relevant.
Aim. To evaluate the tolerability and efficacy of ammonium glycyrrhizinate (Reglisam, VIFITEKH, Russia) in the complex treatment of patients with exacerbation of chronic obstructive pulmonary disease (COPD).
Material and methods. An open prospective observational program involved 60 patients over 18 years of age with exacerbation of COPD: 30 formed the main group and received ammonium glycyrrhizinate for 14 days in addition to standard therapy; the control group consisted of the remaining 30 patients who did not take the study drug. On the 1st and 14th days of observation, clinical, laboratory and instrumental parameters of patients, cases of adverse reactions were recorded in the groups.
Results. In the main group on the 14th day of treatment, compared to the control, a persistent advantage was recorded in reducing cough intensity by 42.2%, dyspnea by 22.1%, quality of life score COPD Assessment Test by 22.6%, increasing the results of the 6-minute walk test by 9.6% and forced exhalation volume in one second (FEV1) by 12.2%; in the control group, these indicators changed less significantly over time: 32.7%, 19.2%, 18.7%, 7.5% and 0.3%, respectively. In a targeted analysis of patients with stages 2 and 3 COPD in the main group in comparison with the control, more significant reliable positive dynamics were determined, both among a larger number of studied clinical and functional parameters (5 vs 2 and 11 vs 9 parameters, respectively), and in relation to their severity.
Conclusion. High therapeutic efficacy of COPD exacerbation therapy regimens with the inclusion of ammonium glycyrrhizinate is shown, in the form of an effective decrease in the severity of important clinical (cough, dyspnea, sputum) and improvement of functional indicators and parameters of the quality of life of patients. The obtained data allow us to recommend ammonium glycyrrhizinate as an additional anti-inflammatory agent in the treatment of patients with exacerbation of COPD.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.