Программа наблюдения ПРОГНОЗ у пациентов с артериальной гипертонией и дополнительными факторами риска мозгового инсульта в клинической практике
- Аннотация
- Статья
- Ссылки



В целях предупреждения развития как самой АГ, так и ее грозных осложнений особую важность представляют вопросы активного и адекватного контроля уровней АД у населения. При этом важно поддерживать уровни АД на целевых значениях, которые сопряжены с наименьшим риском развития различных ССО у пациента.
В крупных рандомизированных плацебо-контролируемых исследованиях продемонстрирован клинический эффект от нормализации уровней АД, выражающийся в снижении на 42% риска развития смертельного и не смертельного мозгового инсульта (МИ), на 21% риска смерти от сердечно-сосудистых заболеваний (ССЗ) и на 14% смерти от всех причин.
Результаты крупномасштабных исследований, например, UKPDS (United Kingdom Prospective Diabetes Study), ABCD (Appropriate Blood Pressure Control in Diabetes), MDRD (Modification of Diet in Renal Disease), HOT (Hypertension Optimal Treatment), AASK (African American Intervention Study of Kidney Disease) и др. указывают на необходимость назначения большинству пациентов для достижения целевого уровня АД нескольких антигипертензивных препаратов, так как эффективность монотерапии всех основных групп антигипертензивных препаратов (АГП) невысокая и сопоставимая. Через год лечения даже при почти идеальной приверженности к нему эффект монотерапии не превышает 50% (2).
Комбинированная терапия в настоящее время – приоритетное направление в лечении больных АГ. Комбинации из двух антигипертензивных препаратов и более особенно рекомендуется назначать пациентам с дополнительными факторами риска (ФР), при субклиническом поражении органов-мишеней, сахарном диабете (СД), метаболическом синдроме, доказанных ССЗ и патологии почек. При этом очевидны преимущества именно фиксированных комбинаций АГП:
- воздействие на различные патогенетические механизмы развития АГ (в формировании АГ участвуют несколько механизмов);
- потенцирование и пролонгирование гипотензивных эффектов препаратов (нейтрализация контррегуляторных механизмов, повышающих АД);
- усиление органопротективных свойств АГП;
- снижение риска побочных явлений из-за уменьшения дозы и возможности противодействия нежелательным явлениям одного АГП другому;
- простота титрования, назначения, оптимальный и безопасный дозовый режим;
- удобство приема для больного и уменьшение стоимости лечения АГ и, как следствие, улучшение приверженности пациента к лечению.
Одним из самых частых и инвалидизирующих пациента осложнений АГ является МИ. Риск развития МИ повышается пропорционально росту АД, как диастолического, так и систолического (даже в большей степени) (3, 4). Но реальность трагедии состоит в том, что первичный МИ в значительной мере можно предотвратить, поскольку большинство главных факторов его развития поддаются модификации и контролю. Среди основных модифицируемых ФР инсульта, помимо АГ, выделяют: курение, СД, гиперхолестеринемию (ГХС), ишемическую болезнь сердца (ИБС), фибрилляцию предсердий, патологию магистральных артерий головы, нарушения гемостаза, злоупотребление алкоголем, низкую физическую активность, ожирение, оральные контрацептивы (5, 6). К ФР инсульта, не поддающихся коррекции, относят возраст, пол, этническую принадлежность и наследственность.
Установлено, что после 55-летнего возраста и у мужчин, и у женщин скорость развития МИ каждые последующие 10 лет удваивается (7). При сочетании двух и более ФР вероятность развития МИ у пациента повышается более заметно. У 20-30% пациентов с АГ встречается гипертрофия левого желудочка (ГЛЖ). Среди пациентов, страдающих АГ III степени, распространенность ГЛЖ может достигать 90%. ГЛЖ рассматривается как самостоятельный ФР развития МИ. Пятилетняя летальность при АГ, сочетающейся с ГЛЖ, составляет у мужчин 35%, у женщин – 20% и у пожилых – 50%. Адекватное лечение АГ позволяет снизить вероятность развития ГЛЖ сердца до 35%.
Первичная профилактика МИ имеет важное социальное значение и включает в себя две стратегии:
- «популяционную» – направленную на распространение знаний среди населения о факторах возникновения МИ и мероприятиях по их коррекции;
- стратегию «групп высокого риска», ставящей своей целью выявление, наблюдение и профилактическое лечение лиц с высоким риском развития МИ.
Активные профилактические меры при АГ существенно снижают заболеваемость инсультом (8). Первый шаг к профилактике МИ начинается с коррекции ФР через изменение стиля жизни пациента. Другой важный шаг – правильный выбор АГП и его дозы. Это, с одной стороны, позволяет достаточно быстро достигать у пациента целевой уровень АД, а с другой – обеспечиваются выраженные кардио- и нейропротективные эффекты. Однако органопротективные и превентивные возможности АГП могут быть сопряжены с их дополнительными свойствами.
Так, в профилактике первичного МИ успешной оказалась медикаментозная стратегия, основанная на приеме лозартана – блокатора ангиотензиновых рецепторов типа 1 (АТ1) в исследовании LIFE (Losartan Intervention For Endpoint reduction), которая у пациентов с АГ и ГЛЖ способствовала снижению риска МИ на 25% (9). Профилактическая активность лозартана (50% пациентов получали лозартан в дозе 100 мг/сут. и в 68% он назначался в сочетании с тиазидным диуретиком – гидрохлортиазидом 12,5-25 мг/сут.) в предотвращении первичного МИ показана при разных его типах (рисунок 1). Очень важно, что лозартан снижал на 70% вероятность смерти от МИ. Даже при развитии первичного МИ его последствия в виде неврологической симптоматики (например, дефекта памяти, нарушения речи) и психологических расстройств (депрессии) на терапии лозартаном были менее выражены.
Одним из возможных благоприятных механизмов действия лозартана является регресс ГЛЖ. Другой важный механизм противодействия лозартана развитию МИ связан с уменьшением размеров левого предсердия, которое происходило параллельно регрессу ГЛЖ. Известно, что увеличение размеров левого предсердия предрасполагает к МИ, поскольку риск развития фибрилляции предсердий повышается и создается почва для активации тромбообразования. Интересным оказался факт снижения (на 33%) на терапии лозартаном частоты развития эпизодов фибрилляции предсердий. В исследовании LIFE показано, что лозартан снижал риск развития МИ у пациентов с изолированной систолической АГ (на 40%), с СД (на 22%), фибрилляцией предсердий (на 49%), потребляющих алкоголь (на 27%) и без болезней сосудов (на 34%).
Снижение вероятности развития первичного МИ на фоне лозартана в исследовании LIFE можно объяснить рядом положительных эффектов препарата, установленных в клинических и экспериментальных работах:
- блокирование лозартаном (а точнее его активным метаболитом ЕХР3174) взаимодействия ангиотензина II с рецепторами АТ1;
- опосредованная положительная стимуляция АТ2-рецепторов;
- плейотропные свойства – антипролиферативный и антифиброзный эффекты, регресс гипертрофии ЛЖ, уменьшение размеров левого предсердия и толщины стенки сонной артерии, вазодилатация, противовоспалительные свойства, антиагрегационное и противоокислительное действия, нефропротекция (уменьшение альбуминурии).
Несмотря на распространенность МИ первичная его профилактика не достаточно эффективна. Для повышения ее успеха в клинической практике целесообразно выделять группу пациентов высокого риска, имеющих дополнительные ФР развития МИ и назначать им АГП с доказанным «противоинсультным» действием. Можно ожидать, что перенос стратегии профилактики первичного МИ, основанной на приеме лозартана и/или его комбинации с гидрохлортиазидом (Гизаар®), например, на Российскую популяцию пациентов с АГ будет также успешен, как и в исследовании LIFE.
Если в России ежегодно регистрируется более 400 тыс. инсультов, летальность при которых составляет 35% (140 тыс. случаев), то при назначении лозартана, в том числе в комбинации с гидрохлортиазидом в течение 5,5 лет, можно ожидать развитие первичного МИ меньше на 550 тыс. случаев, а фатального МИ – на 98 тыс. случаев (10).
К настоящему моменту в России завершена наблюдательная программа ПРОГНОЗ (ПРОГрамма Наблюдения пО ГиЗаару у пациентов с АГ с дополнительными факторами МИ). Цель программы – оценить эффективность и безопасность терапии Гизааром, представляющим собой фиксированную комбинацию блокатора АТ1 (лозартана) с тиазидным диуретиком (гидрохлортиазидом) у пациентов с АГ и дополнительными ФР инсульта в Российской Федерации на современном этапе в условиях первичного звена здравоохранения.
Основными задачами наблюдательной программы ПРОГНОЗ были оценка эффективности (возможность достижения целевого АД, регресс ГЛЖ, снижение уровня факторов атерогенеза) терапии Гизааром (препарат компании «Мерк Шарп и Доум») в лечении АГ, сочетающейся с дополнительными ФР, в амбулаторной практике врача и анализ безопасности терапии Гизааром и возможности снижения величины суммарного риска ССО у пациентов с высоким риском МИ, а также влияния программы ПРОГНОЗ на повышение приверженности пациентов антигипертензивной терапии.
Материал и методы
Пациенты в программе. В программу было включено 513 амбулаторных пациентов из разных медицинских учреждений России с первичной АГ – уровнем систолического АД (САД) > 140 мм рт. ст. и/или диастолического АД (ДАД) > 90 мм рт. ст. (а для больных СД > 130/80 мм рт. ст.) при отсутствии или нерегулярной терапии, или на фоне регулярной антигипертензивной терапии на протяжении как минимум двух недель.
Включенные в программу пациенты помимо АГ имели один и более из ниже перечисленных ФР: курение, ГХС (уровень общего холестерина (ХС) более 5,0 ммоль/л), СД, ГЛЖ (толщиной межжелудочковой перегородки или задней стенки ЛЖ ≥ 1,3 см по данным эхокардиографии), ИБС, признаками утолщения стенки сонных артерий (толщина слоя комплекса интима-медиа ≥ 0,9 мм) или наличием атеросклеротической бляшки, эпизодами фибрилляции предсердий в анамнезе.
В программу не включались пациенты, перенесшие любое нарушение мозгового кровообращения (МИ, транзиторную ишемическую атаку), имеющие вторичную и злокачественную АГ, выраженную почечную и печеночную недостаточность.
По решению лечащего врача (общей практики или кардиолога) применялась одна из следующих терапевтических стратегий (рисунок 2):
- пациентам, не получавшим до включения в программу антигипертензивную терапию, назначался Гизаар® (группа I);
- пациентам, получавшим до включения в программу неэффективную монотерапию, производилась ее замена на препарат Гизаар® (группа II);
- пациентам, получавшим до включения в программу неэффективную антигипертензивную терапию, производилось ее усиление – добавлялся препарат Гизаар® (группа III).
Терапия в программе. Исходно (на визите 1) пациентам рекомендовано было назначать 1 табл. Гизаара (лозартан 50 мг + гидрохлортиазид 12,5 мг). При недостижении целевого уровня АД < 140/90 мм рт. ст. (< 130/80 мм рт. ст для пациентов с СД) на визите 2 (т.е. через 2 недели) рекомендовалось увеличение дозы Гизаара до 2 табл. (лозартан 100 мг + гидрохлортиазид 25 мг). Если целевое значение АД не достигалось, то через 2 мес. от начала программы (на визите 3) или через 6 мес. (на визите 4) к терапии пациента присоединялся дополнительный АГП (по усмотрению лечащего врача). В случае развития клинически значимой гипотонии (уровень САД < 100 мм рт. ст. и/или ДАД < 60 мм рт. ст.) при приеме только Гизаара производилась коррекция его дозы, а при приеме нескольких АГП производилось снижение дозы или даже отмена одного из АГП, кроме Гизаара.
Итак, в течение 6 мес. (с 1 по 4 визиты) в программе осуществлялось активное наблюдение за пациентом. Последующие 6 мес. (с 4 по 5 визиты) пациенту рекомендовалось продолжать подобранную антигипертензивную терапию. При этом от пациента не требовалось обязательного посещения врача. Однако, если врач считал необходимым, он мог в любой момент наблюдения за пациентом попросить его прийти на дополнительный прием.Общая продолжительность программы ПРОГНОЗ составляла 12 месяцев и включала 5 обязательных визитов пациента к врачу. Протокол предусматривал досрочное прекращение участия в программе при возникновении выраженных побочных явлений (рисунок 3).
Обследование пациентов в программе. Перед включением пациентов в программу собирался полный анамнез, учитывались ФР, демографические показатели (пол и возраст). Физикальный осмотр пациента включал в себя определение индекса массы тела (ИМТ), трехразовое измерение АД методом Короткова, проведение эхокардиографии (ЭхоКГ) с оценкой размеров камер сердца, толщины стенок миокарда и фракции выброса, определение уровней липидов, мочевой кислоты и глюкозы (для пациентов с СД) в сыворотке крови.
В программе оценивалось самочувствие пациента и переносимость терапии Гизааром, учитывались нежелательные сердечно-сосудистые явления. Производилась оценка динамики величины сердечно-сосудистого риска в процессе терапии у пациентов с высоким риском развития первичного МИ в условиях реальной клинической практики.
Статистический анализ. При статистической обработке результатов использовали компьютерную программу SAS (версия 6.12). Применялись как стандартные методы описательной статистики (вычисление средних, стандартных отклонений, квинтилей и ранговых статистик и т.д.), так и известные критерии значимости (c2 , t-критерий Стьюдента, F-критерий Фишера). Непрерывные величины представлены в виде М ± SD. Кроме того, были использованы методы аналитической статистики: дисперсионно-ковариационный анализ в версии процедуры SAS PROC GLM (обобщенный линейный анализ).
Результаты и их обсуждение
Антигипертензивный эффект Гизаара. В исследование вошло 513 пациентов (средний возраст 53,1 ± 0,5 лет), из которых 52,6% составляли мужчины. При этом каждый третий в программе пациент был в возрасте до 50 лет (32,4%), а 64,9% – в возрасте от 50 до 60 лет, т.е. преобладали пациенты трудоспособного возраста.
Среди включенных в программу пациентов один ФР был у 13,5%, два ФР – у 36,1%. Чаще у пациентов выявлялась комбинация 3 и более ФР. При этом курило 35,6%, имели повышенный уровень ХС 86,4%, ГЛЖ – 70,2%, утолщение стенок сонных артерий – 30,4%, АГ у близких родственников – 73,9%, ГХС – 86,4%.
У 16,4% пациентов течение АГ осложнено развитием СД, 36,2% ИБС и 10% эпизодами фибрилляции предсердий.
Несмотря на то, что до включения в исследования 82,9% пациентов получало антигипертензивную терапию, а из них 54,9% – два и более АГП, у всех пациентов уровень АД был выше 140/90 мм рт. ст. Очевидно, что важная причина недостаточного гипотензивного эффекта комбинированной терапии при АГ у пациентов с несколькими ФР – назначение АГП в нерациональных комбинациях. Другая причина – нерегулярный прием АГП: 55,4% пациентов принимали АГП курсами или эпизодически. При этом такой показатель, как высокая стоимость препарата не был решающим при отказе пациента от лечения (только 4,2% пациента назвали его как причину нерегулярного приема или отказа от приема АГП).
Следует отметить, что среди пациентов с АГ, имевших ГХС, терапию статинами получали только 33,3%.
Исходно препарат ГизаарÒ впервые был назначен 18,9% пациентов, у 22,6% пациентов он был добавлен к антигипертензивной терапии, а у остальных пациентов заменил неэффективные АГП. Продолжали принимать 1 табл. Гизаара (лозартан 50 мг + гидрохлортиазид 12,5 мг) через 6 мес. 10,3% пациентов и через 12 мес. 9,5%, а остальные получали 2 табл. Гизаара (лозартан 100 мг + гидрохлортиазид 25 мг). Дополнительное назначение другого АГП к такой терапии Гизааром потребовалось лишь у 18,8% к 6 мес. и у 24,5% к 12 мес.
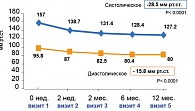
При приеме 1 табл. Гизаара в качестве «сольной» терапии или его добавления к ранее назначенным АГП через 2 недели (на визите 2) отмечено снижение уровней САД на 18,3 мм рт. ст., а ДАД – на 8,9 мм рт. ст. (рисунок 4). Через 6 мес. (к визиту 4) снижение от исходного уровня САД составило 28,6 мм рт. ст. и уровня ДАД – 15,4 мм рт. ст., а через 12 мес., соответственно, 28,5 мм рт. ст. и 15,8 мм рт. ст. Итак, во втором полугодии пациентам при отсутствии контроля со стороны врача удалось на адекватно подобранной терапии сохранить средние уровни АД, достигнутые к 4 визиту (т.е. к 6-му мес.) активного врачебного наблюдения.
Тактика антигипертензивной терапии, основанная на применении комбинированного препарата ГизаарÒ, позволила в повседневной практике врача добиться эффективного контроля АД (по достижению целевого уровня) у пациентов с дополнительными ФР развития МИ уже в ранние сроки: через 2 нед. (на 1 табл. Гизаара) у 41,6% пациентов и через 2 мес. (на 1-2 табл. Гизаара) у 74,2%. В более отдаленные сроки лечения, т.е. через 6 мес. целевой уровень АД достигали 83,9% пациентов и через 12 мес. – 89,8%.
Оценка антигипертензивной терапии, проводимая врачом, указывала на ее высокую эффективность (по снижению уровня АД) у большинства пациентов: очень хорошую у 28,5% и хорошую у 69,3%.
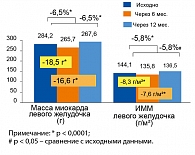
Параметры ЭХоКГ на терапии Гизааром. Анализ изменений ЭХоКГ показателей у пациентов высокого сердечно-сосудистого риска на фоне терапии Гизааром свидетельствовал об уменьшении массы миокарда ЛЖ от исходного через 6 мес. на 6,5% (р < 0,0001) и индекса массы миокарда ЛЖ – на 5,8% (р < 0,0001) (рисунок 5). В последующие 6 мес. наблюдения (т.е. к 12 мес. от начала программы) положительные сдвиги, достигнутые в регрессе ГЛЖ, сохранялись на том же уровне. Следует отметить, что снижение индекса массы миокарда ЛЖ в процессе терапии Гизааром в основном происходило за счет подгруппы пациентов с исходной ГЛЖ. У этих пациентов индекс массы миокарда ЛЖ достоверно уменьшился за год лечения на 10,8% (р < 0,0001). В результате терапии Гизааром количество пациентов с ГЛЖ по данным ЭхоКГ сократилось: с 70,2% пациентов исходно до 62,9% пациентов через 6 мес. и до 54,2% пациентов к году наблюдения.
В процессе терапии Гизааром произошло уменьшение толщины межжелудочковой перегородки ЛЖ с 1,21 ± 0,01 см исходно до 1,14 см через 12 мес. (р < 0,0001) и задней стенки ЛЖ, соответственно, с 1,17 ± 0,01 см до 1,11 ± 0,01 см (р < 0,0001). Индекс относительной толщины стенок ЛЖ за год терапии также достоверно уменьшился на 6,3% (р < 0,0001).
На фоне лечения пациентов препаратом Гизаар® обращало на себя внимание позитивное уменьшение размеров левого предсердия с 3,38 ± 0,02 см исходно до 3,76 ± 0,02 см (р < 0,0001) через 6 мес. и до 3,30 ± 0,02 см (р < 0,0001) через 12 мес. К концу года лечения у пациентов наблюдалось некоторое увеличение фракции выброса ЛЖ на 2,9% (р < 0,0001). При этом через 6 мес. отмечалось хотя и малое (на 1,4%), но достоверное (р < 0,0001) снижение конечного диастолического размера ЛЖ.
Итак, в процессе годичной антигипертензивной терапии, основанной на приеме комбинированного препарата Гизаар® и направленной на достижение целевого уровня АД, у пациентов с АГ удается сдерживать процессы патологического ремоделирования ЛЖ за счет уменьшения ГЛЖ и размеров полостей сердца на фоне некоторого улучшения систолической и диастолической функций ЛЖ.
Липидные и метаболические факторы атерогенеза на терапии Гизааром. Важной характеристикой современного АГП является его метаболическая нейтральность. Годичный прием пациентами препарата Гизаар® (лозартан/гидрохлортиазид) вызывал позитивные изменения ряда метаболических факторов, вовлеченных в атерогенез.
У пациентов АГ, сочетающейся с другими ФР, через 6 мес. отмечено достоверное снижение уровня общего ХС (на 14,9%, р < 0,0001) за счет его атерогенной фракции ХС липопротеидов низкой плотности (на 13,7%, р < 0,0001). Следует отметить, что на комбинации препаратом лозартана с гидрохлортиазидом концентрация в крови антиатерогенного ХС липопротеидов высокой плотности оставалась стабильной (исходно 1,38 ± 0,04 ммоль/л и через 12 мес. 1,19 ± 0,14 ммоль/л, р > 0,05).
Концентрация глюкозы в крови в общей группе достоверно снижалась (на 4%; р < 0,0001). При этом снижение гликемии у пациентов АГ без СД через 6 мес. достигало 2,3% (р < 0,0001), но к 12 мес. возвращалось к исходному (5,20 ± 0,04 ммоль/л). У пациентов с СД 2 типа снижение содержания глюкозы в крови было более выраженным: от исходного на 10,2% к 6 мес. (р < 0,0001) и на 15,5% к 12 мес. (р < 0,0001). Становится очевидным, что АГП из класса блокаторов АТ1-рецепторов в программе ПРОГНОЗ – лозартан – способен нивелировать возможное неблагоприятное влияние тиазидного диуретика (гидрохлортиазида) в дозах 12,5 и 25 мг на углеводный обмен. Это еще один аргумент в пользу более активного использования врачом в своей повседневной практике именно фиксированных комбинаций АГП, основанных на рациональном подборе лекарств.
В программе ПРОГНОЗ, проводимой в условиях реальной клинической практики, подтвердилось гипоурикемическое действие лозартана, входящего в состав препарата Гизаар®. Уже в ранние сроки лечения через 2 мес. отмечено снижение концентрации мочевой кислоты в крови на 6,9% от исходного (р < 0,0001). Следует заметить, что гипоурикемический и урикозурический эффекты не характерны для других блокаторов рецепторов АТ1 и являются особенностью именно лозартана (11). Отмечаемое в других исследованиях дозозависимое влияние лозартана на гиперурикемию подтвердилось и в программе ПРОГНОЗ: через 6 мес. на фоне увеличения доз лозартана в составе препарата Гизаар® с 50 мг до 100 мг содержание в крови мочевой кислоты снизилось на 8,9% (р < 0,0001). Очень важно, что лозартан может уменьшать прирост концентрации мочевой кислоты в крови, индуцированной гидрохлортиазидом (12).
Важность контроля уровня мочевой кислоты в крови у пациентов приобретает все большее значение (13). Так, в литературе активно обсуждается роль мочевой кислоты в регуляции АД и развитии АГ. Известно, что мочевая кислота стимулирует локальную и системную ренин-ангиотензиновую систему, блокирует выделение оксида азота из эндотелиальных клеток. Повышение мочевой кислоты в эксперименте (у крыс) приводит к развитию солечувствительности, повреждению микрососудов почек, развитию интерстициального нефрита (13).
Снижение риска осложнений на терапии Гизааром. Главное условие клинической успешности антигипертензивной терапии, проводимой в условиях практического здравоохранения, – это ее регулярность и адекватность. Хороший контроль уровней АД на фоне терапии Гизааром определяет высокую приверженность пациентов и дает надежду на благоприятный профилактический эффект.
В процессе реализации наблюдательной программы ПРОГНОЗ у пациентов отмечена положительная динамика в снижении риска развития серьезных ССО. Так, если пациенты с АГ и дополнительными ФР непрерывно принимают Гизаар® в течение года, то у них можно ожидать снижение риска развития МИ с 4,47 до 1,57 (т.е. в 2,8 раза, р < 0,0001). Причем достоверное (р < 0,0001) снижение риска развития МИ можно ожидать при любой его исходной величине: при низком риске (с 1,86 до 1,03, т.е. в 1,8 раза), умеренном риске (с 3,56 до 1,75, т.е. в 2,03 раза) и высоком риске (с 6,94 до 3,11, т.е. в 3,8 раза).
При непрерывном в течение года приеме препарата Гизаар® у пациентов с АГ можно ожидать уменьшение смерти от ИБС в 2 раза (исходный риск 10,74 и через 12 мес. 5,26, р < 0,0001) и смерти от любого ССЗ в 2,1 раза (исходный риск 15,32 и через 12 мес. 7,33, р < 0,0001).
Переносимость препарата Гизаар®. В программе ПРОГНОЗ нежелательные явления регистрировались только у 5 пациентов (менее 1% случаев): у 1 пациента отмечалась головная боль, у 1 пациента развился бронхоспазм, у 1 пациента произошло обострение подагры и у 2 пациентов имелась аллергическая реакция в виде крапивницы. В тоже время отмена препарата потребовалась 4 пациентам.
В целом наблюдение за пациентами с АГ, принимающими препарат Гизаар® в течение года, продемонстрировало его хорошую (у 60,2% пациентов) и очень хорошую (у 37,9% пациентов) переносимость, что подтверждает его высокий профиль безопасности для пациентов с АГ, в том числе имеющих дополнительные ФР (9).
Выводы программы ПРОГНОЗ
Анализ полученных в годичной наблюдательной программе ПРОГНОЗ результатов позволяет сделать несколько важных для реальной клинической практики выводов:
- контроль уровней АД у пациентов АГ с высоким риском развития МИ недостаточен;
- информированность пациентов о важности постоянного приема АГП низкая; годичная терапия фиксированной комбинацией (преимущественно полнодозовой) – препаратом Гизаар®, доступным к применению в амбулаторной практике, нормализует уровни АД и поддерживает их на целевых значениях у большинства (89,8%) пациентов АГ и сопутствующими ФР;
- на фоне годичного приема Гизаара можно ожидать снижение риска серьезных ССО (МИ, смерти от ИБС и любого ССЗ) в условиях практического здравоохранения; годичная терапия Гизааром вызывает позитивные органопротективные и антиатерогенные эффекты: регресс ГЛЖ, улучшение структурно-геометрических и функциональных параметров сердца, снижение факторов атерогенеза (содержания в крови общего ХС, ХС ЛНП, глюкозы и мочевой кислоты);
- высокая эффективность и хорошая переносимость препарата Гизаар®, сочетающаяся с удобством его приема, легкостью титрования обеспечивает высокую приверженность пациентов назначаемой терапии.
Заключение
Таким образом, назначение эффективной и безопасной терапии в виде фиксированной (преимущественно полнодозовой) комбинации – препарата Гизаар® – дает основание для более широкого его применения в реальной клинической практике у пациентов с АГ с дополнительными ФР (курение и ГХС) или поражениями органов-мишеней (ГЛЖ, признаки утолщения стенки сонных артерий), или сопутствующей патологией (ИБС, СД, фибрилляция предсердий) с целью органопротекции и профилактики осложнений.
Программа ПРОГНОЗ наглядно продемонстрировала реальность и полезность достижения адекватного контроля АД среди пациентов АГ высокого риска.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.