Регресс ринофимы на фоне фотодинамической терапии базальноклеточного рака кожи кончика носа
- Аннотация
- Статья
- Ссылки
- English

Введение
Ринофима – патологическое состояние, характеризующееся узловатым разрастанием и утолщением кожи носа, иногда с переходом на кожу щек, лба с гиперплазией сальных желез, расширенными фолликулярными отверстиями, а на поздних стадиях – фиброзом, приводящим к деформации и потере нормальных анатомических контуров носа и лица [1, 2]. Данный процесс рассматривается как результат длительно существующей розацеа и чаще встречается у пациентов мужского пола старше 50 лет [3, 4]. Основным видом лечения данной нозологии является хирургическое удаление гипертрофированных тканей с формированием исходных контуров носа и при необходимости восстановление функции носовых дыхательных путей. Возможно комбинированное применение хирургического и лазерного методов с последующей дермабразией для более точного контурирования носа [5–7]. При лечении ринофимы с помощью лазера наибольшее распространение получили карбоновый лазер (CO2; 10,600 мкм), диодный лазер (808 нм), эрбиевый лазер (ER: алюмоиттриевый гранат (YAG), 2940 нм), неодимовый лазер (Nd: YAG, 1064 нм) и лазер KTP (Nd: YAG, 532 мкм) [8]. Любой из перечисленных методов достаточно травматичен и не всегда хорошо переносится пациентами, особенно старшего возраста.
Базальноклеточный рак (БКР) представляет собой медленно растущее, местно-деструирующее злокачественное немеланоцитарное новообразование кожи с низким метастатическим потенциалом [9]. БКР является самым распространенным злокачественным новообразованием кожи в мире с неуклонным ростом заболеваемости [15]. В дополнение к генетическим факторам, способствующим развитию БКР, основным провоцирующим экзогенным агентом является УФ-излучение, где особое значение имеют эпизоды солнечных ожогов в детстве и подростковом возрасте, а также фототипы I–II кожи [10–14]. С учетом редких случаев формирования БКР на фоне ринофимы выявить их корреляционную связь не представляется возможным. Несмотря на различные теории (травматизация, формирование фиброзного рубцевания, присутствующего в ринофиме), одномоментное сочетание этих двух нозологий может объяснять возраст пациентов, а также наиболее частая локализация БКР на коже головы и шеи, включая область носа [1, 16]. Принципы лечения БКР основываются на характеристиках опухоли (размеры, локализация, толщина), количестве очагов, морфологическом типе, а также анамнестических данных (первичное образование или рецидив) и общесоматическом состоянии пациента. На основании этих данных рассматривают следующие методы лечения: хирургический (стандартное иссечение или микрографическая хирургия (Mohs)); лучевая терапия (близкофокусная, дистанционная); местная лекарственная терапия (имиквимод 5%, 5-фторурацил 5%); системная терапия (ингибиторы сигнального пути Hedgehog – висмодегиб, сонидегиб), а также физические деструктивные методы (электроэксцизия, криодеструкция, фотодинамическая терапия (ФДТ)) [17–22]. Принцип ФДТ основан на местном или системном применении светочувствительного соединения – фотосенсибилизатора, интенсивно накапливающегося в патологических тканях. Данные молекулы поглощают свет соответствующей длины волны лазерного излучения, инициируя активацию процессов, приводящих к избирательному разрушению опухолевых клеток путем активации молекул кислорода [23–25]. Широкое распространение получили топические фотосенсибилизаторы с использованием аминолевулиновой кислоты (АМК) и системные фотосенсибилизаторы на основе хлорина (димеглюмин хлорин Е6, моно-L-аспартил-хлорин е6, Фотохлор, Фоторан) в сочетании с длинами волн в диапазоне 600–670 нм при применении диодного лазера [26–29].
Клинический случай
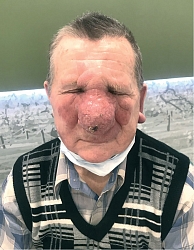
Пациент 79 лет с длительно существующей ринофимой обратился с жалобами на новообразование кожи в области кончика носа. Появление опухоли заметил около 6–8 месяцев назад. Отмечал постепенное увеличение размеров новообразования, появление эрозий на фоне периодической травматизации, без признаков болезненности и зуда.
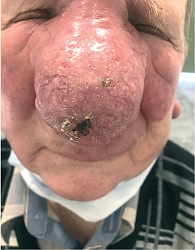
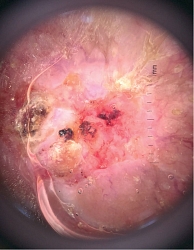
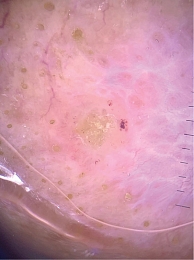
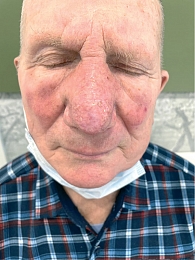
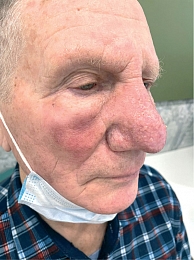
Локальный статус: нос примерно в два раза увеличен в размерах, ярко-красного цвета, его кожа утолщена, содержит расширенные фолликулярные отверстия. Щеки и лоб над переносицей гиперемированы, утолщены, отечны, фолликулярный рисунок подчеркнут. На коже кончика носа определяется новообразование в виде бляшки размерами до 1,8 см в диаметре, округлой формы, темно-красного цвета, на поверхности бляшки – корка черно-бурого цвета. Под коркой – эрозия, которая при снятии корки кровоточит. Регионарные лимфатические узлы не увеличены. Дерматоскопическое исследование новообразования кожи кончика носа: определяются структуры по типу «хризалид», древовидные сосуды среднего и крупного калибра, геморрагическая корка, эрозия и чешуйки, а также гиперплазированные фолликулярные устья.
Остальной кожный покров и видимые слизистые свободны от высыпаний, придатки кожи не изменены. Клинический диагноз: «базальноклеточный рак кожи кончика носа сT1N0M0 I st.» (рис. 1–3).
Проведено цитологическое исследование скарификата с новообразования кончика носа, по результатам которого клинический диагноз БКР подтвержден.
С учетом локализации образования, возраста пациента и наличия сопутствующего дерматологического заболевания (ринофима) онкологическим консилиумом рекомендовано проведение ФДТ новообразования кончика носа.
При госпитализации: через два часа после системного введения раствора Фоторана в дозировке 1 мг/кг проведены флуоресцентная диагностика и спектроскопия. Уточнены границы опухоли, проведен сеанс лазерного облучения. Суммарная доза дистанционного облучения: WS (доза световой энергии) – 100 Дж/см2; PS (плотность мощности излучения) – 250 мВт/см2, длина волны – 662 нм. Одномоментно проведен сеанс лазерной гипертермии опухоли при температуре 43 °C продолжительностью 20 минут с PS 6000 мВт/см2.
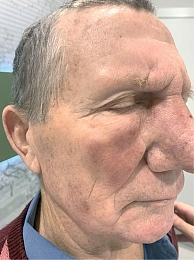
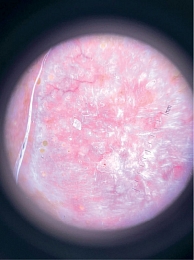
Через шесть месяцев после проведенного лечения пациент приглашен на контрольный осмотр для диспансерного наблюдения. При клиническом осмотре отмечены значительное уменьшение размеров носа, восстановление его естественной анатомической формы, исчезновение эритемы и отечности кожи, уменьшение выраженности фолликулярных отверстий. За предшествующий период наблюдения дополнительное лечение розацеа (ринофимы) не проводилось. На кончике носа определяется рубцовый дефект белесоватого цвета после проведенной ФДТ, с краевым участком рецидива БКР в виде очаговой эритемы до 0,5 см в диаметре, подтвержденного на основании дерматоскопического и цитологического исследований. С учетом результата ФДТ на очаг БКР и положительного эффекта на течение сопутствующего заболевания (ринофимы) онкологическим консилиумом рекомендовано проведение повторной ФДТ рецидива БКР кожи кончика носа с исходными параметрами (рис. 4–6).
При контрольном осмотре через 12 месяцев с момента первого сеанса ФДТ отмечено отсутствие клинических и дерматоскопических признаков БКР кожи кончика носа, а также стойкий регресс ринофимы (рис. 7–9).
Обсуждение
На момент проведения данного исследования в национальной медицинской библиотеке PubMed был описан только один случай применения ФДТ при ринофиме [30]. В представленной публикации от 2004 г. исходно использовалось пероральное введение фотосенсибилизатора из группы порфиринов (АМК). При появлении рецидива, а также индивидуальной непереносимости пероральный метод был заменен на местное применение АМК в виде 20% мази, также с последующим рецидивом ринофимы.
Представленный клинический случай показывает, что однократный сеанс ФДТ с системным (парентеральным) введением фотосенсибилизатора на основе хлорина может давать стойкий регресс ринофимы. С учетом того что метод ФДТ активно применяется при розацеа, следует расширить его терапевтические показания до запущенных форм розацеа-ринофимы, а также ринофимы в сочетании с БКР с применением фотосенсибилизаторов на основе хлорина.
Заключение
Несмотря на редкое сочетание, различный патогенез и клинические проявления, и БКР кожи, и ринофима характеризуются местными изменениями кожи и мягких тканей, приводящими к их деформации и нарушениям анатомических контуров лица. В связи с этим в комплекс лечебных мероприятий должно входить не только радикальное удаление патологически измененных тканей, но и достижение приемлемого эстетического результата без риска осложнений для пациентов. Описанный клинический случай демонстрирует атравматичность метода ФДТ и, несмотря на краевой рецидив БКР, его эффективность в долгосрочной перспективе (через год) как в отношении ринофимы, так и БКР. Предложенный способ лечения легко воспроизводим, хорошо переносится больными, безопасен, позволяет у пациентов с БКР в сочетании с ринофимой достичь полной ремиссии.
R.A. Ravodin, PhD, Prof., L.S. Kruglova, PhD, Prof., S.P. Seleznev
City Clinical Oncological Hospital No. 1, Moscow
Central State Medical Academy of Department of Presidential Affairs, Moscow
Contact person: Larisa S. Kruglova, kruglovals@mail.ru
The article describes a case of regression of rhinophyma against the background of photodynamic therapy of basal cell carcinoma of the skin of the nose tip. After a single session of photodynamic therapy using a systemic photosensitizer based on chloride (photoran), there was a significant decrease in the size of the nose (rhinophyma), the disappearance of erythema, puffiness, and the formation of the initial contours of the face of this anatomical area. Despite the marginal recurrence of basal cell carcinoma after six months at the site of previous treatment and a repeat session of photodynamic therapy, after one year of dynamic follow-up, remission of basal cell carcinoma and regression of rhinophyma persist. The described method of treatment is atraumatic, easily reproducible, well tolerated by patients, safe and allows patients with basal cell carcinoma in combination with rhinophyma to achieve complete remission of both diseases.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.