количество статей
7385
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Результаты применения препарата Cонизин при гиперплазии простаты
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Урология и Нефрология" №4
- Аннотация
- Статья
- Ссылки
В статье приведены результаты обследования и лечения мужчин, страдающих доброкачественной гиперплазией предстательной железы. В качестве терапии 50 пациентов получали препарат Сонизин (0,4 мг) в течение 6–19 месяцев.
В результате лечения улучшились параметры мочеиспускания, повысилось качество жизни. Прием Сонизина позволил снизить риск острой ишурии и в ряде случаев подготовить больных к трансуретральной резекции простаты.
В статье приведены результаты обследования и лечения мужчин, страдающих доброкачественной гиперплазией предстательной железы. В качестве терапии 50 пациентов получали препарат Сонизин (0,4 мг) в течение 6–19 месяцев.
В результате лечения улучшились параметры мочеиспускания, повысилось качество жизни. Прием Сонизина позволил снизить риск острой ишурии и в ряде случаев подготовить больных к трансуретральной резекции простаты.
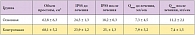
Таблица 1. Результаты проведенной терапии
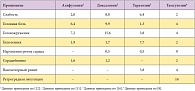
Таблица 2. Частота побочных реакций при лечении различными α-АБ у пациентов, %
Введение
Доброкачественная гиперплазия предстательной железы (ДГПЖ) – заболевание, наиболее часто встречающееся у мужчин пожилого и старческого возраста [9]. При аутопсии морфологические признаки гиперплазии простаты выявляются более чем у 40% мужчин в возрасте 40–50 лет и более чем у 90% мужчин в возрасте 80 лет [4, 15]. Считается, что большинство мужчин старше 50 лет имеют те или иные симптомы ДГПЖ [13]. Социальная значимость и актуальность проблемы ДГПЖ подтверждается демографическими исследованиями ВОЗ, которые свидетельствуют о значительно м увеличении количества людей старше 60 лет среди населения планеты.
Наиболее частыми осложнениями ДГПЖ являются инфекции мочевых путей, острая и хроническая задержка мочеиспускания, формирование камней в мочевом пузыре, развитие хронической почечной недостаточности [14]. Острая ишурия наблюдается у больных ДГПЖ без лечения с частотой от 0,4 до 6% и зачастую возникает у пациентов преклонного возраста с тяжелым интеркуррентным фоном [2, 9]. При наличии интеркуррентных заболеваний своевременное выполнение операции, направленной на восстановление мочеиспускания, не представляется возможным из-за риска развития осложнений, связанных с декомпенсацией сердечно-легочной, пищеварительной, эндокринной и нервной систем больного. Зачастую деривация мочи у этих пациентов осуществляется посредством надлобкового мочепузырного свища [6]. Эпизоды острой ишурии с последующей катетеризацией мочевого пузыря, а возможно, и цистостомией, безусловно, снижают работоспособность пациентов и нередко приводят к их инвалидизации.
Цистостомия у больных гиперплазией простаты, показаниями к которой помимо острой ишурии являются острый простатит, хроническая задержка мочеиспускания с нарушением функции почек, обусловленной ретенцией мочи, нередко становится причиной с циальной дезадаптации [20]. Основные проявления ДГПЖ можно разделить на две группы симптомов: ирритативные (учащенные, повелительные позывы к мочеиспусканию, ночная поллакиурия) и обструктивные (слабая струя мочи, ощущение неполного опорожнения мочевого пузыря, необходимость натуживания при мочеиспускании). Описанная клиническая картина с нарушением пассажа мочи понижним мочевыводящим путям снижает показатели качества жизни пациентов с ДГПЖ (IPSS и QoL) [3].
Каковы же патогенетические аспекты медикаментозной терапии доброкачественной гиперплазии простаты? В исследованиях было установлено, что адренорецепторы подтипа α1А в значительном количестве присутствуют в предстательной железе и составляют более 70% всех ее α1-адренорецепторов [10]. Считается, что именно эти рецепторы преимущественно ответственны за сокращение гладкомышечных элементов предстательной железы и оказывают существенное влияние на развитие динамической обструкции при гиперплазии простаты. В противоположность этому, 60–70% рецепторов подтипа α1D верифицируются в уретре, стенке мочевого пузыря и нижних отделах мочеточников. Одновременно предполагают, что подтип α1В участвует в сокращении гладкомышечных элементов стенок основных артерий человека и отвечает за регуляцию артериального давления и возникновение побочных реакций при применении α1-адреноблокаторов (α1-АБ).
Клинический эффект α1-АБ зависит от избирательности действия на различные подтипы рецепторов. Блокада α1А-адренорецепторов приводит к снижению тонуса гладкомышечных структур шейки мочевого пузыря и предстательной железы, что, в свою очередь, проявляется уменьшением уретрального сопротивления и, как следствие, выраженности инфравезикальной обструкции (фаза опорожнения мочевого пузыря). Блокада α1А- и α1D-адренорецепторов в мочевом пузыре ингибирует сокращение мышечных элементов детрузора, что приводит к уменьшению его чувствительности и снижению выраженности симптомов фазы накопления (ирритативных). Установлено, что дисфункция мочевого пузыря при аденоме предстательной железы во многом связана с развитием гипоксии детрузора, сопровождающейся изменениями на ультраструктурном уровне. По мнению О.Б. Лорана и Е.Л. Вишневского [5], применение α1-АБ не только снижает тонус гладкомышечных элементов шейки мочевого пузыря, предстательной железы и простатического отдела уретры, но и способствует лучшей оксигенации детрузора за счет вазодилатации пузырных артерий, оказывая позитивное влияние на обменные процессы в стенке мочевого пузыря.
Как эффективные препараты для лечения ДГПЖ α1-АБ применяются на протяжении последних 40 лет. В 2000 г. Управлением по контролю за качеством пищевых продуктов и медикаментов США (FDA) был одобрен уроселективный α1-адреноблокатор – тамсулозин [18]. Исследованиями MTOPS [17] определена роль α1-АБ в лечении ДГПЖ – они способствуют уменьшению дизурии, снижают риск развития острой задержки мочеиспускания. Таким образом, в настоящее время комбинированная терапия α1-АБ считается первой линией лечения мужчин с умеренными симптомами ДГПЖ [19].
Цель исследования
Основной задачей нашего исследования была оценка эффективности терапии α1-АБ, возможностей уменьшения риска острой ишурии и использования препаратов в качестве предоперационной подготовки. Предполагалось, что применение α1-АБ улучшает функциональное состояние мочевого пузыря и тем самым позволяет выиграть время, необходимое для проведения терапии, направленной на подготовку больного к ТУР доброкачественной гиперплазии простаты, предупреждает развитие острой задержки мочеиспускания.
Материалы и методы
В клинике урологии им. Р.М. Фронштейна Первого МГМУ им. И.М. Сеченова в период с сентября 2008 по май 2011 г. проводилась оценка клинической эффективности и безопасности применения препарата тамсулозин. В основную группу вошли 50 мужчин в возрасте от 54 до 80 лет, которым проводилась терапия препаратом Сонизин 0,4 мг 1 раз в день в течение 6–19 месяцев. В контрольную группу были включены 13 пациентов в возрасте от 64 до 76 лет, которые не получали лечения из-за невозможности применения α1-АБ в связи с хронической сердечной недостаточностью. Возможность назначения α1-АБ исходя из соматического статуса согласовывалась с терапевтом. Из исследования были исключены больные с подозрением на рак простаты (повышенный уровень ПСА), высоким риском развития острой задержки мочеиспускания (эпизоды острой задержки мочеиспускания в анамнезе, Qmax < 5 мл/сек, более 100 мл остаточной мочи), камнями мочевого пузыря и объемом простаты более 100 см3. Изучалась динамика на основании показателей объема предстательной железы, урофлоуметрии, ПСА, баллов по шкале IPSS.
Результаты исследования
В основной группе через 6 месяцев от начала лечения суммарный балл симптомов по шкале IPSS снизился на 6,2 ± 0,9 (p < 0,05). Максимальная скорость мочеиспускания в среднем увеличилась до 11,5 ± 2,4 мл/сек. В контрольной группе отмечен незначительный рост суммарного балла симптомов по шкале IPSS на 1,3 ± 1,2 (различия статистически недостоверны) и ухудшение параметров мочеиспускания до 7,4 ± 1,5 мл/сек (различия статистически недостоверны). Размеры предстательной железы не изменились в обеих группах (табл. 1). У 1 пациента (2%) основной группы возникла задержка мочеиспускания. В контрольной группе у 2 больных (15,4%) развилась острая ишурия, потребовавшая катетеризации и назначения антибактериальной и противовоспалительной терапии, после чего мочеиспускание восстановилось. Однако спустя некоторое время у одного из этих пациентов повторились задержки мочеиспускания, и была установлена цистостома. В основной группе 6 больным (12%) спустя 6 месяцев консервативной терапии после стабилизации соматического статуса и по желанию пациентов была выполнена ТУР гиперплазии простаты с последующим восстановлением адекватного мочеиспускания. За время приема препаратов значимых нежелательных реакций, в том числе снижения гемодинамических показателей, не возникло (табл. 2) [8].
Наблюдаемые побочные явления чаще были связаны с системным влиянием тамсулозина на тонус сосудистой стенки (ощущение общей слабости, головокружения, сердцебиения, головной боли и заложенности носа). Это не потребовало отмены препарата и дополнительных консультаций специалистов – эффекты были кратковременными и выявлялись лишь при активном расспросе больных. Возникшая у 8 больных (16%) ретроградная эякуляция, на наш взгляд, является не побочным эффектом, а следствием медикаментозно индуцированного снижения тонуса гладкомышечных волокон шейки мочевого пузыря и области сфинктера мочеиспускательного канала. Пациенты были заблаговременно предупреждены о возможности такого изменения и испытывали лишь косметический дискомфорт, исчезнувший спустя неделю после отмены препарата.
Обсуждение результатов
Терапия с применением селективного α1-АБ тамсулозина (Сонизин) продемонстрировала высокую эффективность у пациентов с ДГПЖ: было установлено достоверное улучшение параметров мочеиспускания (увеличение максимальной скорости мочеиспускания достоверно выше, чем в контрольной группе) и качества жизни. При этом не наблюдалось каких-либо значимых нежелательных реакций, в том числе нарушения гемодинамических показателей. Отмечено, что тамсулозин уменьшает обструкцию нижних мочевых путей, cнижаeт риск острой задержки мочеиспускания и не влияет на уровень ПСА.
Заключение
Сонизин удобен в применении (отсутствие необходимости подбора дозировки, прием один раз в сутки), что обеспечивает высокую комплаентность, и безопасен при использовании у пожилых пациентов, поэтому может назначаться после консультации терапевта. Основной побочный эффект, вызываемый препаратом, – ретроградная эякуляция, возникающая вследствие воздействия на α1-адренорецепторы шейки мочевого пузыря и расслабления ее замыкательного аппарата. Применение Сонизина возможно перед ТУР предстательной железы, поскольку обеспечивает время для улучшения соматического статуса пациента.
1. Аляев Ю.Г., Рапопорт Л.М., Цариченко Д.Г. и др. Изменения сосудов предстательной железы под действием аналогов LHRH // Врач. 2010. № 1. С. 68–70.
2. Аляев Ю.Г., Рапопорт Л.М., Цариченко Д.Г., Демидко Ю.Л. Применение альфа-адреноблокаторов в урологической практике // Новая аптека. 2009. № 12. С. 94–95.
3. Аляев Ю.Г., Рапопорт Л.М., Цариченко Д.Г., Демидко Ю.Л. Консервативное лечение аденомы простаты // Новая аптека. 2010. № 3. Ч. 1. С. 26–28.
4. Гориловский Л.М. Эпидемиология, факторы риска развития и биологическое течение доброкачественной гиперплазии предстательной железы // Доброкачественная гиперплазия предстательной железы / Под ред. акад. РАМН, проф. Н.А. Лопаткина. М., 1999. С. 12–20.
5. Лоран О.Б., Вишневский Е.Л., Вишневский А.Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты альфа-адреноблокаторами. М., 1998. С. 124.
6. Лопаткин Н.А. Введение // Доброкачественная гиперплазия предстательной железы / Под ред. акад. РАМН, проф. Н.А. Лопаткина. М., 1999. С. 5–8.
7. Рапопорт Л.М., Цариченко Д.Г., Рапопорт Ю.Л. и др. Комбинированная медикаментозная подготовка к транс- уретральной резекции простаты при ее гиперплазии // Андрология и генитальная хирургия. 2009. № 4. С. 23–25.
8. Сивков А.В., Аполихин О.И. Альфа-1-адреноблокаторы в терапии доброкачественной гиперплазии предстательной железы // Consilium Medicum. 2002. Т.4. № 7. С. 381–384.
9. Boile P., Maisonneuve P., Napalcov P. Prostate diseases beyond the year 2000: present and Future burden of prostate disease // Textbook of behigh prostate hyperplasia. 1995. Р. 543–563.
10. Caine M., Pfau A., Perlsberg S. The use of alpha-adrenergic blockers in benign prostatic obstrucion // Br. J. Urol. 1976. Vol. 48. P. 255–263.
11. Christensen М., Bendix Hoime J., Rasmussen P. et al. Doxazosin treatment in patients with prostatic obstruction // Scand. J. Urol. Nephrol. 1993. Vol. 27. P. 39–44.
12. Jardin A.A. General practitioner multicenter study: fosfomycin trometamol single dose versus pipemidic acid multiple dose // Infection. 1990. Vol. 18 (2). P. 89–93.
13. Jonler M., Riehmann M., Brinkmann R., Bruskewitz R.C. Benign prostatic hyperplasia // Endocrinol. Metab. Clin. North Am. 1994. Vol. 23 (4). Р. 795–807.
14. Kaefer M., Barnewolt C., Retik A.B., Peters C.A. The sonographic diagnosis of infravesical obstruction in children: evaluation of bladder wall thickness indexed to bladder filling // J. Urol. 1997. Vol. 157 (3). P. 989–991.
15. Kortmann B.B.M., Floratos D.L. et al. Urodynemic effects of alpha-adrenoceptors blockers: a review of clinical trials // Urology. 2003. Vol. 62 (1). Р. 1–9.
16. Lepor H., Auerbach S., Puras-Baez A. et al. A randomized, placebo-cntrolled multicenter study of the efficacy and safety of terazosin in the treatment of benign prostatic hyperplasia // J. Urol. 1992. Vol. 148. P. 1467.
17. McConnell J.D., Roehrborn C.G., Bautista O.M. et al. The long-term effect of doxazosin, finasteride, and combination therapy on the clinical progression of benign prostatic hyperplasia // The New England Jornal of Medicine. 2003. Vol. 349. P. 2387–2398.
18. Mohanty N.K. Uday Pratap Singh et al. A comparative study of fixed dose of Tamsulosin with finasteride vs Tamsulosin with dutasteride in the management of benign prostatic hyperplasia // Indian Journal of Urology. 2006. Vol. 22. P. 130–134.
19. Roehrborn C.G. Combination medical therapy for lower urinary tract symptoms and benign prostatic hyperplasia // Rev. Urol. 2005. Vol. 7 (8). P. 43–51.
20. Sassine A.M., Schulman C.C. Intraurethral catheter in high-risk patients with urinary retention: 3 years of experience // Eur. Urol. 1994. Vol. 25 (2). Р. 131–134.
Новости на тему
17.02.2023
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье приведены результаты обследования и лечения мужчин, страдающих доброкачественной гиперплазией предстательной железы. В качестве терапии 50 пациентов получали препарат Сонизин (0,4 мг) в течение 6–19 месяцев.
В результате лечения улучшились параметры мочеиспускания, повысилось качество жизни. Прием Сонизина позволил снизить риск острой ишурии и в ряде случаев подготовить больных к трансуретральной резекции простаты.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
