Роль невропатического компонента и современные возможности его патогенетической фармакологической коррекции при синдроме хронической тазовой боли IIIB категории у мужчин
- Аннотация
- Статья
- Ссылки
- English
его коррекции в рамках оптимизированной комплексной фармакотерапии у мужчин с синдромом хронической тазовой боли (СХТБ) IIIB категории в рутинной урологической практике.
Материал и методы. В исследование включено 90 мужчин с диагнозом СХТБ IIIB категории в возрасте 22–48 лет (средний возраст 40,6 ± 4,6 года) (основная группа) и 30 клинически здоровых мужчин (средний возраст 35,2 ± 2,6 года) (контрольная группа). Для оценки индекса боли использовали Шкалу оценки симптомов хронического простатита и качества жизни мужчин по версии Национального института здоровья США (National Institute of Health Chronic Prostatitis Symptom Index – Quality of Life – NIH-CPSI-QL). Для выявления невропатического компонента хронической боли применяли диагностический опросник невропатической боли DN4. В ходе исследования сравнивались переносимость и клиническая эффективность фармакотерапии в двух подгруппах. Подгруппа 1 (n = 45) получала базовую терапию (нестероидный противовоспалительный препарат + венотонический препарат + альфа-1-адреноблокатор) в течение 30 дней. Подгруппа 2 (n = 45) предварительно получала альфа-липоевую кислоту парентерально, а затем 30-дневную базовую терапию (нестероидный противовоспалительный препарат + венотонический препарат + альфа-1-адреноблокатор) с дополнительным приемом альфа-липоевой кислоты перорально.
Результаты и их обсуждение. У 100% пациентов с СХТБ IIIB категории присутствовал хронический болевой синдром с преимущественной (в 61,1% случаев) локализацией в области малого таза/предстательной железы, который негативно сказывался на их качестве жизни. Невропатический компонент болевого синдрома диагностирован у 35,5% больных с обострением СХТБ IIIB категории, в то время как только у 13,3% мужчин контрольной группы выявлялись признаки, соответствующие аналогам невропатической боли (р < 0,05). Таким образом, общая частота невропатической боли при СХТБ IIIB категории оказалась в 2,7 раза выше, чем в популяции асимптоматических мужчин (р < 0,05). Стандартная фармакотерапия не оказывала патогенетического влияния на невропатический компонент, частота которого к концу лечения увеличилась до 37,8% (р < 0,05). Дополнительное назначение альфа-липоевой кислоты снизило частоту невропатической боли на 11%, общий индекс боли – на 21,1%, побочные эффекты фармакотерапии – на 80% (р < 0,05).
Выводы. У каждого третьего пациента с СХТБ IIIB категории при использовании простого,
но валидного опросника DN4 выявляются признаки невропатической боли, коррекция которой в рамках стандартного консервативного лечения практически невозможна. Патогенетически оправданной и эффективной фармакотерапевтической опцией для данной категории пациентов может считаться дополнительное назначение альфа-липоевой кислоты, которое позволяет достоверно и безопасно улучшить клинические результаты лечения СХТБ IIIB, сочетающегося с невропатической болью.
его коррекции в рамках оптимизированной комплексной фармакотерапии у мужчин с синдромом хронической тазовой боли (СХТБ) IIIB категории в рутинной урологической практике.
Материал и методы. В исследование включено 90 мужчин с диагнозом СХТБ IIIB категории в возрасте 22–48 лет (средний возраст 40,6 ± 4,6 года) (основная группа) и 30 клинически здоровых мужчин (средний возраст 35,2 ± 2,6 года) (контрольная группа). Для оценки индекса боли использовали Шкалу оценки симптомов хронического простатита и качества жизни мужчин по версии Национального института здоровья США (National Institute of Health Chronic Prostatitis Symptom Index – Quality of Life – NIH-CPSI-QL). Для выявления невропатического компонента хронической боли применяли диагностический опросник невропатической боли DN4. В ходе исследования сравнивались переносимость и клиническая эффективность фармакотерапии в двух подгруппах. Подгруппа 1 (n = 45) получала базовую терапию (нестероидный противовоспалительный препарат + венотонический препарат + альфа-1-адреноблокатор) в течение 30 дней. Подгруппа 2 (n = 45) предварительно получала альфа-липоевую кислоту парентерально, а затем 30-дневную базовую терапию (нестероидный противовоспалительный препарат + венотонический препарат + альфа-1-адреноблокатор) с дополнительным приемом альфа-липоевой кислоты перорально.
Результаты и их обсуждение. У 100% пациентов с СХТБ IIIB категории присутствовал хронический болевой синдром с преимущественной (в 61,1% случаев) локализацией в области малого таза/предстательной железы, который негативно сказывался на их качестве жизни. Невропатический компонент болевого синдрома диагностирован у 35,5% больных с обострением СХТБ IIIB категории, в то время как только у 13,3% мужчин контрольной группы выявлялись признаки, соответствующие аналогам невропатической боли (р < 0,05). Таким образом, общая частота невропатической боли при СХТБ IIIB категории оказалась в 2,7 раза выше, чем в популяции асимптоматических мужчин (р < 0,05). Стандартная фармакотерапия не оказывала патогенетического влияния на невропатический компонент, частота которого к концу лечения увеличилась до 37,8% (р < 0,05). Дополнительное назначение альфа-липоевой кислоты снизило частоту невропатической боли на 11%, общий индекс боли – на 21,1%, побочные эффекты фармакотерапии – на 80% (р < 0,05).
Выводы. У каждого третьего пациента с СХТБ IIIB категории при использовании простого,
но валидного опросника DN4 выявляются признаки невропатической боли, коррекция которой в рамках стандартного консервативного лечения практически невозможна. Патогенетически оправданной и эффективной фармакотерапевтической опцией для данной категории пациентов может считаться дополнительное назначение альфа-липоевой кислоты, которое позволяет достоверно и безопасно улучшить клинические результаты лечения СХТБ IIIB, сочетающегося с невропатической болью.




Введение
Синдром хронической тазовой боли (СХТБ) IIIB категории, или хронический невоспалительный абактериальный простатит, до сих пор привлекает внимание клиницистов и исследователей, поскольку многие аспекты его патогенеза изучены не до конца [1, 2]. К настоящему времени сформулировано большое количество теорий этиопатогенеза, что, скорее всего, объясняется отсутствием четкого единого понимания патогенетической сущности этой самой распространенной формы хронического простатита. Именно СХТБ IIIB категории сейчас представляет собой наиболее сложную и поэтому весьма актуальную проблему урологии с точки зрения методологических и диагностических дефиниций, предопределяющих возможность эффективной патогенетической фармакотерапии, результаты которой, согласно данным последнего метаанализа по данной проблематике, остаются малоутешительными [3].
Разнообразие теорий патогенеза СХТБ IIIB категории свидетельствует о его безусловном многофакторном патогенезе. Один из пионеров современного учения о хроническом простатите J.C. Nickel (2000) весьма удачно охарактеризовал его как «мультифакторный взаимосвязанный каскад» патологических превращений, которые инициируются тем или иным агентом (событием или процессом) и приводят к возникновению симптомов и локального болевого синдрома [4]. Вот почему большинство исследователей и клиницистов сегодня все чаще рассматривают СХТБ IIIB категории как многофакторное заболевание, а диагностика и лечение СХТБ IIIB категории должны непременно осуществляться на междисциплинарной основе.
В основе заболевания лежит тесное патогенетическое взаимодействие разнообразных системных и локальных нарушений, сопровождающихся метаболическим дисбалансом в предстательной железе, нарушением всех ее физиологических функций, что приводит к развитию и персистенции ключевого клинического симптома – хронического тазового/простатического болевого синдрома [5, 6]. Именно персистирующий или часто обостряющийся болевой урогенитальный синдром, нередко резистентный к стандартной рекомендованной терапии, оказывает наиболее выраженное негативное влияние на качество жизни мужчин с любой формой хронического простатита. Полноценная этиологическая диагностика причин хронического тазового/простатического болевого синдрома у больных СХТБ IIIB категории имеет ключевое прогностическое значение для эффективности планируемой фармакотерапии. Вместе с тем урологам хорошо известны сложности, которые могут возникнуть с этиологической диагностикой механизмов болевого урогенитального синдрома при хронических простатитах. Особенно это касается СХТБ IIIB категории, когда все анализы в норме, а мужчина жалуется на стойкую или рецидивирующую тазово-простатическую боль. Практика показывает, что, как правило, хронический болевой синдром при хронических абактериальных простатитах представлен известными урологам компонентами. Во-первых, локальной неинфекционной асептической или воспалительной болью, различными вариантами локальной неинфекционной и невоспалительной боли: васкулогенной (ишемической, вено-конгестивной и смешанной), фасциально-миогенной болью. Во-вторых, локальными болями с системными механизмами: психогенной и особенно невропатической. Последняя входит в число этиологических лидеров хронического болевого синдрома любой локализации, включая хронические тазово-простатические болевые синдромы. Урологи с ней почти не знакомы, не умеют ее выявлять и корректировать [7–9].
Любая невропатия, а в данном случае речь идет о метаболической невропатии, практически всегда обусловлена двумя основными патологическими механизмами: нарушением энергетического обмена в нейротелии и окислительным стрессом нервной ткани, которая первой реагирует на любой избыток свободных радикалов кислорода и/или недостаток антиоксидантов в организме [10]. Системные гормонально-метаболические факторы патогенеза метаболической невропатии и хронических простатитов, как ни парадоксально это звучит, во многом одинаковы. Одним из основных механизмов реализации их негативного влияния на метаболизм и функции предстательной железы как раз и является локальная метаболическая невропатия, известная как урогенитальная невропатия. Некоторые симптомы урогенитальной невропатии (тазовая/простатическая боль, нарушения эякуляции, ощущение холода в головке полового члена или промежности) могут напоминать симптомы хронического простатита, но вместе с тем урологи не обнаруживают существенной патологии со стороны предстательной железы. Следовательно, урогенитальная невропатия нередко становится новой клинической маской неинфекционной и невоспалительной боли при СХТБ IIIB категории. Это важно с практической точки зрения, поскольку последствия недиагностированной и, соответственно, некорректированной урогенитальной невропатии для предстательной железы весьма неблагоприятные. Среди них – утяжеление клинической симптоматики независимо от природы (бактериальный или абактериальный простатит), длительная персистенция стойкого хронического болевого синдрома, резистентного к стандартной терапии и нередко сопровождающегося тяжелыми психосоматическими осложнениями (тревожностью, депрессией и т.д.). Все это в ряде случаев резко затрудняет или делает вовсе невозможным оказание пациенту эффективной патогенетической помощи в рамках урологических стандартов [11, 12].
В настоящее время понятна роль метаболической невропатии в патогенезе СХТБ IIIB категории у мужчин. Урологам необходимо научиться выявлять и патогенетически корректировать урогенитальную метаболическую невропатию. Патогенетически ликвидировать невропатию и вызванную ей невропатическую тазовую/простатическую боль не способны ни антибиотики, ни нестероидные противовоспалительные препараты, ни какие-либо другие препараты, рутинно применяющиеся в урологической практике, за исключением нейротропов-антиоксидантов. Последние уменьшают выраженность окислительного стресса в нервной ткани и способствуют регенерации и восстановлению нервных клеток. Это еще раз подчеркивает междисциплинарный и многофакторный характер патогенеза хронического простатита, который ежегодно отмечают в рекомендациях эксперты Европейской ассоциации урологов. В этих рекомендациях можно найти еще один важный момент: «синдром хронической тазовой боли/простатический болевой синдром/хронический простатит (СХТБ/ПБС/ХП) не являются моноэтиологическими состояниями. При СХТБ/ПБС/ХП в патологический процесс вовлекаются механизмы нейропластичности и невропатической боли, поэтому зачастую СХТБ/ПБС/ХП – симптом других патологических состояний. И сегодня требуется индивидуальный фенотипический подход к объему диагностики и терапии каждому пациенту с СХТБ/ПБС/ХП» [13].
Однако, несмотря на то что невропатическая хроническая боль – один из наиболее частых механизмов неинфекционной боли при хронических простатитах, патогенетические препараты для коррекции невропатии и невропатической боли (нейропротекторы-антиоксиданты) в урологической практике до сих пор не востребованы. Между тем на российском рынке уже много десятилетий доступен один из наиболее активных препаратов данной группы, давно использующийся в различных отраслях клинической медицины, – тиоктовая (альфа-липоевая) кислота (АЛК).
АЛК обладает уникальными свойствами, благодаря которым ее можно применять для лечения и профилактики широкого спектра заболеваний, связанных в первую очередь с периферическими нервами и мозговой тканью, поскольку нервная ткань крайне чувствительна к токсическому воздействию свободных радикалов. Она самый эффективный из всех известных антиоксидантов, но ее терапевтическая ценность в этом качестве явно недооценена, а показания к назначению в медицине необоснованно сужены [14]. АЛК способна фармакологически «перекрывать» ключевой фактор патогенеза невропатии и невропатической боли, корректируя и ликвидируя различные проявления избыточного (патологического) окислительного стресса: уменьшать выраженность системного субклинического хронического воспаления, повышать антиоксидантную активность плазмы крови, улучшать детоксикационную функцию митохондрий клеток (антигипоксант) и гепатоцитов (гепатопротектор), защищать нервную ткань от свободных радикалов и улучшать ее регенеративные способности [15, 16]. Принимая во внимание универсальные метаболические эффекты АЛК, можно утверждать, что АЛК не только является универсальным антиоксидантом, антигипоксантом, нейротропом, гепато- и геронтопротектором, но и существенно повышает эффективность любой другой метаболической терапии [17].
Несмотря на актуальность изложенных лечебно-диагностических проблем, связанных с СХТБ IIIB категории, в отечественной урологической литературе имеется недостаток клинических исследований, посвященных этиопатогенетической диагностике невропатической хронической боли при данной форме хронического простатита с использованием простых, но валидных и не требующих много времени тестов. Кроме того, практически не изучены вопросы патогенетической целесообразности и возможной эффективности препаратов АЛК в комплексной фармакотерапии СХТБ IIIB категории, протекающего с невропатическим компонентом хронической боли. Все это послужило поводом для настоящего исследования.
Цель исследования
Изучить частоту и особенности невропатического компонента болевого синдрома, а также оценить клиническую эффективность, переносимость и безопасность его коррекции в рамках оптимизированной комплексной фармакотерапии у мужчин с СХТБ IIIB категории в рутинной урологической практике.
Материал и методы
В клиническое проспективное исследование включено 90 мужчин с диагнозом СХТБ IIIB категории (основная группа) и 30 практически здоровых мужчин без патологии предстательной железы (контрольная группа). Диагноз СХТБ IIIB категории устанавливался на основании клинической картины заболевания (персистирующий хронический тазово-простатический болевой синдром в течение не менее трех месяцев подряд) в сочетании с нормальными цитологическими и микробиологическими показателями секрета предстательной железы при исключении патологии соседних тазовых органов [13].
Средний возраст пациентов с СХТБ IIIB категории (n = 90) составил 40,6 ± 4,6 года (95%-ный доверительный интервал (ДИ) 22–48), контрольной группы (n = 30) – 35,2 ± 2,6 года (95% ДИ 20–40). Длительность течения основного заболевания у 28,1% пациентов составила менее пяти лет, у 38,9% пациентов – от пяти до десяти лет, у 33,0% пациентов – более десяти лет. Минимальная длительность – два года, максимальная – 16 лет (средний период длительности течения – 10,2 ± 2,6 года). У всех пациентов проводился сбор жалоб и анамнеза по общепринятым методикам, после чего выполнялись соответствующие объективные исследования.
Для характеристики болевого синдрома при СХТБ IIIB категории использовали специальный валидный опросник – Шкалу оценки симптомов хронического простатита и качества жизни мужчин по версии Национального института здоровья США (National Institute of Health Chronic Prostatitis Symptom Index – Quality of Life – NIH-CPSI-QL). По NIH-CPSI-QL определялись индекс боли по шкале от 1 до 10 и индекс качества жизни по шкале от 1 до 6 [18]. Для выявления невропатического компонента хронической боли применяли диагностический опросник невропатической боли (DN4), который был специально разработан для широкого использования врачами любых специальностей и не требует специального неврологического образования (табл. 1) [19]. Опросник состоит из двух блоков: первый блок из семи вопросов заполняется на основании ответов пациента, второй блок из трех вопросов – на основании клинического осмотра. Первый блок дает возможность оценить позитивные сенсорные симптомы: спонтанную боль (ощущение жжения, болезненное ощущение холода, ощущение как от ударов током), парестезии и дизестезии (ощущение ползания мурашек, покалывание, онемение, зуд). Второй блок позволяет врачу выявить аллодинию (извращенную реакцию на боль) и негативные сенсорные симптомы. При сумме баллов выше 4 вероятность наличия у пациента невропатической боли или невропатического компонента смешанной боли составляет 86%. Опросник DN4 переведен на большинство европейских языков, в том числе на русский. Русскоязычная версия опросника прошла лингвистическую валидацию с соблюдением всех международных требований и официально принята к использованию в России.
Результаты обследования здоровых мужчин контрольной группы (n = 30) принимали за референсные показатели условной нормы, с которыми сравнивались аналогичные результаты обследования пациентов с СХТБ IIIB категории.
Для изучения и сравнения между собой клинической эффективности различных режимов фармакотерапии СХТБ IIIB категории все пациенты (n = 90) были разделены на две подгруппы (n = 45), отличавшихся видом и объемом лекарственного обеспечения. Пациенты подгруппы 1 получали стандартную базовую терапию (нестероидный противовоспалительный препарат, венотонический препарат, альфа-1-адреноблокатор) в течение 30 дней. Лечение пациентов подгруппы 2 (n = 45) начиналось с монотерапии альфа-липоевой кислотой по 600 мг внутривенно на 200 мл физиологического раствора медленно капельно раз в сутки (всего пять процедур ежедневно). Затем они переводились на базовую 30-дневную терапию, в состав которой, кроме нестероидного противовоспалительного препарата, венотонического препарата и альфа-1-адреноблокатора, входил также препарат альфа-липоевой кислоты, но уже перорально по 600 мг/сут ежедневно утром натощак.
Статистическая обработка выполнялась в программах Microsoft Excel 2007 и Statistica 6.0. Для оценки межгрупповых различий значений признаков, имеющих непрерывное распределение, применялся t-критерий Стьюдента. Для исследования взаимосвязи количественных признаков определялся коэффициент корреляции Спирмена (r). Критический уровень достоверности нулевой статистической гипотезы (об отсутствии значимых межгрупповых различий или факторных влияний) принимали равным 0,05 [20].
Результаты и их обсуждение
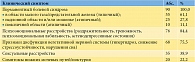
Частота и структура клинических симптомов, наблюдавшихся у пациентов с СХТБ IIIB категории, представлены в табл. 2. У всех 90 (100%) пациентов с СХТБ IIIB категории присутствовал хронический болевой синдром, который в 61,1% случаев преимущественно локализовался в области малого таза/предстательной железы. Степень выраженности боли в основной группе достоверно отличалась от аналогичной характеристики группы контроля, что предопределило достоверное ухудшение качества жизни пациентов с СХТБ IIIB категории (табл. 3).
Согласно данным, полученным при обследовании пациентов по шкале невропатической боли DN4, только у трех (13,3%) здоровых мужчин были признаки, соответствующие аналогам и критериям невропатической боли, в то время как четкие критерии невропатической боли обнаружены у 32 (35,5%) больных с обострением СХТБ IIIB категории (р < 0,05) (табл. 4). Значит, примерно у каждого третьего пациента с хроническим невоспалительным абактериальным простатитом хроническая боль имеет невропатическую природу, что обнаруживается при целенаправленном обследовании с использованием простого валидного специализированного опросника DN4, а общая частота выявления невропатической боли при СХТБ IIIB категории оказалась в 2,7 раза выше, чем в популяции здоровых мужчин (р < 0,05).
После проведенных курсов фармакотерапии у подавляющего большинства пациентов основной группы произошло резкое снижение выраженности болевого синдрома, при этом в подгруппе 1 он был полностью клинически ликвидирован у 18 (40%) больных, а в подгруппе 2 – у 28 (62,2%) (р < 0,05).
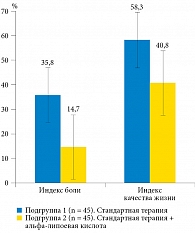
Согласно данным табл. 5, достоверное уменьшение выраженности боли (оценка по индексу боли) отмечалось в обеих подгруппах по сравнению с исходным уровнем, в большей степени оно было выражено у больных подгруппы 2 (-85,3% от исходного значения по сравнению с -64,2% в подгруппе 1) (р < 0,05). В среднем степень регресса значения индекса боли в обеих подгруппах после лечения составила 70,2% от исходного уровня, что свидетельствовало о 70%-ной эффективности консервативной фармакотерапии болевого синдрома. Однако клиническая эффективность в подгруппе 2, дополнительно получавшей препарат альфа-липоевой кислоты, была на 21,1% выше, чем в подгруппе 1, получавшей только стандартную терапию (рис. 1).
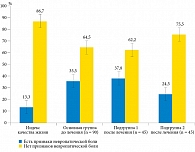
Причина таких различий эффективности стала понятнее после того, как был проведен анализ динамики выявления признаков невропатической боли по шкале DN4 до и после терапии (табл. 5). На фоне лечения в обеих подгруппах происходило неравномерное перераспределение больных с наличием и отсутствием признаков невропатической боли. Если перед началом терапии в целом в обеих подгруппах (n = 90) признаки невропатической боли имели место у 35,5% больных, то после курса лечения – у 31,1%, то есть произошло уменьшение на 4,4% (результаты статистически не значимы, р < 0,1). Однако нельзя не заметить достоверную тенденцию, отмеченную в подгруппе 2: по сравнению с подгруппой 1 количество пациентов, у которых отсутствовали признаки невропатической боли после терапии, в данной группе увеличилось в среднем на 13,3%, а количество пациентов, у которых исходно до лечения обнаруживалась невропатическая боль, соответственно уменьшилось на 11,0% (р < 0,05). Очевидно, из-за этого в подгруппе 2 болевой синдром купировался достоверно лучше, чем в подгруппе 1, поскольку только в подгруппе 1 к окончанию курса фармакотерапии индекс боли максимально приблизился к значениям здоровых мужчин контрольной группы (рис. 2).
Установленная динамика невропатической боли свидетельствовала о том, что стандартная фармакотерапия патогенетически почти не влияет на невропатический компонент боли из-за отсутствия нейротропных эффектов у препаратов, традиционно входящих в схему такой терапии. Предположительно, именно по этой причине у больных подгруппы 1 в ходе стандартной терапии количество пациентов с невропатическим характером боли по шкале DN4 не только не уменьшалось, но и несколько увеличилось с 35,5 до 37,8% (р < 0,05), что свидетельствовало о продолжающемся прогрессировании недиагностированной невропатической боли и в определенной степени предопределило худшие результаты коррекции боли в целом в подгруппе 1 по сравнению с подгруппой 2, дополнительно получавшей препарат альфа-липоевой кислоты.
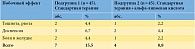
В ходе исследования была также выявлена хорошая переносимость препарата альфа-липоевой кислоты, частота побочных эффектов на фоне терапии с дополнительным назначением препарата альфа-липоевой кислоты оказалась в 1,8 раза меньше, чем на фоне стандартной терапии (р < 0,05), что можно объяснить имеющимся у альфа-липоевой кислоты антиоксидантным, гепатопротективным и детоксикационным эффектом (табл. 6).
Заключение
Ключевая клиническая проблема при ведении пациентов с СХТБ IIIB категории – стойкий и рецидивирующий хронический урогенитальный болевой синдром, который по сравнению с другими клиническими проявлениями заболевания самым негативным образом сказывается на качестве жизни. С учетом не до конца изученного многофакторного патогенеза СХТБ IIIB категории наиболее важная задача клинициста – максимально ранняя и эффективная коррекция болевых проявлений, существенно влияющих на клиническое течение заболевания и формирование его порочного патогенетического круга, а также предопределяющих дальнейшую эффективность всего арсенала фармакотерапевтических мероприятий. Болевой синдром при СХТБ IIIB категории, скорее всего, многокомпонентен, поэтому важную роль играет этиологическая диагностика потенциальных механизмов боли. У каждого третьего пациента с СХТБ IIIB категории имеет место невропатический компонент болевого синдрома, который крайне плохо диагностируется в рутинной клинической практике в силу недостаточности информации об этом болевом механизме среди практикующих урологов. Вместе с тем быструю, точную, легко воспроизводимую и неинвазивную диагностику невропатической боли у больных СХТБ IIIB категории способен обеспечить опросник невропатической боли DN4, специально разработанный и адаптированный для применения врачами различных специальностей. Традиционная стандартная фармакотерапия СХТБ IIIB категории патогенетически не влияет на урогенитальную невропатию, которая нередко является клинической маской и непосредственной причиной формирования невропатического компонента боли при данной патологии. Дополнительное назначение препаратов с нейротропным и антиоксидантным эффектом позволяет улучшить результаты комплексной терапии СХТБ IIIB категории за счет патогенетического воздействия на невропатические механизмы боли. Препаратом выбора в таком случае может быть альфа-липоевая кислота, применение которой в рамках полимодальной фармакотерапии повышает клиническую эффективность лечения болевого синдрома в среднем на 21,1% и снижает частоту побочных эффектов на 80%. Для более эффективного фармакологического управления СХТБ IIIB категории необходимы дальнейшие детальные исследования как общих его механизмов, так и механизмов хронического болевого синдрома.
I.I. Mozhayev, I.A. Tyuzikov, I.S. Shormanov
Yaroslavl State Medical University
Clinic of Professor Kalinchenko, Moscow
Contact person: Igor Igorevich Mozhayev, kafuro@mail.ru
Purpose. Research of the frequency and characteristics of the pain syndrome neuropathic component and to assess the clinical efficacy, tolerability and safety of its correction in the framework of the optimized complex pharmacotherapy in men with category IIIB chronic pelvic pain syndrome (CPPS) in routine urological practice.
Materials and Methods. The study involved 90 men with the diagnosis of category IIIB CPPS aged at 22–48 years (mean age 40.6 ± 4.6 years old) (study group) and 30 clinically healthy men of the same age (control group). For the assessment of pain index was used National Institute of Health Chronic Prostatitis Symptom Index – Quality of Life. To identify the neuropathic component of chronic pain the diagnostic questionnaire of neuropathic pain DN4 was used. In the study it was compared the tolerability and clinical efficacy of pharmacotherapy in two subgroups. Subgroup 1 (n = 45) received standard therapy (nonsteroidal anti-inflammatory drugs + venotonic drug + alpha-1-blocker) for 30 days. Subgroup 2 (n = 45) had previously received alpha-lipoic acid parenteral, and then transferred to 30-day standard therapy (nonsteroidal anti-inflammatory drugs + venotonic drug +alpha-1-blocker) with an additional intake
of alpha-lipoic acid per oral.
Results and Discussion. 100% patients with category IIIB CPPS the chronic pain syndrome was observed with predominant localization (at 61.1%) in the pelvic area/prostate and the negative impact on the quality of life for all patients. Neuropathic component of the pain syndrome was diagnosed in 35.5% patients with exacerbation of category IIIB CPPS, while only for 13.3% of men in the control group there were detected the signs corresponding to the analogues of neuropathic pain (p < 0.05). Thus, the overall frequency of neuropathic pain in category IIIB CPPS were 2.7 times higher than in the population of asymptomatic men (p < 0.05). Standard pharmacotherapy had pathogenic effect on the neuropathic component, which frequency of increased to 37.8% (p < 0.05) by the end of treatment. Additional prescription of alpha-lipoic acid reduced the frequency of neuropathic pain by 11%, the total pain index – by 21.1%, side effects of pharmacotherapy – by 80% (p < 0.05).
Conclusions. By using a simple, but valid questionnaire DN4 it was determined that every third patient with category IIIB CPPS revealed signs of neuropathic pain, which correction of in the frameworks of the standard conservative treatment was almost impossible. Pathogenetically justified and effective pharmacotherapeutic option for these patients may be considered supplemental alpha-lipoic acid which can reliably and safely improve clinical results of treatment of category IIIB CPPS, combined with neuropathic pain.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.