Тазовая боль – междисциплинарная проблема. X Междисциплинарный международный конгресс Manage Pain. Сателлитный симпозиум компании «Берлин-Хеми/А. Менарини»
- Аннотация
- Статья
- Ссылки



Тазовая боль. Взгляд невролога
Как отметила доцент кафедры нервных болезней Первого МГМУ им. И.М. Сеченова, к.м.н. Наталья Васильевна ВАХНИНА, тазовая боль может локализоваться в нижней части живота, тазовых органах, области паха, промежности, поясницы и крестца. По оценкам, распространенность синдрома тазовой боли составляет 9–24% среди взрослого населения, причем женщины страдают в два раза чаще мужчин.
С учетом особенностей иннервации области таза поражение одних органов таза часто имитирует патологический процесс в других органах и приводит к перекрестной сенситизации структур периферической и центральной нервной системы, которые участвуют в регуляции деятельности органов таза и мышечно-суставного аппарата тазового пояса. Вовлечение в патологический процесс мышц тазового дна и периферических нервов рассматривается как важная часть процесса хронизации боли.
Главная цель обследования пациента с острой тазовой болью заключается в диагностике ее первопричины и исключении потенциально опасных состояний (выявлении «красных флажков»)1:
- злокачественных новообразований;
- аневризмы или диссекции брюшного отдела аорты;
- почечной колики или перекрута яичника;
- кровотечения при разрыве кисты яичника, внематочной беременности;
- эндометриоза, опухолей, цервицита;
- перитонита/аппендицита, дивертикулита;
- переломов костей таза/позвоночника;
- инфекционных процессов;
- инфекционно-воспалительных заболеваний желудочно-кишечного тракта;
- параректального абсцесса или опухолей, кишечной непроходимости;
- остеопорозных переломов;
- спинальной/параспинальной опухоли;
- объемного процесса в области конского хвоста, стенозирующего спинального канала, грыжи межпозвонкового диска, кисты Тарлова.
Следует отметить, что специфические (опасные) причины боли в спине встречаются довольно редко, чаще к тазовой боли приводит повреждение или дисфункция нервной системы и опорно-двигательного аппарата. Боли неврогенного происхождения представлены туннельными невропатиями, фибромиалгией, каналопатиями (проктодинией, вульводинией) и новообразованиями спинного мозга. Боли суставно-мышечной природы, как правило, вызваны растяжением, гематомой, миофасциальным синдромом брюшной стенки, промежности, патологией тазобедренного сустава, остеоартритом крестцово-подвздошного сочленения, дисфункцией лонного сочленения, травмой позвоночника и костей таза, кокцигодинией2.
Выявить первопричину тазовой боли непросто. Несмотря на то что пациент получает консультацию целого ряда специалистов (гинеколога, проктолога, уролога, психиатра и др.), в итоге он нередко остается со своей болью один на один в течение длительного времени.
Диагностика тазовой боли предусматривает определение патофизиологического типа боли и ее длительности, далее выявление ее природы (наличие/отсутствие скелетно-мышечной дисфункции, невропатии, специфических причин) и, наконец, определение типа личности пациента, наличие/отсутствие коморбидности.
С точки зрения патофизиологии выделяют три типа боли: ноцицептивную, невропатическую и дисфункциональную. Если при ноцицептивной боли эффективно применение нестероидных противовоспалительных препаратов (НПВП) и различных физических и интервенционных методов, то терапию невропатической боли следует начинать с приема антиконвульсантов, а дисфункциональная боль требует использования психотерапевтических методов и назначения антидепрессантов и нейролептиков. В основе данного подхода лежит знание об имеющемся при острой и хронической боли разном удельном весе структурных и психических нарушений. Если при острой боли отмечается выраженное повреждение тканей и воспаление, то при хронической боли на первое место выходят когнитивные и аффективные составляющие. Следовательно, ведение пациентов с хронической болью подразумевает использование методик, направленных на коррекцию эмоционального состояния и поведения.
Н.В. Вахнина рассмотрела принципы диагностики и лечения тазовой боли на примере из практики.
Пациентка В., 28 лет. Поступила в Клинику нервных болезней с жалобами на боли в правой подвздошной области жгучего характера, которые уменьшались в положении лежа на животе в позе лягушки или после прикладывания грелки. Длительность болевых приступов – 20–25 минут.
Впервые жгучие боли в пахово-подвздошной области возникли в 2016 г. после физической нагрузки (качала пресс в тренажерном зале). Важно отметить, что в то время пациентка уже находилась в стрессовой ситуации, поскольку проходила лечение по поводу инфильтративного туберкулеза легких. В марте 2016 г. она обратилась за консультацией к урологу. Рентген с контрастом патологии не выявил. Магнитно-резонансная томография (МРТ) пояснично-крестцового отдела – тоже без патологий. В мае 2016 г. гинеколог направил ее на ультразвуковое исследование (УЗИ) органов малого таза, которое показало правосторонний нефроптоз. В то же время боли участились, их интенсивность постепенно возрастала. Невролог, к которому пациентка пришла на прием в марте 2017 г., предположил тазовую туннельную невропатию. Дуплексное сканирование вен нижних конечностей не выявило патологии. В ноябре 2017 г. больная вновь побывала на приеме у гинеколога, а через год (ноябрь 2018 г.) – у травматолога. Однако ни МРТ органов малого таза и УЗИ вен таза, ни МРТ и УЗИ тазобедренного сустава ничего нового не показали. Приступы боли значительно участились и отмечались каждые два-три часа.
Наконец, в феврале 2019 г. пациентка с длительными болями, возникавшими несколько раз в сутки, была госпитализирована в Клинику нервных болезней. По результатам нейроортопедического осмотра, диагностированы спазм подвздошно-поясничной мышцы и болезненность мышцы под пупартовой связкой с выявлением миофасциальных триггерных точек. В неврологическом статусе – гиперестезия в паховой области и передневерхней поверхности бедра. Обращает на себя внимание плохое эмоциональное состояние пациентки (клинически значимые тревога и депрессия). В заключении УЗИ нервов поясничного сплетения указывалось на ультразвуковые признаки асимметричного утолщения справа подвздошно-поясничной мышцы и бедренно-полового нерва с сохранностью кабельного строения.
Пациентке поставлен клинический диагноз «синдром хронической тазовой боли на фоне миофасциального болевого синдрома подвздошно-поясничной мышцы, компрессионная невропатия бедренно-полового нерва» и назначен комплекс терапевтических мероприятий:
- блокада бедренно-полового нерва раствором беклометазона дипропионата 1 мл и 2%-ным раствором лидокаина;
- прием прегабалина 150 мг два раза в сутки с постепенным снижением дозы;
- прием тизанидина 6 мг/сут;
- прием нимесулида (препарата Нимесил) 100 мг при возникновении приступа боли;
- прием дулоксетина 60 мг/сут (в течение трех месяцев);
- ежедневная постизометрическая релаксация мышц и комплекс лечебной гимнастики;
- пять сеансов когнитивно-поведенческой терапии.
Комментируя лечение, которое проводилось пациентке В., Н.В. Вахнина отметила, что фармакотерапия тазовой боли воспалительного характера предусматривает использование НПВП, миорелаксантов, а невропатической природы – антиконвульсантов и антидепрессантов. Нелекарственные методы включают индивидуализированную интервенционную, мануальную терапию, кинезиотерапию, ортопедическую помощь.
Среди НПВП докладчик выделила Дексалгин (декскетопрофен) – оригинальный анальгетик с быстрым началом действия. Так, при приеме декскетопрофена 25 мг максимальная концентрация в плазме крови достигается в 2,5 раза быстрее по сравнению с кетопрофеном 100 мг. По обезболивающей силе при острой боли в спине Дексалгин превосходит трамадол, демонстрируя более низкую частоту нежелательных явлений3. В рандомизированном контролируемом исследовании оценивалась эффективность внутривенного введения 50 мг декскетопрофена и 8 мг лорноксикама два раза в сутки у пациентов, перенесших эндопротезирование тазобедренных или коленных суставов4. Согласно полученным данным, Дексалгин эффективнее лорноксикама купировал острую боль с первого часа после операции. Дексалгин отличается хорошим профилем безопасности по сравнению с другими НПВП. В когортном исследовании при купировании слабого/умеренно выраженного болевого синдрома Дексалгин 25 мг показал хорошую переносимость в сравнении с другими НПВП (диклофенаком, пироксикамом, напроксеном, ибупрофеном)5.
Дексалгин выпускается в виде раствора для внутривенного и внутримышечного введения, в форме таблеток и гранул для приготовления раствора для приема внутрь, что позволяет осуществлять ступенчатую терапию боли. При сильном болевом синдроме Дексалгин назначают внутримышечно или внутривенно в дозе 50 мг до трех раз в сутки в течение одного-двух дней с дальнейшим приемом препарата в таблетированной или гранулированной форме по схеме: 25 г (одна таблетка или один пакетик) каждые восемь часов, но не более 75 г/сут, в течение трех – пяти дней.
После краткого курса лечения Дексалгином рекомендуется перейти на прием Нимесила (нимесулида), который обладает низким риском желудочно-кишечных и сердечно-сосудистых осложнений и не вызывает тромбозов даже при длительном применении. Хороший профиль безопасности Нимесила во многом обусловлен тем, что он ингибирует преимущественно циклооксигеназу 2. Нимесил характеризуется многофакторным действием. Он подавляет синтез металлопротеиназ, выработку медиаторов воспаления (интерлейкина 6) и гистамина, агрегацию и миграцию нейтрофилов, нейтрализует токсичные радикалы6. Доказано, что Нимесил эффективно уменьшает болевой синдром в спине при радикулопатии7. По результатам рандомизированного исследования, Нимесил (нимесулид) купировал боль у пациентов с остеоартрозом коленного сустава эффективнее целекоксиба8.
Применение НПВП – первый этап лечения воспаления и боли, благодаря которому пациенты могут вернуться к привычной жизни. Для быстрейшего восстановления им можно рекомендовать кинезиотерапию, систематические занятия лечебной гимнастикой, регулярную ходьбу. Еще один эффективный консервативный метод – постизометрическая релаксация мышц, основанная на правильном движении, расслаблении мышц, растяжении мягких тканей, нормализации мышечного сокращения.
Резюмируя вышесказанное, Н.В. Вахнина констатировала, что алгоритм диагностики тазовой боли в первую очередь предусматривает исключение специфических причин («красных флажков»), оценку патофизиологии (ноцицептивная, невропатическая, дисфункциональная), длительности (острая или хроническая) и причины (невропатия, скелетно-мышечная) боли, а также личностных характеристик пациента.
Роль вертеброневролога в лечении хронической тазовой боли
По мнению заведующего курсом неврологии, мануальной терапии, рефлексотерапии ВолГМУ, профессора, д.м.н. Александра Евгеньевича БАРУЛИНА, хроническую тазовую боль можно назвать «терапевтической головоломкой», поскольку по количеству причин она сопоставима с головной болью.
Синдром тазовой боли, с точки зрения невролога, представляет собой острую или хроническую тазовую боль, которая имеет нейрогенное происхождение, но в структуре облигатно содержит невропатические и/или психогенные компоненты, обусловленные снижением активности антиноцицептивной системы и/или феноменом сенситизации нейронов и развитием нейрогенного воспаления. В соответствии с биопсихосоциальной моделью хроническая боль – это результат биологических, социально-культурных и психологических факторов. Подчеркнув важность всех составляющих, профессор А.Е. Барулин сфокусировал выступление на анализе нарушений биомеханики.
По оценкам, 35% всех тазовых болей обусловлено миофасциальным синдромом, 22% – спазмом и формированием триггерных точек в мышце, поднимающей анус, 14% – спазмом грушевидной мышцы. Но они вторичны и возникают в ответ на ослабление тех или иных «первичных» мышц. Как правило, при лечении миофасциального болевого синдрома основное воздействие направлено на болезненные мышечные уплотнения и триггерные точки. «Однако без выявления и коррекции биомеханических нарушений триггерная зона будет возникать снова и снова», – пояснил докладчик.
Обнаружение проблемной зоны требует определенных врачебных навыков, поскольку при осмотре пациент всегда укажет на чрезмерно укороченную мышцу, но не на область настоящей проблемы. С помощью кинезиологического тестирования, основанного на изменении миотатического рефлекса, можно выявить мышцы, находящиеся в состоянии гипотонуса. Они неправильно включаются в работу при совершении двигательного акта, что приводит к перегрузке мышц-синергистов и формированию в них болевых реакций.
По словам докладчика, УЗИ органов малого таза, МРТ пояснично-крестцового отдела и другие стандартные обследования пациента с тазовой болью можно рассматривать в качестве дополнительных методов, и к их назначению нужно подходить индивидуально в каждом конкретном случае. Рентгенологические методы исследования достаточно «грубы» для выявления причин боли и используются преимущественно для определения травматических костных повреждений.
На терапевтическую тактику влияют множество факторов, в первую очередь выраженность болевого синдрома и его продолжительность. Медикаментозное лечение включает применение широкого спектра разных классов препаратов в зависимости от механизма боли, в том числе НПВП9. Как показывает собственный клинический опыт докладчика, в купировании острой боли эффективен Дексалгин, подострой – препарат Нимесил. Алгоритм немедикаментозного лечения включает коррекцию структурных нарушений, программу восстановления двигательной активности, переобучение двигательного паттерна, контроль локомоции.
Изменение биомеханики тазового дна требует коррекции с использованием различных мануальных техник. Для облегчения миофасциального компонента тазовой боли применяется постизометрическая релаксация мышц тазового дна. Суть метода заключается в двухфазном воздействии на мышцу.
С точки зрения памяти и обучения хроническую боль можно определить как устойчивое сохранение воспоминаний о боли или неспособность аннулировать эти воспоминания. По мнению профессора А.Е. Барулина, без реедукации двигательного паттерна с помощью простых двигательных упражнений разрушить этот стереотип невозможно. Реедукация двигательного стереотипа может осуществляться с использованием стабилоплатформы.
К современным и перспективным методам немедикаментозного лечения относится кинезиотейпирование. Метод появился в середине 1970-х гг. и основан на применении специальных эластичных хлопковых лент, покрытых гипоаллергенным клеем для закрепления на коже. С помощью кинезиотейпирования можно нормализовать мышечный тонус, улучшить микроциркуляцию тканей.
Пациент может самостоятельно тренировать мышцы по принципу напряжения и расслабления мускулатуры тазового дна. Однако комплекс упражнений и то, какие группы мышц нужно задействовать, определяет только врач.
Используя различные методы коррекции мышечно-тонического компонента хронического болевого синдрома, не стоит забывать о том, что тазовая и брюшная диафрагмы должны работать синхронно. Вот почему также целесообразно выполнять дыхательные упражнения, которые способствуют достижению хорошего реабилитационного потенциала.
Таким образом, реабилитация пациентов с хронической тазовой болью предусматривает прежде всего поведенческую терапию, главная задача которой изменить отношение к болезненному состоянию. Необходимо объяснять пациентам механизм боли, внушать уверенность в возможности полного восстановления, обучать правильным позам при работе и методам релаксации. Огромную роль играет движение, которое должно быть достаточным, регулярным и безопасным.
Тазовая боль. Взгляд гинеколога
Доцент кафедры акушерства и гинекологии Первого МГМУ им. И.М. Сеченова, к.м.н. Александр Викторович ВОРОБЬЕВ отметил, что ежегодно свыше 60% женщин обращаются за помощью акушера-гинеколога по поводу тазовой боли10. Согласно данным Национального института здоровья США, распространенность хронической тазовой боли среди женщин достигает 15%11. При этом многие женщины с умеренной тазовой болью не прибегают к медицинской помощи или остаются без установленного диагноза.
Хроническая тазовая боль определяется при наличии хотя бы одного из симптомов: собственно тазовой боли (постоянных болезненных ощущений в нижних отделах живота, паховых областях, пояснице), дисменореи (болезненных менструаций), диспареунии (болезненного полового акта).
Этиологическими факторами, приводящими к развитию хронической тазовой боли, считаются эндометриоз и аденомиоз, синдром венозного полнокровия, дисменорея, воспалительные заболевания органов малого таза, хроническая цервикальная инфекция и послеоперационные осложнения. Следует учитывать, что у одной пациентки может присутствовать сразу несколько факторов.
Тазовое венозное полнокровие встречается у женщин всех возрастов, особенно в репродуктивном периоде. В большинстве случаев оно обусловлено варикозным расширением вен яичников и гораздо реже вен широкой связки матки. Необходимо отметить, что варикозная болезнь вен малого таза – проявление системного поражения (дисплазии) соединительной ткани, которая широко распространена в популяции. К наиболее характерным клиническим симптомам тазового венозного полнокровия относятся ноющая боль с иррадиацией в пояснично-крестцовую и паховую область, выраженный предменструальный синдром, дисменорея. Почти у каждой второй пациентки обнаруживают варикозное расширение вен промежности, ягодичной области, наружной поверхности бедра. Основной вклад в развитие тазового венозного полнокровия вносят такие факторы риска, как гиподинамия, нерациональные физические нагрузки, поднятие тяжестей, переохлаждение, половая фрустрация (сексуальная неудовлетворенность) и половая депривация (длительное воздержание), употребление алкоголя и острой пищи, воспалительные заболевания органов малого таза, гормональная терапия.
Эндометриозу сопутствуют не только тазовая боль (не связанная с менструацией), дисменорея, диспареуния, но и дизурия, дисхезия (боль при дефекации), нерегулярные маточные кровотечения и анергия. Какие патогенетические факторы лежат в основе развития эндометриоза? Прежде всего воспалительная реакция с выделением различных медиаторов воспаления и боли (простагландинов, гистаминов и кининов), повышение экспрессии фактора роста нервов в очагах эндометриоза, потенцирующее развитие невропатической боли. Образование рубцов и спайки приводят к деформации, натяжению тканей и органов и боли при физической нагрузке. Патогенез боли зависит от фиксации матки в ретропозиции, рубцовых поражений кишечника и мочевого пузыря. Свой вклад вносит активное вовлечение в патологический процесс центральной нервной системы, головного мозга с признаками так называемой центральной сенситизации, а кроме того, раздражение соматических рецепторов брюшины вследствие микрокровоизлияний в ткань эндометриоидных гетеротопий и сопутствующих этому явлений перифокального асептического воспаления12.
Хронический сальпингоофорит на современном этапе диагностируется достаточно быстро. Он проявляется постоянными, тупыми, ноющими болями в нижней части живота, которые в 60% случаев иррадиируют в крестец. Усиление боли наблюдается при менструации, физическом напряжении, половом акте (боль исчезает после его прекращения), гинекологическом обследовании.
Для миомы характерны тянущие, схваткообразные боли в нижних отделах и пояснице без иррадиации в другие анатомические области. Она может сопровождаться патологическими менструальными кровотечениями со сгустками, продолжающимися шесть – восемь дней, и сопутствующими болезненными ощущениями.
Дисменорей страдают 50–70% женщин репродуктивного возраста, 60% девушек-подростков отмечают ее признаки в первые три года после менархе. Первичная дисменорея часто носит функциональный характер, вторичная развивается на фоне органического поражения половых органов.
После того как А.В. Воробьев рассмотрел этиологические факторы тазовой боли, он дал несколько рекомендаций по ее лечению, которое должно быть направлено на подавление гиперактивности ноцицептивных нейронов, разрушение генераторов патологически усиленного возбуждения для частичной или полной ликвидации алгической системы. В целом этиотропная терапия хронической тазовой боли включает прием НПВП и спазмолитиков, антибактериальных, противовирусных, противогрибковых средств, эндоваскулярное и эндохирургическое лечение варикозного расширения вен малого таза.
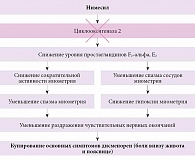
Значимую роль в купировании тазовой боли играют НПВП, которые обладают выраженным противовоспалительным и анальгезирующим воздействием. Известно, что НПВП подразделяются на неселективные, которые блокируют циклооксигеназу 1 и 2, в частности декскетопрофен, и селективные, которые блокируют только циклооксигеназу 2, например нимесулид. Среди основных механизмов многофакторного действия нимесулида (Нимесила) А.В. Воробьев выделил его способность подавлять выработку медиаторов воспаления, ингибировать синтез и высвобождение субстанции Р и блокировать выработку гистамина – тех участков патогенеза, которые имеют дополнительное значение в отношении развития синдрома тазового венозного полнокровия и эндометриоза (рисунок)13.
Как показало рандомизированное плацебоконтролируемое исследование, терапия Нимесилом по 100 мг два раза в сутки на 50% снижает интенсивность боли у женщин с дисменореей13. В многоцентровом рандомизированном двойном слепом исследовании была продемонстрирована способность Нимесила более эффективно по сравнению с диклофенаком купировать боль при дисменорее14. В другом исследовании врачи оценили терапию воспалительных заболеваний органов малого таза нимесулидом в гранулах (200 мг/сут) как эффективную в 90,5% случаев15. Нимесулид характеризуется высоким профилем безопасности. Так, на фоне применения нимесулида риск развития кровотечений из верхних отделов желудочно-кишечного тракта ниже, чем у мелоксикама и эторикоксиба, в три и два раза соответственно16.
В 2016 г. группа экспертов опубликовала консенсус по оценке роли нимесулида в купировании острой боли. Основной вывод заключался в том, что нимесулид при правильном использовании остается особенно ценным лекарственным средством для лечения ряда состояний, характеризующихся острой болью при воспалении, из-за быстрого начала обезболивающего эффекта, а также основанного на доказательствах положительного соотношения «польза – риск»6.
«С учетом большого клинического опыта применения Нимесила, а также результатов клинических исследований, подтверждающих его эффективность и безопасность, препарат можно рекомендовать к использованию при хронической тазовой боли у женщин», – отметил А.В. Воробьев, завершая выступление.
Заключение
Тазовая боль остается одной из наиболее сложных междисциплинарных проблем, различия в этиологии и патогенезе которой обусловливают разнообразие вариантов ее лечения. Большое значение в терапии боли имеют НПВП, среди которых эксперты выделили декскетопрофен (Дексалгин) и нимесулид (Нимесил). Дексалгин успешно купирует боль различного генеза. Нимесил не только обладает высокой эффективностью, но и характеризуется низким риском возникновения сердечно-сосудистых и желудочно-кишечных нежелательных явлений. При тазовой боли после короткого курса лечения препаратом Дексалгин рекомендуется проводить терапию препаратом Нимесил в течение 14 дней.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.